Experimentalvortrag zum Thema Einfhrung in die Halogenalkane PhilippsUniversitt


























- Slides: 48

Experimentalvortrag zum Thema: „Einführung in die Halogenalkane“ Philipps-Universität Marburg Elmar Schneider Datum: 26. 06. 2008

Gliederung n Allgemeine Informationen n Physikalische Eigenschaften n Synthesemöglichkeiten in der Schule n Möglichkeiten der Weiterreaktion n Verwendung n Umweltproblematik

Allgemeine Informationen Was macht ein Halogenalkan aus? ¨ Wasserstoffatome eines Alkans werden durch Halogenatome ersetzt n Mehrere Wasserstoffatome können ausgetauscht werden n Unterschiedliche Halogenatome können in ein Molekül eingefügt werden n Ab drei C-Atomen Möglichkeit der Isomerie

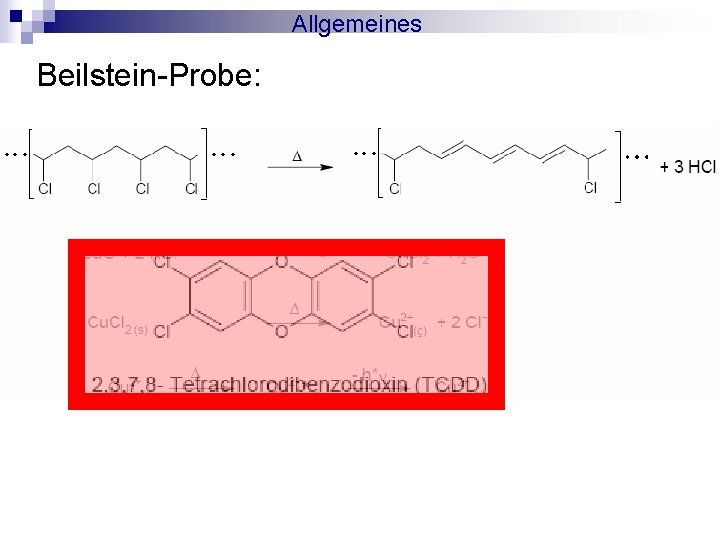
Allgemeines Versuch 1: Beilsteinprobe als Nachweis von Halogenen in Halogenalkanen

Allgemeines Beilstein-Probe:

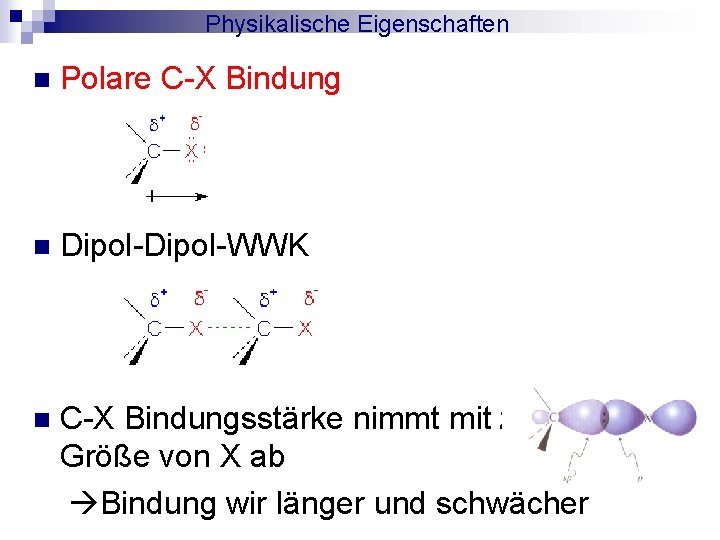
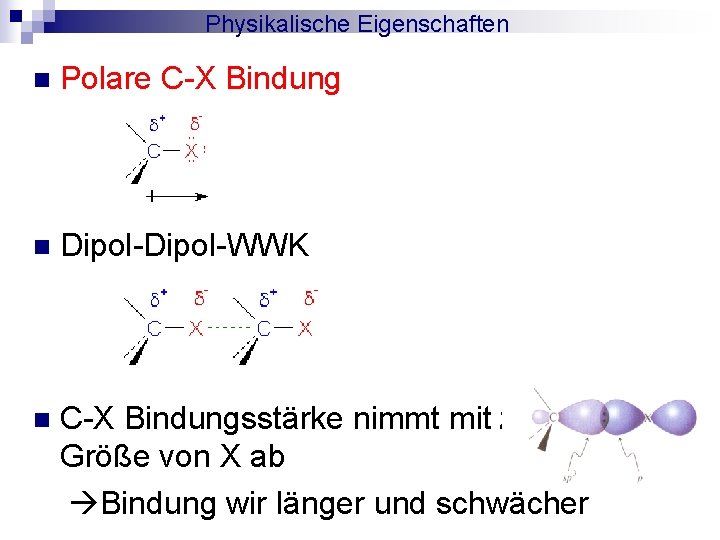
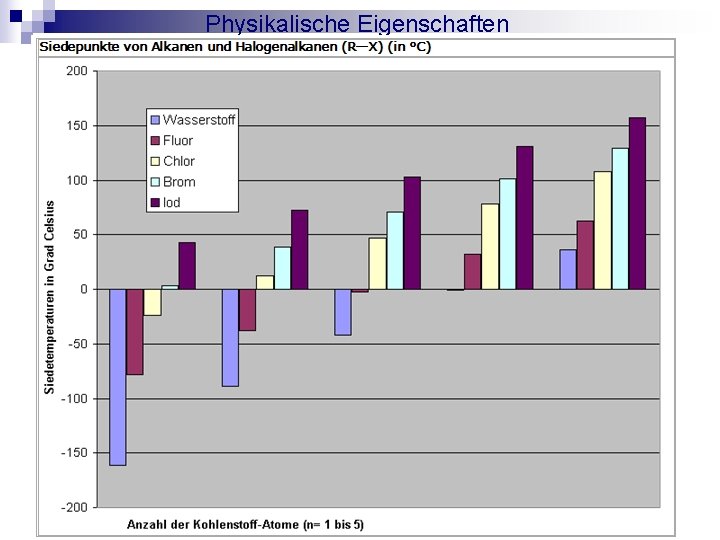
Physikalische Eigenschaften n Polare C-X Bindung n Dipol-WWK n C-X Bindungsstärke nimmt mit zunehmender Größe von X ab Bindung wir länger und schwächer

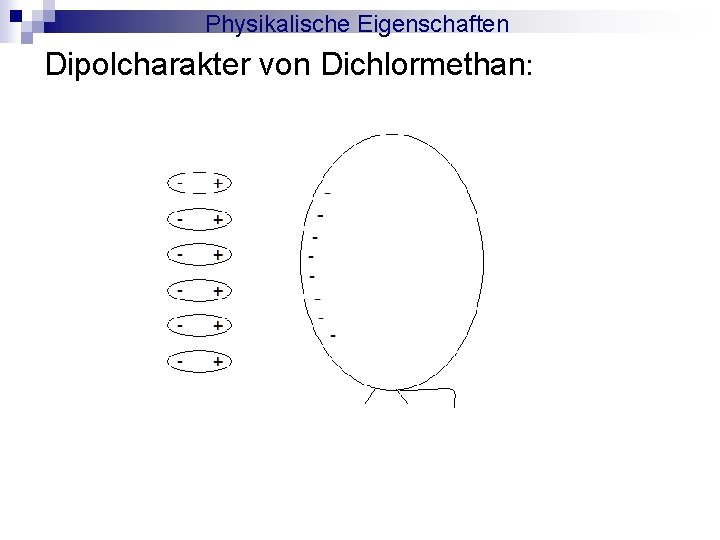
Physikalische Eigenschaften Demo 1: Dipolcharakter von Dichlormethan

Physikalische Eigenschaften Dipolcharakter von Dichlormethan:

Physikalische Eigenschaften n Polare C-X Bindung n Dipol-WWK n C-X Bindungsstärke nimmt mit zunehmender Größe von X ab Bindung wir länger und schwächer

Physikalische Eigenschaften n Polarisierbarkeit nimmt von R-F zu R-I zu

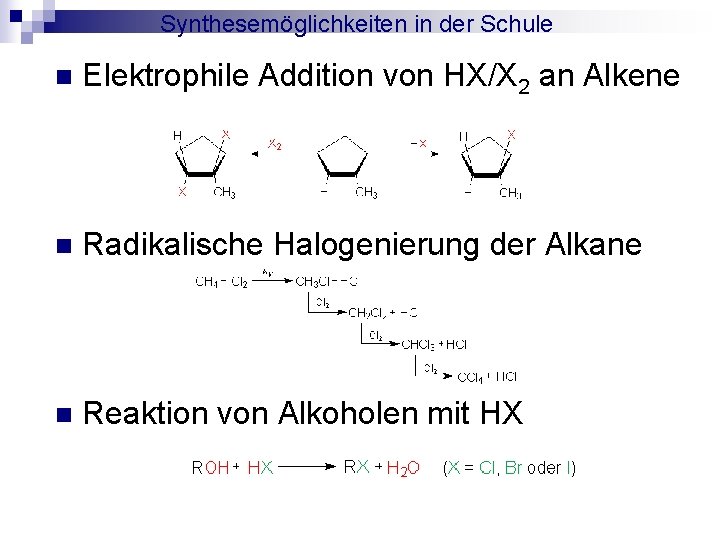
Synthesemöglichkeiten in der Schule n Elektrophile Addition von HX/X 2 an Alkene n Radikalische Halogenierung der Alkane n Reaktion von Alkoholen mit HX

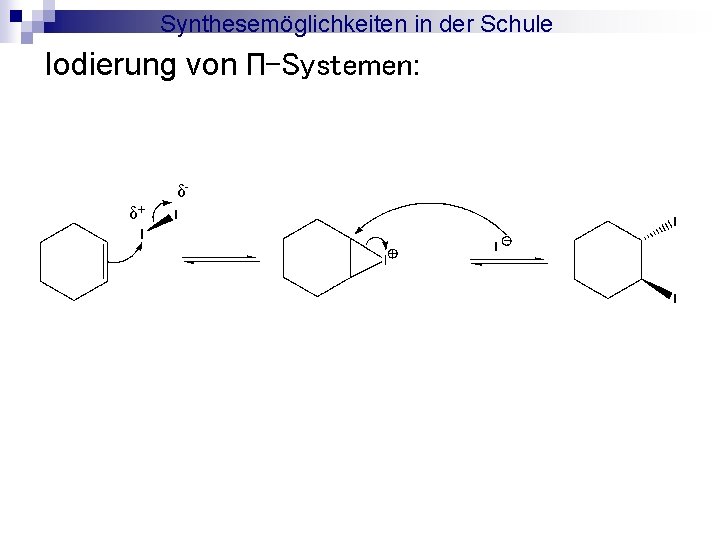
Synthesemöglichkeiten in der Schule Versuch 2: Iodierung von π-Systemen

Synthesemöglichkeiten in der Schule Iodierung von ∏-Systemen: δδ+

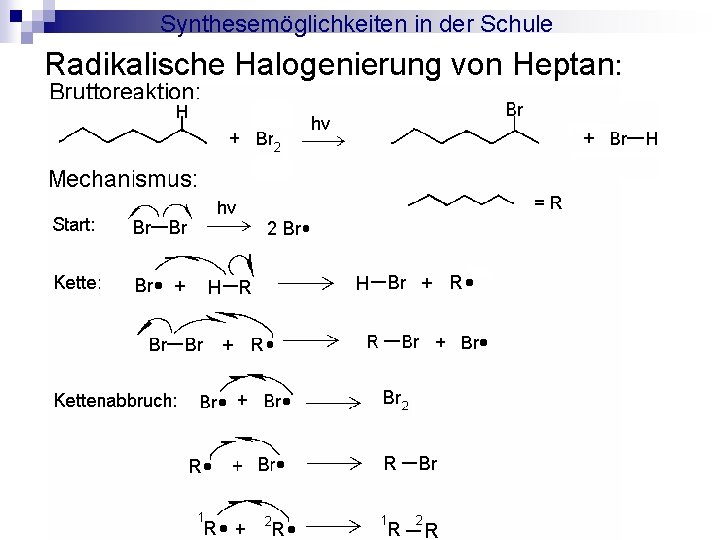
Synthesemöglichkeiten in der Schule Versuch 3: Radikalische Halogenierung von Heptan

Synthesemöglichkeiten in der Schule Radikalische Halogenierung von Heptan:

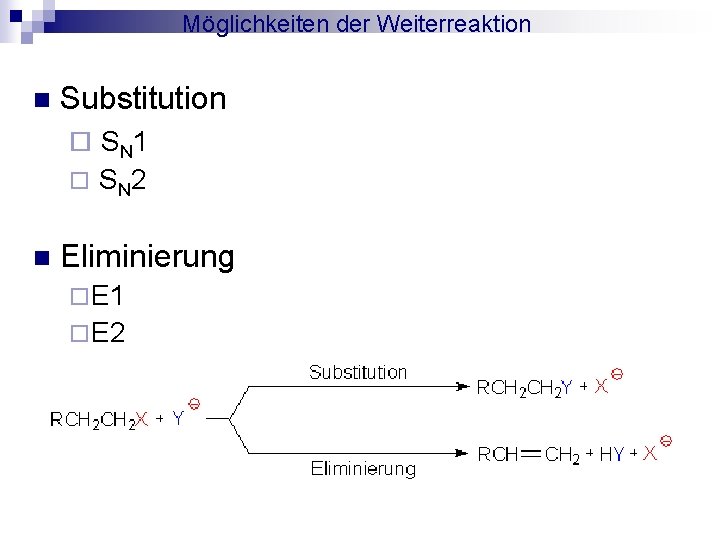
Möglichkeiten der Weiterreaktion n Substitution ¨ S N 1 ¨ n S N 2 Eliminierung ¨ E 1 ¨ E 2

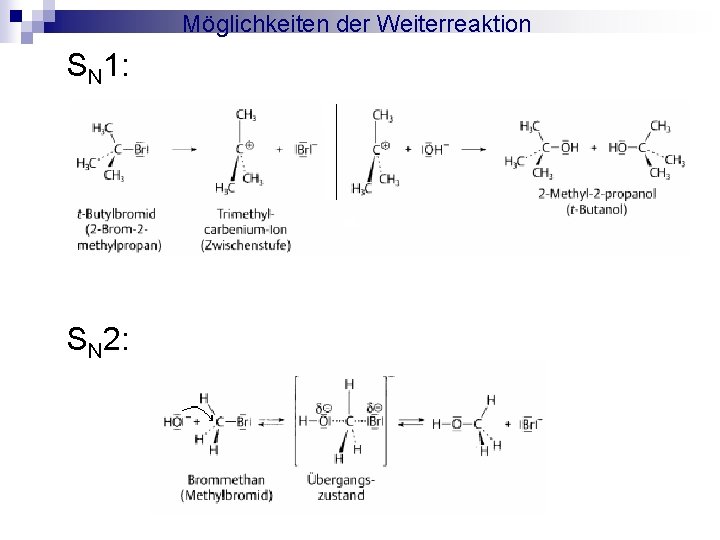
Möglichkeiten der Weiterreaktion SN 1: SN 2:

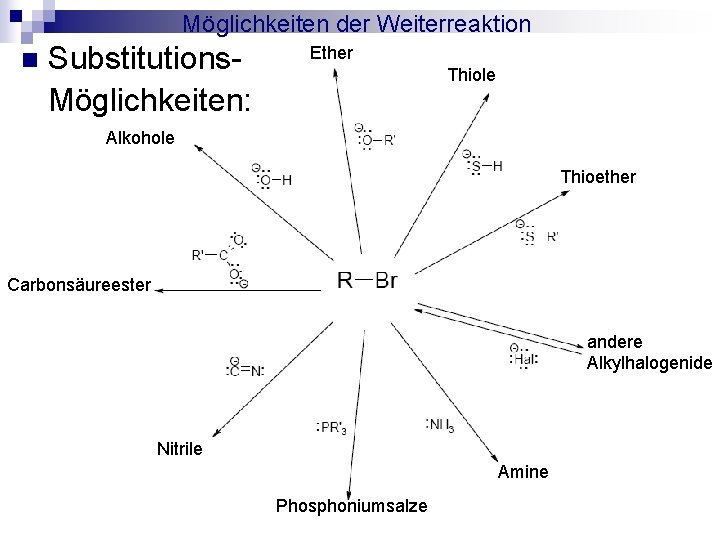
Möglichkeiten der Weiterreaktion n Substitutions. Möglichkeiten: Ether Thiole Alkohole Thioether Carbonsäureester andere Alkylhalogenide Nitrile Amine Phosphoniumsalze

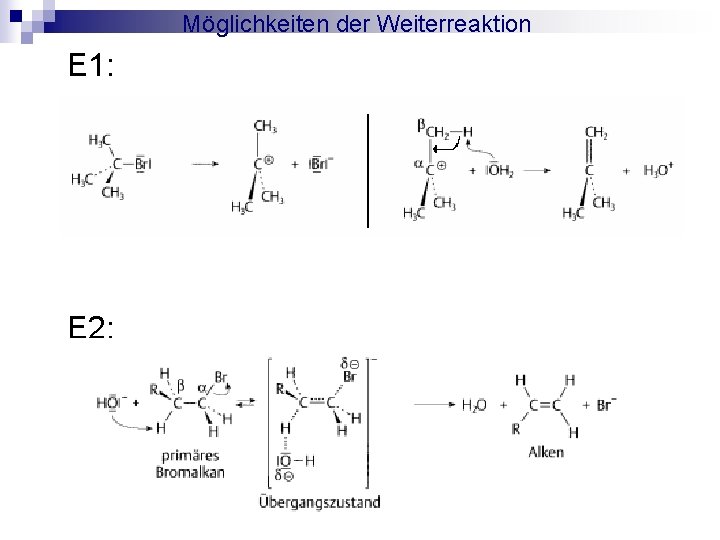
Möglichkeiten der Weiterreaktion E 1: E 2:

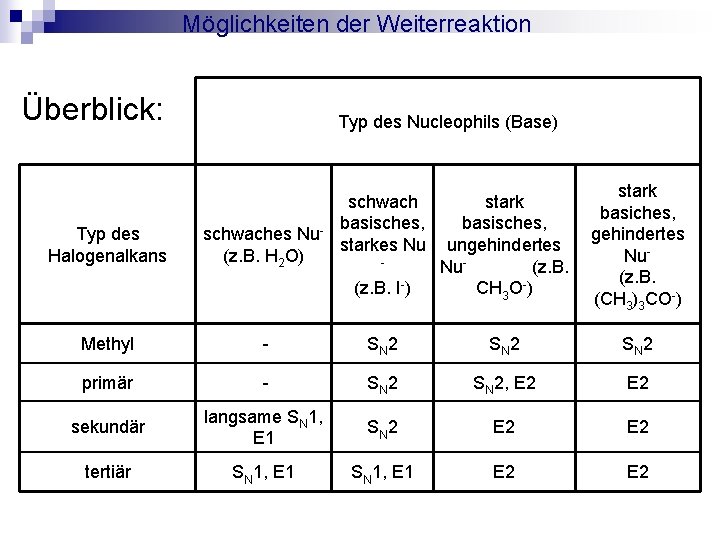
Möglichkeiten der Weiterreaktion Überblick: Typ des Halogenalkans Typ des Nucleophils (Base) schwaches Nu(z. B. H 2 O) (z. B. I-) stark basisches, ungehindertes Nu(z. B. CH 3 O-) stark basiches, gehindertes Nu(z. B. (CH 3)3 CO-) schwach basisches, starkes Nu - Methyl - SN 2 primär - SN 2, E 2 sekundär langsame SN 1, E 1 SN 2 E 2 tertiär SN 1, E 1 E 2

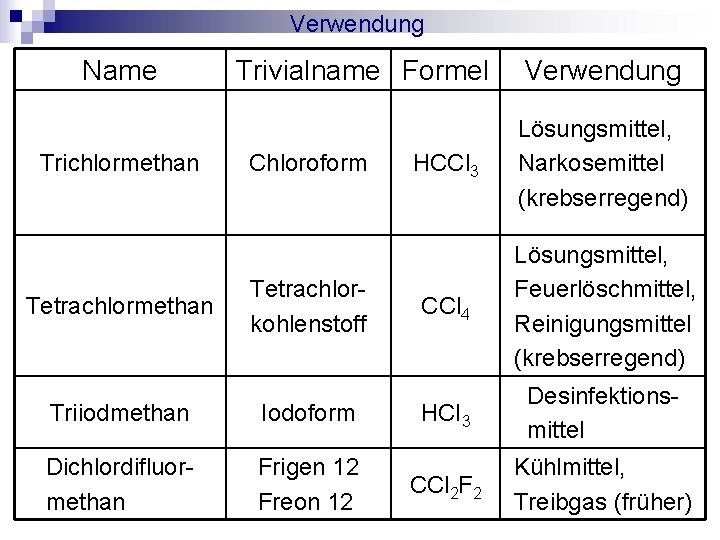
Verwendung Name Trichlormethan Tetrachlormethan Trivialname Formel Chloroform Tetrachlorkohlenstoff Triiodmethan Iodoform Dichlordifluormethan Frigen 12 Freon 12 Verwendung HCCl 3 Lösungsmittel, Narkosemittel (krebserregend) CCl 4 Lösungsmittel, Feuerlöschmittel, Reinigungsmittel (krebserregend) HCI 3 Desinfektionsmittel CCl 2 F 2 Kühlmittel, Treibgas (früher)

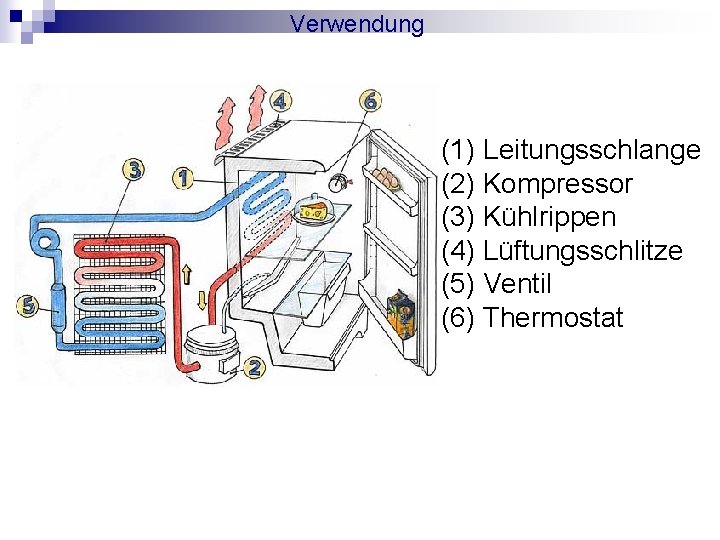
Verwendung (1) Leitungsschlange (2) Kompressor (3) Kühlrippen (4) Lüftungsschlitze (5) Ventil (6) Thermostat

Verwendung Demo 2: Kondensation bei Druckerhöhung

Verwendung Kondensation bei Druckerhöhung: Je höher der Druck, je höher der Siedepunkt einer Substanz Gas wird flüssig (wenn kritische Temperatur nicht überschritten ist)

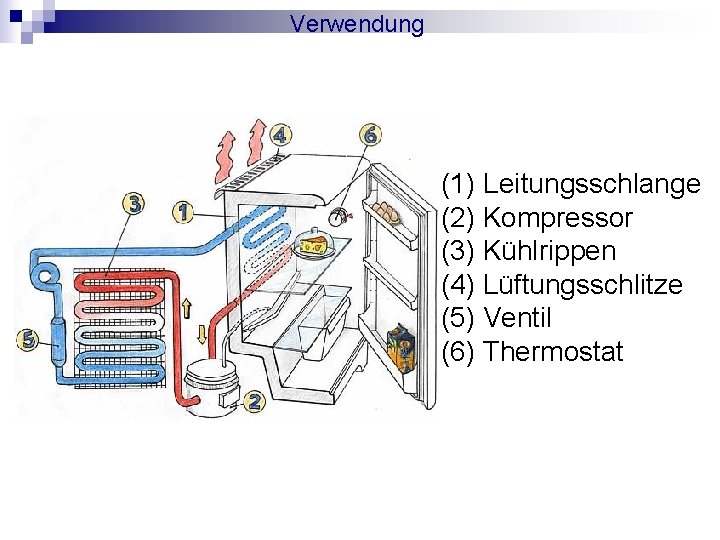
Verwendung (1) Leitungsschlange (2) Kompressor (3) Kühlrippen (4) Lüftungsschlitze (5) Ventil (6) Thermostat

Verwendung Demo 3: Verdunstungskälte

Verwendung Verdunstungskälte: Joule-Thomson-Effekt: Bei der Expansion wird Arbeit gegen die intermolekularen Anziehungskräfte geleistet Energie wird der kinetischen Energie der Moleküle entnommen Abkühlung

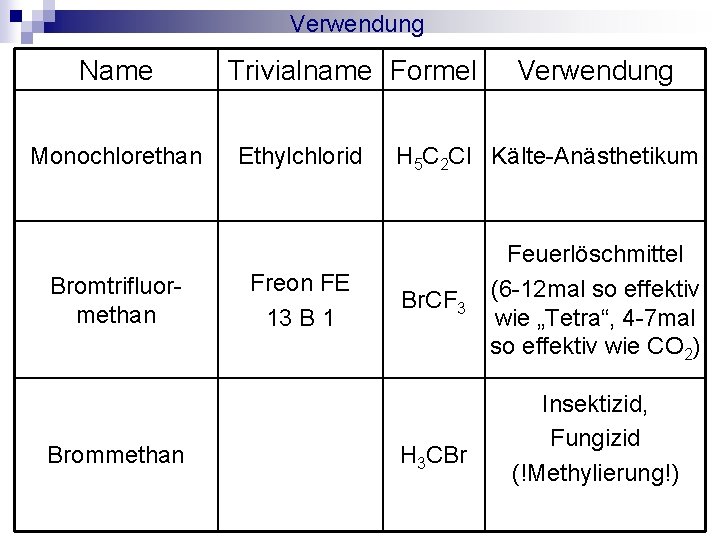
Verwendung Name Monochlorethan Bromtrifluormethan Brommethan Trivialname Formel Ethylchlorid Freon FE 13 B 1 Verwendung H 5 C 2 Cl Kälte-Anästhetikum Br. CF 3 H 3 CBr Feuerlöschmittel (6 -12 mal so effektiv wie „Tetra“, 4 -7 mal so effektiv wie CO 2) Insektizid, Fungizid (!Methylierung!)

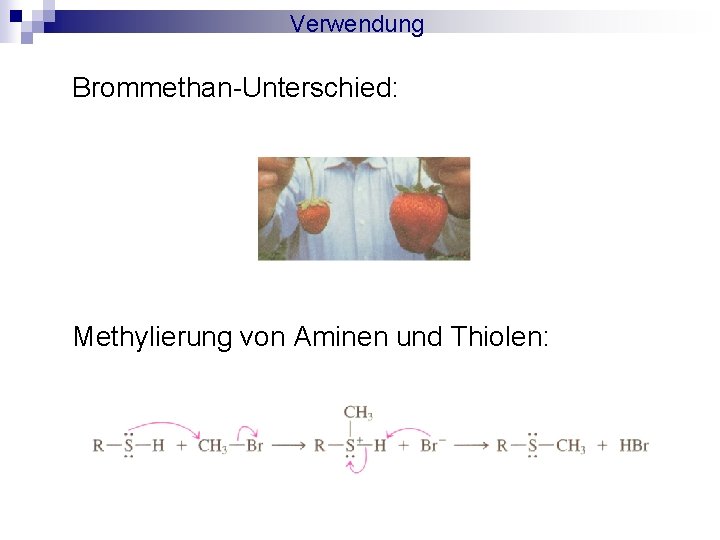
Verwendung Brommethan-Unterschied: Methylierung von Aminen und Thiolen:

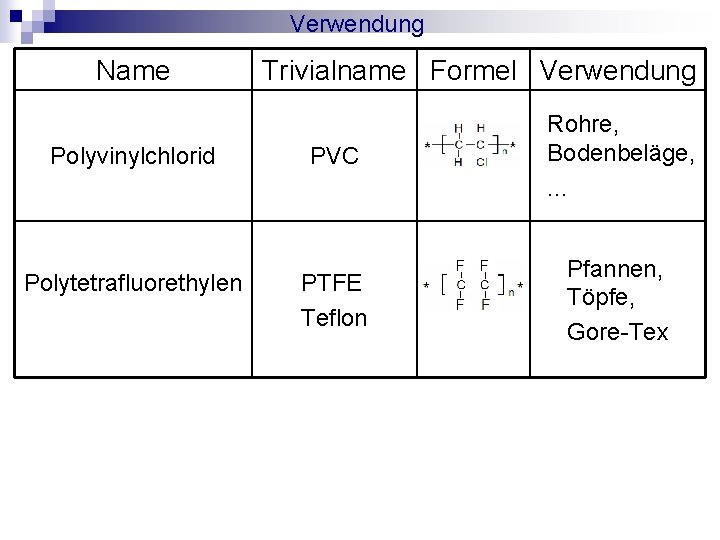
Verwendung Name Trivialname Formel Verwendung Polyvinylchlorid PVC Rohre, Bodenbeläge, . . . Polytetrafluorethylen PTFE Teflon Pfannen, Töpfe, Gore-Tex

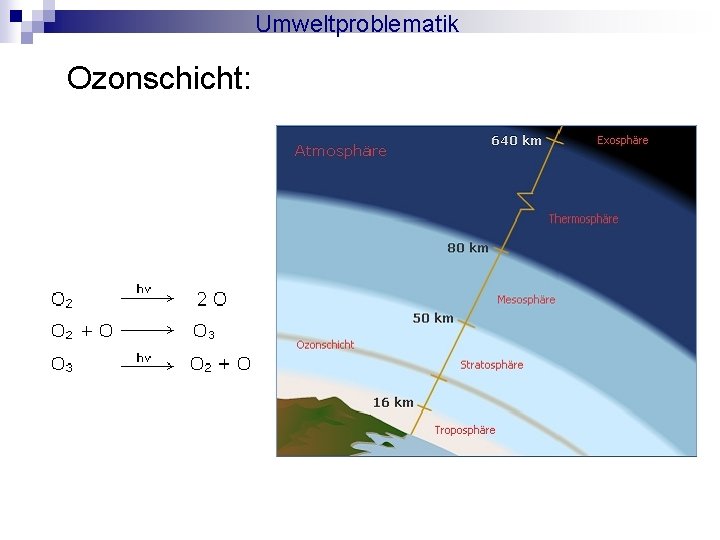
Umweltproblematik Ozonschicht:

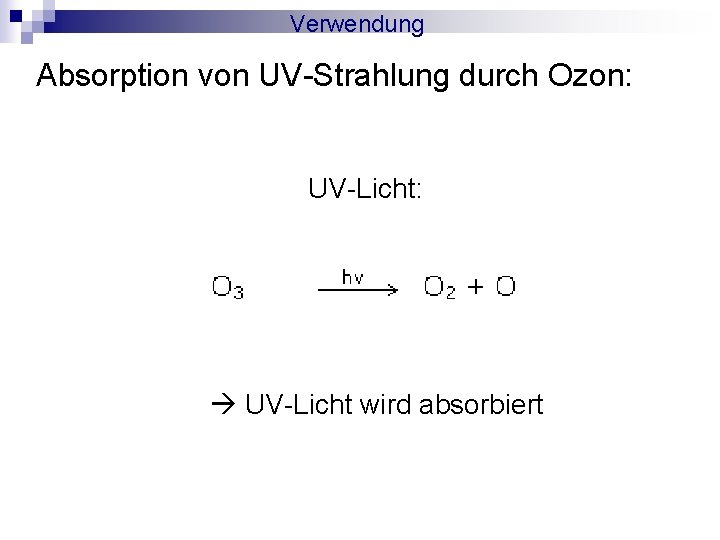
Verwendung Versuch 4: Absorption von UV-Strahlung durch Ozon

Verwendung Absorption von UV-Strahlung durch Ozon: UV-Licht: UV-Licht wird absorbiert

Umweltproblematik FCKW zerstören Ozon:

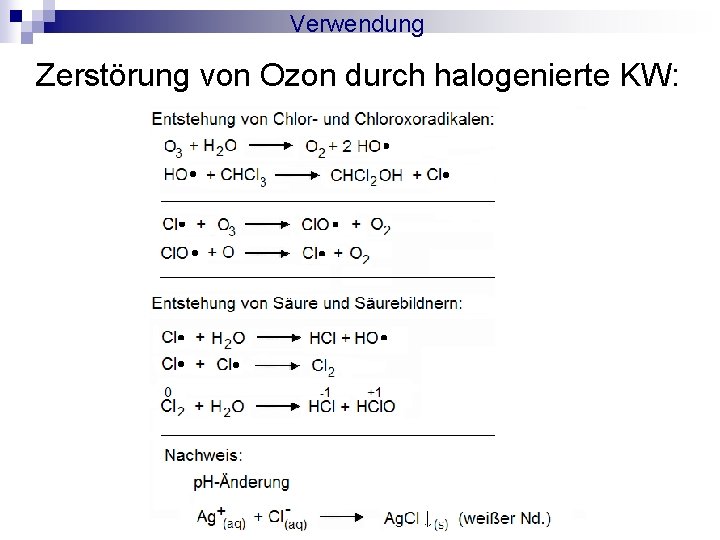
Verwendung Versuch 5: Zerstörung von Ozon durch halogenierte Kohlenwasserstoffe

Verwendung Zerstörung von Ozon durch halogenierte KW:

Umweltproblematik Konsequenz: § Montreal-Abkommen (1987) 31. 12. 1995 Produktionsstop § Regenerierung bis 2010? ? ? Summenformel CFCl 3 CF 2 Cl 2 C 2 F 4 Cl 2 Lebensdauer in der Atmosphäre 50 Jahre 102 Jahre 300 Jahre

Schulrelevanz (G 8 -Lehrplan) § GK 11. G 1 Kohlenstoffchemie I: Mechanismus der Addition von Molekülen des Typs X 2 § LK 11. G 1 Kohlenstoffchemie I: Typ und Mechanismus der Addition von Molekülen des Typs X 2 und HX und der Eliminierung; Alkanole: Reaktionstypen (Substitution) § 10. G 2 Einführung in die Kohlenstoffchemie: Halogenkohlenwasserstoffe (Halogenalkane): Eigenschaften und Reaktionen / Nachweisreaktion; Umweltgefährdung durch FCKW in der Atmosphäre

Schulrelevanz (G 8 -Lehrplan) § 10. G 2 Einführung in die Kohlenstoffchemie: Mechanismus der radikalischen Substitution § 9. G 2 Säuren und Laugen: Nachweis ausgewählter Kationen § 8. G 2 Ordnung in der Vielfalt Atombau und Periodensystem: Verwendung verschiedener Halogene in Alltag und Technik § 7. G 1 Stoffe unterscheiden und isolieren: Aggregatzustände eines Stoffes in Abhängigkeit von der Temperatur deuten

Vielen Dank für Ihre Aufmerksamkeit!

Versuch 1: Beilsteinprobe als Nachweis von Halogenen in Halogenalkanen

Versuch 2: Iodierung von π-Systemen

Versuch 3: Radikalische Halogenierung von Heptan

Versuch 4: Absorption von UV-Strahlung durch Ozon

Versuch 5: Zerstörung von Ozon durch halogenierte Kohlenwasserstoffe

Demo 1: Dipolcharakter von Dichlormethan

Demo 2: Kondensation bei Druckerhöhung

Demo 3: Verdunstungskälte