ELEKTROKIMIA Elektrolisis a Pada Anoda terjadi oksidasi Ion




















- Slides: 24

ELEKTROKIMIA Elektrolisis a. Pada Anoda (+) : terjadi oksidasi Ø Ion OH ¯ dioksidasi menjadi H 2 O & O 2 4 OH ¯(aq) → 2 H 2 O ( l ) + O 2 (g) + 4 e¯ Ø Ion sisa asam yang mengandung oksigen tidak dioksidasi, yang dioksidasi air. 2 H 2 O ( l ) → 4 H+(aq) + O 2 (g) + 4 e¯ Ø Ion sisa asam yang lain dioksidasi menjadi molekul. Contoh: 2 Cl ¯(aq) → Cl 2 (g) + 2 e¯

b. Pada Katoda (–) : terjadi reduksi ØIon H+ direduksi menjadi H 2. 2 H+(aq) + 2 e¯ → H 2 (g) Ø Ion logam alkali (IA) & alkali tanah (IIA) tidak direduksi, yang direduksi air. 2 H 2 O (aq) + 2 e¯ → H 2 (g) + 2 OH ¯(aq) ØIon logam lain direduksi. Contoh: Al 3+ (aq) + 3 e¯ → Al (s) Ni 2+ (aq) + 2 e¯ → Ni (s) Ag+(aq) + e¯ → Ag (s)

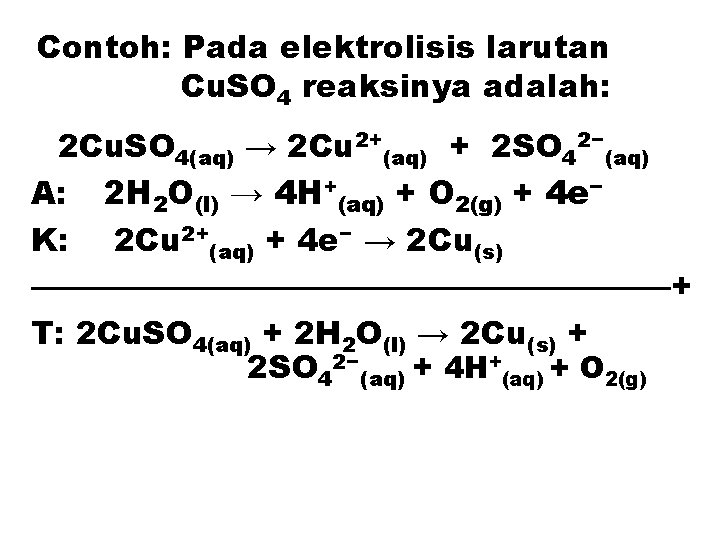
Contoh: Pada elektrolisis larutan Cu. SO 4 reaksinya adalah: 2 Cu. SO 4(aq) → 2 Cu 2+(aq) + 2 SO 42−(aq) A: 2 H 2 O(l) → 4 H+(aq) + O 2(g) + 4 e− K: 2 Cu 2+(aq) + 4 e− → 2 Cu(s) ——————————+ T: 2 Cu. SO 4(aq) + 2 H 2 O(l) → 2 Cu(s) + 2 SO 42−(aq) + 4 H+(aq) + O 2(g)

Hukum Faraday (Michael Faraday: 1834) Hukum Faraday I: Contoh soal: Larutan Cu. SO 4 dielektrolisis menggunakan arus listrik 0, 5 A selama 30 menit. Berapa massa Cu dan O 2 yang dihasilkan ? (Ar Cu = 64, O = 16)

Jawab: 64 g/mol x 0, 5 A x 30 menit x 60 dt/menit massa Cu = ————————— 2 x 96 500 C/mol = 0, 298 g 16 g/mol x 0, 5 A x 30 menit x 60 dt/menit massa O = ————————— 2 x 96 500 C/mol = 0, 0746 g

Hukum Faraday II: Pada elektrolisis dengan listrik sama, perbandingan massa zat = perbandingan massa ekivalennya (Ar/n) Contoh: Laruran Cu. SO 4 dan larutan Ag 2 SO 4 dielektrolisis dengan jumlah listrik yang sama. a. Berapa perbandingan massa Cu dan Ag yang dihasilkan ? b. Jika dihasilkan Cu = 0, 32 g, maka berapa gram Ag yang dihasilkan ? (Ar Cu = 64, Ag = 108).

Jawab: a. WCu : WAg = (Ar/n)Cu : (Ar/n)Ag = (64/2) : (108/1) = 32 : 108 b. WCu / WAg = 32 / 108 WAg = WCu / (32 / 108) = 0, 32 / (32 / 108) = 1, 08 g

Sel Galvani a. Sel kimia dengan transference. Contohnya sel Daniell. Kutub (–): Zn (s) → Zn 2+ (aq) + 2 e¯ (Oksidasi) E°oks = + 0, 76 V 2+ Kutub (+): Cu (aq) + 2 e¯ → Cu (s) (Reduksi) E°red = + 0, 34 V ——————————————— + Total: Zn (s) + Cu 2+ (aq) → Zn 2+ (aq) + Cu (s) (Redoks) E°sel = + 1, 10 V E°sel = E° reduksi + E° oksidasi = E°reduksi kutub positif – E°reduksi kutub negatif

Contoh: Sel elektrokimia dengan transference menggunakan elektroda Fe dalam larutan Fe. SO 4 dan elektroda Zn dalam larutan Zn. SO 4. Jika Zn 2+/Zn = – 0, 76 V, Fe 2+/Fe = – 0, 44 V, maka: a. Tuliskan reaksi yang terjadi dan hitung berapa E°sel yang dihasilkan ? b. Manakah elektroda positip dan negatifnya, Fe atau Zn ?

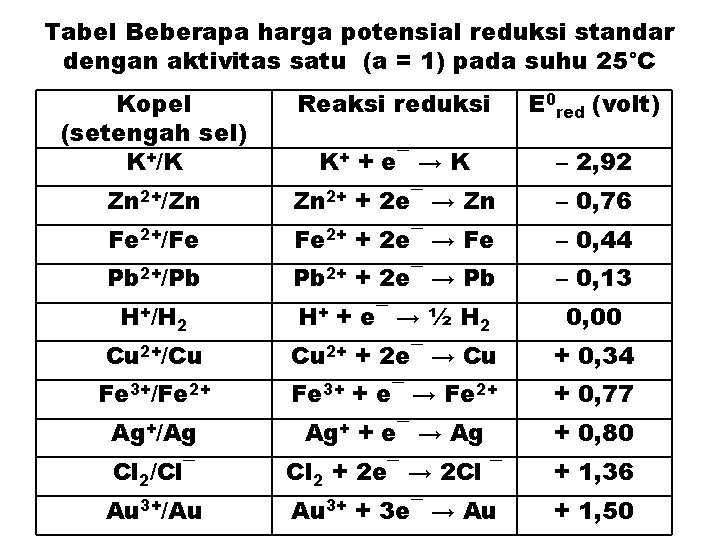
Tabel Beberapa harga potensial reduksi standar dengan aktivitas satu (a = 1) pada suhu 25°C Kopel (setengah sel) K+/K Reaksi reduksi E 0 red (volt) K+ + e¯ → K – 2, 92 Zn 2+/Zn Zn 2+ + 2 e¯ → Zn – 0, 76 Fe 2+/Fe Fe 2+ + 2 e¯ → Fe – 0, 44 Pb 2+/Pb Pb 2+ + 2 e¯ → Pb – 0, 13 H+/H 2 H+ + e¯ → ½ H 2 0, 00 Cu 2+/Cu Cu 2+ + 2 e¯ → Cu + 0, 34 Fe 3+/Fe 2+ Fe 3+ + e¯ → Fe 2+ + 0, 77 Ag+/Ag Ag+ + e¯ → Ag + 0, 80 Cl 2/Cl¯ Cl 2 + 2 e¯ → 2 Cl ¯ + 1, 36 Au 3+/Au Au 3+ + 3 e¯ → Au + 1, 50

Contoh soal: Hitunglah E°sel untuk reaksi: Zn / Zn 2+ (a = 1) // Pb 2+ (a = 1) / Pb Jawab: E°sel = E° Zn/Zn 2+ + E° Pb 2+/Pb = – (– 0, 76 V) + (– 0, 13 V) = + 0, 63 V

Sel kimia tanpa transference, contoh: Ø Sel Accu Pb(s) + SO 42¯(aq) → Pb. SO 4(s) + 2 e¯ Pb. O 2(s) + SO 42¯(aq) + 4 H+(aq) + 2 e¯ → Pb. SO 4(aq) + 2 H 2 O(l) ———————————— + Pb(s) + Pb. O 2(s) + 2 H 2 SO 4(aq) → 2 Pb. SO 4(s) + 2 H 2 O(l)

ØSel Leclanche (sel kering) Zn (s) → Zn 2+ (aq) + 2 e¯ 2 Mn. O 2 (s) + H 2 O ( l ) + 2 e¯ → Mn 2 O 3 (s) + 2 OH ¯(aq) ——————————— + Zn (s) + 2 Mn. O 2 (aq) + H 2 O ( l ) → Zn 2+(aq) + 2 OH ¯ (aq) + Mn 2 O 3 (s) Terjadi juga reaksi lain, yaitu OH¯ yang terbentuk bereaksi dengan NH 4 Cl menghasilkan NH 3, selanjutnya NH 3 yang terjadi diikat Zn 2+ 2 NH 4 Cl (aq) + 2 OH ¯(aq) → 2 NH 3 (aq) + 2 Cl ¯(aq) + 2 H 2 O ( l ) Zn 2+(aq) + 4 NH 3 (g) + 4 Cl ¯(aq) → [Zn(NH 3)4]Cl 2 (s)

Pada batu baterai biasa yang menggunakan anoda logam Zn, katoda batang C, dan elektrolitnya pasta berair dari campuran NH 4 Cl, Mn. O 2, dan serbuk C, reaksi oksidasi dan reduksi yang terjadi adalah: Zn (s) → Zn 2+ (aq) + 2 e¯ 2 Mn. O 2 (s) + 2 H 2 O ( l) + 2 e¯ → 2 Mn. O(OH) (s) + 2 OH ¯(aq) ——————————— + Zn (s) + 2 Mn. O 2 (aq) + 2 H 2 O ( l ) → Zn 2+(aq) + 2 Mn. O(OH) (s) + 2 OH ¯ (aq)

Reaksi lainnya yaitu OH ¯ yang terbentuk bereaksi dengan NH 4+ menghasilkan NH 3, selanjutnya NH 3 yang terjadi diikat Zn 2+ 2 NH 4+ (aq) + 2 OH ¯ (aq) → 2 NH 3 (aq) + 2 H 2 O ( l ) Zn 2+ (aq) + 2 NH 3 (g) + 2 Cl ¯ (aq) → [Zn(NH 3)2]Cl 2 (s) Pada batu baterai alkaline, sebagai anoda digunakan Zn, sebagai katoda Mn. O 2, dan sebagai elektrolitnya KOH. Potensial listrik yang dihasilkan ± 1, 5 volt. Reaksi oksidasi reduksi yang terjadi adalah:

Zn 2+(aq) + 2 OH ¯ (aq) → Zn(OH)2 (s) + 2 e¯ 2 Mn. O 2 (s) + 2 H 2 O ( l ) + 2 e¯ → 2 Mn. O(OH) (s) + 2 OH ¯(aq) ——————————— + Zn (s) + 2 Mn. O 2 (aq) + 2 H 2 O ( l ) → Zn(OH)2 (s) + 2 Mn. O(OH) (s) Pada baterai perak oksida - zink seperti yang biasa digunakan pada arloji, sebagai anoda digunakan Zn, sebagai katoda digunakan Ag 2 O, dan sebagai elektrolitnya KOH. Potensial listrik yang dihasilkan ± 1, 5 volt. Reaksi oksidasi dan reduksi yang terjadi adalah:

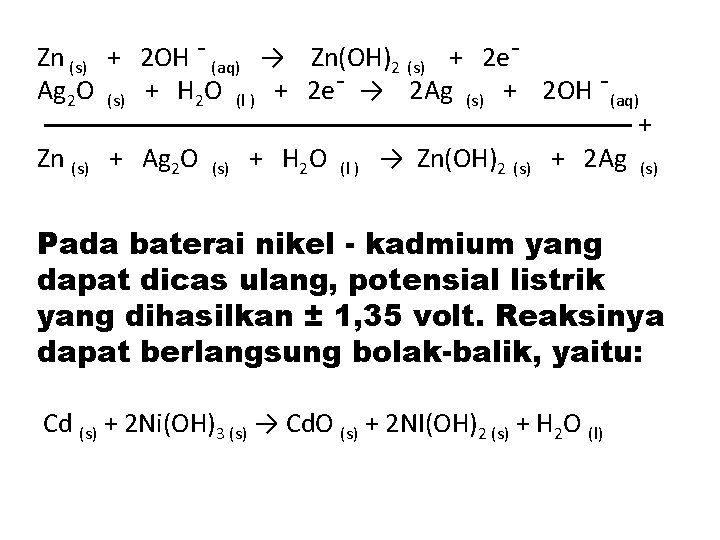
Zn (s) + 2 OH ¯ (aq) → Zn(OH)2 (s) + 2 e¯ Ag 2 O (s) + H 2 O (l ) + 2 e¯ → 2 Ag (s) + 2 OH ¯(aq) ——————————— + Zn (s) + Ag 2 O (s) + H 2 O (l ) → Zn(OH)2 (s) + 2 Ag (s) Pada baterai nikel - kadmium yang dapat dicas ulang, potensial listrik yang dihasilkan ± 1, 35 volt. Reaksinya dapat berlangsung bolak-balik, yaitu: Cd (s) + 2 Ni(OH)3 (s) → Cd. O (s) + 2 NI(OH)2 (s) + H 2 O (l)

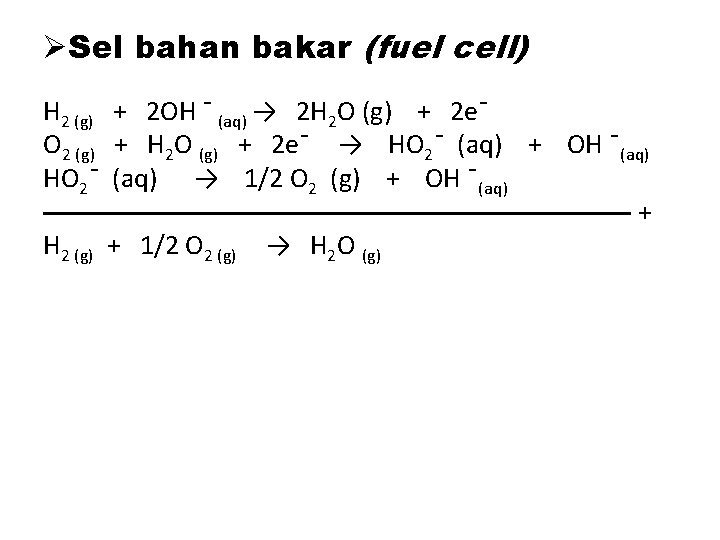
ØSel bahan bakar (fuel cell) H 2 (g) + 2 OH ¯ (aq) → 2 H 2 O (g) + 2 e¯ O 2 (g) + H 2 O (g) + 2 e¯ → HO 2¯ (aq) + OH ¯(aq) HO 2¯ (aq) → 1/2 O 2 (g) + OH ¯(aq) ——————————— + H 2 (g) + 1/2 O 2 (g) → H 2 O (g)

Soal latihan: 1. Larutan Cu. SO 4 dielektrolisis menggunakan arus listrik 0, 5 A selama 1 jam. Berapa gram Cu yang diendapkan pada katoda? (Ar Cu = 64) 2. Laruran Cu. SO 4 dan larutan Ni. SO 4 dielektrolisis dengan jumlah listrik yang sama. Jika Cu yang dihasilkan 0, 32 g, maka berapa gram Ni yang dihasilkan ? (Ar Cu = 64, Ni = 59).

3. Larutan Zn. SO 4 dielektrolisis menggunakan arus listrik 0, 5 A selama 1 jam. a. Tuliskan reaksi yang terjadi ! b. Berapa gram Zn yang diendapkan pada katoda? (Ar Zn = 65) 4. Berapa gram Ni yang diendapkan pada elektrolisis larutan Ni. SO 4 jika digunakan arus listrik 20 000 C ?

5. Berapa waktu yang diperlukan untuk elektrolisis larutan Ag. NO 3 menggunakan arus listrik 0, 5 A agar diperoleh 0, 1 gram endapan Ag ? 6. Berapa waktu yang diperlukan untuk elektrolisis 10 m. L larutan Ag. NO 3 0, 001 M menggunakan arus listrik 1, 5 A sampai elektrolisis terhenti karena semua perak telah mengendap ?

7. Jika campuran larutan Cu. SO 4 dan Ni. SO 4 dielektrolisis sehingga dihasilkan 0, 1 gram endapan, maka berapa gram Cu dan berapa gram Ni yang telah diendapkan dari larutan tersebut ? 8. Larutan Cu. SO 4, Au. Cl 3, dan Ag. NO 3 yang terpisah masing-masing dielektrolisis dengan arus listrik 0, 5 A dalam waktu yang sama. Jika Cu yang diendapkan sebanyak 0, 1 gram, maka masing-masing berapa gram Au dan Ag yang diendapkan ?

9. Masing-masing pasangan reaksi berikut aktivitasnya satu (a = 1). Masing-masing tentukan reaksi (i) atau (ii) yang dapat berlangsung, kemudian hitunglah potensial sel yang dihasilkan ! a. (i). Cu/Cu 2+//Ag+/Ag atau (ii). Ag/Ag+//Cu 2+/Cu b. (i). Cu/Cu 2+//Pb 2+/Pb atau (ii). Pb/Pb 2+//Cu 2+/Cu c. (i). Pb/Pb 2+//Ag+/Ag atau (ii). Ag/Ag+//Pb 2+/Pb d. (i). Zn/Zn 2+//Ag+/Ag atau (ii). Ag/Ag+//Zn 2+/Zn

10. Sel elektrokimia dengan transference / jembatan garam K 2 SO 4 menggunakan elektroda Fe dalam larutan Fe. SO 4 dan elektroda Zn dalam larutan Zn. SO 4. a. Tuliskan reaksi yang terjadi dan hitung berapakah potensial sel yang dihasilkan ? b. Manakah elektroda positip dan negatifnya, Fe atau Zn ?