SEL ELEKTROKIMIA A Volta B Elektrolisis A Sel

SEL ELEKTROKIMIA A. Volta B. Elektrolisis
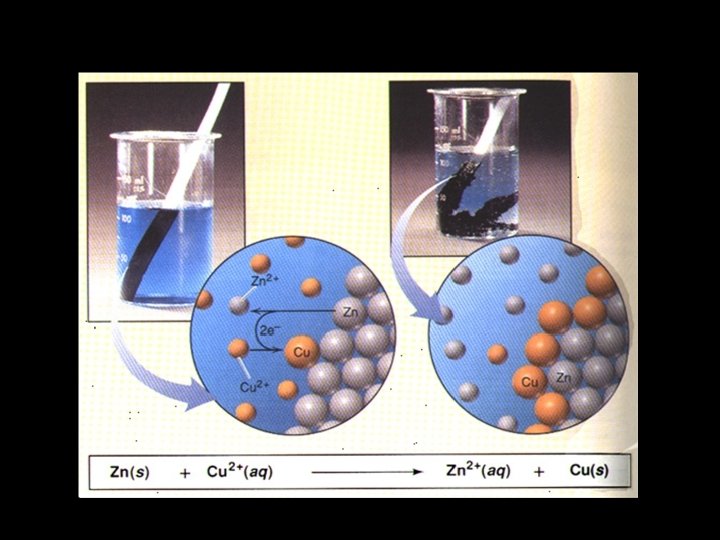

A. Sel Volta 1. 2. 3. 4. Gambar Sel Volta Notasi Sel Potensial Reduksi Memperkirakan Berlangsungnya Reaksi dengan Potensial Sel
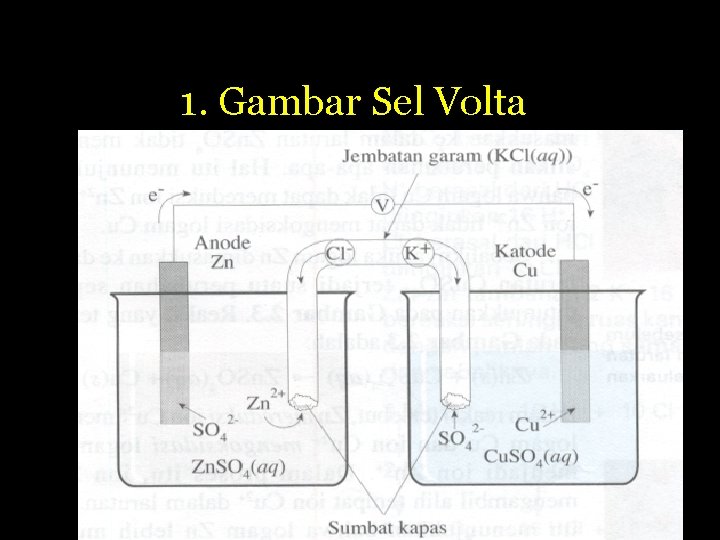
1. Gambar Sel Volta

Deret Volta Li K Ba Ca Na Mg Al Mn Zn Fe Co Ni Sn Pb H Cu Hg Ag Pt Au

2. Notasi Sel jembatan garam anode katode Zn (s) / Zn 2+ (aq) // Cu 2+ (aq) / Cu (s) elektrode anode Elektrode katode elektrolit anode Elektrolit katode
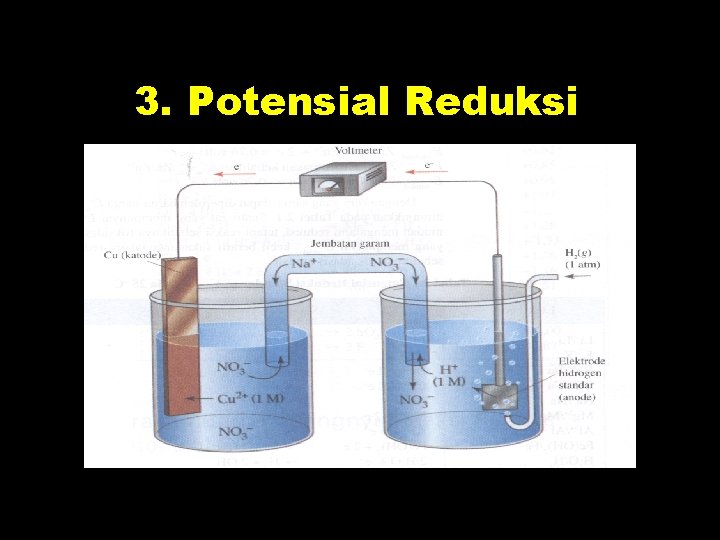
3. Potensial Reduksi


4. Memperkirakan Berlangsungnya Reaksi Redoks dengan Potensial Sel E°sel = E°reduksi - E°oksidasi Reaksi berlangsung spontan jika E°sel > 0

Contoh: 1. Tentukan potensial sel dan notasi sel dari reaksi Zn (s) + Cu 2+ → Zn 2+ + Cu Diketahui : Zn 2+ + 2 e → Zn E°= -0. 76 volt Cu 2+ + 2 e → Cu E°= +0. 34 volt

Jawab: E°oksidasi Zn → Zn 2+ + 2 e = +0. 76 volt E°reduksi Cu 2+ + 2 e → Cu = +0. 34 volt E°sel Zn(s) +Cu 2+ →Zn 2+ +Cu = +1. 10 volt Notasi Sel Zn(s)/Zn 2+(aq) // Cu 2+(aq) / Cu(s)


LATIHAN - 1 Ditahui potensial elektroda Cu 2+(aq) + 2 e Cu(s) E° = + 0, 34 V Ni 2+(aq) +2 e Ni(s) E° = 0, 28 V Ag+(aq) + e Ag(s) E° = + 0, 80 V ü Sel Volta dibuat dari elektroda Cu dan Ni, Berapa potensial sel yang terjadi ? ü Tuliskan reaksi selnya ü Tuliskan notasi selnya ü Gambarkan diagram selnya ü Apakah reaksi : Cu(NO 3)2(aq) + 2 Ag(s) Cu(s) + 2 Ag. NO 3 dapat berlangsung spontan ? Jelaskan jawabanmu.

LATIHAN - 2 Ditahui potensial elektroda Cu 2+(aq) + 2 e Cu(s) E° = +0, 34 V Al 3+(aq) +3 e Al(s) E° = 1, 66 V Ag+(aq) + e Ag(s) E° = +0, 80 V • Sel Volta dibuat dari elektroda Cu dan Al. Berapa potensial sel yang terjadi ? • Tuliskan reaksi selnya • Tuliskan notasi selnya • Jelaskan bagan/diagram selnya • Jelaskan reaksi 3 Ag. NO 3 (aq) + Al (s) 3 Ag(s) + Al(NO 3)3 berlangsung spontan atau tidak. • Jelaskan jawabanmu.

LATIHAN 3 • • Jika diketahui : Sn 2+ + 2 e → Sn Cu 2++ 2 e → Cu Zn + Cu 2+→ Zn 2+ + Cu Eo = 0, 14 V Eo = +0, 34 V Eo = +1, 10 V Maka potensial standar untuk reaksi Zn + Sn 2+ → Zn 2++ Sn A. 0, 62 V D. 1, 24 V B. 0, 76 V E. 1, 44 V C. 0, 96 V

LATIHAN - 3 Diketahu potensial sebagai berikut : Pb | Pb 2+ || Mg 2+ | Mg Eo = 2, 21 V Zn | Zn 2+ || Cu 2+ | Cu Eo = +1, 10 V Pb | Pb 2+ || Cu 2+ | Cu Eo = + 0, 47 V Harga potensial sel untuk reaksi Mg | Mg 2+ || Zn 2+ | Zn adalah …. A. 0, 64 V D. 1, 58 V B. 1, 11 V E. 3, 78 V C. 1, 57 V

PERSAMAN NERST ( SEL KONST BERBEDA)




Sel Volta dalam kehidupan sehari – hari : 1. BATERAY 2. SEL AKI 3. SEL PERAK OKSIDA 4. SEL NIKEL KADMIUM 5. SEL BAHAN BAKAR


1. Sel Kering (Sel Leclanche- primer ØDikenal sebagai batu baterai biasa ØTerdiri dari katode yang berasal dari karbon(grafit) dan anode logam zink ØElektrolit yang dipakai berupa pasta campuran Mn. O 2, serbuk karbon dan NH 4 Cl Persamaan reaksinya : Katode : 2 Mn. O 2 + 2 H+ + 2 e Mn 2 O 3 + H 2 O Anode : Zn 2+ + 2 e Reaksi sel : 2 Mn. O 2 + 2 H+ + Zn Mn 2 O 3 + H 2 O + Zn 2+


2. Sel Kering - Alkalin (Sel Leclanche -primer) ØDikenal sebagai batu baterai Alakalin ØTerdiri dari katode yang berasal dari karbon(grafit) dan anode logam zink ØElektrolit yang dipakai berupa pasta campuran Mn. O 2, serbuk karbon dan KOH Persamaan reaksinya : Katode : 2 Mn. O 2 + 2 H 2 O + 2 e → 2 Mn. O(OH)2 + 2 OH Anode : Zn + 2 OH- → Zn(OH)2 + 2 e Reaksi sel : 2 Mn. O 2 + 2 H 2 O + Zn → 2 Mn. O(OH)2 + Zn(OH)2
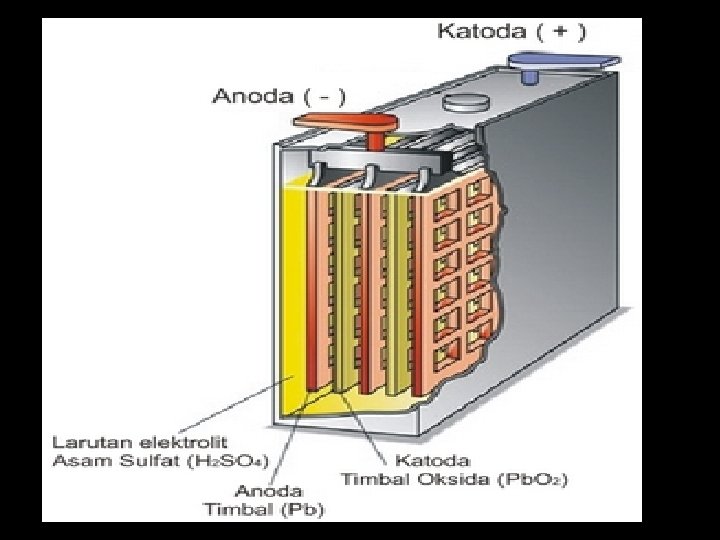

2. Sel Aki Sel aki disebut juga sebagai sel penyimpan, karena dapat berfungsi penyimpan listrik dan pada setiap saat dapat dikeluarkan. Anodenya terbuat dari logam timbal (Pb) dan katodenya terbuat dari logam timbal yang dilapisi Pb. O 2. Reaksi penggunaan aki : Anode : Pb + SO 4 2 - Pb. SO 4 + 2 e Katode : Pb. O 2 + SO 42 -+ 4 H++ 2 e Pb. SO 4 + 2 H 2 O Reaksi sel : Pb + 2 SO 4 2 - + Pb. O 2 + 4 H+ 2 Pb. SO 4 + 2 H 2 O Reaksi Pengisian aki : 2 Pb. SO 4 + 2 H 2 O Pb + 2 SO 4 2 - + Pb. O 2 + 4 H+ ACCU

3. Sel Perak Oksida Sel ini banyak digunakan untuk alroji, kalkulator dan alat elektronik. Reaksi yang terjadi : Anoda : Zn(s) + 2 OH (l) Zn(OH)2(s) + 2 e Katoda : Ag 2 O(s) + H 2 O(l) + 2 e 2 Ag(s) + 2 OH (aq) Reaksi Sel : Zn(s) + Ag 2 O(s) + H 2 O(l) Zn(OH)2(s) + 2 Ag(s) Potensial sel yang dihasilkan adalah 1, 34 V


4. Sel Nikel Cadmium (Nikad) Sel Nicad merupakan sel kering yang dapat diisi kembali (rechargable). Anodenya terbuat dari Cd dan katodenya berupa Ni 2 O 3 (pasta). Beda potensial yang dihasilkan sebesar 1, 29 V. Reaksinya dapat balik : Ni. O(OH). x. H 2 O + Cd + 2 H 2 O 2 Ni(OH)2. y. H 2 O + Cd(OH)2

5. Sel Bahan Bakar Sel Bahan bakar merupakan sel Galvani dengan pereaksi – pereaksinya (oksigen dan hidrogen) dialirkan secara kontinyu ke dalam elektrode berpori. Sel ini terdiri atas anode dari nikel, katode dari nikel oksida dan elektrolit KOH. Reaksi yang terjadi : Anode : 2 H 2(g) + 4 OH-(aq) Katode : O 2(g) + 2 H 2 O(l) + 4 e Reaksi sel : 2 H 2(g) + O 2 4 H 2 O(l) + 4 e 4 OH-(aq) 2 H 2 O(l)

B. Elektrolisis Penguraian zat-zat kimia oleh arus listrik searah. Pada peristiwa ini terjadi perubahan energi listrik menjadi energi kimia.

Contoh: 1. Elektrolisis lelehan Ag 2 O dengan elektroda Pt Jawab: Ag 2 O(l) 2 Ag+ + O 2– Katoda(–) : Ag+ + e Ag(s) Anoda (+) : 2 O 2– O 2(g) + 4 e 2 Ag 2 O(l) )x 2 )x 4 )x 1 4 Ag(s) + O 2(g)

Bentuk larutan dengan elektroda inert Kation 1. Jika golongan utama, yang direduksi H 2 O 2. Jika golongan transisi, yang direduksi kation tersebut

Anion 1. Jika mengandung atom O, yang dioksidasi H 2 O 2. Jika tidak mengandung atom O, yang dioksidasi anion tersebut

Contoh: Reaksi elektrolisis Ni. SO 4 dengan elektroda karbon Katoda (-): Ni 2+ + 2 e Ni(s) )x 2 Anion (+): 2 H 2 O O 2(g) + 4 H+ + 4 e )x 1 2 Ni 2+ + 2 H 2 O 2 Ni(s) + O 2(g) + 4 H+

• Karena Eooks Cl /Cl 2 > Eo oks H 2 O/O 2, di anoda terjadi oksidasi Cl menjadi Cl 2 • Karena Eored H 2 O/H 2 > Eored Na+/Na, di katoda terjadi reduksi H 2 O menjadi H 2 Na. Cl(aq) Na+ (aq) + Cl (aq) Reaksi yang terjadi dalam sel tersebut adalah: anoda : 2 Cl Cl 2 + 2 e katoda : 2 H 2 O + 2 e H 2 + 2 OH 2 H 2 O + 2 Cl Cl 2 + H 2 + 2 OH anoda katoda Na(aq) + 2 OH (aq) Na. OH(aq)

Ex : Tuliskan rekasi elektrolisis jika digunkan elektroda inert ( C, Pt ) : 1. larutan Na 2 SO 4 2. lelehan Na. Cl 3. Larutan KI 4. larutan Cu. SO 4 Jika elektrodanya tidak inert ( mudah bereaksi maka anodanya aklan larut ( bereaksi ) 5. Tuliskan reaksi elektrolisis larutan Cu. SO 4 dengan elekltroda Cu 38

Elektrolisis Larutan KI dengan elektroda C KCl(aq) K+ (aq) + I (aq) Reaksi yang terjadi dalam sel tersebut adalah: anoda : 2 I I 2 + 2 e katoda : 2 H 2 O + 2 e H 2 + 2 OH 2 H 2 O + 2 Cl Cl 2 + H 2 + 2 OH anoda katoda K+ (aq) + OH KOH (Aq)

Elektrolisis lelehan Na. Cl dengan elektrotrode Pt anoda : 2 Cl (aq) Cl 2(aq) + 2 e Katode : Na+(aq) + e Na(l) x 2 ________________ reaksi sel : 2 Na+(aq) + 2 Cl (aq) 2 Na(l) + Cl 2(g)

Bentuk larutan dengan elektroda aktif Kation a. Jika golongan utama, yang direduksi H 2 O b. Jika golongan transisi, yang direduksi kation tersebut Anion elektroda tersebut yang dioksidasi

Contoh: Reaksi elektrolisis Ni. SO 4 dengan elektroda perak Katoda(–) : Ni 2+ + 2 e Ni(s) )x 1 Anoda(+) : Ag(s) Ag+ + e )x 2 Ni 2+ + 2 Ag(s) Ni(s) + 2 Ag+

Elektrolisis Larutan Cu. SO 4 dengan anoda Mg dan katoda C Cu. SO 4(aq) Cu 2+ (aq) + SO 42 (aq) Reaksi yang terjadi dalam sel tersebut adalah: anoda : Mg(s) Mg 2+ + 2 e katoda : Cu 2+ + 2 e Cu(s) Mg(s) + Cu 2+ (aq) Cu(s) + Mg 2+ (aq) + SO 42 (aq) Mg. SO 4 (Aq)

(a) A silver-plated teapot. (b) Schematic of the electroplating of a spoon. Houghton Mifflin Company and G. Hall. All rights reserved. 44

Latihan elektrolisis Tuliskan reaksi elektrolisis berikut dengan elektroda karbon/Pt 1. Tuliskan rekasi elektrolisis larutan : • Na 2 SO 4 • Cu(NO 3)2 • Na. Cl 2. Tuliskan elektrolisis leburan Na. Cl 3. Tuliskan elektrolisis larutan KI

Faktor-faktor yang menyebabkan terjadinya korosi: 1. Udara 2. H 2 O 3. Asam kuat seperti H 2 SO 4, HCl & HNO 3 Cara mencegah terjadinya korosi: 1. Proses pelapisan dengan pengecatan ataupun penyepuhan. 2. Proteksi katodik
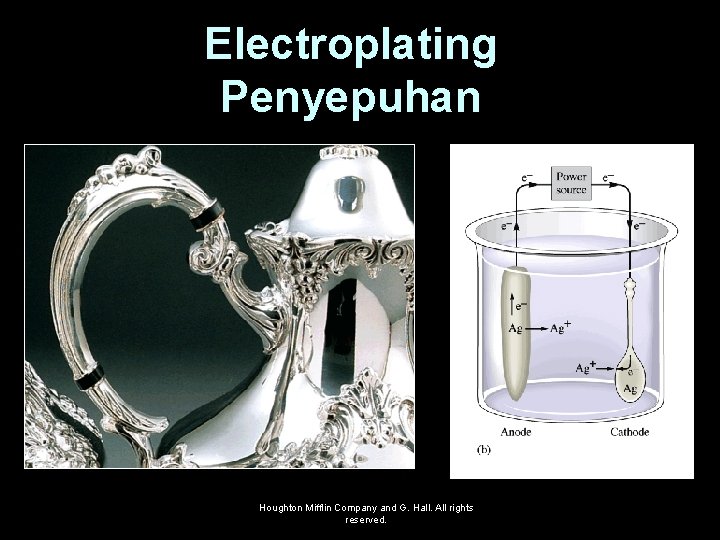
Electroplating Penyepuhan Houghton Mifflin Company and G. Hall. All rights reserved.


KETERANGAN G = massa ekuivalen i = kuat arus ( Ampere) t = waktu (detik) F = mol elektron 1 mol e 1 F 96500 C (Coulomb)

Hukum Faraday II G 1 = massa zat 1 G 2 = massa zat 2 e 1 = massa ekuivalen 1 e 2 = massa ekuivalen 2

G 1 = massa zat 1 G 2 = massa zat 2 e 1 = massa ekuivalen 1 e 2 = massa ekuivalen 2

Contoh 1 : Arus listrik sebesar 5 ampere dialirkan ke dalam 1 liter larutan Cu. SO 4 selama 10 menit dengan elektroda karbon 1. Berapa gram logam Cu yang dapat dihasilkan ? (Ar Cu = 63, 5) 0, 98 2. Hitung volume gas yang terjadi di anoda pad STP ( Ar O = 16 ) 3. Hitung p. H larutan yang terjadi jika volumenya 1 liter (volume dianggap tetap) 4. Jika arus tersebut dialirkan ke larutan Ag. NO 3 berapa Ag yang mengendap ?

Contoh 2 • Suatu arus listrik dialirkan melalui larutan Cu 2+ menghasilkan endapan 15, 9 gram logam Cu. (Ar Cu=63, 5, Ag=108 ). Dengan jumlah listrik yang sama, berapa massa Ag yang dapat dihasilkan dari larutan Ag+ ?

Contoh 3 • Larutan Cu. Cl 2(Ar Cu=63, 5) dielektrolisis menggunakan elektroda C dengan arus sebesar 5 ampere selama 1 jam. Berapa masa Logam Cu yang diendapkan di katode. Berapa volume gas klorin yang dihasilkan pada STP ( Ar Cl = 35, 5 )

Contoh 4 • Pada elektrolisis Cu. SO 4 yang menggunakan elektroda platina terbentuk endapan logam Cu sebanyak 3, 175 gram pada katode. Jika di ukur pada keadaan dimana 5 dm 3 gas N 2 massanya 7 gram berapakah volume oksigen yang terjadi ? ( Ar Cu = 63, 5, O = 16, N =

A. 0, 5 dm 3 B. 0, 56 dm 3 C. 1, 00 dm 3 D. 1, 12 dm 3 E. 2, 00 dm 3

Jawab: Cu. SO 4 Cu 2+ + SO 42– Cu 2+ + 2 e Cu Val. (PBO) = Cu = 2 t = 2 jam 3600 detik/jam = 7200 detik I = 5 Ampere Ar = 63, 5 gram/mol G = 11, 84 gram

Jawab: 2 H 2 O 4 H+ + O 2 + 4 e Val. (PBO) = O 2 = 4 t = 2 jam 3600 detik/jam = 7200 detik I = 5 Ampere Ar = 63, 5 gram/mol G = 2. 98445 gram

Hukum Faraday II G 1 = massa zat 1 G 2 = massa zat 2 e 1 = massa ekuivalen 1 e 2 = massa ekuivalen 2

Contoh: Ke dalam 2 sel larutan Ag. NO 3 dan larutan Cu. SO 4 yang disusun secara seri dialirkan arus listrik. Ternyata diendapkan 5, 4 gram logam Ag. Tentukan jumlah logam Cu yang diendapkan! (Ar: Ag = 108, Cu = 63, 5)

Jawab: Ag. NO 3 Ag+ + NO 3– valensi Ag = 1 Cu. SO 4 Cu 2+ +SO 42– valensi Cu = 2

Pertanyaan 1. Reaksi : 4 Na + O 2 2 Na 2 O Zat yang mengalami oksidasi adalah. . . a. Na b. O 2 c. Na 2 O

2. Reaksi yang terjadi pada katode dalam elektrolisis adalah … a. Reduksi b. Oksidasi c. Redoks
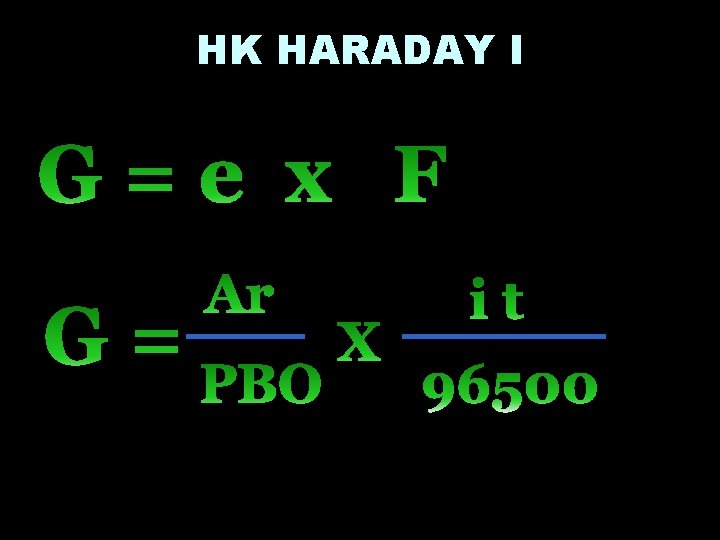
HK HARADAY I
- Slides: 64