Sel Elektrolisis KIMIA KELAS XII PERTEMUAN 8 Ajang




- Slides: 6

Sel Elektrolisis KIMIA KELAS XII PERTEMUAN 8 Ajang Desi Kurniawan ST. SMA AL ISLAM BOARDING SCHOOL

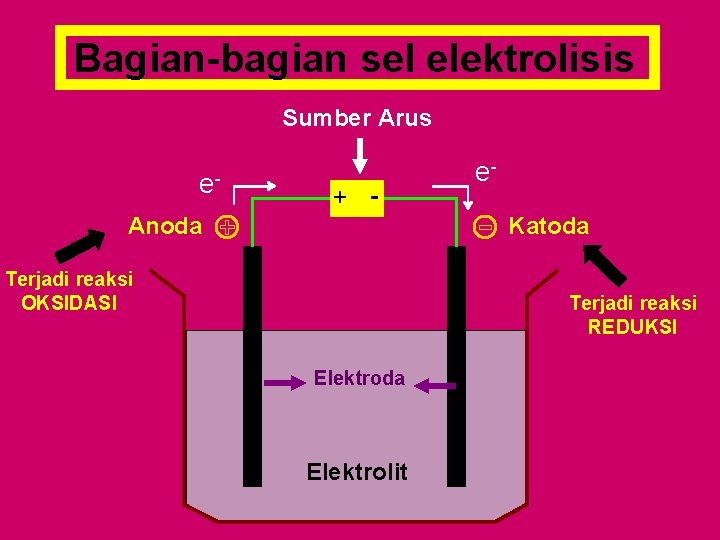
Bagian-bagian sel elektrolisis Sumber Arus e- + - Anoda e. Katoda Terjadi reaksi OKSIDASI Terjadi reaksi REDUKSI Elektroda Elektrolit

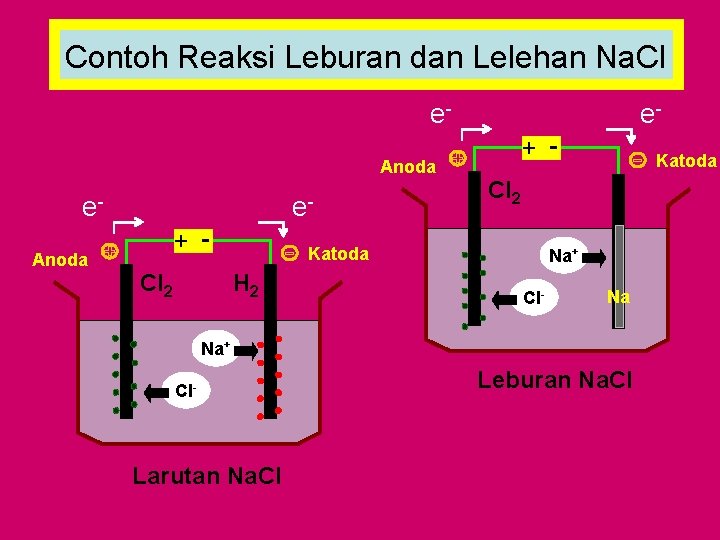
Contoh Reaksi Leburan dan Lelehan Na. Cl e. Anoda e+ - Cl 2 Katoda H 2 Katoda Na+ Cl- Na Na+ Cl- Larutan Na. Cl Leburan Na. Cl

Reaksi elektrolisis larutan Reaksi Reduksi di Katode Deret volta: Li-K-Ba-Na-Mg-Al-Mn-Zn-Cr-Fe-Cd-Co-Ni-Sn-Pb-(H)-Sb-Bi-Cu-Hg-Ag-Pt. Au • Ion positif dari logam-logam di sebelah kanan hidrogen pada deret volta akan tereduksi dan mengendap pada katode. • Ion positif dari logam-logam di sebelah kiri hidrogen pada deret volta tidak akan tereduksi (kecuali Fe, Ni, Sn, dan Pb). Hal ini disebabkan karena ion H+ dari H 2 O lebih mudah tereduksi: 2 H 2 O (l)+ 2 e. H 2 (g) + 2 OH-(aq) • Jika larutan elektrolit berupa asam, maka ion H+ dari asam akan tereduksi, bukan ion H+ dari H 2 O. 2 H+ (aq)+ 2 e. H 2 (g)

Reaksi Reduksi di Anoda • Jika anode tidak inert seperti Cu, maka logam anode akan teroksidasi. • Jika anode inert (Pt, Au, C), maka ion negatif yang tidak mengandung oksigen seperti Cl-, Br-, dan I- akan teroksidasi. 2 Cl-(aq) Cl 2(g) + 2 edan Ion negatif yang mengandung oksigen seperti SO 42 -, NO 3 -, dan PO 43 - tidak akan teroksidasi. Tetapi yang teroksidasi adalah ion O 2 - dari H 2 O. 2 H 2 O (l) O 2(g) + 4 H+ (aq) + 4 e-

Reaksi elektrolisis leburan Elektrolisis leburan melibatkan raksi redoks sederhana karena berlangsung tanpa air. Beberapa logam seperti Na, Mg, Ca, dan Al diperoleh dari elektrolit lelehan senyawa logamnya menggunakan sel ini. Ion-ion logam tersebut akan tereduksi menghasilkan logam-logam tersebut.