Elektrolisis Edi Nasra S Si M Si Sel








- Slides: 14

Elektrolisis Edi Nasra, S. Si. , M. Si

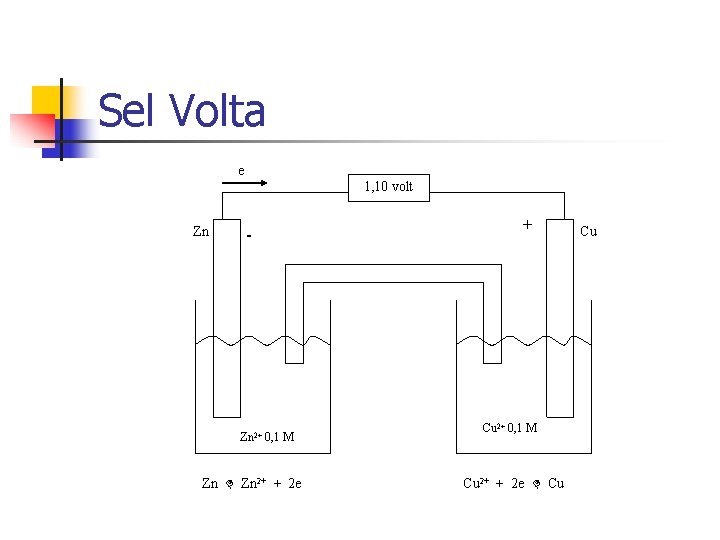
Sel Volta e 1, 10 volt Zn - Zn 2+ 0, 1 M Zn 2+ + 2 e + Cu 2+ 0, 1 M Cu 2+ + 2 e Cu Cu

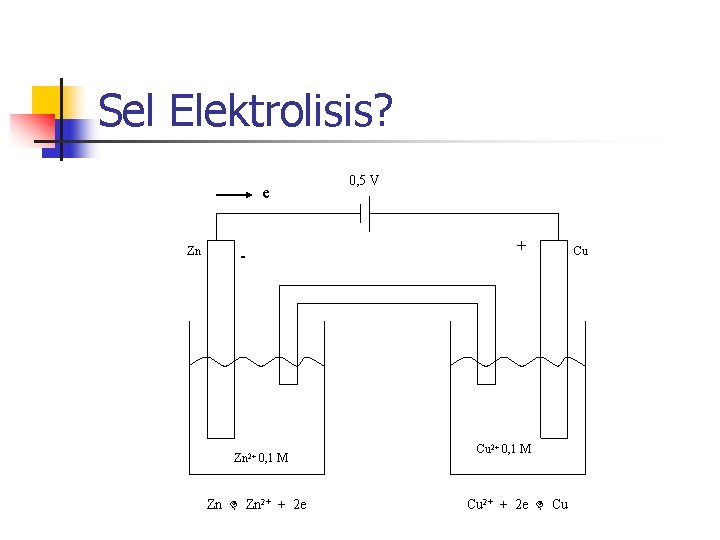
Sel Elektrolisis? e Zn - Zn 2+ 0, 1 M Zn 2+ + 2 e 0, 5 V + Cu 2+ 0, 1 M Cu 2+ + 2 e Cu Cu

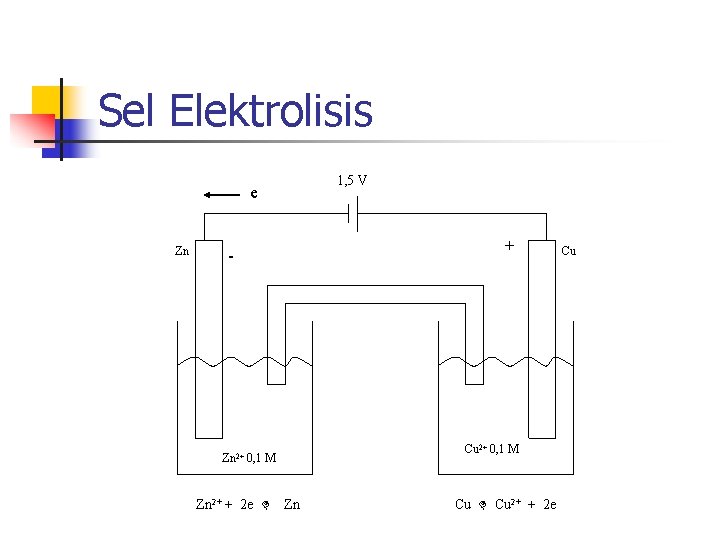
Sel Elektrolisis 1, 5 V e Zn + - Cu 2+ 0, 1 M Zn 2+ + 2 e Zn Cu 2+ + 2 e Cu

Potensial Elektrolisis Wapp = Ea – Ek + i. R Wapp = potensial elektrolisis Ea = potensial anoda Ek = potensial katoda I = arus R = hambatan sel

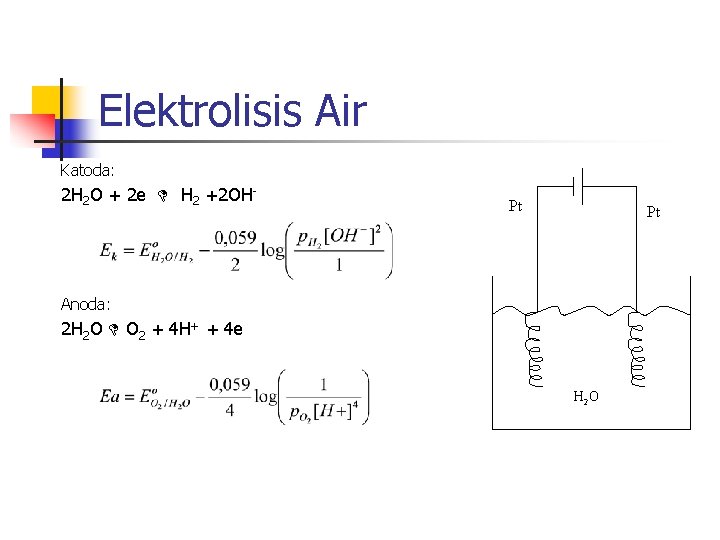
Elektrolisis Air Katoda: 2 H 2 O + 2 e H 2 +2 OH- Pt Pt Anoda: 2 H 2 O O 2 + 4 H+ + 4 e H 2 O

Potensial elektroda Katoda: Anoda:

Potensial lebih pembentukan gas n n n Gas H 2 dan O 2 sebelumnya tidak ada dalam larutan Diperlukan energi lebih untuk menghasilkan gas Pada katoda diperlukan energi ekstra untuk membentuk gas H 2, sehingga reaksi terjadi pada potensial yang lebih negatif dari – 0, 417 V (Ek - k) Pada anoda diperlukan energi ekstra untuk membentuk gas O 2, sehingga reaksi terjadi pada potensial yang lebih positif dari 0, 817 V (Ea + a) Eapp = (Ea + a) - (Ek - k) + i. R Eapp = Ea – Ek + a + i. R

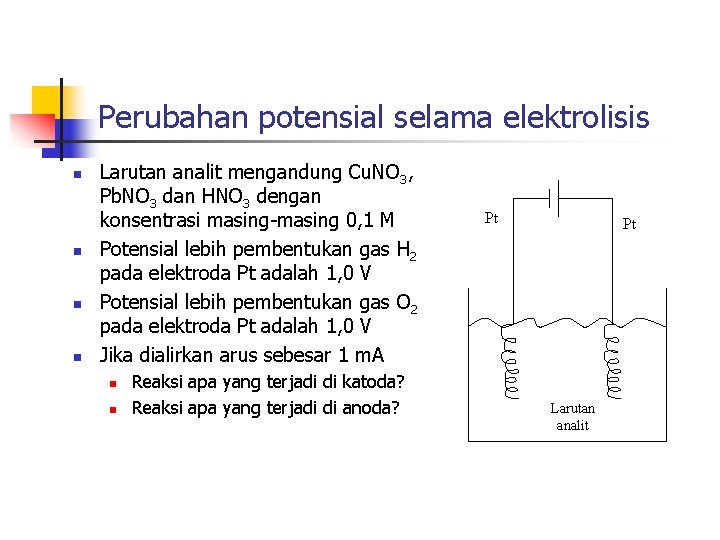
Perubahan potensial selama elektrolisis n n Larutan analit mengandung Cu. NO 3, Pb. NO 3 dan HNO 3 dengan konsentrasi masing-masing 0, 1 M Potensial lebih pembentukan gas H 2 pada elektroda Pt adalah 1, 0 V Potensial lebih pembentukan gas O 2 pada elektroda Pt adalah 1, 0 V Jika dialirkan arus sebesar 1 m. A n n Reaksi apa yang terjadi di katoda? Reaksi apa yang terjadi di anoda? Pt Pt Larutan analit

Reaksi yang mungkin? Katoda: Cu 2+ + 2 e Cu Pb 2+ + 2 e Pb 2 H+ + 2 e H 2 2 H 2 O + 2 e H 2 + 2 OHAnoda: 2 H 2 O O 2 + 4 H+ + 4 e

Potensial reduksi

Reaksi pada elektroda Urutan reaksi pada katoda: n Reduksi Cu 2+ (Ek =0, 308 V) n Reduksi Pb 2+ (Ek =-0, 155 V) n Reduksi H+ (Ek =-0, 059 -1, 000=-1, 059 V) n Reduksi H 2 O (Ek =-0, 063 -1, 000=-1, 063 V) Reaksi pada anoda: Oksidasi H 2 O

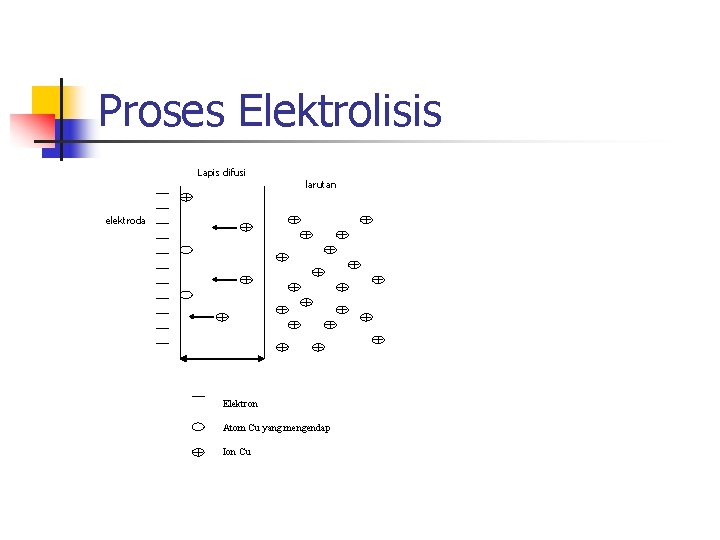
Proses Elektrolisis Lapis difusi larutan elektroda Elektron Atom Cu yang mengendap Ion Cu

Pemisahan secara elektrolisis Berapa potensial katoda pada saat 99, 99 %Cu 2+ telah mengendap? Konsentrasi Cu 2+ yang tersisa dalam larutan 0, 01% x 0, 1 M = 10 -5 M