DISOLUCIONES QUMICAS Objetivo Sintetizar contenidos sobre disoluciones qumicas

DISOLUCIONES QUÍMICAS

Objetivo • Sintetizar contenidos sobre disoluciones químicas.
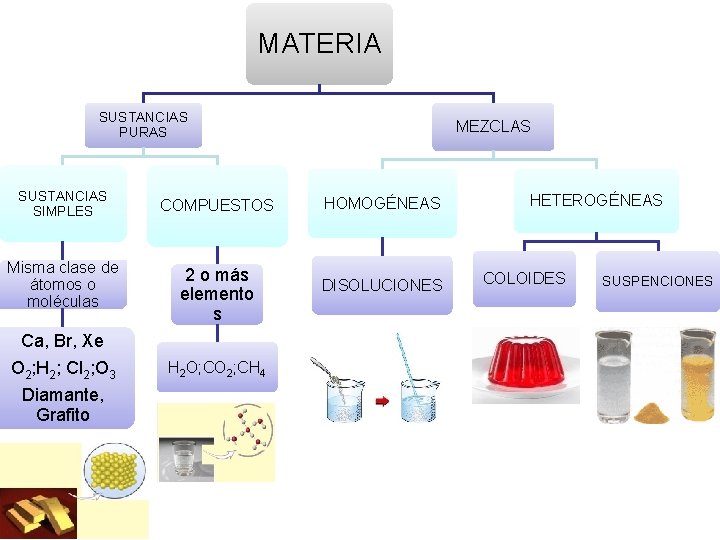
MATERIA SUSTANCIAS PURAS SUSTANCIAS SIMPLES Misma clase de átomos o moléculas COMPUESTOS 2 o más elemento s Ca, Br, Xe O 2; H 2; Cl 2; O 3 Diamante, Grafito H 2 O; CO 2; CH 4 MEZCLAS HOMOGÉNEAS DISOLUCIONES HETEROGÉNEAS COLOIDES SUSPENCIONES

DISOLUCIÓN • Es una mezcla homogénea de dos o mas sustancias químicas tal que el tamaño molecular de la partículas sea inferior a 10 --9 m. • Se llama mezcla coloidal cuando el tamaño de partícula va de 10 -9 m a 2 · 10 -7 m. • Se llama suspensión cuando el tamaño de las partículas es del orden de 2 · 10 -7 m. 4

COMPONENTES DE UNA DISOLUCION SOLUTO: Es la sustancia que se encuentra en menor cantidad y por lo tanto, se disuelve SOLVENTE O DISOLVENTE: Es la sustancia que se encuentra en mayor cantidad y por lo tanto, disuelve

EL AGUA COMO DISOLVENTE El agua es el disolvente más universal, es decir, el líquido que más sustancias disuelve y ello hace que sea una de las sustancias más importantes en el ámbito de las disoluciones. üSoluto polar: Si se disuelve en agua. üSoluto no polar: Solo algunos se disuelve en agua
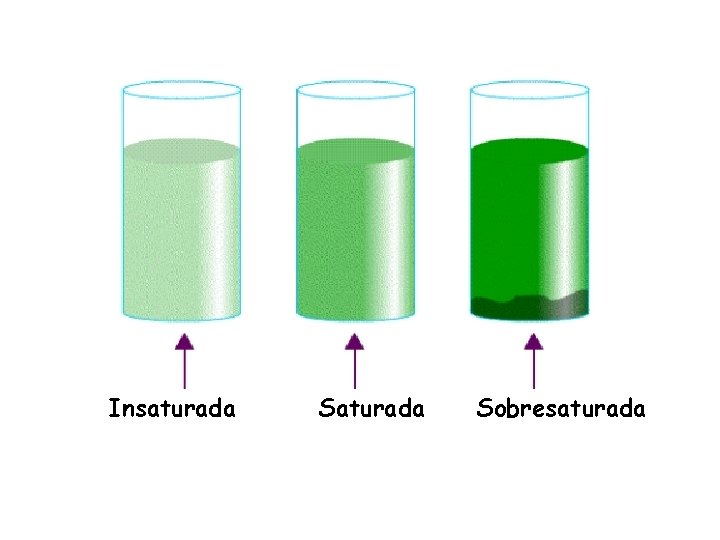
Insaturada Sobresaturada
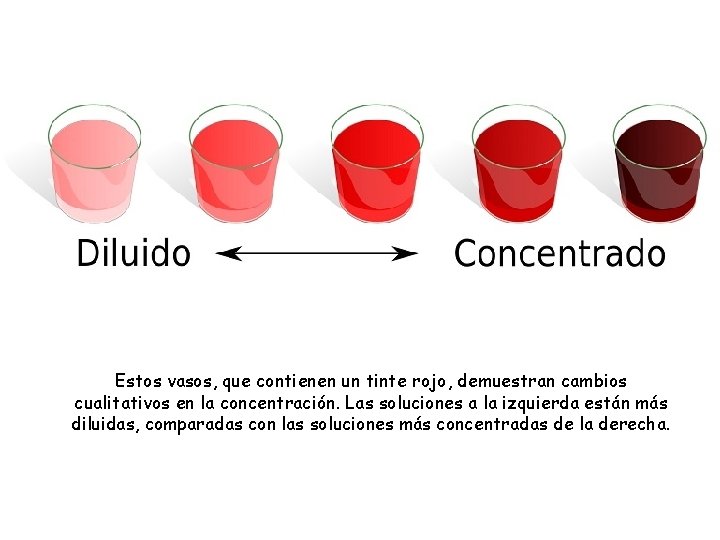
Estos vasos, que contienen un tinte rojo, demuestran cambios cualitativos en la concentración. Las soluciones a la izquierda están más diluidas, comparadas con las soluciones más concentradas de la derecha.

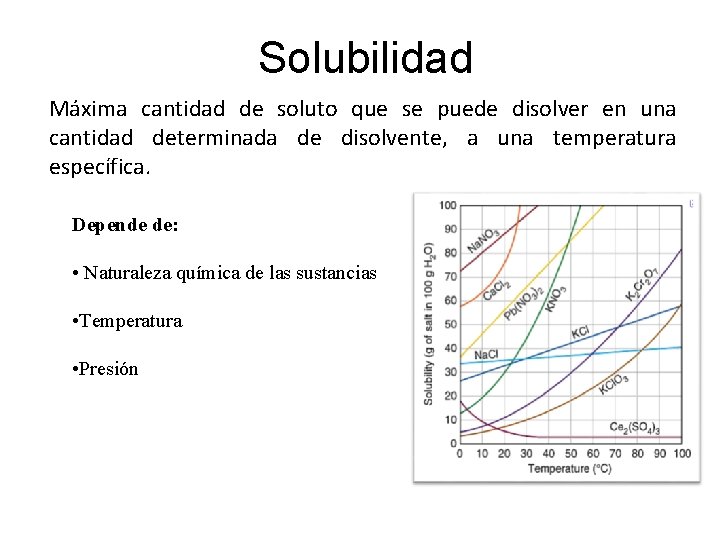
Solubilidad Máxima cantidad de soluto que se puede disolver en una cantidad determinada de disolvente, a una temperatura específica. Depende de: • Naturaleza química de las sustancias • Temperatura • Presión
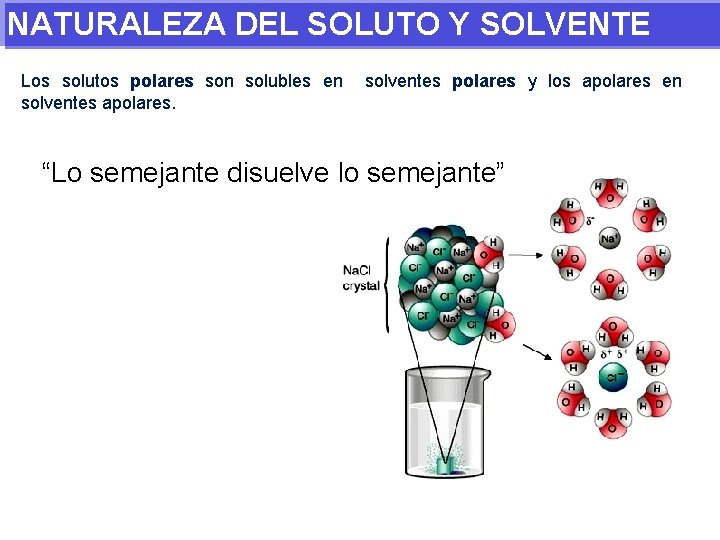
NATURALEZA DEL SOLUTO Y SOLVENTE Los solutos polares son solubles en solventes apolares. solventes polares y los apolares en “Lo semejante disuelve lo semejante”

EFECTO DE LA TEMPERATURA La mayoría de los sólidos aumentan su solubilidad al aumentar la temperatura para procesos endotérmico, es decir, cuando se absorbe calor del medio. En caso contrario, cuando el proceso es exotérmico un aumento de temperatura disminuye la solubilidad, como sucede con la mayoría de los solutos gaseosos en agua.
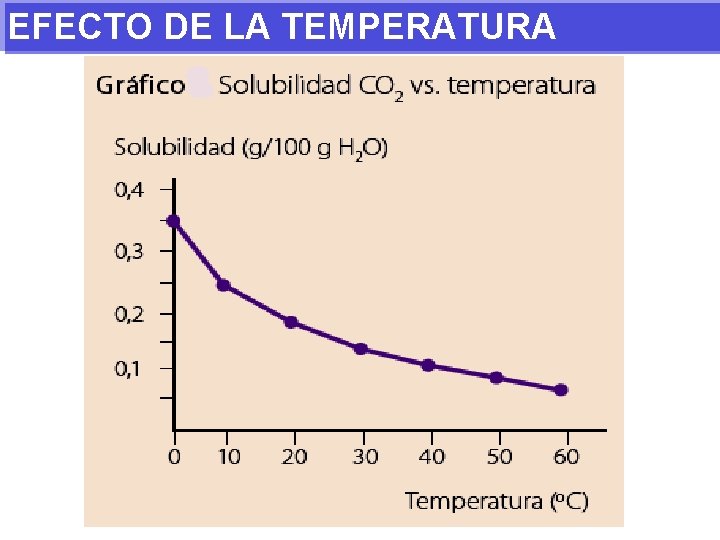
EFECTO DE LA TEMPERATURA
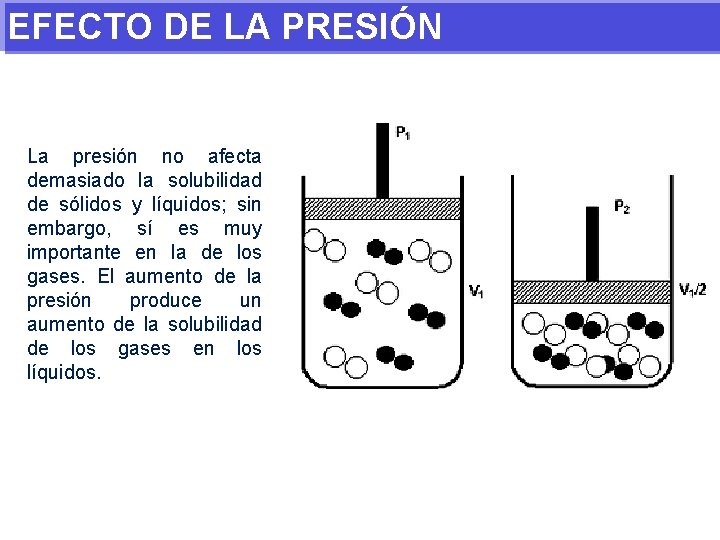
EFECTO DE LA PRESIÓN La presión no afecta demasiado la solubilidad de sólidos y líquidos; sin embargo, sí es muy importante en la de los gases. El aumento de la presión produce un aumento de la solubilidad de los gases en los líquidos.
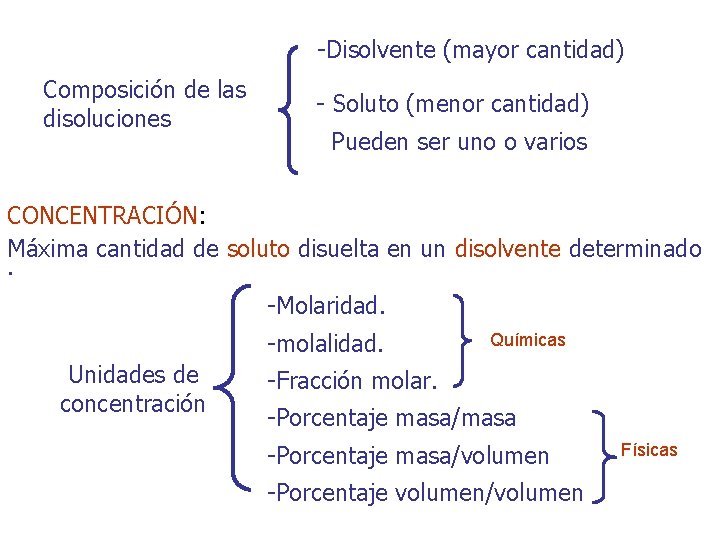
-Disolvente (mayor cantidad) Composición de las disoluciones - Soluto (menor cantidad) Pueden ser uno o varios CONCENTRACIÓN: Máxima cantidad de soluto disuelta en un disolvente determinado. -Molaridad. -molalidad. Unidades de concentración Químicas -Fracción molar. -Porcentaje masa/masa -Porcentaje masa/volumen -Porcentaje volumen/volumen Físicas

Porcentaje en masa (%m/m) Es la unidad de concentración de la medida de la cantidad de masa de soluto con la medida de la cantidad de masa de disolución acuosa. Se representa por el símbolo % m/m y se define como gramos de soluto disueltos en 100 gramos de disolución acuosa, según la siguiente expresión: ¿Qué significa que una solución de nitrato de sodio (Na. NO 3) tenga una concentración de 3% m/m? R: Significa que 3 g del soluto nitrato de sodio están

Porcentaje masa en volumen (%m/v) Indica la masa de soluto en gramos disuelto en 100 m. L de solución. Xg soluto → 100 m. L solución Una solución salina contiene 30 g de Na. Cl en 80 m. L de solución. Calcular su concentración en % p/v. 30 g Na. Cl → 80 m. L solución Xg Na. Cl → 100 m. L solución X = 30 * 100 =

Porcentaje en volumen (% v/v) Indica el volumen de soluto, en m. L, presente en 100 m. L de solución. X m. L soluto → 100 m. L solución Calcular la concentración en volumen de una solución alcohólica, que contiene 15 m. L de alcohol disueltos en 65 m. L de solución. → 65 m. L 15 m. L solución alcohol X m. L alcohol → = 100 m. L X = 15 * 100 23 65 solución%v/v

Unidades químicas Molaridad (M): Es la unidad de concentración química que relaciona la medida de la cantidad de masa de soluto con la medida del volumen de disolución acuosa. Se representa por M y se define como la cantidad de moles de soluto disueltos en 1 litro de disolución, según la siguiente expresión:

Molalidad (m): Es la unidad de concentración química que relaciona la medida de la cantidad de masa de soluto disueltos en la medida de un kilogramo (Kg) de disolvente, se representa por m y se define como la cantidad de moles de soluto disueltos en 1 Kg de disolvente, según la siguiente expresión: (n) soluto = cantidad de materia de soluto (mol)

Ppm (partes por millón) Se usa cuando la cantidad de soluto es muy pequeña. Indica las partes en masa de soluto disueltas en un millón de partes en masa de disolución, o bien miligramos de soluto en 1 kg de disolución o un litro de disolución. Ejemplo: Una disolución de CO 2 se prepara disolviendo 0, 0063 g de este gas en 2. 500 g de agua. Encontrar la concentración en ppm de este gas: ppm = (6, 3 mg) = 2, 5 ppm (2, 5 Kg)

Fracción molar (X): expresa el número de moles de un componente de la solución, en relación con el número total de moles, incluyendo todos los componentes presentes. Se calcula dividiendo el numero de moles de uno de los componentes por el numero total de moles de la disolución mediante la expresión: Para una solución de dos componentes, llamando n. A y n. B al número de moles de A y B, la expresión matemática es: La suma de las fracciones molares de una solución es igual a uno.
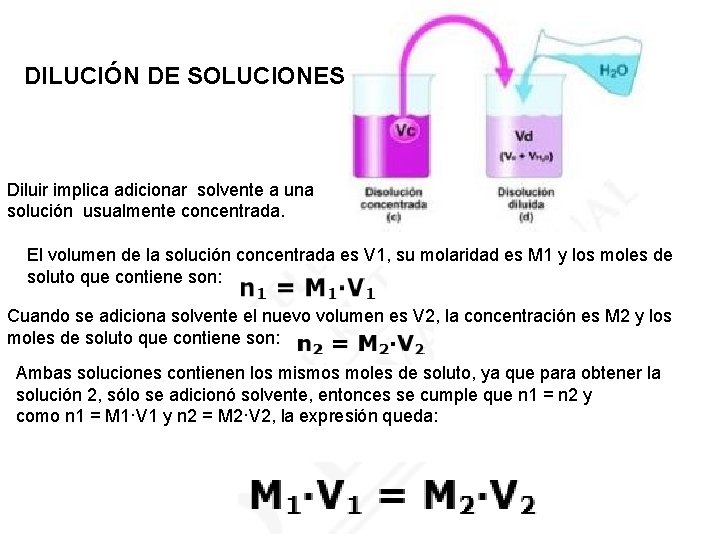
DILUCIÓN DE SOLUCIONES Diluir implica adicionar solvente a una solución usualmente concentrada. El volumen de la solución concentrada es V 1, su molaridad es M 1 y los moles de soluto que contiene son: Cuando se adiciona solvente el nuevo volumen es V 2, la concentración es M 2 y los moles de soluto que contiene son: Ambas soluciones contienen los mismos moles de soluto, ya que para obtener la solución 2, sólo se adicionó solvente, entonces se cumple que n 1 = n 2 y como n 1 = M 1·V 1 y n 2 = M 2·V 2, la expresión queda:

Si partimos de una solución inicial n 1 = M 1 x V 1, para obtener una segunda solución n 2 = M 2 x V 2, debe cumplirse que el número inicial de moles sea igual al número final de moles (n 1 = n 2 ). De ahí deducimos que M 1 x V 1= M 2 x V 2. Esta expresión es la clave para determinar el volumen final, V 2, o la concentración final, M 2, según sea el caso. Cuando la concentración de la solución se expresa como normalidad, podemos basarnos en una generalización de la expresión anterior: C 1 x V 1= C 2 x V 2 , en donde C indica la concentración de la solución.
- Slides: 24