Indicaciones Esta presentacin tiene como objetivo apoyar a

Indicaciones: Esta presentación tiene como objetivo apoyar a las guías de trabajo enviadas anteriormente. El día viernes se enviara un video a mi Instagram para apoyar esta presentación. Quédate en casa y cuídate, porque te extraño. Un abrazo

Disoluciones Químicas 1. 2. 3. 4. 5. Repaso de conceptos Tipos de mezclas químicas. Concepto de Disolución. Solubilidad. Concentración en disoluciones. *

Objetivos Identificar los tipos de mezclas y saber aplicar criterio de clasificación de ellas. Comprobar la existencia de las reacciones químicas en una disolución. Clasificar reactivos en disolvente y soluto(s) y conocer las características de cada uno. Relacionar el concepto de solubilidad a las variables temperatura, cantidad de soluto y solvente y características de estos últimos. Calcular concentraciones porcentuales en una disolución.

1. Repaso de conceptos 1. 1 El mol Aplicación: calcular la cantidad de moles de carbono en 45 gramos de carbono
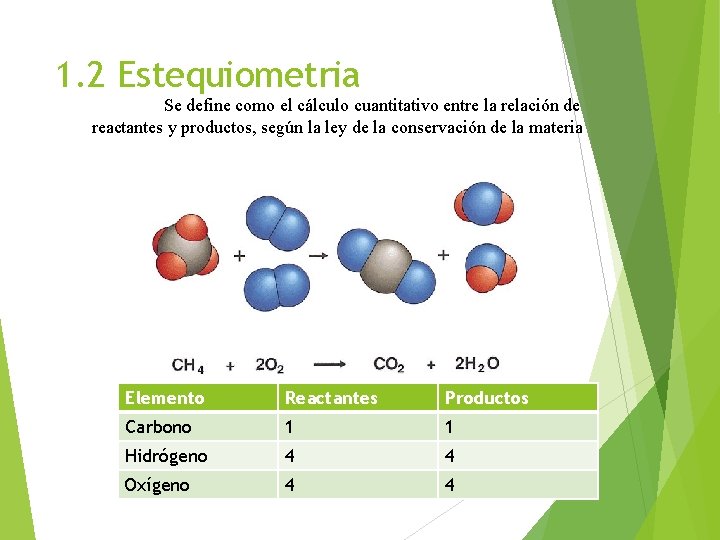
1. 2 Estequiometria Se define como el cálculo cuantitativo entre la relación de reactantes y productos, según la ley de la conservación de la materia Elemento Reactantes Productos Carbono 1 1 Hidrógeno 4 4 Oxígeno 4 4

2. Tipos de mezclas Básicamente se dividen en homogéneas y heterogéneas, según el criterio de fases en que sus componentes se encuentran (sólido, liquido o gaseoso) o la manera en la cual se mezclan.

3. Disoluciones Químicas Cuando una mezcla es homogénea totalmente a nivel molecular, nos referimos a una “disolución”. La que está compuesta por un disolvente y soluto(s). • Identifica el soluto, solvente y solución en esta imagen

3. 1 Tipos de disoluciones Estado de la disolución Estado del disolvente Estado del soluto Ejemplo Liquido Cloro doméstico Gas Bebida Sólido Leche con chocolate Líquido Neblina Gas Aire Sólido Humo Liquido Amalgamas Gas Hidrógeno en paladio Sólido Bronce Gas Sólido
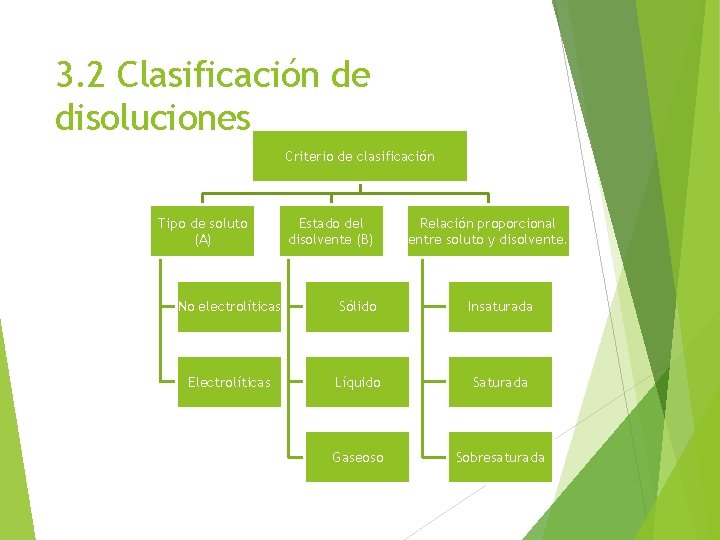
3. 2 Clasificación de disoluciones Criterio de clasificación Tipo de soluto (A) Estado del disolvente (B) Relación proporcional entre soluto y disolvente. No electrolíticas Sólido Insaturada Electrolíticas Líquido Saturada Gaseoso Sobresaturada

3. 3 Relación del soluto y solvente Insaturadas Sobresaturadas
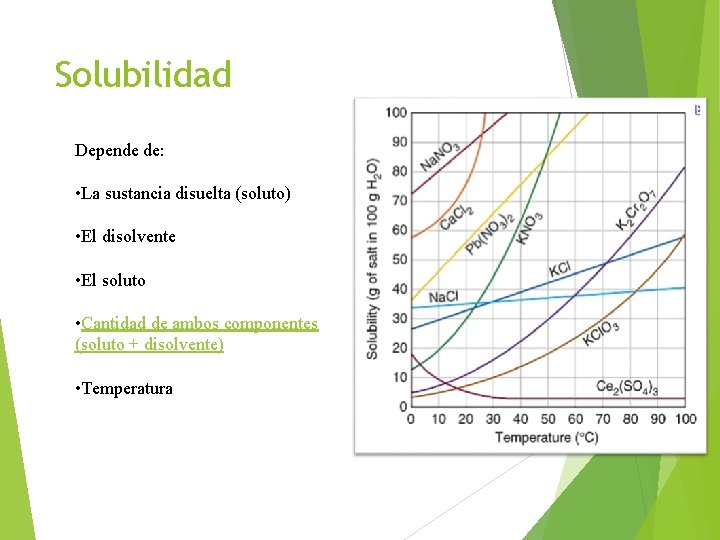
Solubilidad Depende de: • La sustancia disuelta (soluto) • El disolvente • El soluto • Cantidad de ambos componentes (soluto + disolvente) • Temperatura
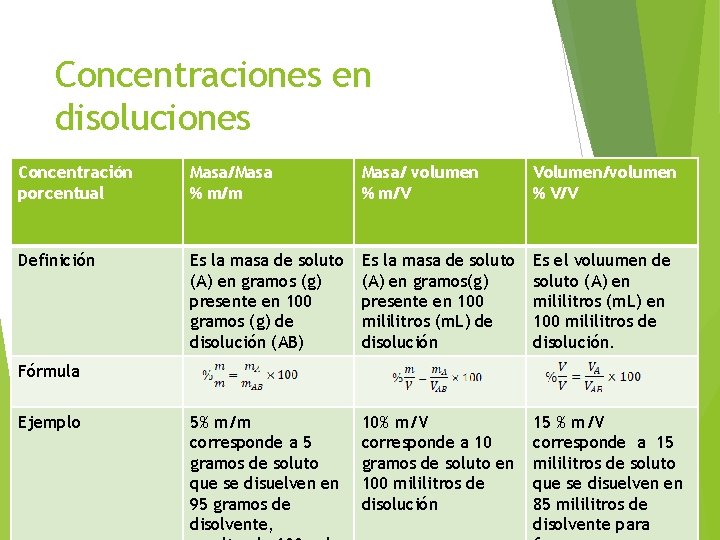
Concentraciones en disoluciones Concentración Masa/Masa Concentraciones porcentuales. porcentual % m/m Masa/ volumen % m/V Volumen/volumen % V/V Definición Es la masa de soluto (A) en gramos (g) presente en 100 gramos (g) de disolución (AB) Es la masa de soluto (A) en gramos(g) presente en 100 mililitros (m. L) de disolución Es el voluumen de soluto (A) en mililitros (m. L) en 100 mililitros de disolución. 5% m/m corresponde a 5 gramos de soluto que se disuelven en 95 gramos de disolvente, 10% m/V corresponde a 10 gramos de soluto en 100 mililitros de disolución 15 % m/V corresponde a 15 mililitros de soluto que se disuelven en 85 mililitros de disolvente para Fórmula Ejemplo
- Slides: 12