Chemie der Allene und Cumulene Ein Vortrag im



![[4+2]-Cycloaddition von Allenen 3. 5 Diels-Alder-Reaktionen von Allenen a) Reaktion konjugierten Allensysteme mit Dienophilen [4+2]-Cycloaddition von Allenen 3. 5 Diels-Alder-Reaktionen von Allenen a) Reaktion konjugierten Allensysteme mit Dienophilen](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-21.jpg)

![Literatur n n n [1] N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Literatur n n n [1] N. Krause, A. S. K. Hashmi Modern Allene Chemistry,](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-29.jpg)

![[2+2]-Cycloaddition von Allenen 3. 7 Allene als Vorstufen in der Naturstoffsynthese Periplanone B ist [2+2]-Cycloaddition von Allenen 3. 7 Allene als Vorstufen in der Naturstoffsynthese Periplanone B ist](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-33.jpg)
- Slides: 33

Chemie der Allene und Cumulene Ein Vortrag im Rahmen des organisch-chemischen Fortgeschrittenenpraktikums 1

1. Allene und Cumulene von lat. : cumulare = anhäufen. Bez. Für solche org. Verb. , bei denen sich zwei oder mehrere Doppelbindungen in ununterbrochener Folge aneinander reihen J. H. van't Hoff (1852 – 1911) 2

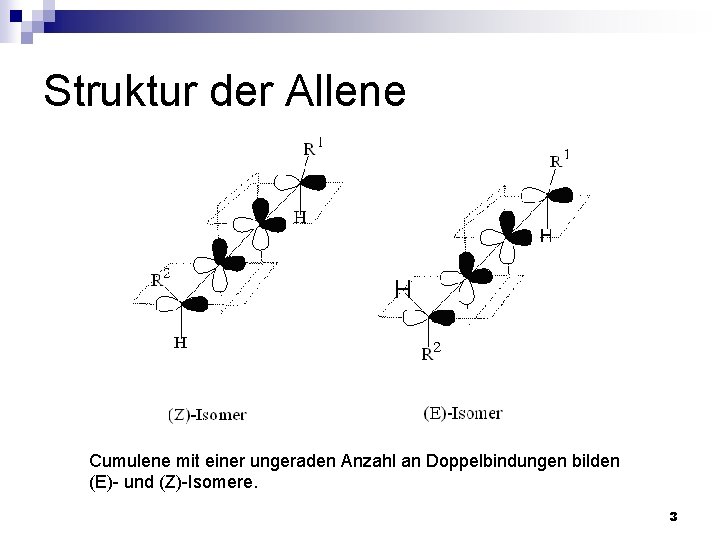
Struktur der Allene Cumulene mit einer ungeraden Anzahl an Doppelbindungen bilden (E)- und (Z)-Isomere. 3

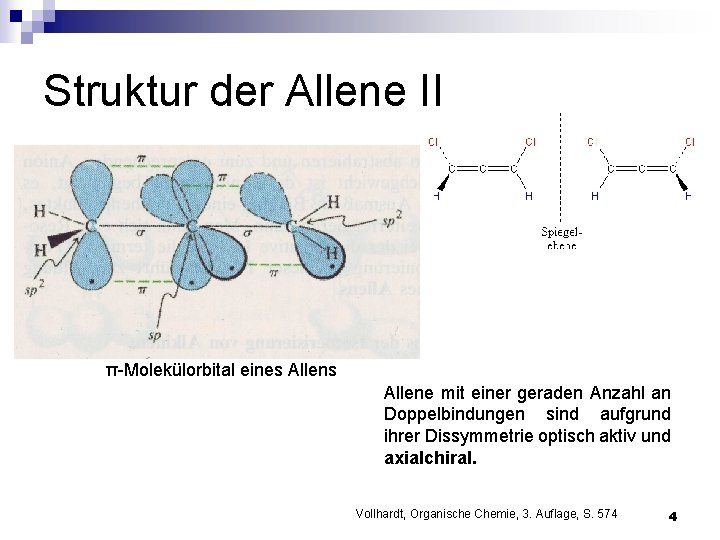
Struktur der Allene II π-Molekülorbital eines Allene mit einer geraden Anzahl an Doppelbindungen sind aufgrund ihrer Dissymmetrie optisch aktiv und axialchiral. Vollhardt, Organische Chemie, 3. Auflage, S. 574 4

Das kleinste Allen Das thermodynamisch stabile Isomer ist das Acetylen. Zur Synthese von Allenen ist eine kinetisch kontrollierte Reaktionsführung notwendig. Isomere des kleinsten Allens C 3 H 4 5

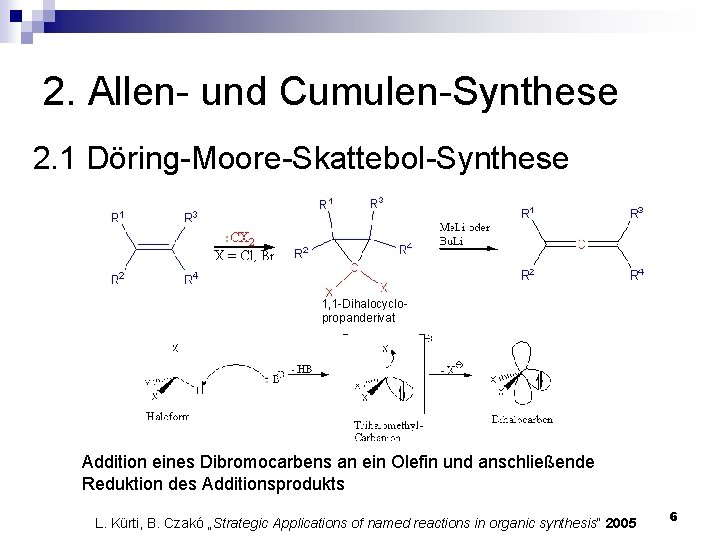
2. Allen- und Cumulen-Synthese 2. 1 Döring-Moore-Skattebol-Synthese 1, 1 -Dihalocyclopropanderivat Addition eines Dibromocarbens an ein Olefin und anschließende Reduktion des Additionsprodukts L. Kürti, B. Czakó „Strategic Applications of named reactions in organic synthesis“ 2005 6

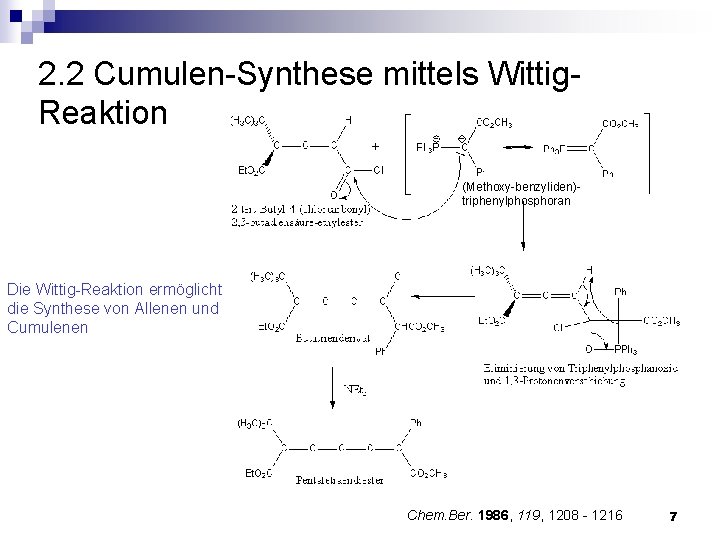
2. 2 Cumulen-Synthese mittels Wittig. Reaktion (Methoxy-benzyliden)triphenylphosphoran Die Wittig-Reaktion ermöglicht die Synthese von Allenen und Cumulenen Chem. Ber. 1986, 119, 1208 - 1216 7

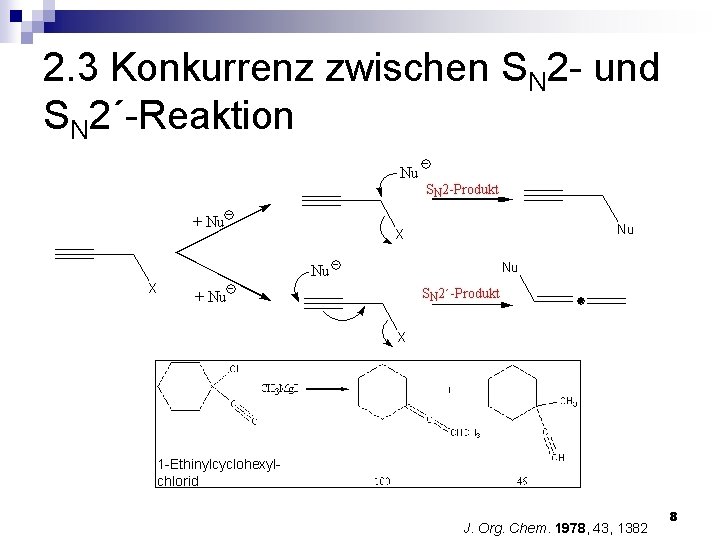
2. 3 Konkurrenz zwischen SN 2 - und SN 2´-Reaktion 1 -Ethinylcyclohexylchlorid J. Org. Chem. 1978, 43, 1382 8

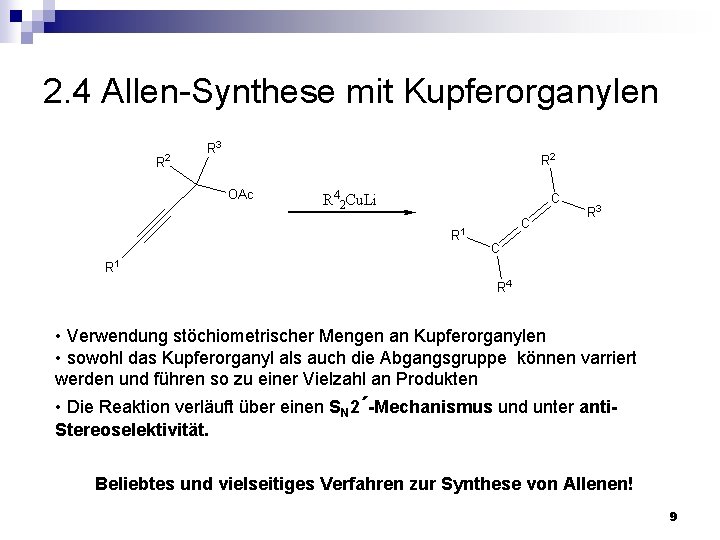
2. 4 Allen-Synthese mit Kupferorganylen • Verwendung stöchiometrischer Mengen an Kupferorganylen • sowohl das Kupferorganyl als auch die Abgangsgruppe können varriert werden und führen so zu einer Vielzahl an Produkten • Die Reaktion verläuft über einen SN 2´-Mechanismus und unter anti. Stereoselektivität. Beliebtes und vielseitiges Verfahren zur Synthese von Allenen! 9

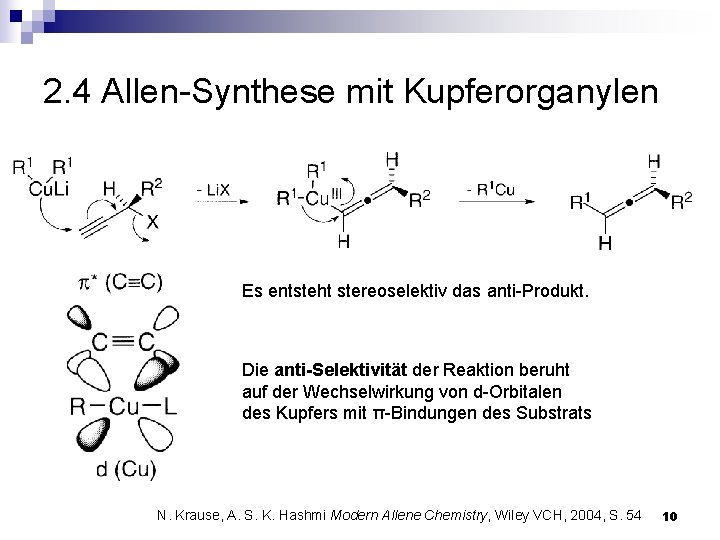
2. 4 Allen-Synthese mit Kupferorganylen Es entsteht stereoselektiv das anti-Produkt. Die anti-Selektivität der Reaktion beruht auf der Wechselwirkung von d-Orbitalen des Kupfers mit π-Bindungen des Substrats N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 54 10

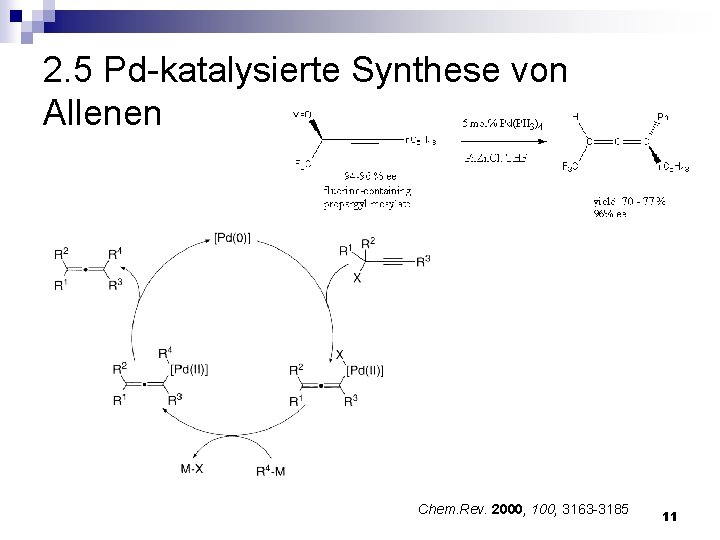
2. 5 Pd-katalysierte Synthese von Allenen Chem. Rev. 2000, 100, 3163 -3185 11

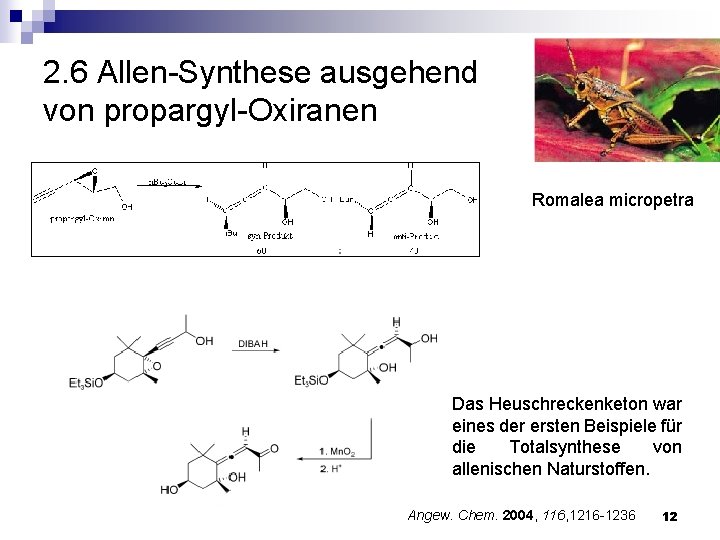
2. 6 Allen-Synthese ausgehend von propargyl-Oxiranen Romalea micropetra Das Heuschreckenketon war eines der ersten Beispiele für die Totalsynthese von allenischen Naturstoffen. Angew. Chem. 2004, 116, 1216 -1236 12

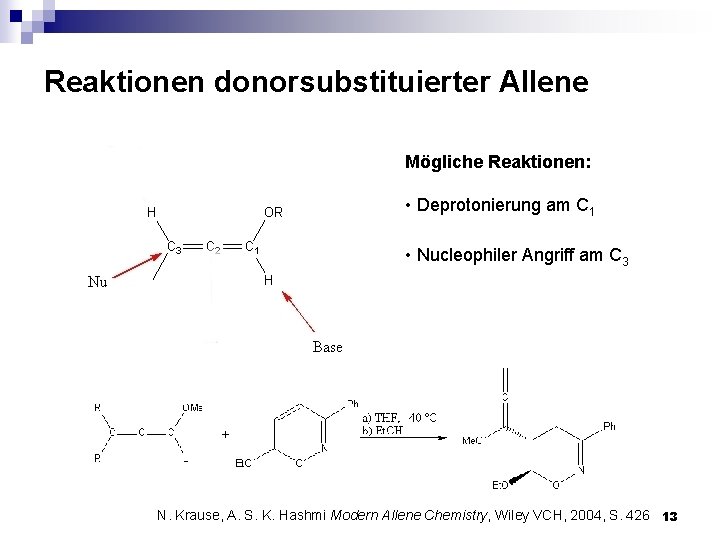
Reaktionen donorsubstituierter Allene Mögliche Reaktionen: • Deprotonierung am C 1 • Nucleophiler Angriff am C 3 N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 426 13

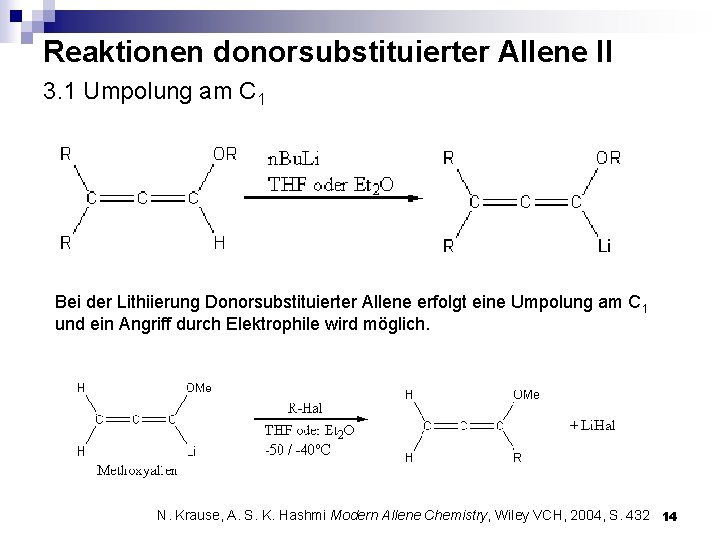
Reaktionen donorsubstituierter Allene II 3. 1 Umpolung am C 1 Bei der Lithiierung Donorsubstituierter Allene erfolgt eine Umpolung am C 1 und ein Angriff durch Elektrophile wird möglich. N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 432 14

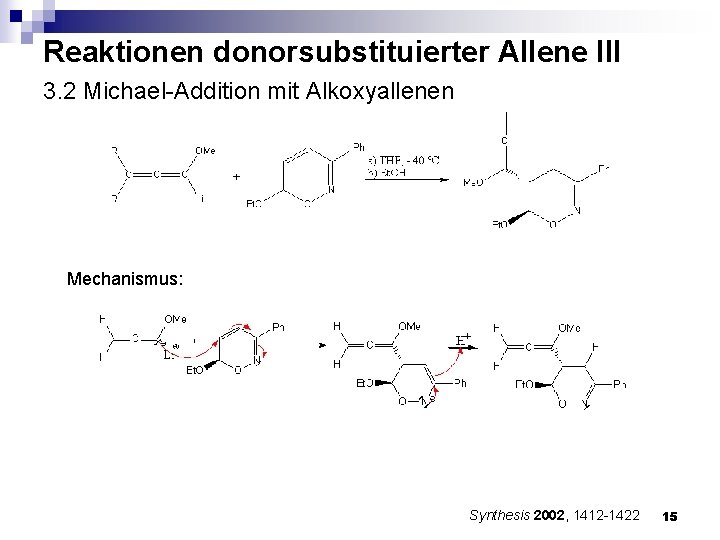
Reaktionen donorsubstituierter Allene III 3. 2 Michael-Addition mit Alkoxyallenen Mechanismus: Synthesis 2002, 1412 -1422 15

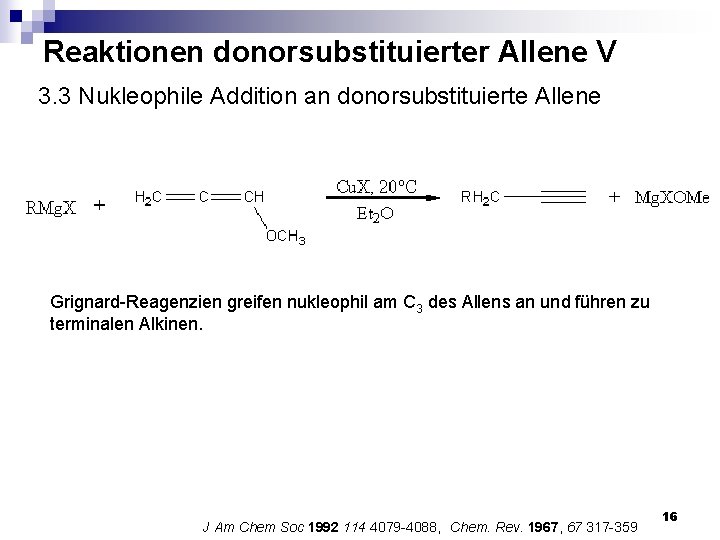
Reaktionen donorsubstituierter Allene V 3. 3 Nukleophile Addition an donorsubstituierte Allene Grignard-Reagenzien greifen nukleophil am C 3 des Allens an und führen zu terminalen Alkinen. J Am Chem Soc 1992 114 4079 -4088, Chem. Rev. 1967, 67 317 -359 16

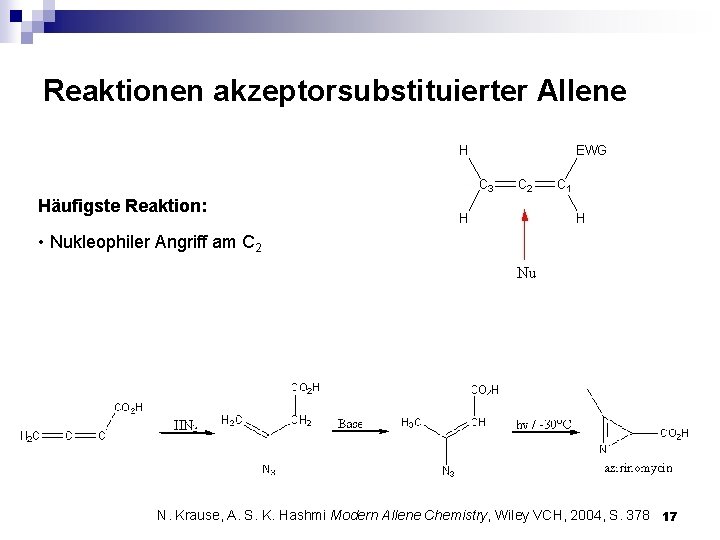
Reaktionen akzeptorsubstituierter Allene Häufigste Reaktion: • Nukleophiler Angriff am C 2 N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 378 17

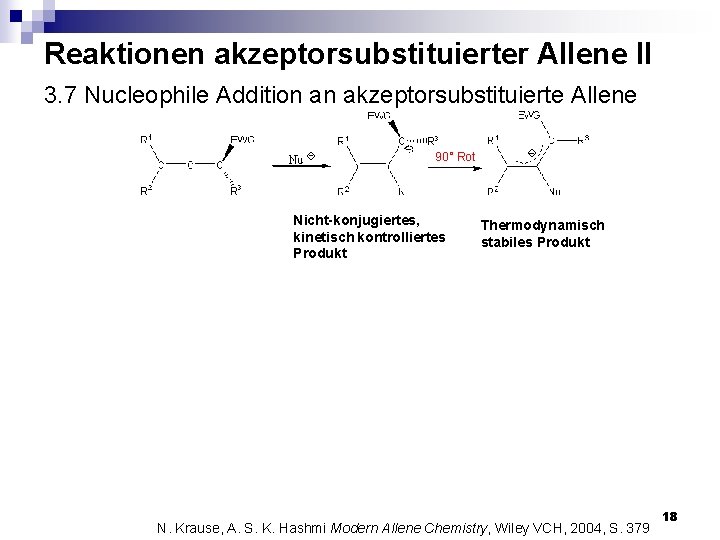
Reaktionen akzeptorsubstituierter Allene II 3. 7 Nucleophile Addition an akzeptorsubstituierte Allene 90° Rot Nicht-konjugiertes, kinetisch kontrolliertes Produkt Thermodynamisch stabiles Produkt N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 379 18

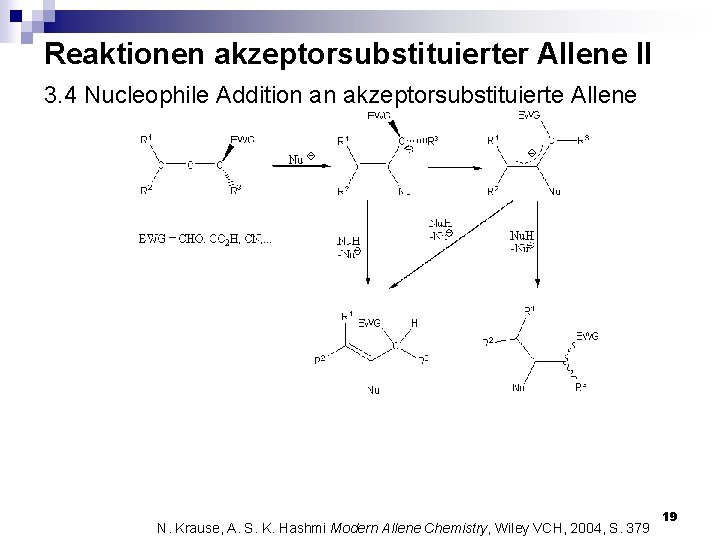
Reaktionen akzeptorsubstituierter Allene II 3. 4 Nucleophile Addition an akzeptorsubstituierte Allene N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 379 19

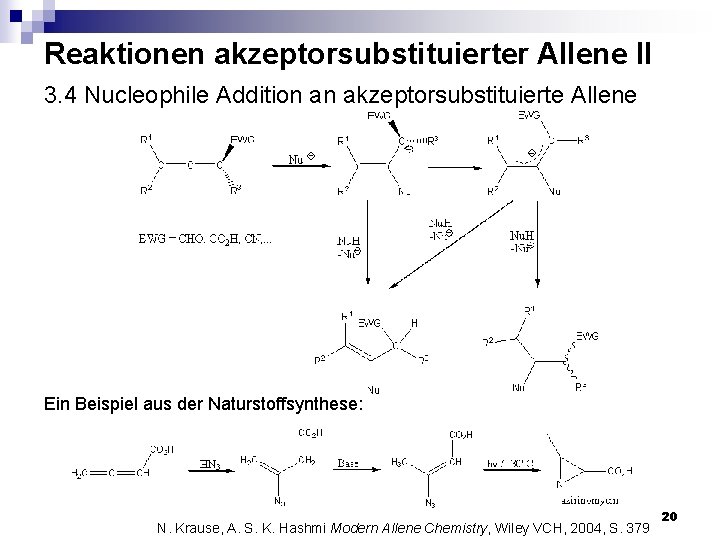
Reaktionen akzeptorsubstituierter Allene II 3. 4 Nucleophile Addition an akzeptorsubstituierte Allene Ein Beispiel aus der Naturstoffsynthese: N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 379 20
![42Cycloaddition von Allenen 3 5 DielsAlderReaktionen von Allenen a Reaktion konjugierten Allensysteme mit Dienophilen [4+2]-Cycloaddition von Allenen 3. 5 Diels-Alder-Reaktionen von Allenen a) Reaktion konjugierten Allensysteme mit Dienophilen](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-21.jpg)
[4+2]-Cycloaddition von Allenen 3. 5 Diels-Alder-Reaktionen von Allenen a) Reaktion konjugierten Allensysteme mit Dienophilen b) Reaktion von Allenen mit konjugierten Dienen Ausbeute: 90 % Verhältnis endo : exo = 64 : 36 X = CH 2, O, NR´ J. Org. Chem. 1990, 55, 5439 -5442 21

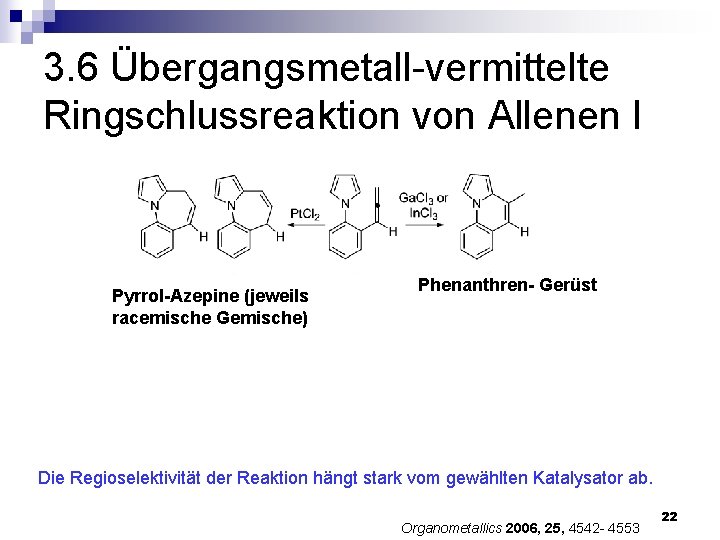
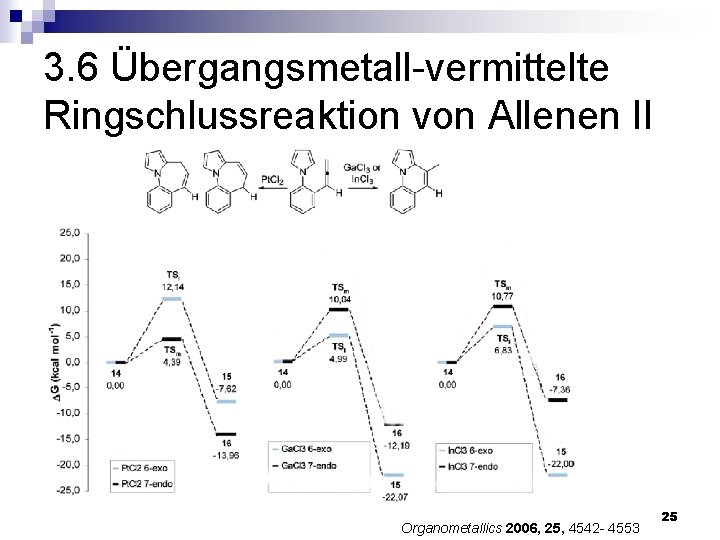
3. 6 Übergangsmetall-vermittelte Ringschlussreaktion von Allenen I Pyrrol-Azepine (jeweils racemische Gemische) Phenanthren- Gerüst Die Regioselektivität der Reaktion hängt stark vom gewählten Katalysator ab. Organometallics 2006, 25, 4542 - 4553 22

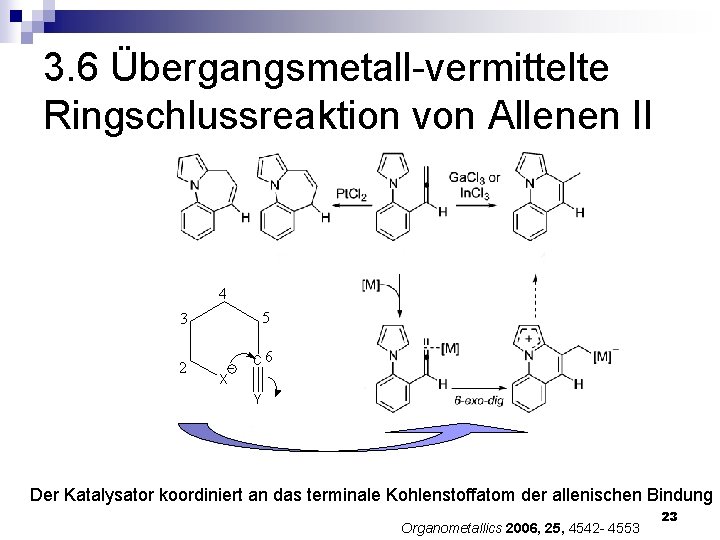
3. 6 Übergangsmetall-vermittelte Ringschlussreaktion von Allenen II Der Katalysator koordiniert an das terminale Kohlenstoffatom der allenischen Bindung Organometallics 2006, 25, 4542 - 4553 23

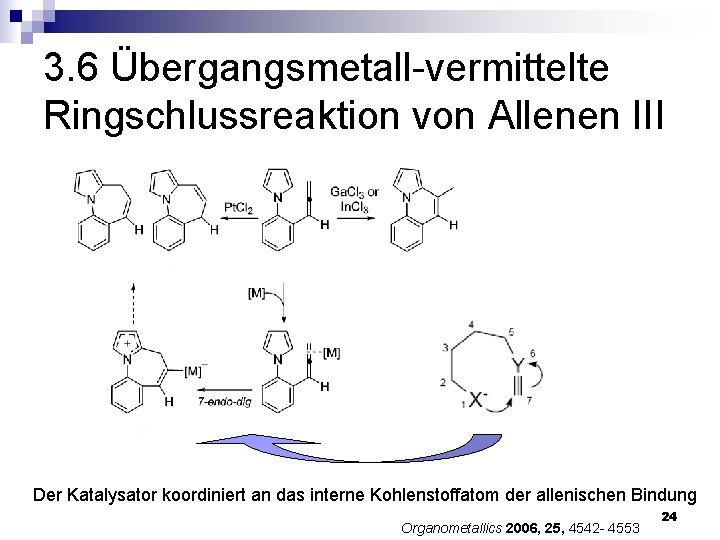
3. 6 Übergangsmetall-vermittelte Ringschlussreaktion von Allenen III Der Katalysator koordiniert an das interne Kohlenstoffatom der allenischen Bindung Organometallics 2006, 25, 4542 - 4553 24

3. 6 Übergangsmetall-vermittelte Ringschlussreaktion von Allenen II Organometallics 2006, 25, 4542 - 4553 25

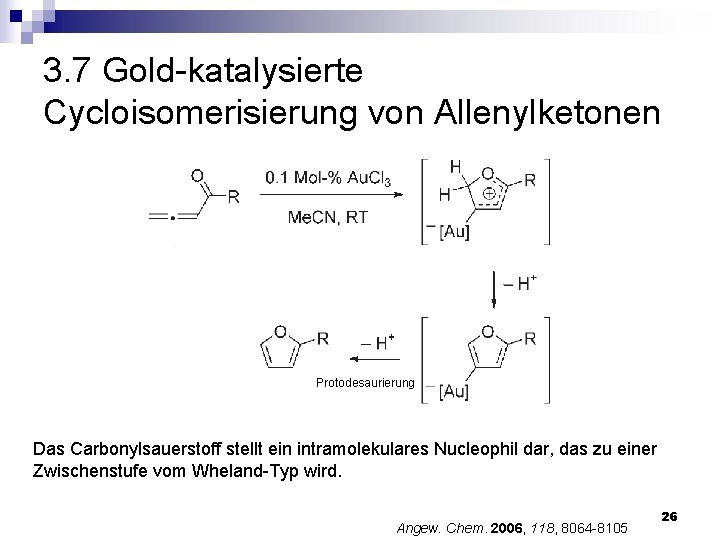
3. 7 Gold-katalysierte Cycloisomerisierung von Allenylketonen Protodesaurierung Das Carbonylsauerstoff stellt ein intramolekulares Nucleophil dar, das zu einer Zwischenstufe vom Wheland-Typ wird. Angew. Chem. 2006, 118, 8064 -8105 26

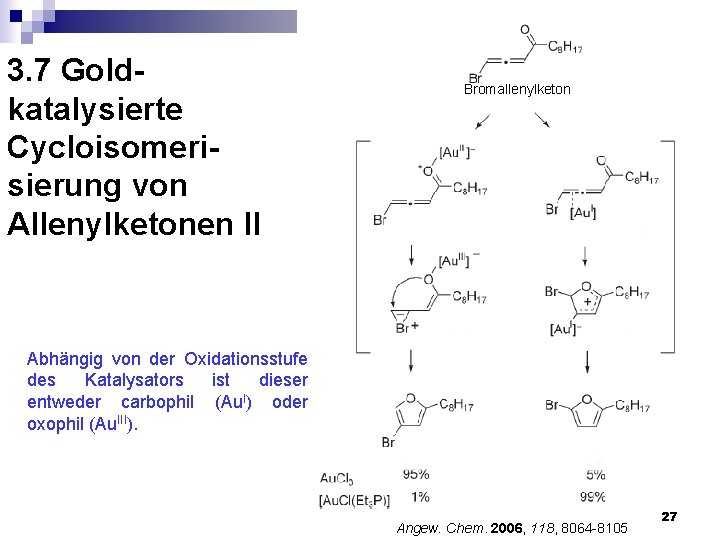
3. 7 Goldkatalysierte Cycloisomerisierung von Allenylketonen II Bromallenylketon Abhängig von der Oxidationsstufe des Katalysators ist dieser entweder carbophil (Au. I) oder oxophil (Au. III). Angew. Chem. 2006, 118, 8064 -8105 27

Ausblick Allene sind außerordentlich nützliche Zwischenstufen in der selektiven Synthese komplexer Naturstoffen. Die Möglichkeiten, die Allene hier bieten sind noch lange nicht erschöpft. 28
![Literatur n n n 1 N Krause A S K Hashmi Modern Allene Chemistry Literatur n n n [1] N. Krause, A. S. K. Hashmi Modern Allene Chemistry,](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-29.jpg)
Literatur n n n [1] N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 1042 [2] Nader, Brecht, Kreisz Chem. Ber. 1986, 119, 1208 – 1216 [3] Marshall, Chem. Rev. 2000, 100, 3163 -3185 [4] Krause Angew. Chem. 2004, 116, 1216 -1236 [5] Buchholz, Reissig Synthesis 2002, 1412 -1422 [6] Taylor Chem. Rev. 1967, 67 317 -359 [7] Boger, Curran J. Org. Chem. 1990, 55, 5439 -5442 [8] Soriano, Marco-Contelles Organometallics 2006, 25, 4542 - 4553 [9] Hashmi, Hutchings Angew. Chem. 2006, 118, 8064 -8105 [10] Krause, Hoffmann-Röder Synthesis 2002, 1759 -1774 29

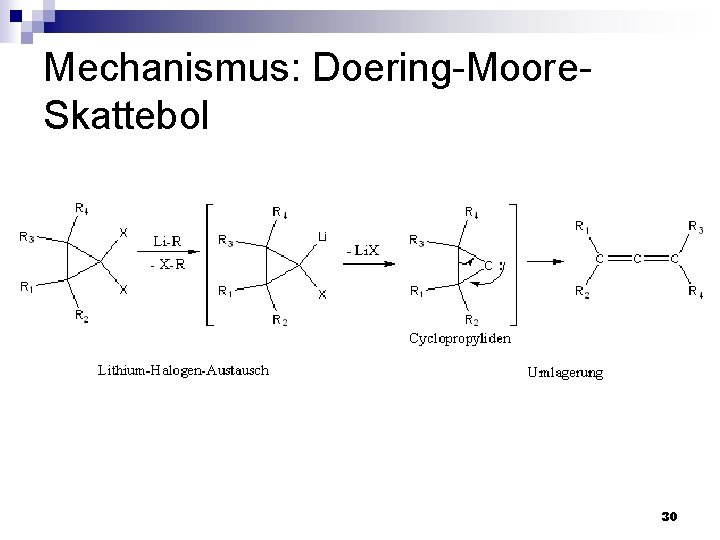
Mechanismus: Doering-Moore. Skattebol 30

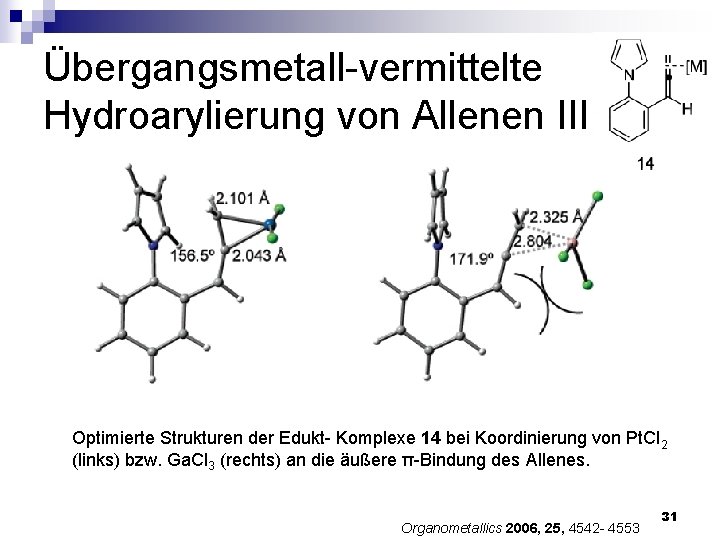
Übergangsmetall-vermittelte Hydroarylierung von Allenen III Optimierte Strukturen der Edukt- Komplexe 14 bei Koordinierung von Pt. Cl 2 (links) bzw. Ga. Cl 3 (rechts) an die äußere π-Bindung des Allenes. Organometallics 2006, 25, 4542 - 4553 31

Übergangsmetall-vermittelte Hydroarylierung von Allenen IV NPA = natural population analysis Organometallics 2006, 25, 4542 - 4553 32
![22Cycloaddition von Allenen 3 7 Allene als Vorstufen in der Naturstoffsynthese Periplanone B ist [2+2]-Cycloaddition von Allenen 3. 7 Allene als Vorstufen in der Naturstoffsynthese Periplanone B ist](https://slidetodoc.com/presentation_image_h/c4c217188ad334f5711da9dc9e72cfc5/image-33.jpg)
[2+2]-Cycloaddition von Allenen 3. 7 Allene als Vorstufen in der Naturstoffsynthese Periplanone B ist das Pheromon der Amerikanischen Kakerlake und wird als Insektizid eingesetzt. N. Krause, A. S. K. Hashmi Modern Allene Chemistry, Wiley VCH, 2004, S. 1042 33