Anorganick molekulov sloueniny Katedra obecn a anorganick chemie

Anorganické molekulové sloučeniny Katedra obecné a anorganické chemie Fakulta chemicko-technologická Univerzita Pardubice Milan Erben
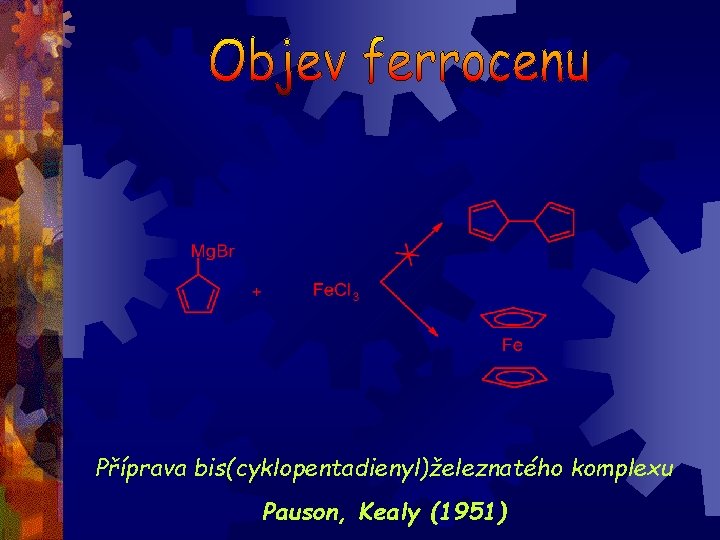
Příprava bis(cyklopentadienyl)železnatého komplexu Pauson, Kealy (1951)
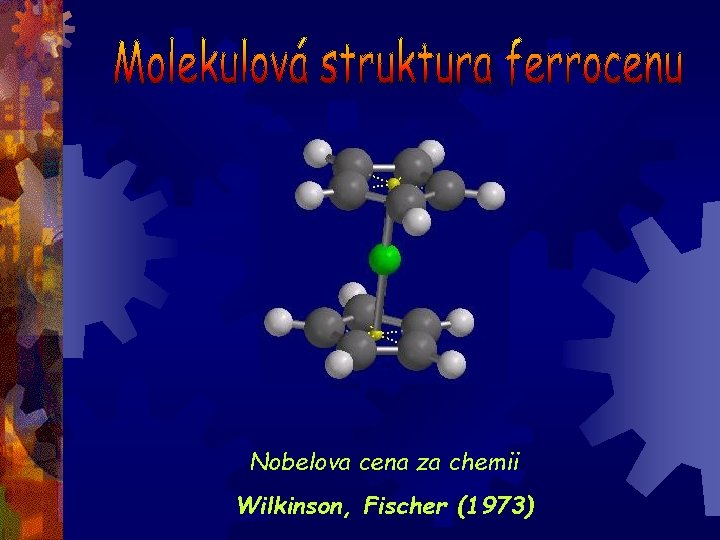
Nobelova cena za chemii Wilkinson, Fischer (1973)

komplex barva reaktivita Cp 2 V fialový pyroforický Cp 2 Cr červený vysoce pyroforický Cp*2 Mn hnědý lze redukovat na Cp*2 Mn- Cp 2 Fe oranžový na vzduchu stálý Cp 2 Co purpurový snadno se oxiduje na Cp 2 Co+ Cp 2 Ni zelený pomalá oxidace na Cp 2 Ni+ Proč je právě ferrocen tak výjimečně stabilní ?

Termodynamicky stabilní sloučenina přechodného kovu vzniká tehdy, je-li součet d-elektronů kovu a elektronů, jež přinášejí ligandy roven 18. zásady pro určení počtu VE: a) intramolekulární rozdělení náboje musí být takové, aby celkový náboj komplexu zůstal nezměněn b) vazba kov-kov přispívá 1 e- každému kovu c) můstkový oxid uhelnatý přináší 1 e- každému kovu

n VE příklady ligandů 0 BF 3, Al. X 3 1 s-vázané ligandy: R, Ar, acyl, X, H, OR, NR 2, PR 2 2 h 2 -vázané ligandy, H 2 O, NR 3, PR 3, CO, =CR 2 3 h 3 -vázané ligandy (allyl, cyklopropenyl), ≡N , ≡CR 4 h 4 -vázané ligandy (cyklobutadienyl, dieny aj. ) 5 h 5 -vázané ligandy (cyklopentadienyl) 6 h 6 -vázané ligandy (areny, trieny, pyrrol) n hn-vázané ligandy (h 7 -tropylium, h 8 -COT)
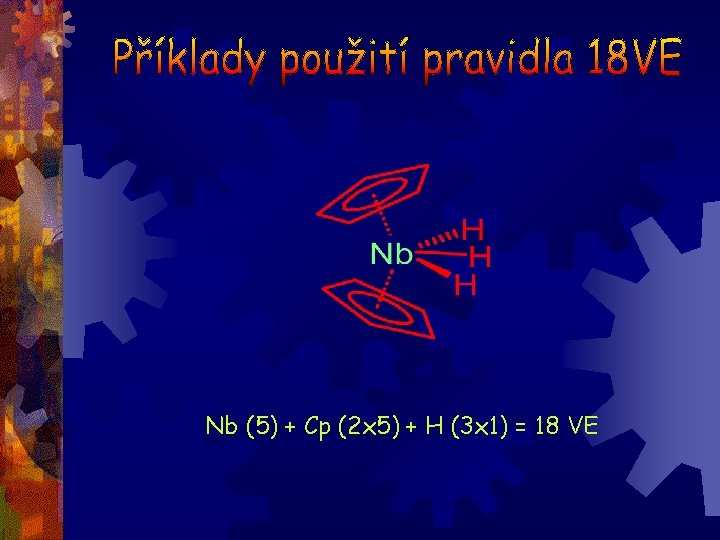
Nb (5) + Cp (2 x 5) + H (3 x 1) = 18 VE
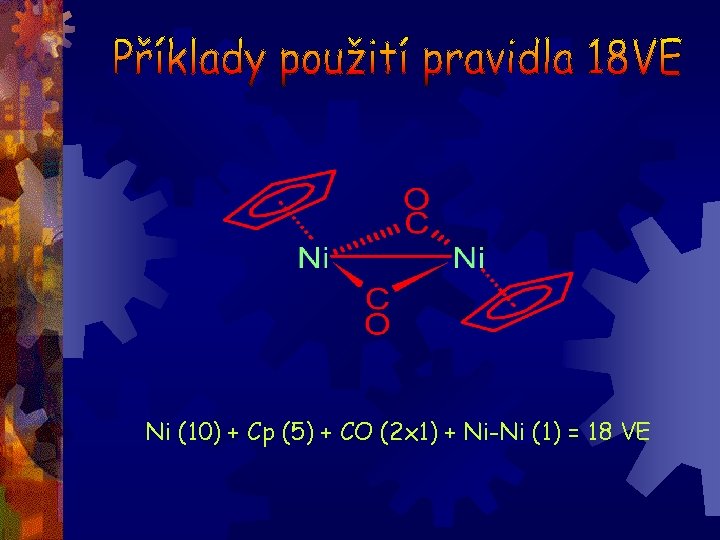
Ni (10) + Cp (5) + CO (2 x 1) + Ni-Ni (1) = 18 VE
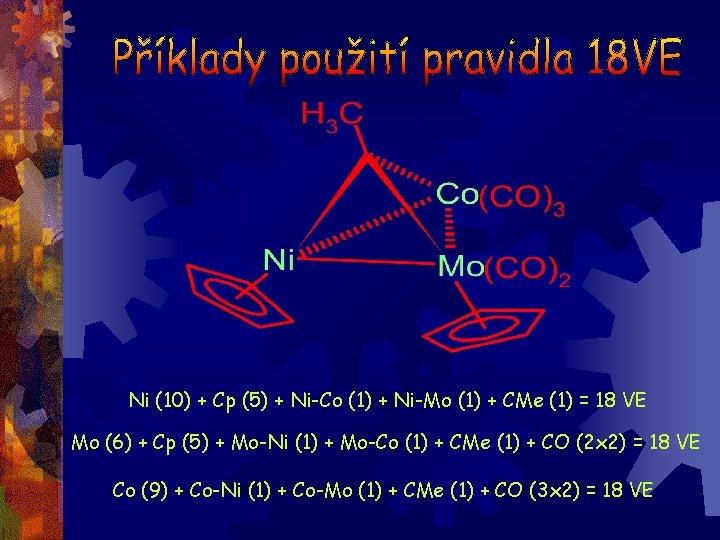
Ni (10) + Cp (5) + Ni-Co (1) + Ni-Mo (1) + CMe (1) = 18 VE Mo (6) + Cp (5) + Mo-Ni (1) + Mo-Co (1) + CMe (1) + CO (2 x 2) = 18 VE Co (9) + Co-Ni (1) + Co-Mo (1) + CMe (1) + CO (3 x 2) = 18 VE
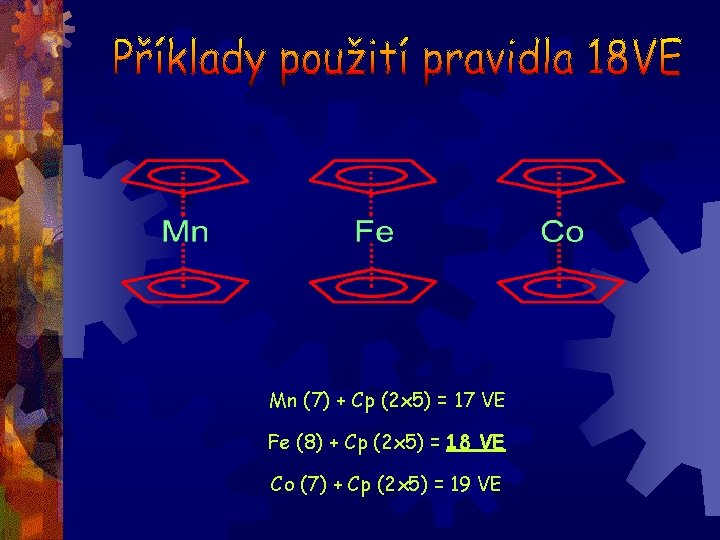
Mn (7) + Cp (2 x 5) = 17 VE Fe (8) + Cp (2 x 5) = 18 VE Co (7) + Cp (2 x 5) = 19 VE

1. elektronově deficitní metalloceny: n. VE < 18 - rovinné sloučeniny jsou málo stálé (dimerizace) - tendence nabýt 18 VE adiční reakce na kovu 2. elektronově bohaté metalloceny : n. VE > 18 - pro n. VE = 20 jsou rovinné sloučeniny stálé - tendence nabýt 18 VE reakce na ligandu 3. metalloceny s 18 VE 4. - velmi stabilní částice 5. - reakce na kruzích (Friedel-Crafts)
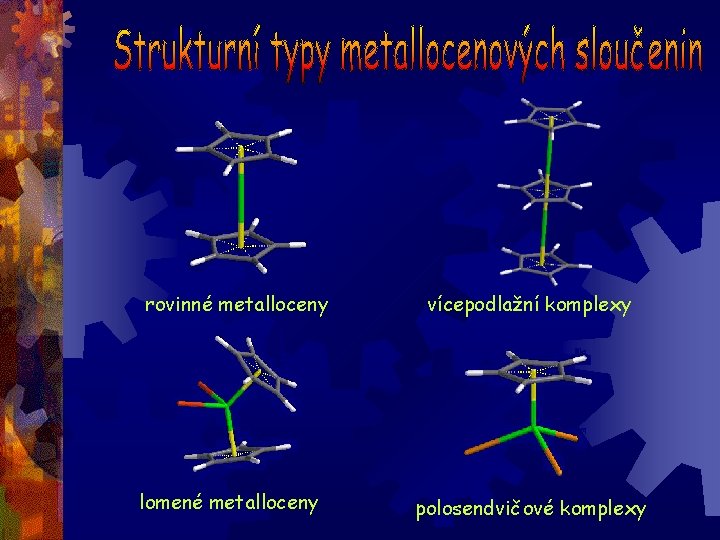
rovinné metalloceny lomené metalloceny vícepodlažní komplexy polosendvičové komplexy

• významné postavení v organokovové chemii • vhodná velikost (2 -3 Å) pro koordinaci ke kovům • aromatický systém (6 p-elektronů) • stabilizující účinky (sterické, b-eliminace) • je dobrým donorem i akceptorem elektronů • může být substituován EA nebo ED substituenty • různé způsoby vazby (proměnlivá hapticita) • uhlíky pětičlenného cyklu lze nahradit heteroatomy

h 3 -cyklopropenyl 2 pe- h 4 - cyklobutadienyl 6 pe- h 5 - cyklopentadienyl 6 pe- Hückelovo pravidlo: 4 n + 2 (pe-) h 6 -aren 6 pe- h 7 -cykloheptatrienyl 6 pe- h 8 -cyklooktatetraenyl 10 pe-
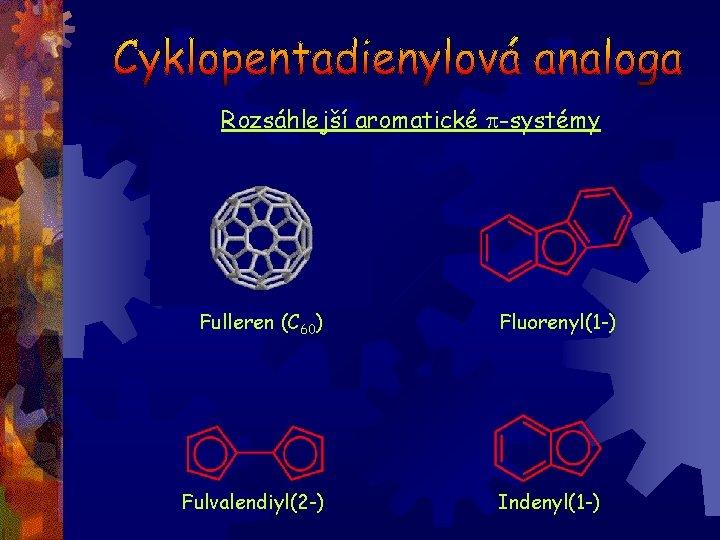
Rozsáhlejší aromatické p-systémy Fulleren (C 60) Fulvalendiyl(2 -) Fluorenyl(1 -) Indenyl(1 -)
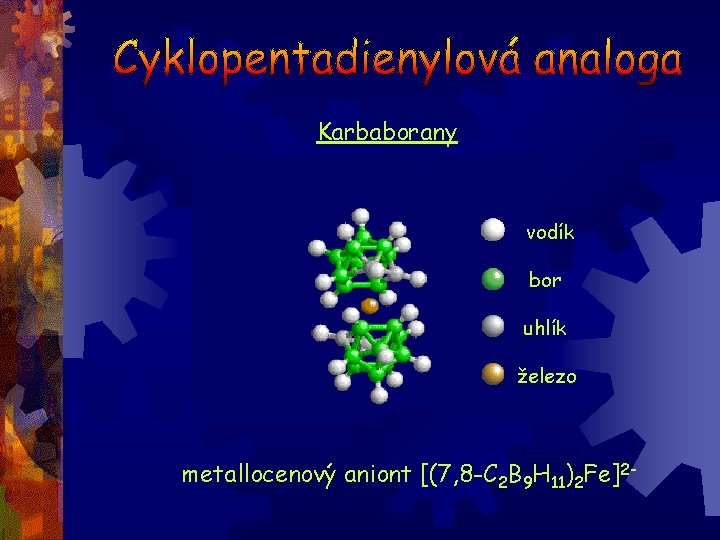
Karbaborany vodík bor uhlík železo metallocenový aniont [(7, 8 -C 2 B 9 H 11)2 Fe]2 -
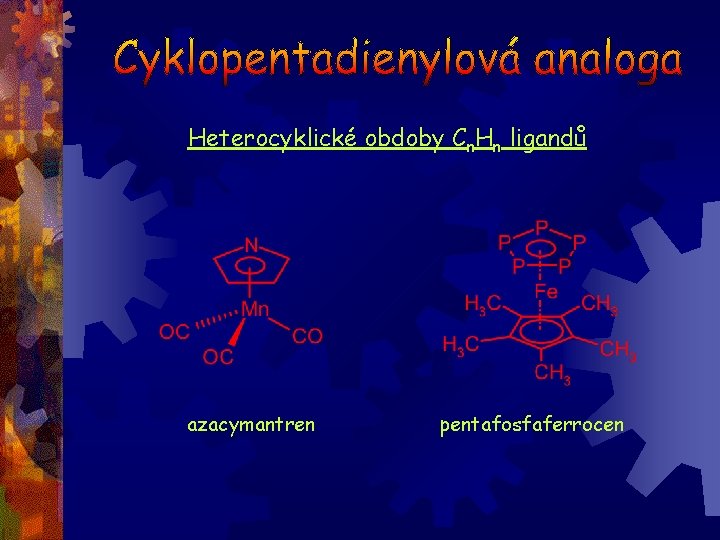
Heterocyklické obdoby Cn. Hn ligandů azacymantren pentafosfaferrocen
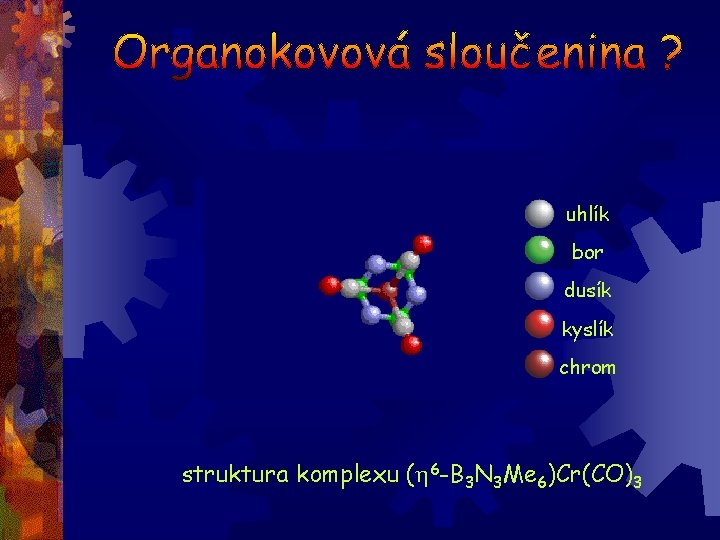
uhlík bor dusík kyslík chrom struktura komplexu (h 6 -B 3 N 3 Me 6)Cr(CO)3

• struktura ferrocenu • pravidlo 18 -ti valenčních elektronů ! • h-způsob vazby ligandů k přechodnému kovu • strukturní typy metallocenů • modifikace cyklopentadienylového ligandu

Katalytické vlastnosti Ing. Milan Erben Ph. D. Ing. Michal Dušek Ing. Vít Šťáva Biologické vlastnosti Dr. Ing. Jaromír Vinklárek Ing. Jan Honzíček, Ph. D. Mgr. Hana Paláčková
- Slides: 20