Anorganick chemie Obecn pojmy a vpoty Obecn pojmy
Anorganická chemie Obecné pojmy a výpočty

Obecné pojmy- hmotnost m(1 H) = 1, 67355. 10 -27 kg m(12 C) = 1, 99267. 10 -26 kg m(63 Cu) = 1, 04496. 10 -25 kg Atomová hmotnostní jednotka u 1 u = 1, 66057. 10 -27 kg její hmotnost má Atomová hmotnostní konstanta mu, která je definována jako dvanáctina klidové hmotnosti atomu nuklidu uhlíku 12 C: mu = m(12 C)/12 = 1, 66057. 10 -27 kg

Obecné pojmy- hmotnost • Relativní atomová hmotnost Ar(X) • Ar(X)= m(X)/ mu je rovna podílu hmotnosti m(X) a atomové hmotnosti konstanty • Mr(X) …relativní molekulová hmotnost • Množství částic v látce je vyjádřeno veličinou nazvanou látkové množství n a jeho jednotkou je mol • Avogadrova konstanta NA … vzorek ze stejnorodé látky má látkové množství 1 mol, obsahuje–li právě tolik částic (atomů, molekul, iontů, …), kolik je ve vzorku nuklidu uhlíku 12 C o hmotnosti 12 g • NA= 6, 023. 1023 • n= N/ NA

Látkové množství • Molární hmotnost je v podstatě hmotnost jednoho molu částic M s jednotkou kg/mol – dílčí jednotka g/mol. • Přímé měření látkového množství není prakticky proveditelné. • K jeho výpočtu se používá následující vztahy:

Základní pojmy • • w M n Vm k. Pa) = = hmotnostní zlomek molární hmotnost (g/mol) látkové množství ( mol) molární objem 22, 4 dm 3 (p=101, 3 • NA = počet částic v jednom molu ( 6, 022. 1023)
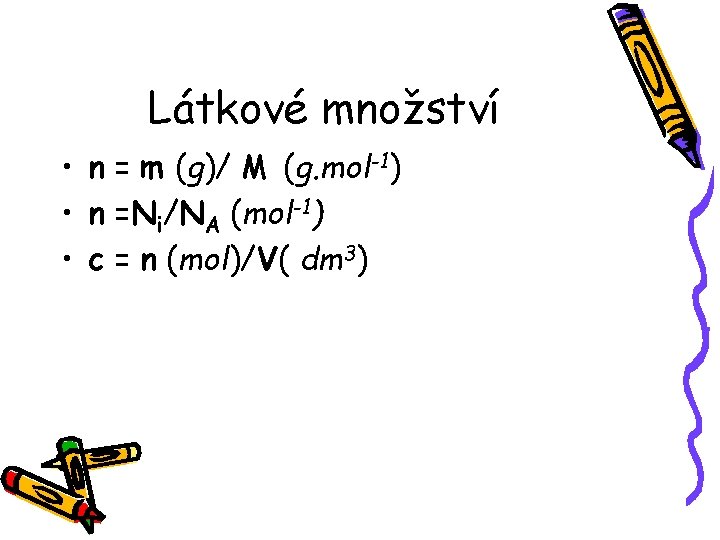
Látkové množství • n = m (g)/ M (g. mol-1) • n =Ni/NA (mol-1) • c = n (mol)/V( dm 3)

Hmotnostní zlomek • w(s) = m(s)/ m® Složení roztoku ( hmotnostní zlomek látky rozpuštěné v roztoku) • w(s) = m(č)/ m© Složení sloučeniny ( hmotnostní zlomek části k celku • Φ= Včásti /Vcelku

Redoxní děje Definování pojmů oxidace a redukce • Oxidace – název podle slučování s kyslíkem • děj při kterém dochází ke zvyšování oxidačního čísla atomů • Redukce, děj při kterém dochází ke snižování oxidačního čísla atomů • V jedné reakci dochází vždy k redukci a oxidaci současně – Redoxní reakce

Redoxní děje Definování pojmů oxidace a redukce na základě přesunu elektronů • Oxidace – děj, při kterém dochází k uvolňování elektronů a tím ke zvyšování nábojového čísla částic • Redukce, děj při kterém dochází k přijímání elektronů a tím ke snižování nábojového čísla částic. • Počet přijatých a uvolněných elektronů v jedné reakci je vždy stejný.

Úprava redox rovnic • 1. Napsat známé reaktanty a produkty • 2. Napsat poloreakce (není-li znám průběh reakce, je možné jej stanovit podle výše redokčního potenciálu: Poloreakce s vyšším redukčním potenciálem porbíhjí ve směru redukce a poloreakce s nižším redukčním potenciálem probíhají ve směru oxidace.

Redoxní děje Oxidační činidlo • Druhou částici oxiduje tím, že jí odebírá elektrony. Dochází u ní ke zvýšením nábojového nebo oxidačního čísla. • Oxidační činidlo se samo se redukuje přibranými elektrony • Kyslík, kovy a podobně

Redoxní děje Redukční činidlo • Druhou částici redukuje tím, že jí předává elektrony. Dochází u ní ke snížení nábojového nebo oxidačního čísla. • Redukční činidlo se samo oxiduje odevzdanými elektrony • Uhlík, koks, kovy a podobně
Redoxní děje Schéma Redukuje se Činidlo oxidační (oxidovadlo) přijímá elektrony od činidla redukčního (redukovadla) oxiduje se
- Slides: 13