vod do chemie Anorganick chemie Stavba atomu Anorganick

Úvod do chemie Anorganická chemie Stavba atomu

Anorganická chemie – Názvosloví • • Značky prvků Názvosloví binárních sloučenin Názvosloví kyselin a zásad Názvosloví solí

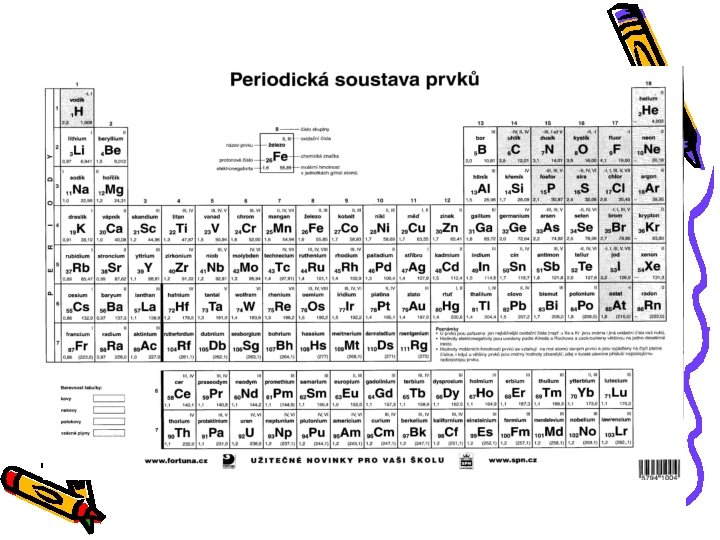
Značky a názvy prvků • • Název český Název latinský Značka prvku http: //cs. wikipedia. org/wiki/Periodic k%C 3%A 1_tabulka • http: //cs. wikipedia. org/wiki/Periodick %C 3%A 1_tabulka

Stavba atomu • Atomové jádro tvoří protony a neutrony. Zahrnujeme pod společným názvem nukleony. Ze struktury atomového jádra plynou následující důležité pojmy. • Protonové (atomové) číslo Z je počet protonů v jádře, u elektroneutrálního stavu atomu i počet elektronů. Zapisuje se jako dolní index před značkou prvku H, He, Li, Be, B, C, N, O, F, . . . , Sc, . . . , Au, . . . , U, . . . , Md. • Neutronové číslo N je počet neutronů v jádře. Neuvádí se u značky prvku. • Nukleonové (hmotnostní) číslo A udává počet protonů a neutronů v jádře (A = Z + N). Zapisuje se jako horní index před značkou prvku.

Stavba atomu • Prvek je soubor atomů, které mají stejné Z, např. kyslík (O, O, O), vodík (H – protium, H – deuterium, H – tritium) Značka prvku, odvozená z latinského nebo řeckého názvu, se uvádí ve spojení s protonovým číslem Z a nukleonovým • • • A Z Značka prvku
Stavba atomu • Nuklid tvoří soubor atomů se stejným Z a N (a tím i A), např. 11 H, 168 O, 178 O 33 S, 46 Ti, 209 Bi (nejtěžší stabilní 16 22 83 nuklid). • Izotopy tvoří dva a více nuklidů téhož prvku, např. kyslík 16 O, 17 O, 18 O nebo vodík 1 H, 2 H, 3 H. Izotopie znamená, že daný prvek je tvořen více než jediným nuklidem. • Izobary jsou atomy různých prvků, které mají stejné nukleonové číslo A, ale jiné protonové číslo Z, např. dvojice 2658 Fe a 2858 Ni. •

Nuklidy • V přírodě se vyskytuje asi 329 nuklidů, většina (273, tj. 83 %) je stabilních, ostatní jsou nestabilní, jsou radioaktivní. Mononuklidické prvky (nepřesně monoizotopické), tzv. čisté, jsou např. 4 Be, 9 F, 11 Na, 13 Al, 15 P, 21 Sc, . . . , 53 I, . . . , 79 Au, . . . , (celkem 20 prvků). • Zvlášť hojně jsou rozšířeny nuklidy 816 O, 1224 Mg, 1428 Si a 40 20 Ca, které tvoří téměř 70 % hmotnosti zemské kůry. Ve vesmíru je však nejvíce zastoupen vodík 11 H, který vznikl jako praprvek. Nejtěžšími stabilními nuklidy jsou nuklidy olova 82208 Pb a bismutu 83209 Bi. • Velké kolísání počtu izotopů je pouze u Pb (konečný člen přirozených radioaktivních rozpadových řad: 204, 206, 207, 2087)

Elektronový obal • Korpuskulárně-vlnová teorie Při experimentálním zkoumání rozptylu částic α při průchodu kovovými fóliemi (Geiger, Marsden, 1911) bylo zjištěno, že paprsky se jen málo odchylují od směru pohybu, avšak v jednotlivých případech dochází k mimořádně velkému odchýlení. Z toho odvodil Rutherford (1911), že kladný náboj atomu musí být soustředěn ve zcela malé oblasti uvnitř atomu (jádro atomu), která má ve srovnání s velikostí atomu nepatrné rozměry: • efektivní průměr atomu je 100 -600 pm • efektivní průměr jádra je asi 0, 01 pm (pikometr) = 10 -12 m = 10 -2 Å; „picco, piccolo“ (ital. ) = malý.

Elektronový obal • Klasická fyzika důsledně rozlišuje pojem • a) částice (korpuskule) a • b) vlnění. Podstatným znakem částice je • 1) možnost přesné lokalizace v prostoru, • 2) existence definované dráhy pohybu a • 3) ostré vymezení povrchu. Podstatným znakem vlnění je • 1) šíření vlnění (vzruchu) v jakémkoliv hmotném prostředí, • 2) ohybové (difrakční) a interferenční jevy. 1 pm (pikometr) = 10 -12 m = 10 -2 Å; „picco, piccolo“ (ital. ) = malý.

Elektronový obal • U mikroobjektů je nutné připustit dualismus jejich chování (částice a vlnění). Vlastnosti mikroobjektů jsou tak zvláštní, že srovnávání a názorná představa na základě makroobjektů (a makrosvěta vůbec!) selhává. • Korpuskulárně-vlnová "představa" tedy není součtem dvou představ.
Atomové orbitaly • Atomový orbital (AO) je vlnová funkce elektronu v atomu. Jejím grafickým znázorněním je oblast nejpravděpodobnějšího výskytu elektronu získaná z vlnové funkce pro jeden elektron.
Atomové orbitaly Kvantová čísla • Atomové orbitaly jsou charakterizovány třemi celými čísly - tzv. kvantovými čísly n, ℓ a m, přičemž je: • n - hlavní kvantové číslo. Určuje energii AO: En = -kn-2, kde n = 1, 2, 3, . . . • ℓ - vedlejší kvantové číslo. Určuje tvar rozložení elektronového obalu, u složitějších atomů poněkud ovlivňuje energii AO. Platí, že ℓ = 0, 1, . . . , (n - 1). • m ℓ - magnetické kvantové číslo. Souvisí s polární částí vlnové funkce a určuje konkrétní orientaci AO k souřadnému systému. Danému ℓ přísluší celkem (2ℓ + 1) hodnot m = -l, . . . , 0, 1, . . . , +1. Kvantová čísla n, ℓ, a m plně charakterizují každý orbital. •
Atomové orbitaly Kvantová čísla • s - spinové kvantové číslo je pro každý elektron stejné, jeho hodnota je rovna 1/2 a nemění se. Pomocí tohoto čísla nelze elektrony rozlišit. • Obecně platí , že v jednom atomu nemohou existovat dva elektrony, jejichž všechna kvantová čísla jsou stejná (Pauliho princip výlučnosti) • Jelikož energii AO určuje zejména hodnota n (případně ℓ), leží orbitaly se stejnými hodnotami n a ℓ na téže energetické úrovni, tj. jsou energeticky degenerované.

Tvar orbitalů

Kvantová čísla a atomové orbitaly • • • • • Kvant. čísla n ℓ m 1 0 0 2 1 +1 2 1 0 2 1 -1 3 0 0 3 1 +1 3 1 0 3 1 -1 3 2 +2 3 2 +1 3 2 0 3 2 -1 3 2 -2 Symbol AO 1 s 2 s 2 px 2 pz 2 py 3 s 3 px 3 pz 3 py 3 dx 2 -y 2 3 dxz 3 dz 2 3 dyz 3 dxy Symbol plně obsazených AO 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 Degenerace 1 krát (není) 3 krát 5 krát
- Slides: 16