CHEMIE BORU CH3 Anorganick chemie DUM 3 druh


CHEMIE BORU CH-3 Anorganická chemie, DUM č. 3 druhý ročník čtyřletého studia Mgr. Radovan Sloup Gymnázium Sušice Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II

bor Osnova: Jaká je značka boru a jeho postavení v tabulce? Elektronová konfigurace a oxidační čísla boru. Kdo a kdy bor poprvé připravil? Jaká je struktura boru a jeho hlavních sloučenin? K čemu se používají hlavní sloučeniny boru? Biochemický význam boru

bor značka boru je odvozena z latinského názvu: BORUM Bo Br Bm Ba Be vyberte správnou značku boru:
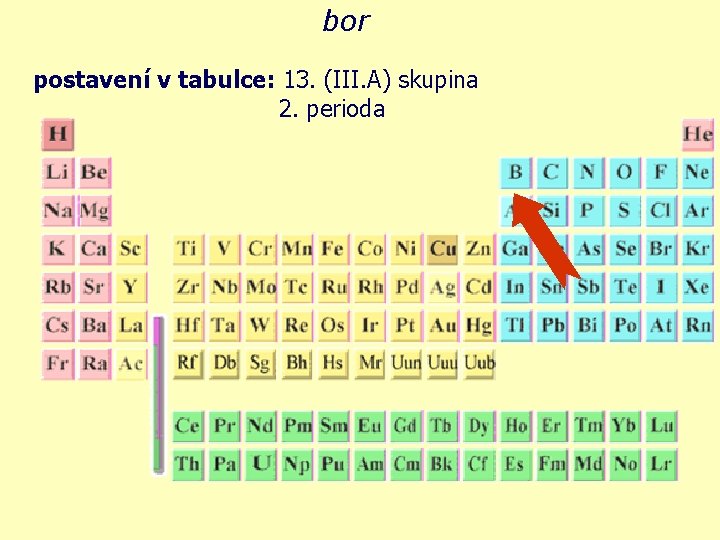
bor postavení v tabulce: 13. (III. A) skupina 2. perioda
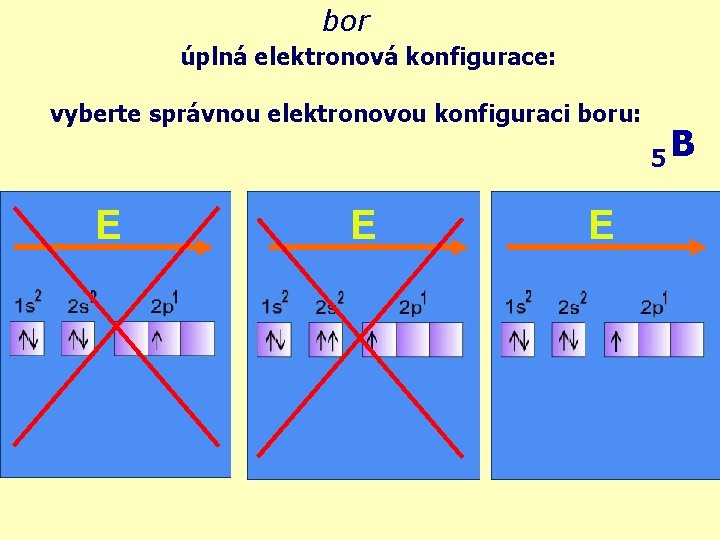
bor úplná elektronová konfigurace: vyberte správnou elektronovou konfiguraci boru: E E E 5 B

bor elektronová konfigurace - excitovaný stav, po dodání E se poslední párový elektron přesune do prvního volného orbitalu 5 B E v důsledku tohoto jevu je bor ve sloučeninách trojvazný a jeho oxidační čísla ve sloučeninách jsou +III a -III

historie přípravy boru: Bor je v zemské kůře je vzácnější než např. lithium. Vyskytuje se vždy vázaný na kyslík, nejznámějším nerostem boru je borax. Elementární (znečištěný) bor připravili r. 1808 poprvé Gay-Lussac a Thenard v Paříži a současně Davy (obr. ) elektrolyticky v Londýně. V roce 1824 obr. 1 jej Berzelius klasifikoval jako samostatný prvek. Čistý krystalický bor získal poprvé Weintraub r. 1909 tavením „amorfního“ boru ve vakuu. „Krystalický“ bor se dnes získává rozkladem chloridu boritého v přítomnosti vodíku vysokofrekvenčními jiskrami mezi wolframovými elektrodami. Redukcí oxidu boritého kovovým sodíkem nebo hořčíkem se získá tzv. „amorfní“ bor jako hnědočerný prášek. B 2 O 3 + 3 Mg → 2 B + 3 Mg. O

bor: Existuje v několika alotropických modifikací, jejichž základní strukturou je ikosaedr B 12. obr. 2 ikosaedr = dvacetistěn

sloučeniny boru: Významnými sloučeninami boru jsou borax a kyselina boritá. Borax Na 2 B 4 O 5(OH)4. 8 H 2 O patří mezi hydroxoboritany a používá se například jako tavidlo nebo hnojivo. Vyrábí se z něj slabá kyselina boritá H 3 BO 3. Tato kyselina se používá ve sklářství, keramickém průmyslu a ve zdravotnictví např. v roztoku k vyplachování očí. Zahříváním na vysokou teplotu ztrácí kyselina boritá vodu (dehydratuje) a přechází na oxid boritý B 2 O 3, který je ve vodě obtížně rozpustný. Jeho pozvolným rozpouštěním vzniká opět roztok kyseliny borité. borax: kyselina boritá: oxid boritý:

sloučeniny boru: dehydrogenace kyseliny borité a její následný vznik: 2 H 3 BO 3 (t) → B 2 O 3 + 3 H 2 O → 2 H 3 BO 3
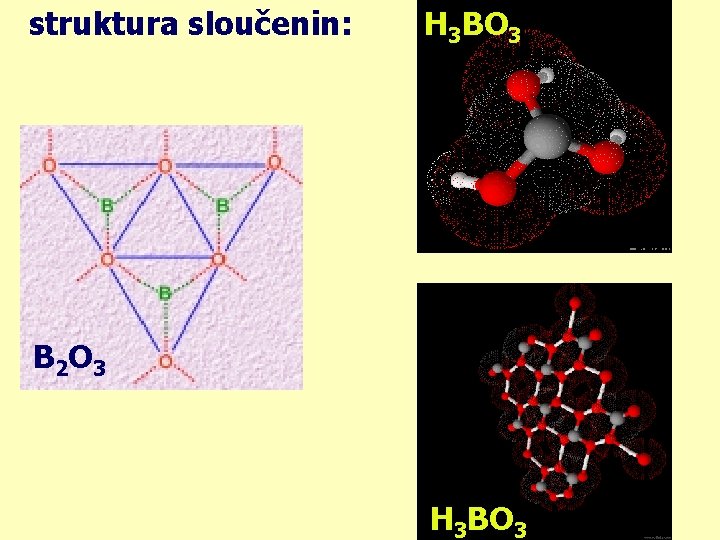
struktura sloučenin: H 3 BO 3 B 2 O 3 H 3 BO 3

sloučeniny boru: kyselina boritá v analytice: používá se k odlišení methanolu a ethanolu: methanol

sloučeniny boru: kyselina boritá v analytice: používána k odlišení kovových iontů – boraxové perličky:

chemické vlastnosti boru - shrnutí: doplňte reakce podle předpokládaného průběhu: B 2 O 3 + 3 Mg → 2 B + 3 Mg. O B 2 O 3 + 6 Na → 2 B + 3 Na 2 O B 2 O 3 + 3 H 2 O → 2 H 3 BO 3 (t) → B 2 O 3 + 3 H 2 O

biochemický význam boru: Bor je prvek významný hlavně pro rostliny. Je nezbytný pro správný vývoj listů a plodů. Jeho nedostatek způsobuje zasychání okrajů listů a například u broskví praskání pecek uvnitř plodu (viz obr. ). Jeho nedostatek je v půdě je možné vyřešit přihnojováním boraxem.

CHEMIE BORU Vytvořeno v rámci projektu Gymnázium Sušice - Brána vzdělávání II Autor: Mgr. Radovan Sloup, Gymnázium Sušice Předmět: Chemie (Anorganická chemie) Třída: druhý ročník čtyřletého gymnázia Označení: VY_32_INOVACE_Ch-3_03 Datum vytvoření: 8. října 2012 Anotace a metodické poznámky Prezentace je určena ke shrnutí chemie boru v rozsahu SŠ, k zopakování základních reakcí vedoucích k zisku čistého boru. Obsahuje přehled jeho základních sloučenin, jejich využití v analýze (např. methanol hoří zeleně s H 3 BO 3) a biochemických účinků. Materiál je vhodné podle možností doplnit reálným experimentem. Pro reálný experiment je možné demonstrovat hoření methanolu s boraxem nebo kyselinou boritou, případně vytvořením boraxové perličky tavením H 3 BO 3 nebo boraxu s roztokem měďnaté soli, nebo solí samotnou v nesvítivém plameni kahanu. Závěrečné shrnutí je možné použít ke krátkému zkoušení. Použité materiály: Honza, J. ; Mareček, A. ; Chemie pro čtyřletá gymnázia (1. díl). Brno: Da. Ta. Print, 1995; ISBN 80 -900066 -6 -3 Greenwood, N. N. ; Earnshaw, A. ; Chemie prvků I. Praha: Informatorium, 1993, ISBN 80 -85427 -38 -9 Obr č. 1 Davy (6. 10. 2012), autor: Shuster, Shipley: http: //commons. wikimedia. org/wiki/File: SS-davy. jpg Obr č. 2 (6. 10. 2012), autor: Wikipedista: PDD: http: //commons. wikimedia. org/wiki/File: Icosahedron_grey. png Ostatní obrázky jsou dílem autora prezentace. Vše je vytvořeno pomocí nástrojů Power Point 2003, Zoner. Photo. Studio 14, Chem. Sketch 10. 1, Malování
- Slides: 17