Chemie kyslku CH3 Anorganick chemie DUM 8 2









- Slides: 13


Chemie kyslíku CH-3 Anorganická chemie, DUM č. 8 2. ročník čtyřletého studia Mgr. Radovan Sloup Gymnázium Sušice Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II

Osnova: kyslík Jaká je značka kyslíku a jeho postavení v tabulce? Elektronová konfigurace kyslíku. Kdo kyslík poprvé připravil a jaké jsou jeho fyzikální vlastnosti? Jak probíhá výroba a příprava kyslíku? Jaké jsou chemické vlastnosti kyslíku? K čemu se kyslík používá? Oxidační účinky kyslíku. Biochemický význam kyslíku … 3

kyslík značka kyslíku je odvozena z latinského názvu: OXYGENIUM značka kyslíku je? Ox O Om Og On Ou 4

kyslík postavení v tabulce: 16. (VI. A) skupina 2. perioda 5

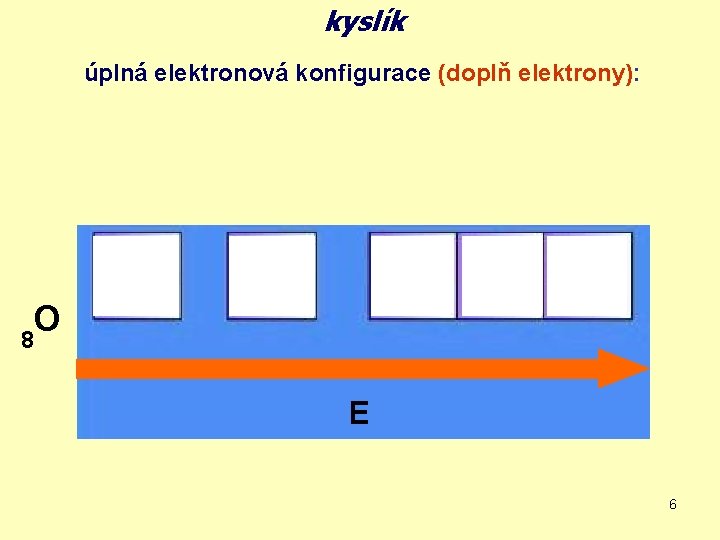
kyslík úplná elektronová konfigurace (doplň elektrony): O 8 E 6

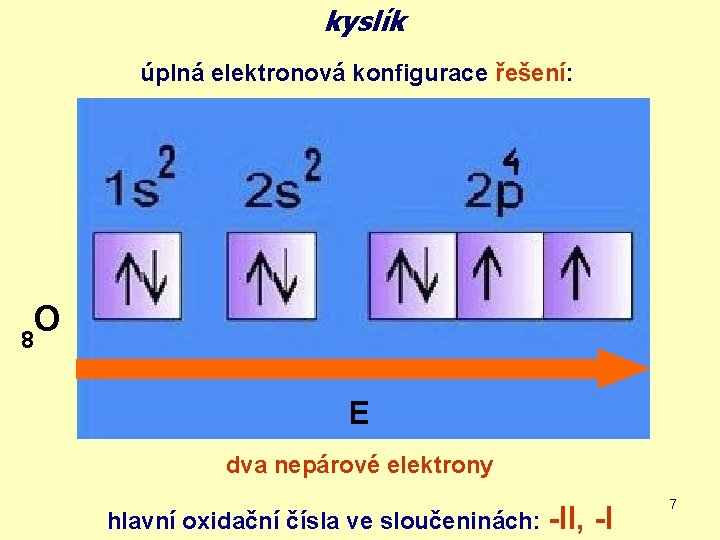
kyslík úplná elektronová konfigurace řešení: O 8 E dva nepárové elektrony hlavní oxidační čísla ve sloučeninách: -II, -I 7

historie přípravy kyslíku: obr. 1 Kyslík popsal jako první němec Carl Wilhelm Scheele v roce 1772 a pojmenoval jej „ohnivý vzduch“. 1779 A. Lavoisier navrhuje název „oxygen“ – neboli „kyselinu tvořící“, udržel se v latinském označení oxygenium. Český název kyslík navrhl Jan Svatopluk Presl. fyzikální vlastnosti kyslíku: Tt ≈ -219 °C, Tv ≈ -183 °C bez zápachu, bez chuti, nejedovatý, podporuje hoření, rozpustný ve vodě, hustota 1, 43 kg/m 3, součást atmosféry, tvoří 21 jejích objemových procent v podobě molekul O 2 (příp. O 3) 8 bezbarvý plyn za norm. podmínek,

kyslík příprava a důkaz kyslíku v laboratoři např. : 2 KMn. O 4 → O 2 + K 2 Mn. O 4 + Mn. O 2 2 KNO 3 → O 2 + 2 KNO 2 2 H 2 O 2 → O 2 + 2 H 2 O výroba kyslíku: destilace zkapalněného vzduchu: Metoda oddělování složek homogenní směsi (roztoku) na základě rozdílné teploty varu. dusík: Tv = -195, 7 °C kyslík: Tv = -183 °C argon: Tv = -186 °C 9

kyslík chemické vlastnosti např. reakce hliníku s O 2 doplň: O 2 + Al → 10

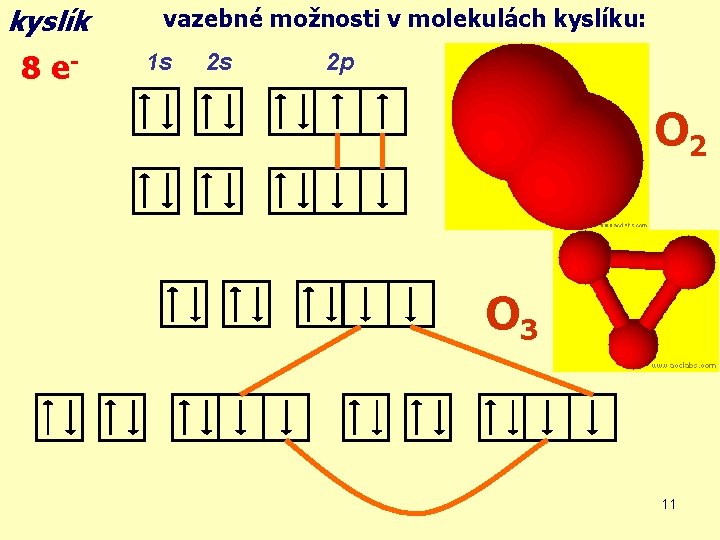
kyslík 8 e- vazebné možnosti v molekulách kyslíku: 1 s 2 s 2 p O 2 O 3 11

kyslík ! výrazné oxidační účinky ! doplň reakce úplných oxidací (hoření): O 2 + Al → 3 O 2 + 4 Al → 2 Al 2 O 3 O 2 + C → CO 2 + Fe → 3 O 2 + 4 Fe → 2 Fe 2 O 3 O 2 + Li → O 2 + 4 Li → 2 Li 2 O O 2 + Na → 2 Na + O 2 → Na 2 O 2 + S → SO 2 12

obr 1. (29. 10. 2012), autor: neznámý: http: //commons. wikimedia. org/wiki/File: PSM_V 31_D 740_Carl_Wilhelm_Scheele. jpg