International Union of Pure and Applied Chemistry Sociedade






























- Slides: 64


International Union of Pure and Applied Chemistry Sociedade Portuguesa de Química Guia IUPAC para a Nomenclatura de Compostos Orgânicos Tradução Portuguesa nas Variantes Europeia e Brasileira LIDE L Red = > 1860 hits per million population. Orange = 465 -1860 hits per million population. Yellow = 143 -465 hits per million population. Green = 31. 7 -143 hits per million population. Blue = 4. 53 -31. 7 hits per million population. Violet = < 4. 53 hits per million population.

FUNÇÕES ORG NICAS • Cada função orgânica é caracterizada por um grupo funcional. • A nomenclatura oficial é desenvolvida pela IUPAC (União Internacional de Química Pura e Aplicada). • Algumas substâncias ainda são identificadas por nomes consagrados (nomenclatura usual). • A IUPAC leva em consideração o número de carbonos, os tipos de ligações e a função a que pertencem.

Os Hidrocarbonetos • Alifáticos • Aromáticos

Hidrocarbonetos > Alifáticos > Alcanos • Formula geral: – Cadeia aberta – Cn. H 2 n+2 – Cíclicos – Cn. H 2 n • Estrutura - Todas as ligações são simples • Nomenclatura – Sufixo – ano – No caso dos compostos cíclicos o nome deverá ser antecedido pela palavra ciclo

Nomenclatura IUPAC l A nomenclatura orgânica oficial começou a ser criada em 1892 em um congresso internacional em Genebra, após várias reuniões surgiu a nomenclatura IUPAC (União Internacional de Química Pura e Aplicada). A nomenclatura IUPAC obedece aos seguintes princípios: I. Cada composto tenha um único nome que o distinga dos demais; II. Dada a fórmula estrutural de um composto, seja possível elaborar seu nome, e vice-versa. l l Obs. : Apesar de a nomenclatura IUPAC ser a oficial, existem outros tipos de nomenclatura como por exemplo a nomenclatura usual.

Nomenclatura dos Compostos Orgânicos Regras para nomear compostos Nomenclatura de Hidrocarbonetos

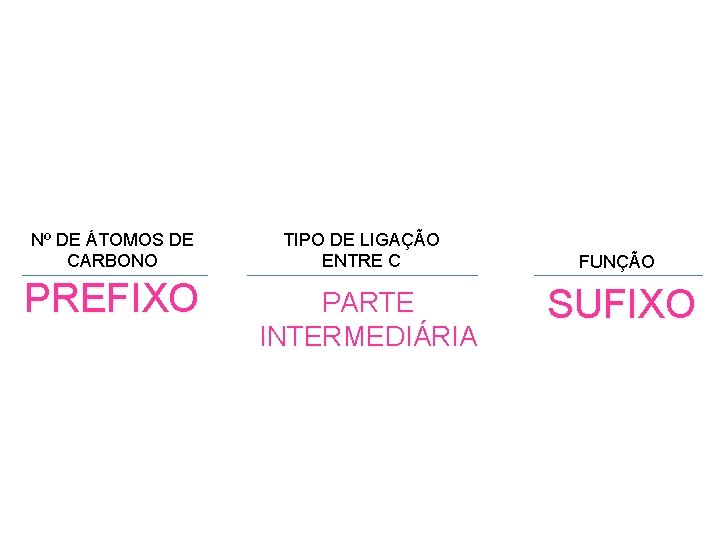
Primeiras noções de Nomenclatura Estrutura dos Nome: é formado por três partes: l Prefixo – diz o número de carbonos l Parte intermediária – diz o tipo de ligação l Sufixo – diz a função orgânica Número de C 1 2 3 4 5 6 7 8 9 Prefixo Número de Ligações Simples Dupla Tripla Dupla+Dupla Nome MET ET PROP BUT PENT HEX HEPT OCT NON Nome AN EN IN DIEN Parte intermediária Grupo Funcional Hidrocarboneto Álcool Cetona Adeído Sufixo Fenol Éteres Ac. Carboxílicos Éteres Amina Amida. . . Nome O OL ONA AL HIDROXI ATO de Radical ÁC. ___ ÓICO ETER ___ICO AMINA AMIDA. . .

Nº DE ÁTOMOS DE CARBONO PREFIXO TIPO DE LIGAÇÃO ENTRE C PARTE INTERMEDIÁRIA FUNÇÃO SUFIXO

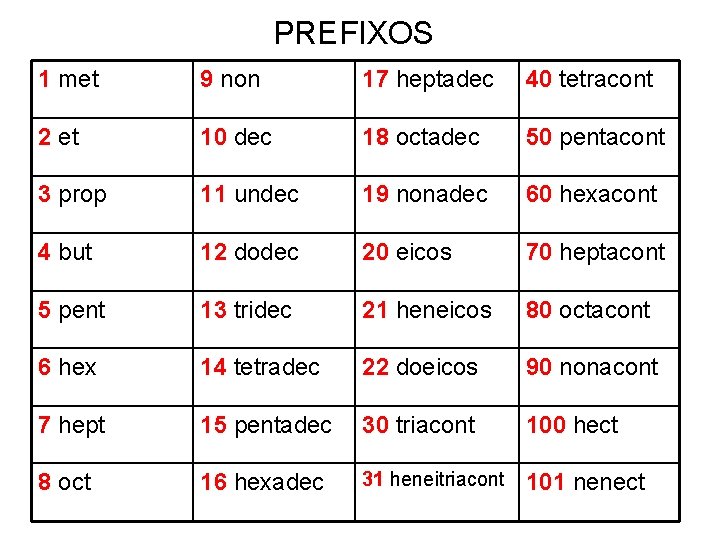
PREFIXOS 1 met 9 non 17 heptadec 40 tetracont 2 et 10 dec 18 octadec 50 pentacont 3 prop 11 undec 19 nonadec 60 hexacont 4 but 12 dodec 20 eicos 70 heptacont 5 pent 13 tridec 21 heneicos 80 octacont 6 hex 14 tetradec 22 doeicos 90 nonacont 7 hept 15 pentadec 30 triacont 100 hect 8 oct 16 hexadec 31 heneitriacont 101 nenect

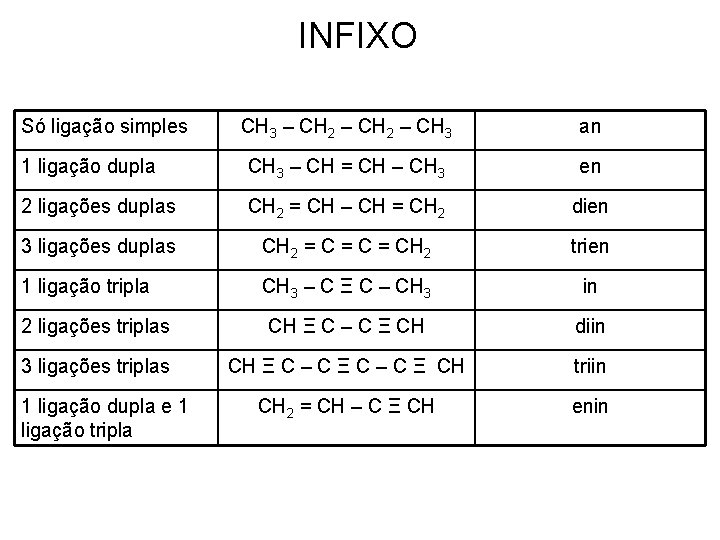
INFIXO Só ligação simples CH 3 – CH 2 – CH 3 an 1 ligação dupla CH 3 – CH = CH – CH 3 en 2 ligações duplas CH 2 = CH – CH = CH 2 dien 3 ligações duplas CH 2 = C = CH 2 trien 1 ligação tripla CH 3 – C Ξ C – CH 3 in 2 ligações triplas CH Ξ C – C Ξ CH diin 3 ligações triplas CH Ξ C – C Ξ CH triin CH 2 = CH – C Ξ CH enin 1 ligação dupla e 1 ligação tripla

RESUMIDAMENTE: PREFIXO 1 C 2 C 3 C 4 C 5 C 6 C 7 C 8 C 9 C 10 C 11 C 12 C MET ET PROP BUT PENT HEX HEPT OCT NON DEC UNDEC DODEC PARTE INTERMEDIÁRIA SATURADA AN INSATURADAS: 1 DUPLA EN 2 DUPLAS DIEN 3 DUPLAS TRIEN 1 TRIPLA IN 2 TRIPLAS DIIN 3 TRIPLAS TRIIN 1 DUPLA E 1 TRIPLA SUFIXO HIDROCARBONETO ÁLCOOL OL ALDEÍDO AL CETONA ÁCIDO CARBOXÍLICO ENIN O ÓICO

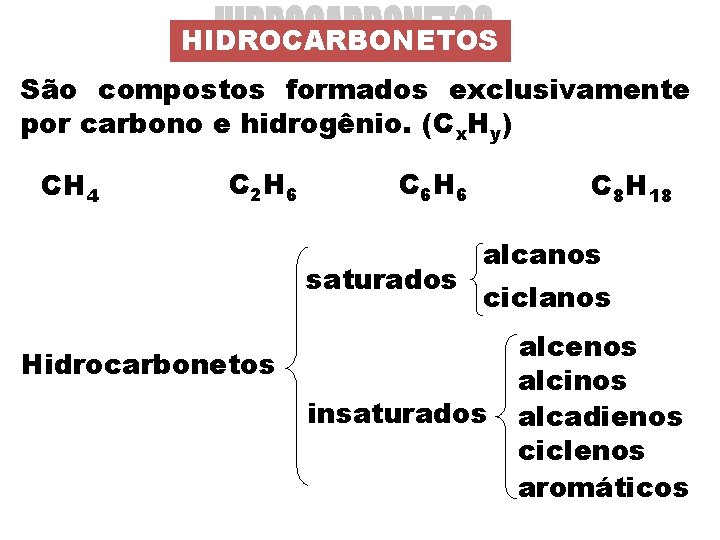
HIDROCARBONETOS São compostos formados exclusivamente por carbono e hidrogênio. (Cx. Hy) CH 4 C 2 H 6 C 6 H 6 saturados C 8 H 18 alcanos ciclanos Hidrocarbonetos insaturados alcenos alcinos alcadienos ciclenos aromáticos

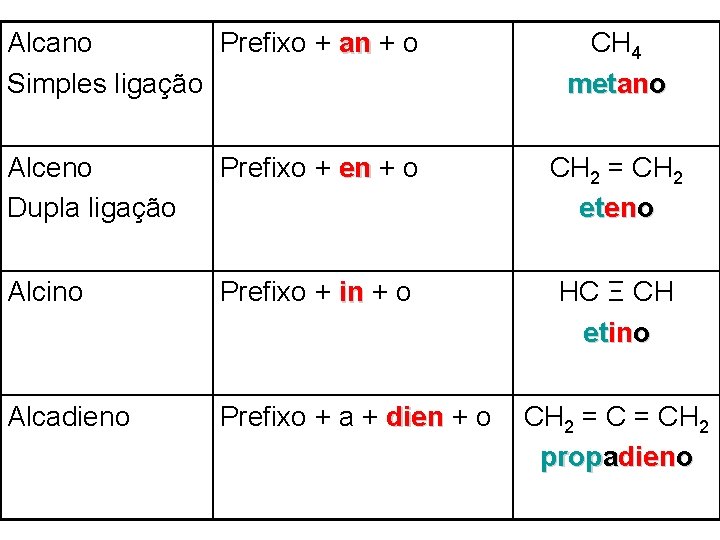
Alcano Prefixo + an + o Simples ligação CH 4 metano Alceno Dupla ligação Prefixo + en + o CH 2 = CH 2 eteno Alcino Prefixo + in + o HC Ξ CH etino Alcadieno Prefixo + a + dien + o CH 2 = CH 2 propadieno

HIDROCARBONETOS • ALCANOS ou parafinas (parum=pequena + affinis=afinidade). São hidrocarbonetos alifáticos saturados. Relatórios da ONU apontam “ emissões bovinas” são perigosas ao planeta. Metano tem efeito de aquecimento 24 vezes maior que o gás carbônico.

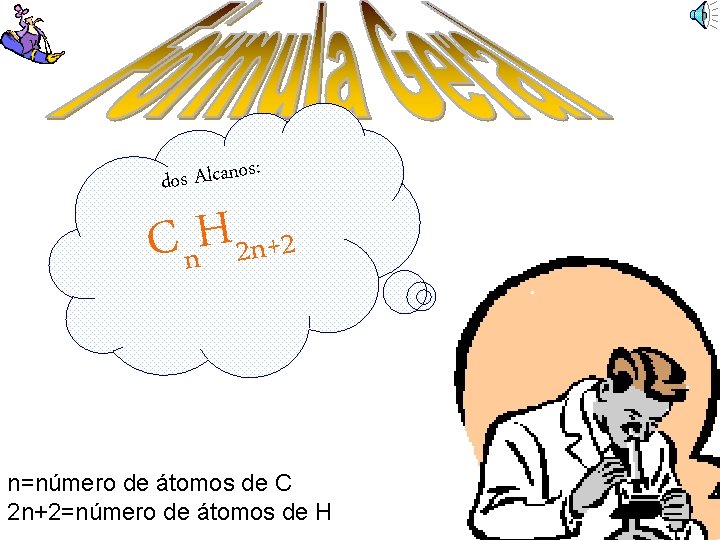
: s o n a c l A s o d C n. H 2 n+2 n=número de átomos de C 2 n+2=número de átomos de H

Nomenclatura para Hidrocarbonetos de cadeia normal 1. Ligações Simples - ALCANOS Nome - Fórmula Molecular Fórmula Estrutural Condensada Metano - CH 4 Etano - C 2 H 6 CH 3 – CH 3 Propano - C 3 H 8 CH 3 – CH 2 – CH 3 Butano - C 4 H 10 CH 3 – CH 2 – CH 3 Pentano - C 5 H 12 CH 3 – CH 2 – CH 3 Hexano - C 6 H 14 CH 3 – CH 2 – CH 3 Heptano - C 7 H 16 CH 3 – CH 2 – CH 2 – CH 3 Fórmula Geral: Cn. H 2 n+2 l Obs: molécula de heptano, por exemplo: CH 3 – CH 2 – CH 2 – CH 3 pode também ser representada por : CH 3 – (CH 2)5 – CH 3

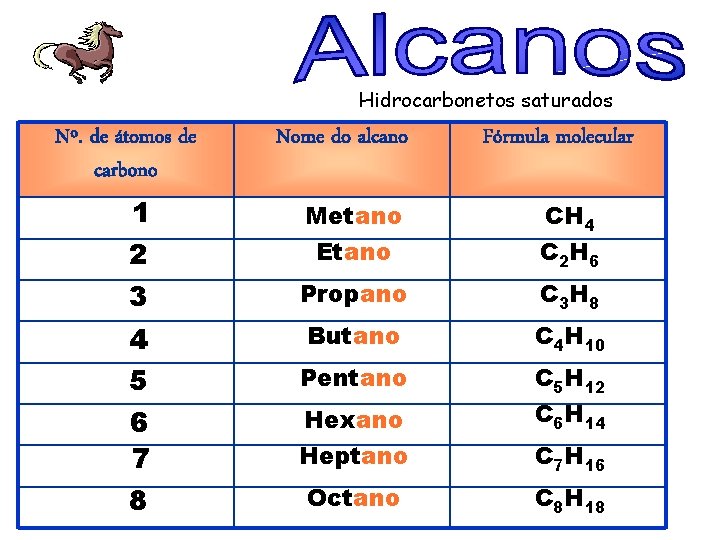
Hidrocarbonetos saturados Nº. de átomos de carbono Nome do alcano Fórmula molecular 1 2 Metano Etano CH 4 C 2 H 6 3 Propano C 3 H 8 4 5 6 7 8 Butano C 4 H 10 Pentano Hexano C 5 H 12 C 6 H 14 Heptano C 7 H 16 Octano C 8 H 18

1º exemplo H 3 C – CH 2 – CH 2 – CH 3 Prefixo: número de carbonos – 7 – HEPT Parte intermediária: tipo de ligação – simples – AN Sufixo: função – hidrocarboneto - O

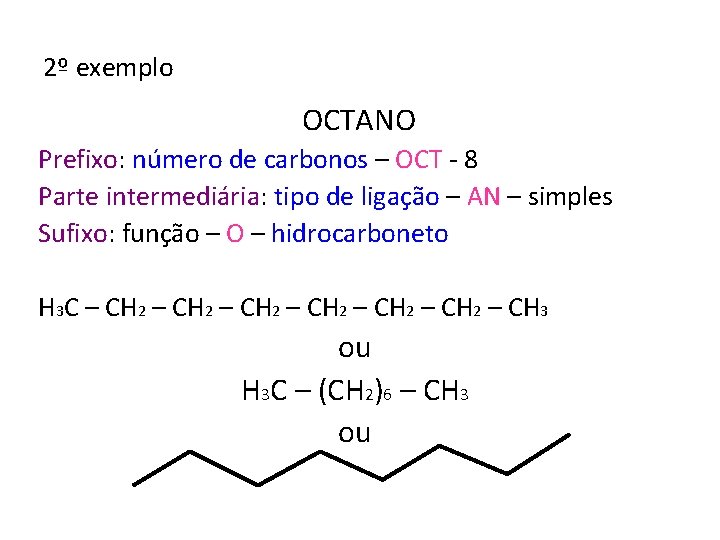
2º exemplo OCTANO Prefixo: número de carbonos – OCT - 8 Parte intermediária: tipo de ligação – AN – simples Sufixo: função – O – hidrocarboneto H 3 C – CH 2 – CH 2 – CH 3 ou H 3 C – (CH 2)6 – CH 3 ou

Nomenclatura de hidrocarbonetos ramificados

RADICAIS ALQUILAS São radicais monovalentes, derivados alcanos.

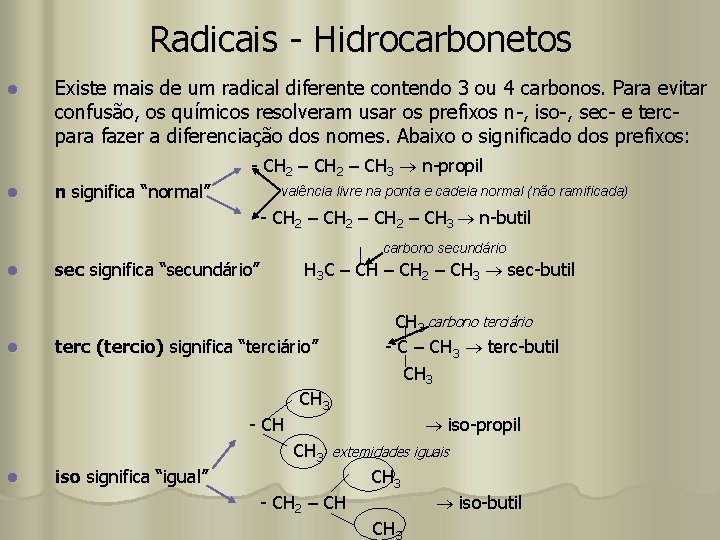
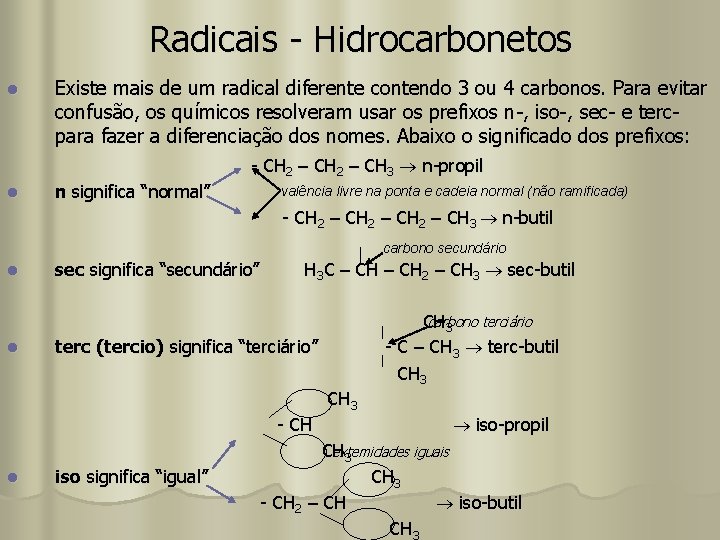
Radicais - Hidrocarbonetos l Existe mais de um radical diferente contendo 3 ou 4 carbonos. Para evitar confusão, os químicos resolveram usar os prefixos n-, iso-, sec- e tercpara fazer a diferenciação dos nomes. Abaixo o significado dos prefixos: - CH 2 – CH 3 n-propil l n significa “normal” valência livre na ponta e cadeia normal (não ramificada) - CH 2 – CH 3 n-butil carbono secundário l l sec significa “secundário” H 3 C – CH 2 – CH 3 sec-butil terc (tercio) significa “terciário” CH 3 carbono terciário - C – CH 3 terc-butil CH 3 - CH l iso significa “igual” iso-propil CH 3 extemidades iguais CH 3 - CH 2 – CH iso-butil CH 3

Radicais - Hidrocarbonetos l Existe mais de um radical diferente contendo 3 ou 4 carbonos. Para evitar confusão, os químicos resolveram usar os prefixos n-, iso-, sec- e tercpara fazer a diferenciação dos nomes. Abaixo o significado dos prefixos: - CH 2 – CH 3 n-propil l n significa “normal” valência livre na ponta e cadeia normal (não ramificada) - CH 2 – CH 3 n-butil carbono secundário l l sec significa “secundário” H 3 C – CH 2 – CH 3 sec-butil carbono terciário CH 3 - C – CH 3 terc-butil CH 3 terc (tercio) significa “terciário” CH 3 - CH l iso significa “igual” iso-propil extemidades iguais CH 3 - CH 2 – CH iso-butil CH 3

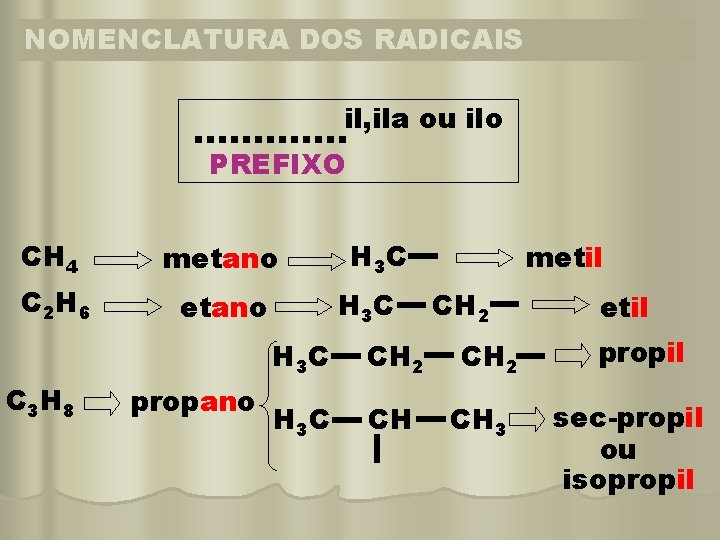
NOMENCLATURA DOS RADICAIS il, ila ou ilo PREFIXO CH 4 metano C 2 H 6 etano C 3 H 8 propano H 3 C CH 2 H 3 C CH metil CH 2 CH 3 etil propil sec-propil ou isopropil

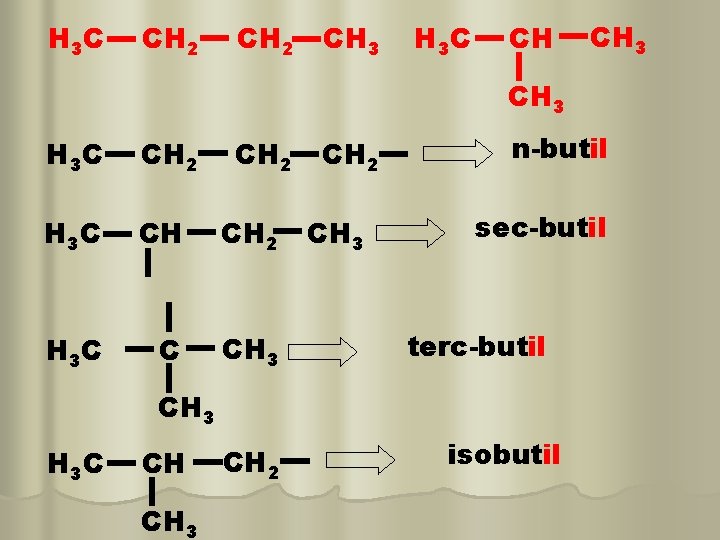
H 3 C CH 2 CH 3 H 3 C CH CH 3 H 3 C CH 2 H 3 C CH CH 2 H 3 C C CH 3 CH 2 CH 3 n-butil sec-butil terc-butil CH 3 H 3 C CH CH 3 CH 2 isobutil

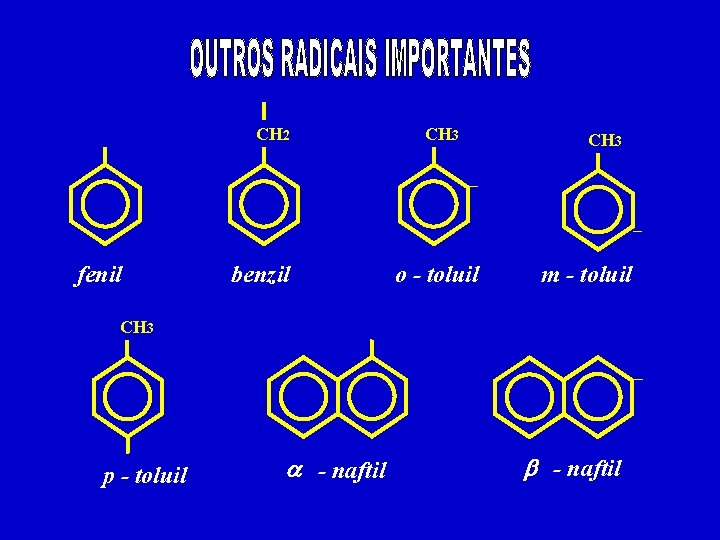
CH 2 CH 3 – – fenil benzil o - toluil m - toluil CH 3 – p - toluil a - naftil b - naftil

Regras para Nomenclatura dos alcanos 1. Determinar a cadeia principal Apresenta maior número de carbonos A cadeia mais ramificada A cadeia de radicais menos complexos 2. Numerar a cadeia As ramificações recebem o menor número possível 3. Nomear o composto citando os radicais ramificados em ordem alfabética precedidos e separados por hífen pelo número onde eles ocorrem, finalizando com o acréscimo do nome correspondente à cadeia principal.

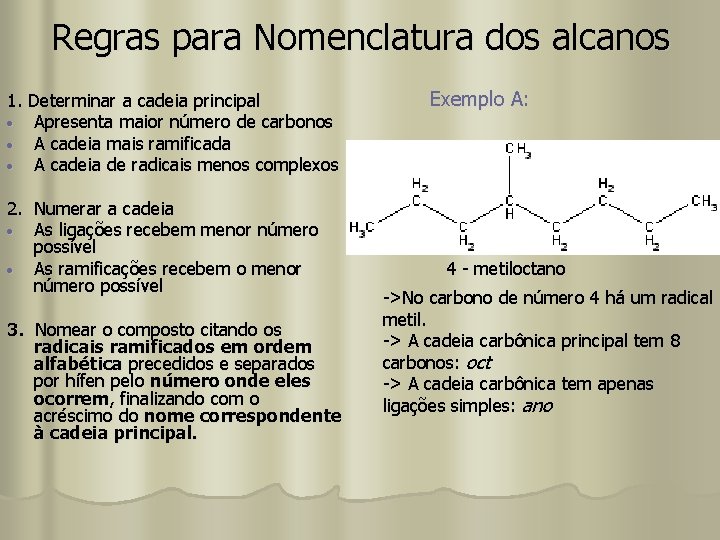
Regras para Nomenclatura dos alcanos 1. Determinar a cadeia principal Apresenta maior número de carbonos A cadeia mais ramificada A cadeia de radicais menos complexos 2. Numerar a cadeia As ligações recebem menor número possível As ramificações recebem o menor número possível 3. Nomear o composto citando os radicais ramificados em ordem alfabética precedidos e separados por hífen pelo número onde eles ocorrem, finalizando com o acréscimo do nome correspondente à cadeia principal. Exemplo A: 4 - metiloctano ->No carbono de número 4 há um radical metil. -> A cadeia carbônica principal tem 8 carbonos: oct -> A cadeia carbônica tem apenas ligações simples: ano

Regras para Nomenclatura dos alcanos 1. Determinar a cadeia principal Apresenta maior número de carbonos A cadeia mais ramificada A cadeia de radicais menos complexos 2. Numerar a cadeia As ligações recebem menor número possível As ramificações recebem o menor número possível 3. Nomear o composto citando os radicais ramificados em ordem alfabética precedidos e separados por hífen pelo número onde eles ocorrem, finalizando com o acréscimo do nome correspondente à cadeia principal. Exemplo B: CH 3 | CH 3 – CH 2 – CH 3 | | CH 3 2, 3, 3 -Trimetil Pentano -> No carbono 2 há radical metil e no carbono 3 há dois radicais metil: 2, 3, 3 – -> Como são três radicais metil na cadeia, nomeamos: trimetil -> A cadeia carbônica principal tem 5 carbonos: pent -> Só há ligações simples entre os carbonos: ano

Regras para Nomenclatura dos alcanos 1. Determinar a cadeia principal Apresenta maior número de carbonos A cadeia mais ramificada A cadeia de radicais menos complexos 2. Numerar a cadeia As ligações recebem menor número possível As ramificações recebem o menor número possível 3. Nomear o composto citando os radicais ramificados em ordem alfabética precedidos e separados por hífen pelo número onde eles ocorrem, finalizando com o acréscimo do nome correspondente à cadeia principal. Exemplo C: CH 3 – CH 2 – CH 3 | | CH 2 | | CH 3 3, 5 -dimetil Heptano -> No carbono 3 há radical metil e no carbono 5 também há um radical metil: 3, 5 -> Como são dois radicais metil na cadeia, nomeamos: dimetil -> A cadeia carbônica principal tem 7 carbonos: hept -> Só há ligações simples entre os carbonos: ano

Regras para Nomenclatura dos alcanos 1. Determinar a cadeia principal Comporta todas as ligações necessárias (duplas ou triplas) Apresenta maior número de carbonos A cadeia mais ramificada A cadeia de radicais menos complexos 2. Numerar a cadeia As ligações recebem menor número possível As ramificações recebem o menor número possível 3. Nomear o composto citando os radicais ramificados em ordem crescente de complexibilidade precedidos e separados por hífen pelo número onde eles ocorrem, finalizando com o acréscimo do nome correspondente à cadeia principal Exemplo D: CH 3 – CH 3 | | CH 3 2, 3 -dimetil butano -> No carbono 2 há radical metil e no carbono 3 também há um radical metil: 2, 3 -> Como são dois radicais metil na cadeia, nomeamos: dimetil -> A cadeia carbônica principal tem 4 carbonos: but -> Só há ligações simples entre os carbonos: ano Nomenclatura dos Compostos Orgânicos

l Vamos aplicar as regras!

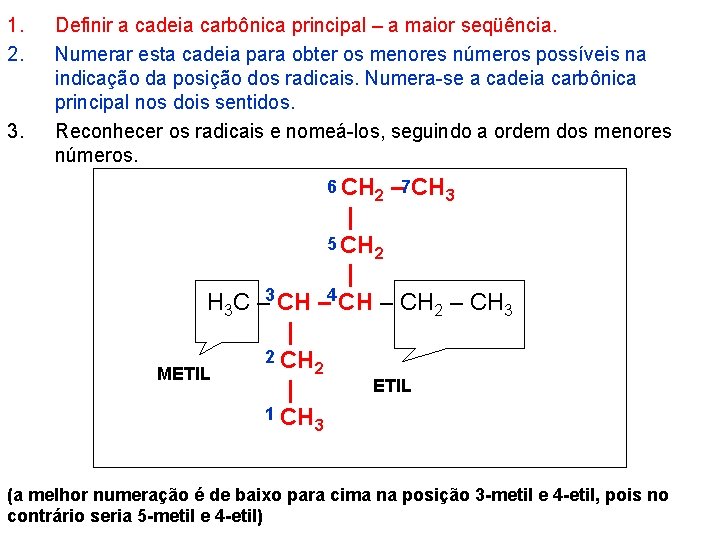
1. 2. 3. Definir a cadeia carbônica principal – a maior seqüência. Numerar esta cadeia para obter os menores números possíveis na indicação da posição dos radicais. Numera-se a cadeia carbônica principal nos dois sentidos. Reconhecer os radicais e nomeá-los, seguindo a ordem dos menores números. 6 CH 2 – 7 CH 3 | 5 CH 2 | H 3 C – 3 CH – 4 CH – CH 2 – CH 3 | 2 CH 2 METIL | 1 CH 3 (a melhor numeração é de baixo para cima na posição 3 -metil e 4 -etil, pois no contrário seria 5 -metil e 4 -etil)

O nome correto e completo do alcano ramificado deverá apresentar, nesta ordem: As posições numéricas ocupadas pelos radicais Os nomes dos radicais O nome da cadeia principal Entre número e nome separa-se por hífen Entre número separa-se por vírgula Para os radicais diferentes a IUPAC recomenda que sejam escritos em ordem alfabética, sendo que os prefixos sec, terc, di, tri, . . . NÃO são considerados para efeito de ordem alfabética. No Brasil costuma-se escrever o nome dos radicais em ordem crescente de complexidade. O nome do último –R deve vir ligado ao nome da cadeia principal. Para os radicais iguais, os nomes destes devem vir todos juntos e precedidos de prefixo que indicam quantidades: di, tri, tetra, etc. Quando, numa estrutura, duas ou mais cadeias carbônicas tiverem o mesmo número máximo de C, será considerada a cadeia principal, aquela que tiver maior número de ramificações. Assim sendo o nome do alcano é: em ordem alfabética: 4 -etil-3 -metileptano ou 4 -etil-3 -metil-heptano em ordem crescente: 3 -metil-4 -etileptano ou 3 -metil-4 -etil-heptano (ordem complexidade)

Cadeias saturadas : Se a cadeia for saturada (contenha somente ligações simples), inicie pela extremidade mais próxima da ramificação. Se houver mais que uma ramificação, inicie pela extremidade que permita dar as ramificações os menores números possíveis. Ex: 1 2 3 4 5 6 (correto, as ramificações estão nos C (2, 3) H 3 C—CH—CH—CH 2 — CH 3 6 5 4 CH 3 3 2 1 (errado, as ramificações estão nos C(4, 5) Essa regra chama-se : REGRA DOS MENORES NÚMEROS.

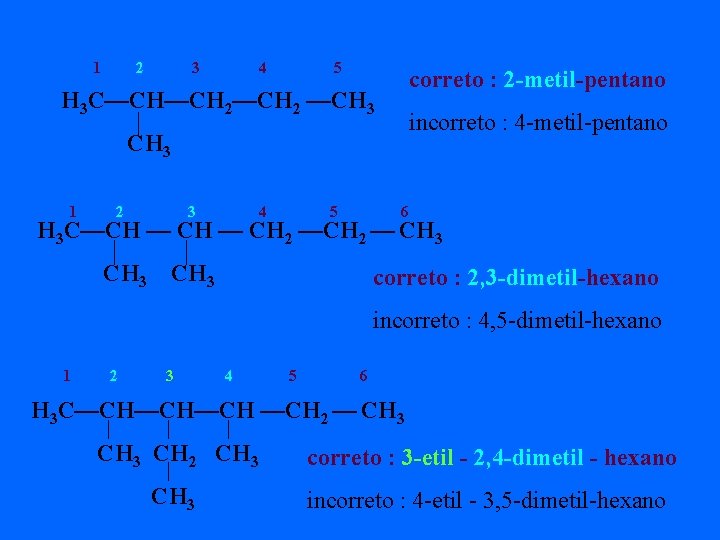
1 2 3 4 5 correto : 2 -metil-pentano H 3 C—CH—CH 2 —CH 3 incorreto : 4 -metil-pentano CH 3 1 2 3 4 5 6 H 3 C—CH — CH 2 — CH 3 correto : 2, 3 -dimetil-hexano incorreto : 4, 5 -dimetil-hexano 1 2 3 4 5 6 H 3 C—CH—CH—CH 2 — CH 3 CH 2 CH 3 correto : 3 -etil - 2, 4 -dimetil - hexano CH 3 incorreto : 4 -etil - 3, 5 -dimetil-hexano

No ISOOCTANO, molécula da gasolina, cuja índice de octanagem tem valor 100, e é considerado uma gasolina de ótima qualidade. Agora podemos dar o nome oficial para o ISOOCTANO. 1 CH 3 2 3 4 5 H 3 C—C—CH 2—CH 3 Regra dos menores números – A soma das posições dos grupos orgânicos ou insaturações, devem ser as menores possíveis. 2, 2, 4 -trimetil-pentano (correto, pois 2 + 4 = 8) 2, 4, 4 -trimetil-pentano (incorreto, pois 2 + 4 = 10)

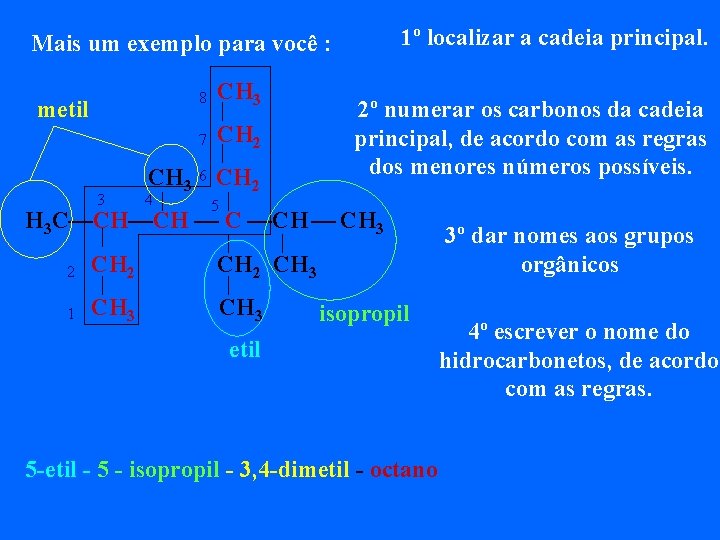
1º localizar a cadeia principal. Mais um exemplo para você : metil 3 8 CH 3 7 CH 2 CH 3 6 CH 2 4 2º numerar os carbonos da cadeia principal, de acordo com as regras dos menores números possíveis. 5 H 3 C—CH—CH — CH 3 2 CH 3 1 CH 3 isopropil etil 5 -etil - 5 - isopropil - 3, 4 -dimetil - octano 3º dar nomes aos grupos orgânicos 4º escrever o nome do hidrocarbonetos, de acordo com as regras.

Observe atentamente os dois compostos abaixo, com seus respectivos nomes oficiais, segundo as regras. 1 2 3 4 5 H 3 C—CH—CH 2 —CH 3 1 2 2 -metil-pentano Grupo - metil 3 4 5 6 H 3 C—CH—CH—CH 2 — CH 3 3 - etil-2, 4 -dimetil -hexano CH 3 CH 2 CH 3 Grupos - metil Grupo - etil

Quais as possibilidades ? Lembrando que cadeia principal é a maior seqüência de carbonos. H 3 C—CH—CH 2 —CH 3 A cadeia principal tem 5 carbonos, e tem 1 grupo orgânico fora da cadeia principal 1ª possibilidade – 3 carbonos 2ª possibilidade – 5 carbonos 3ª possibilidade – 5 carbonos No caso de 2 cadeias serem igualmente longas, será a principal aquela de deixar para fora o maior número de grupos orgânicos. Se ambas forem iguais, nesse caso tanto faz, qual será a cadeia principal.

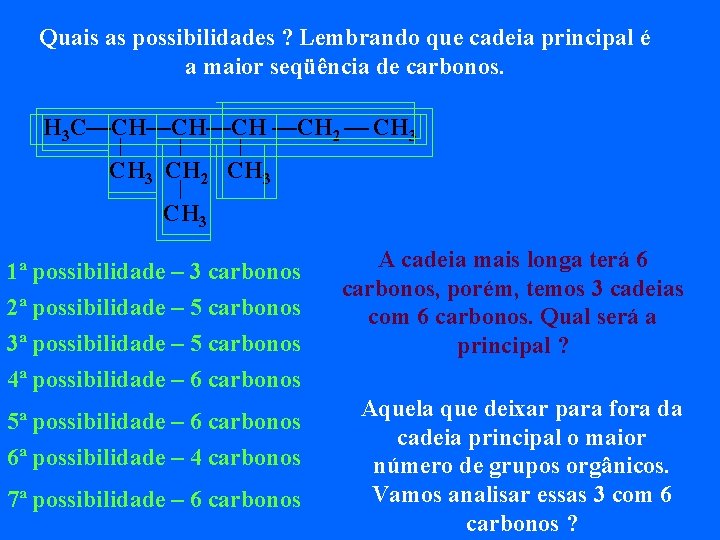
Quais as possibilidades ? Lembrando que cadeia principal é a maior seqüência de carbonos. H 3 C—CH—CH—CH 2 — CH 3 CH 2 CH 3 1ª possibilidade – 3 carbonos 2ª possibilidade – 5 carbonos 3ª possibilidade – 5 carbonos 4ª possibilidade – 6 carbonos 5ª possibilidade – 6 carbonos 6ª possibilidade – 4 carbonos 7ª possibilidade – 6 carbonos A cadeia mais longa terá 6 carbonos, porém, temos 3 cadeias com 6 carbonos. Qual será a principal ? Aquela que deixar para fora da cadeia principal o maior número de grupos orgânicos. Vamos analisar essas 3 com 6 carbonos ?

H 3 C—CH—CH—CH 2 — CH 3 CH 2 CH 3 • A primeira opção, deixa para fora três grupos orgânicos • A segunda opção, também deixa para fora três grupos orgânicos • A terceira opção, deixa para fora dois grupos orgânicos Portanto a cadeia principal será a primeira ou segunda opção, pois ambas deixam para fora três grupos orgânicos.

2 - Quem vem primeiro na hora de escrever, Metil, etil ? ? ? Considere os grupos metil, etil e propil. Se estes grupos forem listados em ordem de complexidade (número de carbonos), teremos: Metil < propil Se forem listados em ordem alfabética, teremos : Etil < metil < propil Até 1979, a IUPAC, aceitava a duas formas para a colocação do nome dos grupos orgânicos relativas às ramificações: a ordem de complexidade ou a ordem alfabética. A partir daquele ano, julgando ser mais adequado como procedimento geral de nomenclatura a IUPAC, decidia que apenas a ordem alfabética deve ser empregada. No Brasil, tal regra não é muito difundida nos livros de Química, portanto poderemos adotar qualquer uma das formas como correta.

3 – Quando eu vou montar um composto a partir do nome, por onde começo a numerar os carbonos ? • Se você está montando o composto, você escolhe de que lado começar, porém uma vez iniciado por um extremidade, deverá sempre continuar pela mesma. Ex : 2, 3 -dimetil-hexano 1 2 3 4 5 6 H 3 C—CH — C — CH 3 Eu começei pela extremidade esquerda.

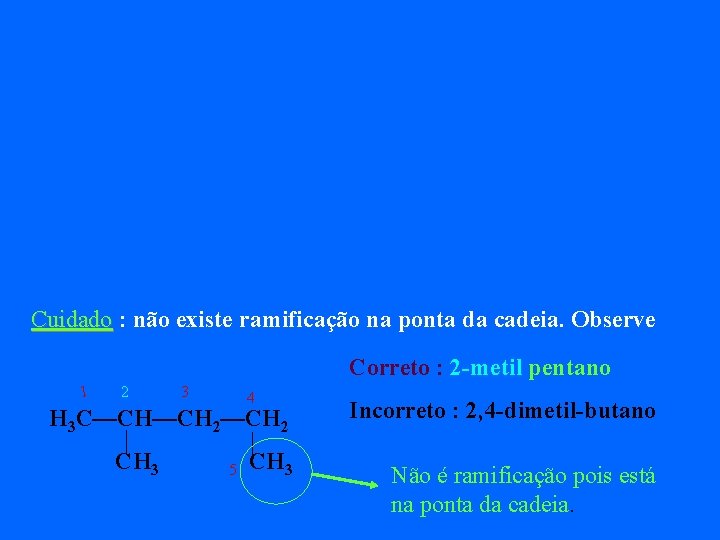
Cuidado : não existe ramificação na ponta da cadeia. Observe Correto : 2 -metil pentano 1 2 3 4 H 3 C—CH—CH 2 CH 3 5 CH 3 Incorreto : 2, 4 -dimetil-butano Não é ramificação pois está na ponta da cadeia.

• VAMOS A OUTROS EXEMPLOS!


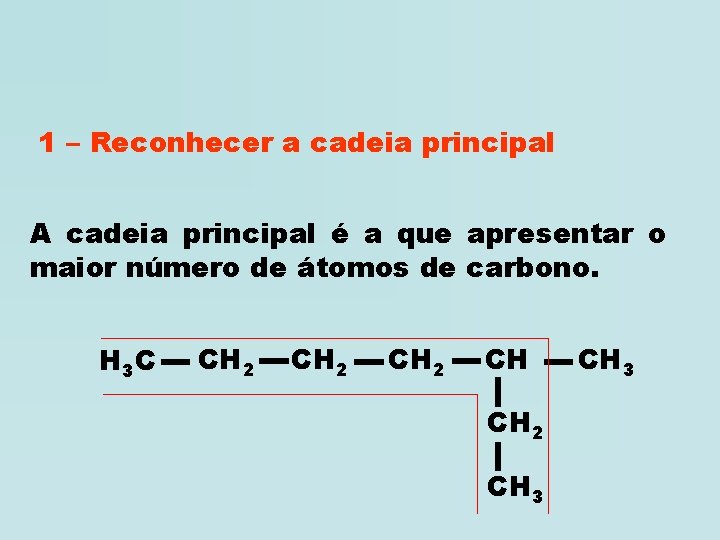
1 – Reconhecer a cadeia principal A cadeia principal é a que apresentar o maior número de átomos de carbono. H 3 C CH 2 CH 3

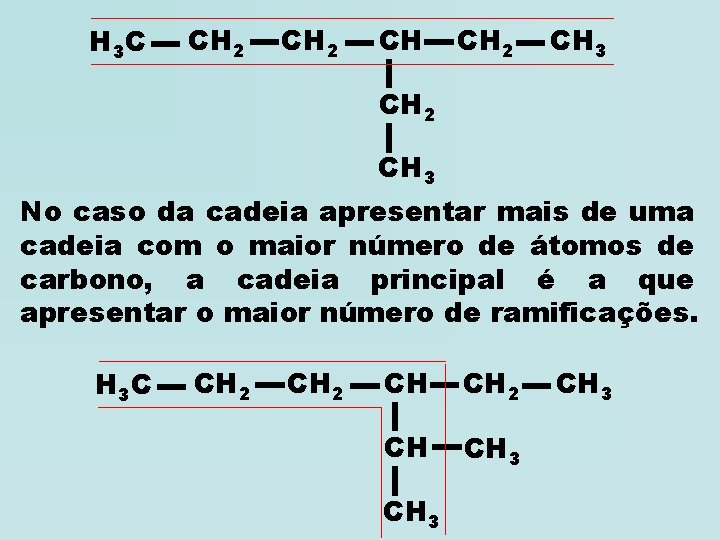
H 3 C CH 2 CH 3 No caso da cadeia apresentar mais de uma cadeia com o maior número de átomos de carbono, a cadeia principal é a que apresentar o maior número de ramificações. H 3 C CH 2 CH CH 3

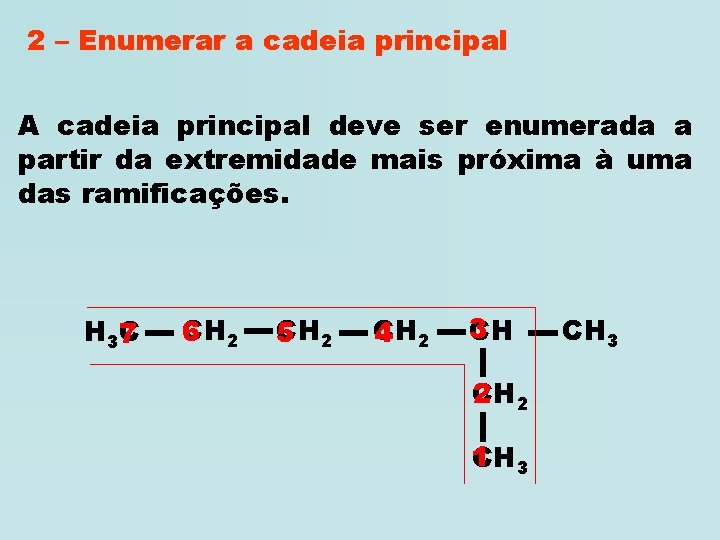
2 – Enumerar a cadeia principal A cadeia principal deve ser enumerada a partir da extremidade mais próxima à uma das ramificações. H 37 C CH 6 2 CH 5 2 CH 4 2 3 CH 2 2 CH 1 CH 3

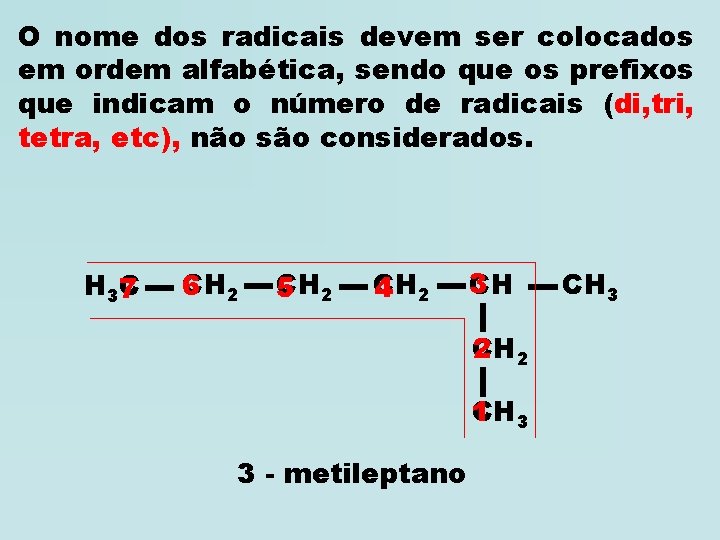
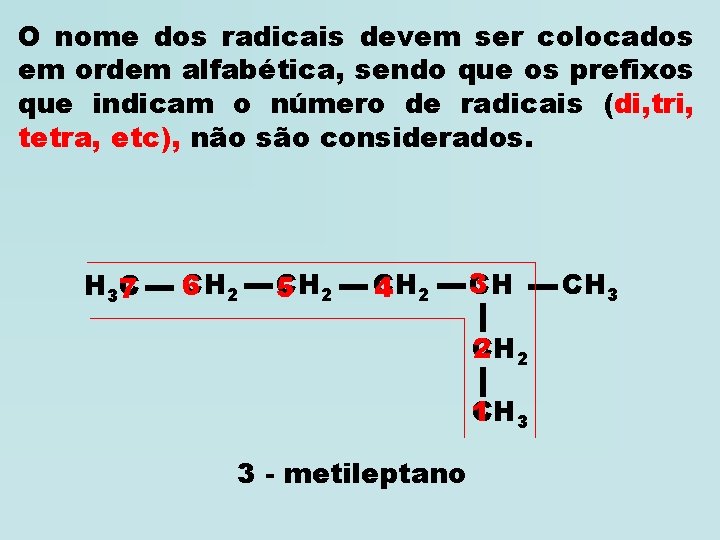
O nome dos radicais devem ser colocados em ordem alfabética, sendo que os prefixos que indicam o número de radicais (di, tri, tetra, etc), não são considerados. H 37 C CH 6 2 CH 5 2 CH 4 2 3 CH 2 2 CH 1 CH 3 3 - metileptano CH 3

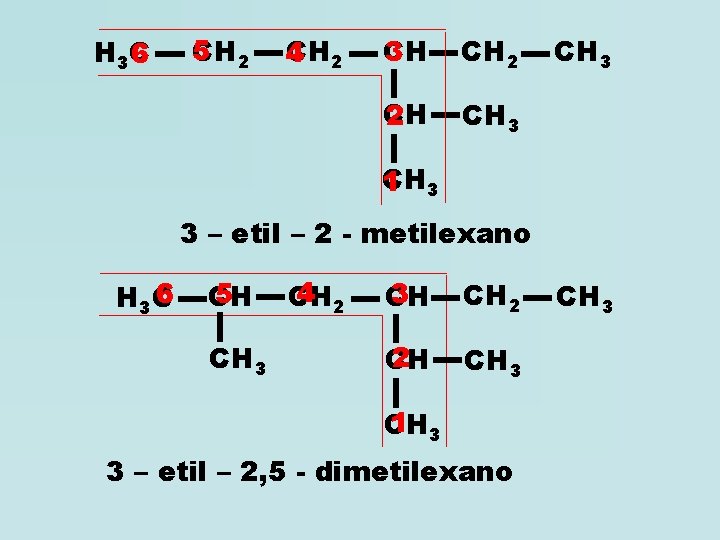
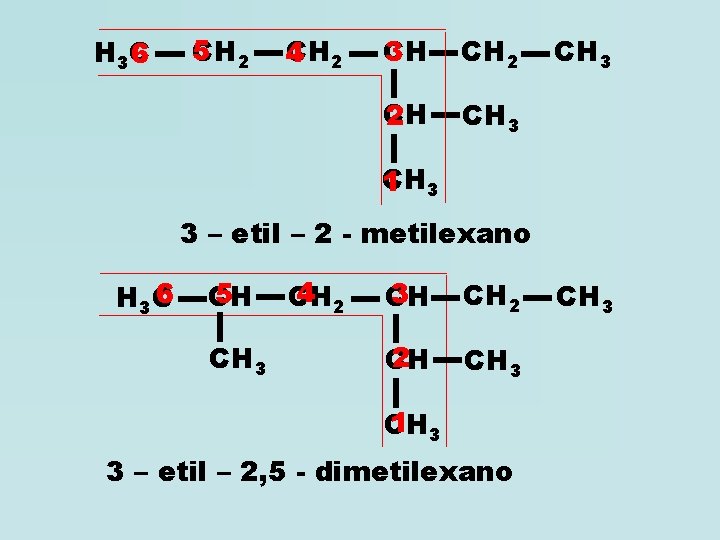
H 3 C 6 5 CH 2 4 3 CH CH 2 CH 3 CH 1 3 3 – etil – 2 - metilexano 6 H 3 C 5 CH CH 3 4 2 CH 3 CH CH 2 2 CH CH 3 1 3 CH 3 – etil – 2, 5 - dimetilexano CH 3

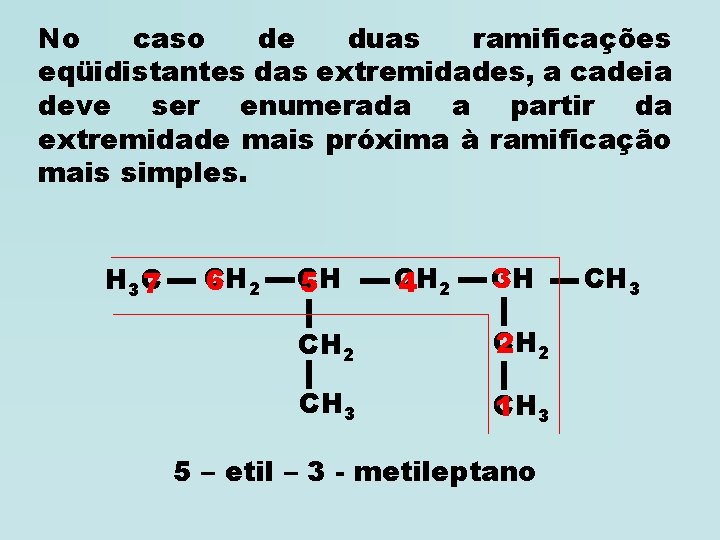
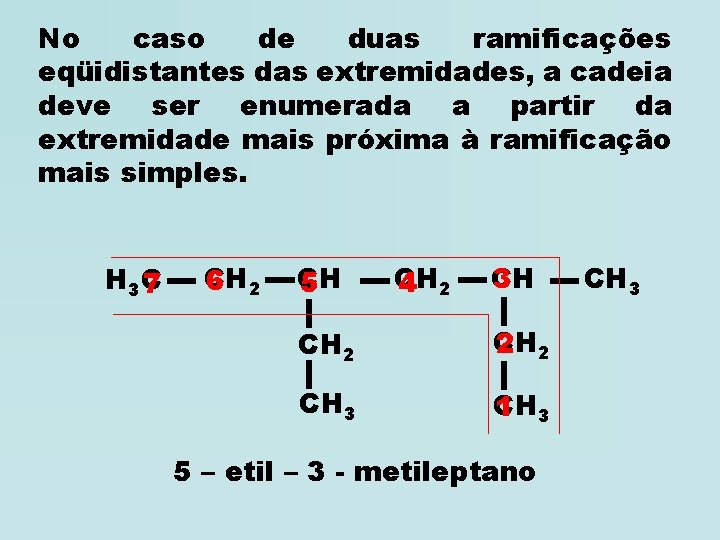
No caso de duas ramificações eqüidistantes das extremidades, a cadeia deve ser enumerada a partir da extremidade mais próxima à ramificação mais simples. H 3 C 7 CH 6 2 CH 5 CH 4 2 CH 3 CH 2 2 CH 3 CH 1 3 5 – etil – 3 - metileptano CH 3

3 – Dar nome ao alcano Primeiro damos o nome para as ramificações e em seguida o nome da cadeia principal. Antes do nome de cada ramificação, deve ser colocado o número do carbono da cadeia principal no qual a ramificação está ligada. No caso de um radical aparecer mais de uma vez, deve ser colocado antes do seu nome os prefixos di, tri, tetra, penta, etc, para indicar o número de radicais existentes.

O nome dos radicais devem ser colocados em ordem alfabética, sendo que os prefixos que indicam o número de radicais (di, tri, tetra, etc), não são considerados. H 37 C CH 6 2 CH 5 2 CH 4 2 3 CH 2 2 CH 1 CH 3 3 - metileptano CH 3

H 3 C 6 5 CH 2 4 3 CH CH 2 CH 3 CH 1 3 3 – etil – 2 - metilexano 6 H 3 C 5 CH CH 3 4 2 CH 3 CH CH 2 2 CH CH 3 1 3 CH 3 – etil – 2, 5 - dimetilexano CH 3

No caso de duas ramificações eqüidistantes das extremidades, a cadeia deve ser enumerada a partir da extremidade mais próxima à ramificação mais simples. H 3 C 7 CH 6 2 CH 5 CH 4 2 CH 3 CH 2 2 CH 3 CH 1 3 5 – etil – 3 - metileptano CH 3

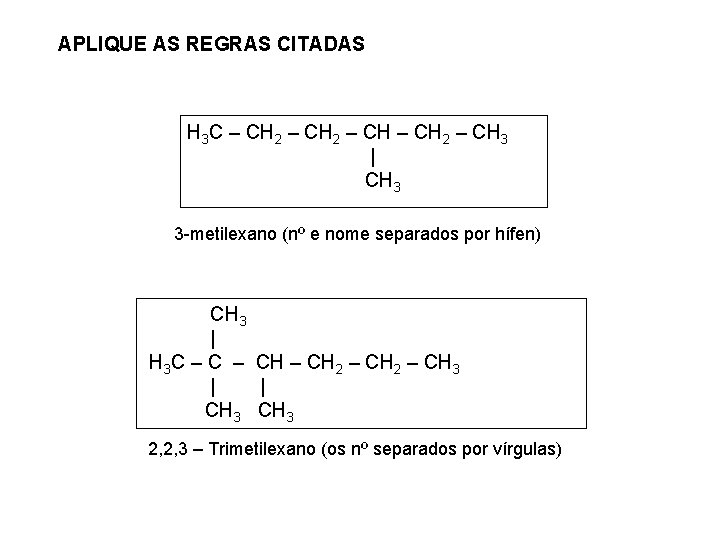
APLIQUE AS REGRAS CITADAS H 3 C – CH 2 – CH 3 | CH 3 3 -metilexano (nº e nome separados por hífen) CH 3 | H 3 C – CH 2 – CH 3 | | CH 3 2, 2, 3 – Trimetilexano (os nº separados por vírgulas)

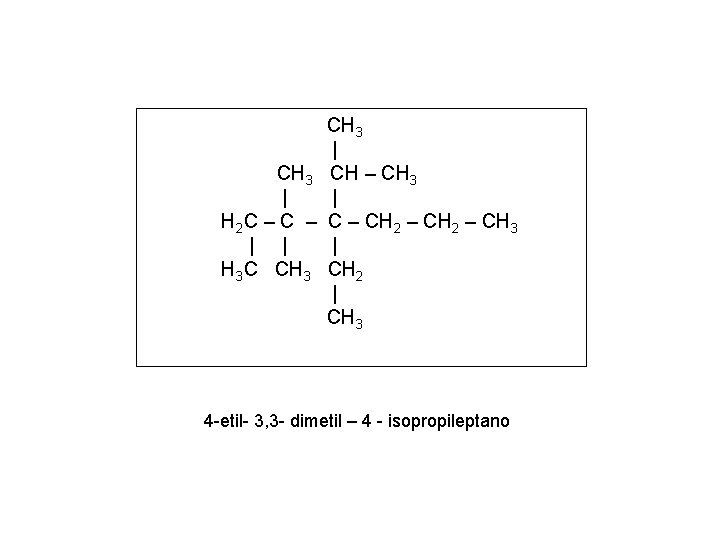
CH 3 | CH 3 CH – CH 3 | | H 2 C – C – CH 2 – CH 3 | | | H 3 C CH 3 CH 2 | CH 3 4 -etil- 3, 3 - dimetil – 4 - isopropileptano

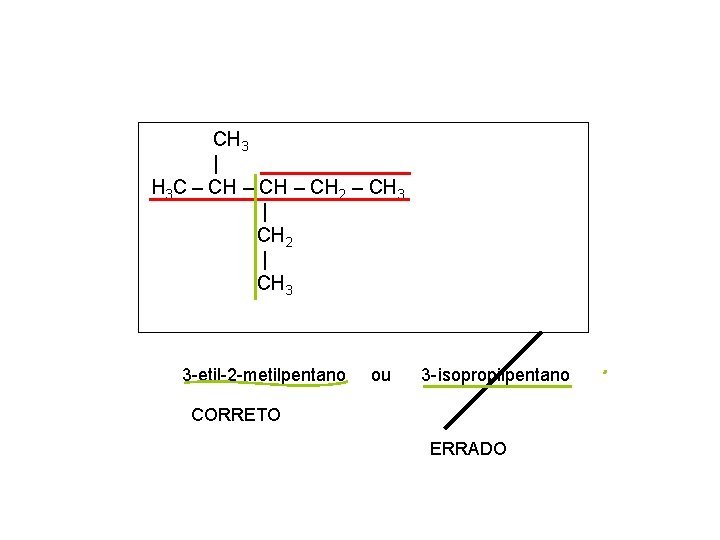
CH 3 | H 3 C – CH 2 – CH 3 | CH 2 | CH 3 3 -etil-2 -metilpentano ou 3 -isopropilpentano CORRETO ERRADO

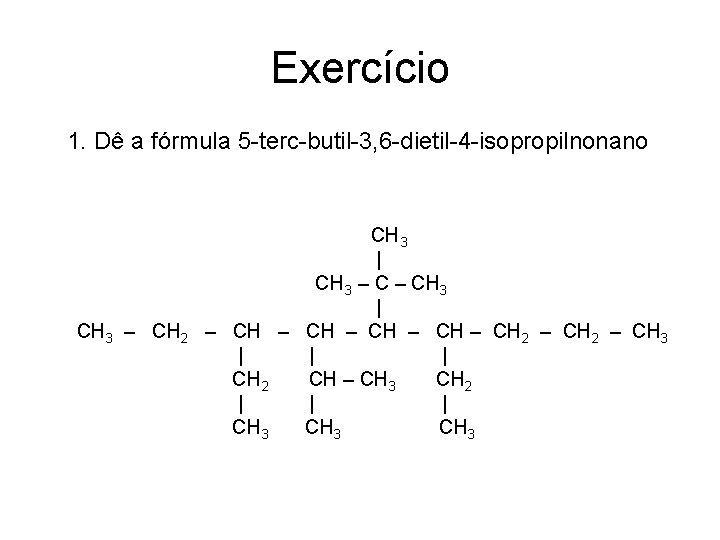
Exercício 1. Dê a fórmula 5 -terc-butil-3, 6 -dietil-4 -isopropilnonano CH 3 – CH 2 CH 3 | CH 3 – CH 3 | – CH – CH 2 – CH 3 | | | CH 2 CH – CH 3 CH 2 | | | CH 3

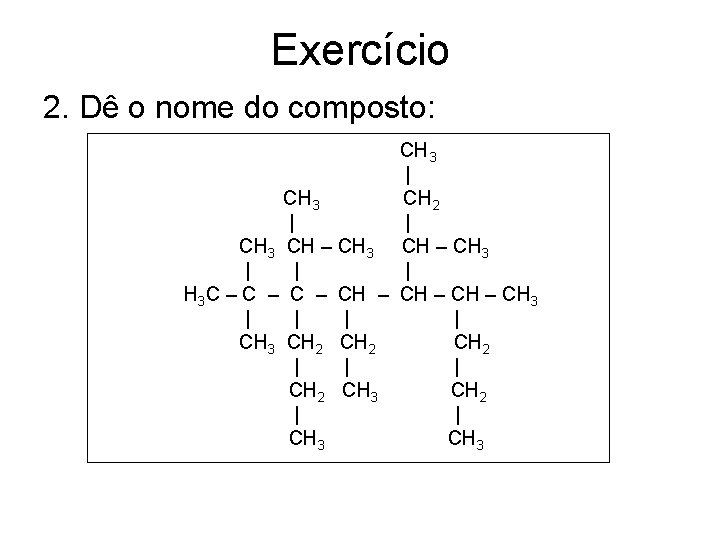
Exercício 2. Dê o nome do composto: CH 3 | CH 3 CH 2 | | CH 3 CH – CH 3 | | | H 3 C – C – CH 3 | | CH 3 CH 2 | | | CH 2 CH 3 CH 2 | | CH 3

• Sucesso só vem antes de trabalho no dicionário. ( Albert Einstein)