10 HIDROLIZA Hydrolysis kisela reakcija sol H 2

















- Slides: 21

10. HIDROLIZA (Hydrolysis) kisela reakcija sol + H 2 O neutralna reakcija = f (priroda soli) alkalna reakcija Hidroliza: reakcija između iona soli i iona vode uz stvaranje slabe kiseline, slabe baze ili obje. Odjel za kemiju

Odjel za kemiju

10. 1. Hidroliza soli jakih kiselina i jakih baza Na. Cl + H 2 O ⇋ Na+ + Cl- + H+ + OH- [H+] = [OH-] = 10 -7 mol/L → p. H = 7 Zaključak: soli ne hidroliziraju; neutralna reakcija Odjel za kemiju

Odjel za kemiju

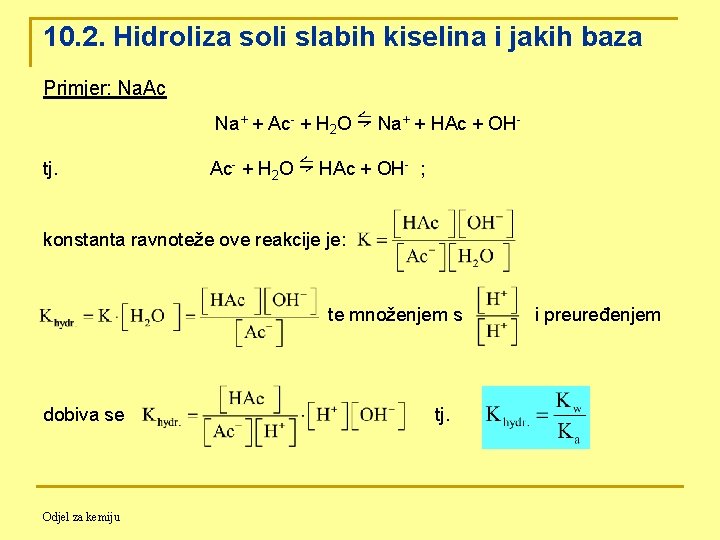
10. 2. Hidroliza soli slabih kiselina i jakih baza Primjer: Na. Ac Na+ + Ac- + H 2 O ⇋ Na+ + HAc + OHtj. Ac- + H 2 O ⇋ HAc + OH- ; konstanta ravnoteže ove reakcije je: te množenjem s dobiva se Odjel za kemiju tj. i preuređenjem

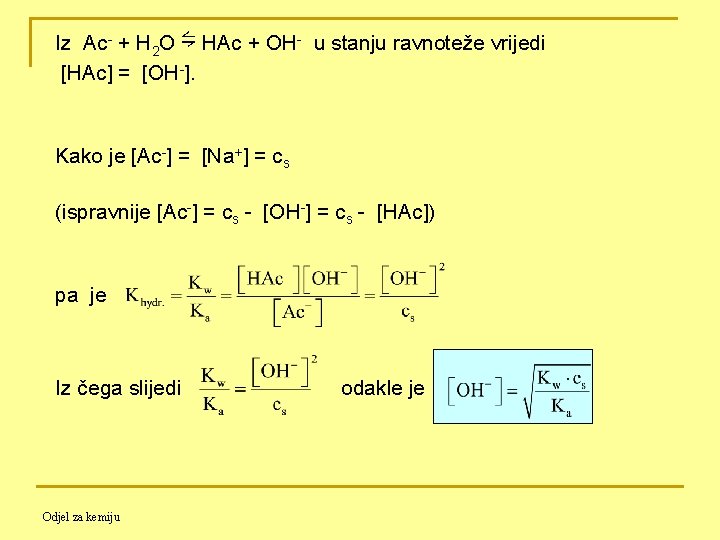
Iz Ac- + H 2 O ⇋ HAc + OH- u stanju ravnoteže vrijedi [HAc] = [OH-]. Kako je [Ac-] = [Na+] = cs (ispravnije [Ac-] = cs - [OH-] = cs - [HAc]) pa je Iz čega slijedi Odjel za kemiju odakle je

Primjer : Izračunati p. H vrijednost 0. 05 M otopine Na. Ac (Ka = 1. 8 x 10 -5). p. OH = -log [OH-] = 5. 28, pa je p. H = 14 – p. OH = 8. 72 Odjel za kemiju

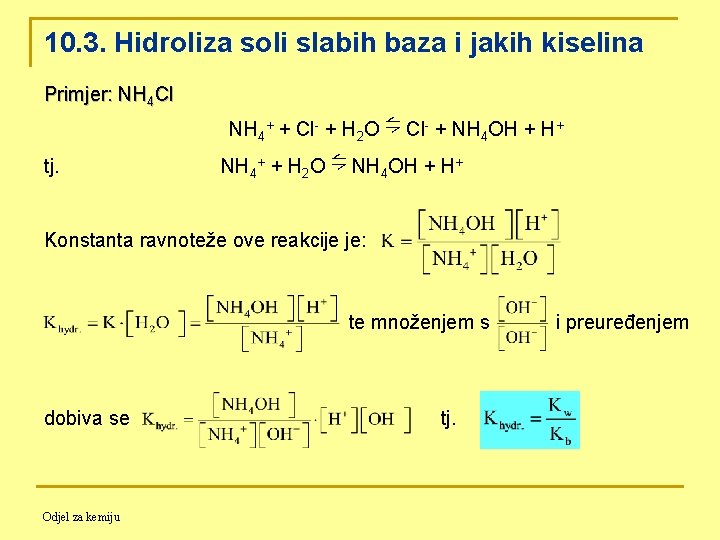
10. 3. Hidroliza soli slabih baza i jakih kiselina Primjer: NH 4 Cl NH 4+ + Cl- + H 2 O ⇋ Cl- + NH 4 OH + H+ tj. NH 4+ + H 2 O ⇋ NH 4 OH + H+ Konstanta ravnoteže ove reakcije je: te množenjem s dobiva se Odjel za kemiju tj. i preuređenjem

Iz NH 4+ + H 2 O ⇋ NH 4 OH + H+, u stanju ravnoteže [NH 4 OH] = [H+]. Kako je [NH 4+] = cs (ispravnije [NH 4+] = cs - [NH 4 OH] = cs - [H+]) pa je odakle je Odjel za kemiju , tj.

Primjer : Izračunati p. H vrijednost 0. 1 M otopine NH 4 Cl (Kb = 1. 75 x 10 -5). p. H = 5. 12 Odjel za kemiju

10. 4. Hidroliza soli slabih baza i slabih kiselina - vodena otopina amonijeva acetata - oba će iona reagirati s vodom, a p. H će ovisiti o konstanti ionizacije odgovarajuće kiseline i baze - u slučaju amonijeva acetata konstante ionizacije CH 3 COOH i NH 4 OH su jednake pa će p. H biti neutralan. Odjel za kemiju

- otopimo li u vodi sol nastalu neutralizacijom slabe kiseline slabom bazom, oba nastala iona bit će podložna hidrolizi - nastali ioni podliježu hidrolizi: Odjel za kemiju

- Ako pomnožimo i podijelimo ovu jednadžbu ionskim produktom vode Odjel za kemiju

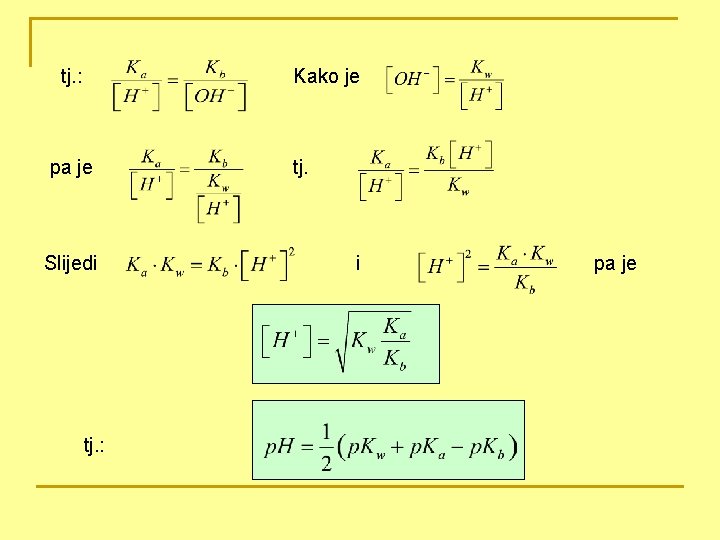
p. H vrijednost soli slabe baze (MOH) i slabe kiseline (HA) Sol MA disocira: pa je tj. : pretpostavka: HA i MOH imaju sličan stupanj hidrolize, tj.

tj. : Kako je pa je Slijedi tj. : tj. i pa je

Primjer 1 Izračunaj stupanj hidrolize i p. H otopine amonij – acetata koncentracije c = 0. 1 mol/L, ako su koncentracijske konstante disocijacije Odjel za kemiju

Odjel za kemiju

Odjel za kemiju

Odjel za kemiju

10. 5. Učinak zajedničkog iona (Common ion effect) - Učinak zajedničkog iona je poseban slučaj primjene zakona kemijske ravnoteže na reakcije ionizacije. - Na primjer, u otopini slabe baze, amonijevog hidroksida, postoji ravnoteža: - Dodatak NH 4 Cl, (NH 4)2 SO 4, ili bilo koje druge topljive amonijeve soli, + povećat će koncentraciju NH 4 , i zbog toga povećati broj sudara u + sekundi između NH 4 i OH. - Ravnoteža će biti pomaknuta u lijevo, i koncentracija OH bit će + smanjena. NH 4 , budući je zajednički i amonij hidroksidu i dodanoj soli amonijaka, nazvan je „zajednički ion“. Odjel za kemiju -

- Na isti način soli koje su samo slabo topljive, mogu se učiniti čak još manje topljivim povećavajući koncentraciju zajedničkog iona. - Na primjer, ravnoteža između slabo topljivih soli gipsa, Ca. SO 4· 2 H 2 O, i njegovih iona u otopini predstavlja jednadžba: - Dodatak bilo Ca 2+ ili SO 42 - , iz bilo koje topljive soli koja sadržava jedan od ovih iona, pomaknut će ravnotežu u lijevo i smanjiti topljivost. Odjel za kemiju