KISELINE BAZE I SOLI VJEBANJE I PONAVLJANJE GRADIVA

KISELINE, BAZE I SOLI VJEŽBANJE I PONAVLJANJE GRADIVA

Ponovi! 1. Što su kiseline, a što baze prema Brønstedu? 2. Navedi nekoliko primjera polarnih molekula. 3. O čemu ovisi jakost kiselina? 4. Što je ionizacija?

Prisjeti se ionizacije na primjeru vode koja je slab elektrolit ali ipak ionizira. Koji je naziv iona nastalih disocijacijom vode?
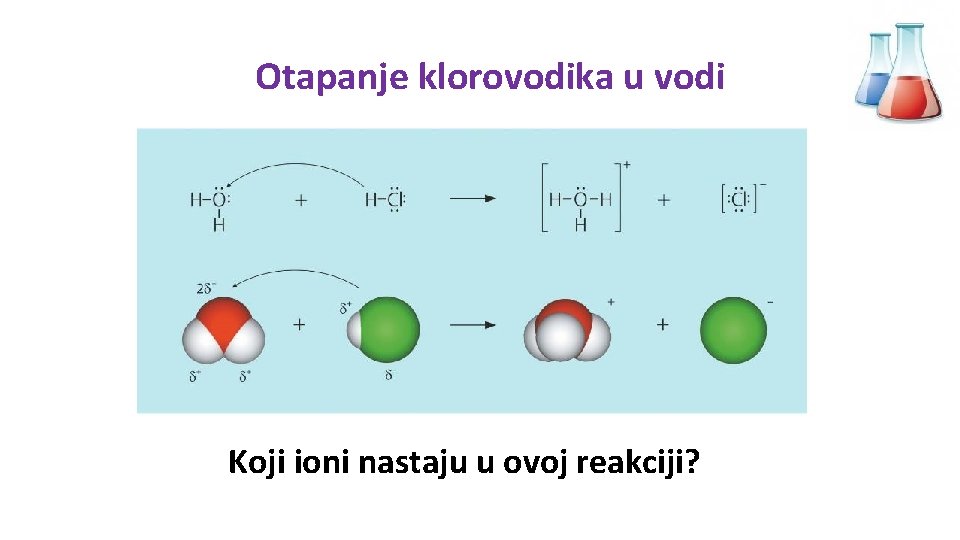
Otapanje klorovodika u vodi Koji ioni nastaju u ovoj reakciji?

Otapanjem klorovodika u vodi nastaje oksonijev ion (H 30+ ) i kloridni ion H 30+ hidratizirani proton (H+) Kako smo podijelili kiseline s obzirom na broj atoma vodika? -prisjeti se ionizacije sumporne kiseline
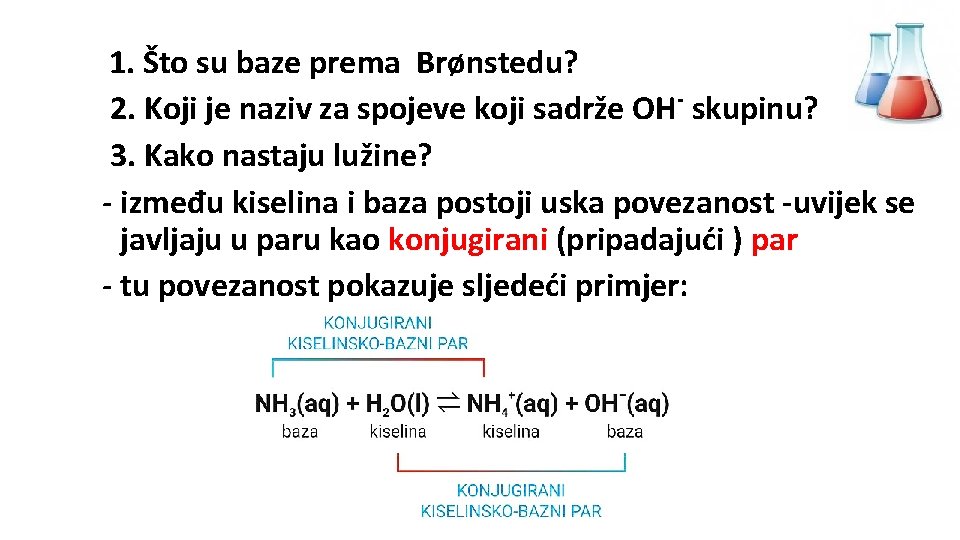
1. Što su baze prema Brønstedu? 2. Koji je naziv za spojeve koji sadrže OH- skupinu? 3. Kako nastaju lužine? - između kiselina i baza postoji uska povezanost -uvijek se javljaju u paru kao konjugirani (pripadajući ) par - tu povezanost pokazuje sljedeći primjer:

Ø Što je kiselina jača, lakše otpušta proton, a konjugirana baza je slabija jer teže prima proton Ø Neke tvari se mogu ponašati i kao kiseline i kao baze ovisno s kojom je jedinkom u paru (H 2 O)

ZADATCI – 1. DIO RIJEŠI ZADATKE 1. Napiši formule za konjugirane baze sljedećih kiselina: a) CH 3 COOH b) H 2 O c) HCO 3 - 2. Napiši formule za konjugirane kiseline sljedećih baza: a) HSb) H 2 O c) CO 32 -

ZADATCI – 1. DIO 3. Prikaži reakciju dihidrogen fosfatnog iona (H 2 PO 4 -) s vodom i označi konjugiranu bazu. 4. Izdvoji molekule i ione koje mogu biti: a) kiseline b) baze : HNO 2, CN-, Cl-, HS-

ZADATCI – 1. DIO 5. Koje su jedinke u kemijskoj reakciji Brønsted-Lowryjeve konjugirane baze? CN- + H 20→ HCN + OH – 6. Napiši jednadžbe postupne disocijacije sulfidne kiseline i imenuj njihove kiselinske ostatke. 7. Napiši jednadžbe disocijacije: a) kalcijevog hidroksida b) amonijeve lužine
Pogledaj video na https: //www. youtube. com/watch? v=t 5 e. UOXm-wi. E i odgovori na pitanja: 1. Što označava konstanta Kw? 2. Kako se označava mjera za kiselost otopina? 3. Što su indikatori?

ZADATCI – 2. DIO RIJEŠI ZADATKE 1. Koliki je p. OH otopine ako je množinska koncentracija vodikovih iona 10 -5 mol/dm 3 ? 2. Izračunaj p. H otopine ako je c(H+) =2, 2 · 10 -3 mol/dm 3. 3. Neka vodena otopina ljubičaste boje sadrži fenolftalein. Boju otopine možemo promijeniti dodatkom: a) Na. Br c) H 20 b) KOH d) HF

NASTAJANJE SOLI, HIDROLIZA SOLI 1. Nabroji nekoliko načina dobivanja soli. 2. Što je hidroliza soli?

ZADATCI – 3. DIO RIJEŠI ZADATKE 1. Izjednači H 2 SO 3 (aq) kemijske jednadžbe i napiši ih u ionskom obliku: a) Ca(OH)2 (aq) + → Ca. SO 3 (aq) + H 2 O (l) b) NH 4 OH (aq) + H 2 SO 4 (aq)→ (NH 4)2 SO 4 (aq) + H 20 (l) 2. Napiši produkte sljedećih reakcija, a spojeve koji disociraju prikaži u ionskom obliku: a) Al (s) + H 3 PO 4 (aq)→ b) Sn (s) + HCl(aq) →

ZADATCI – 3. DIO 3. Metodom neutralizacije prikaži nastajanje sljedećih soli: a) kalcijev sulfid b) barijev nitrat 4. Vodena otopina NH 4 Cl reagira kiselo. Napiši reakciju amonijevih iona s vodom! 5. Hoće li vodena otopina Na 2 C 03 reagirati bazično ili kiselo? Prikažite reakciju!

ZADATCI – 3. DIO 6. U vodi otopimo natrijev acetat (CH 3 COONa). Hoće li p. H vrijednost vodene otopine natrijevog acetata biti veća ili manja od 7? 7. U otopini octene kiseline množinske koncentracije 0, 1 mol/dm 3 odredite koncentraciju oksonijevih iona. Konstanta ionizacije octene kiseline iznosi 1, 8 · 10 -5 mol/dm 3. 8. Kolika je množinska koncentracija otopine natrijevog hidroksida ako se 20 ml te otopine neutralizira s 50 ml klorovodične kiseline množinske koncentracije 0, 2 mol/dm 3?

RJEŠENJA ZADATAKA: 1. dio: 1. a) CH 3 COO- b) OH- c) CO 32 - 2. a) H 2 S b) H 30+ c) HCO 33. H 2 PO 4 - + H 20 H 30+ +HP 042 kiselina 4. a) kiseline: HNO 2, HSb) baze : CN-, Cl-, HS- baza

RJEŠENJA ZADATAKA: 1. dio: 5. CN- + H 20→ HCN + OH baza 1 kis 2(KK) baza 2 (KB) 6. Disocija sulfidne kiseline po stupnjevima: H 2 S(aq) <=> H+(aq) + HS-(aq) hidrogen sulfidni ion HS-(aq) <=> H+(aq) + S 2 -(aq) sulfidni ion 7. a) Ca(OH)2(aq) <=> Ca 2+(aq) + 0 H-(aq) b) NH 4 OH(aq) <=> NH 4+(aq) + OH-(aq)

RJEŠENJA ZADATAKA: 2. dio: 1. c(H+)= 10 -5 mol/dm 3 p. H=5, p. OH= 9 2. c(H+) =2, 2 · 10 -3 mol/dm 3 p. H= -log c( H+) = 2, 65 3. d)

RJEŠENJA ZADATAKA: 3. dio: 1. a) H 2 S 03(aq) + 2 Na. OH(aq) Na 2 S 03 (aq) + 2 H 20(l) b) 2 HNO 3 (aq)+ Mg(OH)2(aq) Mg (NO 3)2 (aq) + 2 H 20(l) 2. a) 2 Al (s) + 2 H 3 PO 4 (aq)→ Al. PO 4(aq) + 3 H 2(g) 2 Al (s) + 6 H+ +2 PO 43 -→ Al 3+(aq) + PO 4 3 -(aq) + 3 H 2(g) b) Sn(s) + 2 HCl(aq) →Sn. Cl 2(aq)+ H 2 (g) Sn(s) + 2 H+(aq) + 2 Cl-(aq) →Sn 2+(ag) +2 Cl-(aq) + H 2 (g)

RJEŠENJA ZADATAKA: 3. dio: 3. a) H 2 S(aq) + Ca(OH)2(ag) →Ca. S(aq) + 2 H 20 (l) b) HNO 3(aq) + Ba(OH)2(ag) →Ba(NO 3)2(aq) + 2 H 20 (l) 4. Reagirati će bazično. CO 32 - + H 20→HCO 3 -+ OH 5. NH 4+ +H 20→NH 3+ OH 6. CH 3 COO- +H 20 →CH 3 COOH + OH- p. H vodene otopine biti će veći od 7. 7. p. H= 2, 87 8. c(Na. OH)= 0, 5 mol/dm 3

ISTRAŽI I POVEŽI SA ŽIVIM SVIJETOM Halofiti ili slanuše su biljke koje su razvile različite prilagodbe koje su im omogućile preživljavanje na tlima bogatim solima. KAKO TO USPIJEVAJU? Ø izlučuju vodu pomoću žlijezda Ø odbacuju neke dijelove u kojima su nakupljene soli Ønakupljaju veće količine vode u staničnom soku Na našim plažama uz more možeš vidjeti biljku sa slike, motar ili petrovac. Jestiva je i konzumira se sirova ili konzervirana. Spartina alterniflora L.

ISTRAŽI I POVEŽI SA ŽIVIM SVIJETOM Biljke preferiraju različite kiselosti tla. ØPovrće najbolje uspijeva na blago kiselim do neutralnim tlima od p. H 6 – 7 ØVoću treba nešto kiselije tlo od p. H 6 - 6. 5 ØPaprati i šparoge najbolje uspijevaju u neutralnom do blago lužnatom tlu. Preuzeto s: http: //www. aljanh. net/flowerbeds-in-the-park-wallpapers/115139104. html

ISTRAŽI I POVEŽI SA ŽIVIM SVIJETOM Znaš li koja je ovo biljka? HORTENZIJA O čemu ovisi boja njezinih cvjetnih latica? O KISELOSTI TLA! Ako je tlo kiselo hortenzija ima plave cvjetne glavice (p. H 3 – 4, 5) Ako je tlo neutralno do lužnato (do p. H 7) cvjetne glavice bit će ružičaste ili crvene. Hydrangea
- Slides: 24