AROMATICI PROIECT REALIZAT DE CUSTRIN ANDREEA TOMASCU DOMNICA













- Slides: 20

AROMATICI PROIECT REALIZAT DE: CUSTRIN ANDREEA TOMASCU DOMNICA

Definiţii: Hidroxiacizii sunt compuşi organici cu funcţiuni mixte: -COOH si –OH Acidul salicilic este preparat chimic pe bază de fenol, în formă de cristale albe, întrebuinţat în medicină, în industria coloranţiilor şi al conservelor alimentare.

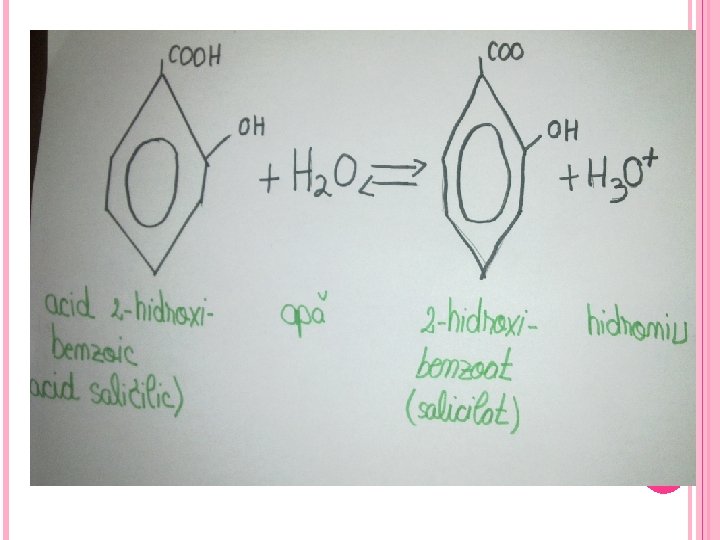
CARACTERUL ACID AL ACIDULUI SALICILIC Acidul salicilic este o substanţă cristalină foarte solubilă în apă. Solubilitatea se datorează legăturilor de hidrogen care se pot stabili între grupele carboxil şi hidroxil ale moleculelor de acid salicilic în moleculele de apă. Acidul salicilic dizolvat reactionează cu apa, stabilinduse un echilibru cu schimb de protoni:


Soluţia apoasă de acid salicilic este acidă (are p. H< 7) deoarece, aşa cum se vede din echilibrul, ea conţine o concentraţie de ioni hidroniu, H 3 O+ mai mare decât cea provenită numai din ionizarea apei. Acidul salicilic este un acid slab mai puternic decât acidul benzoic şi decât acidul hidroxibenzoic.

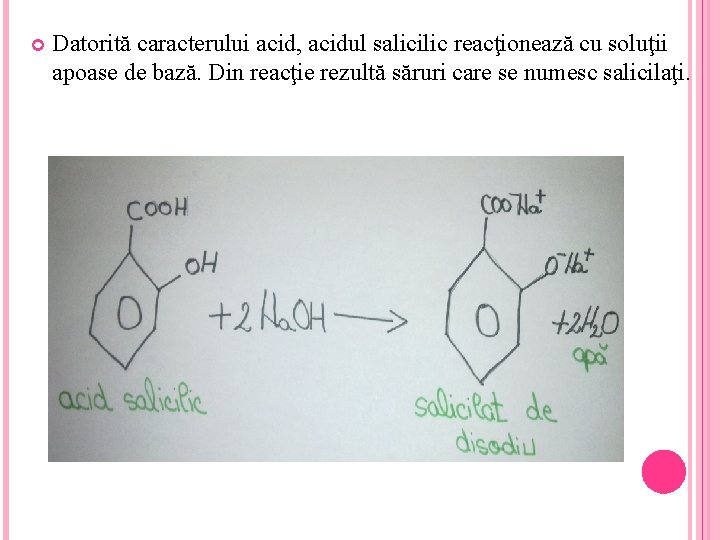
Datorită caracterului acid, acidul salicilic reacţionează cu soluţii apoase de bază. Din reacţie rezultă săruri care se numesc salicilaţi.

Salicilaţii sunt substanţe ionice, uşor solubile în apă. Acidul salicilic şi salicilatul de sodiu se folosesc drept conservanţi în îndustria alimentară.

REACŢII DE ESTERIFICARE ALE ACIDULUI SALICILIC Acidul salicilic poate participa la reacţii de esterificare, cu ambele grupe funcţionale, în funcţie de reactivii chimici şi de condiţiile de lucru:

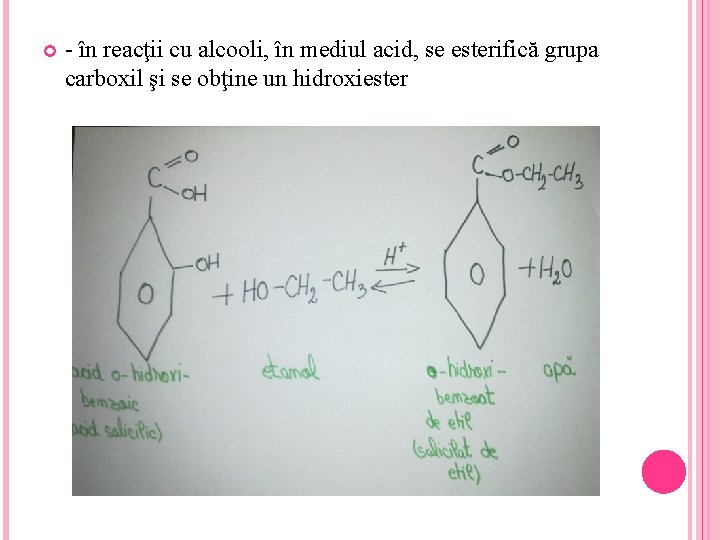
- în reacţii cu alcooli, în mediul acid, se esterifică grupa carboxil şi se obţine un hidroxiester

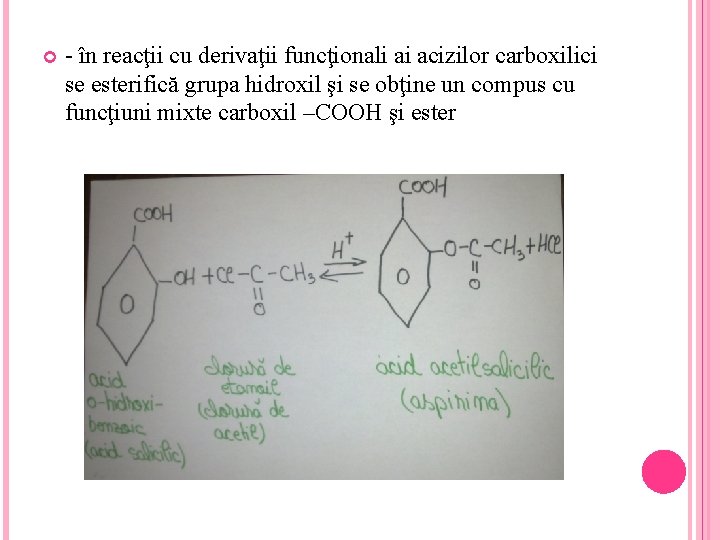
- în reacţii cu derivaţii funcţionali ai acizilor carboxilici se esterifică grupa hidroxil şi se obţine un compus cu funcţiuni mixte carboxil –COOH şi ester

Acidul acetil salicilic este folosit ca medicament sub denumirea de aspirină.

FABRICAREA INDUSTRIALĂ A ASPIRINEI Sinteza acidului salicilic. Industrial, prima etapă în sinteza aspirinei este obţinerea acidului salicilic prin procedeul Kolbe-Schmitt care la bază reacţia de carboxilare dintre ionii fenolat. C 6 H 5 -O- şi dioxid de carbon, CO 2

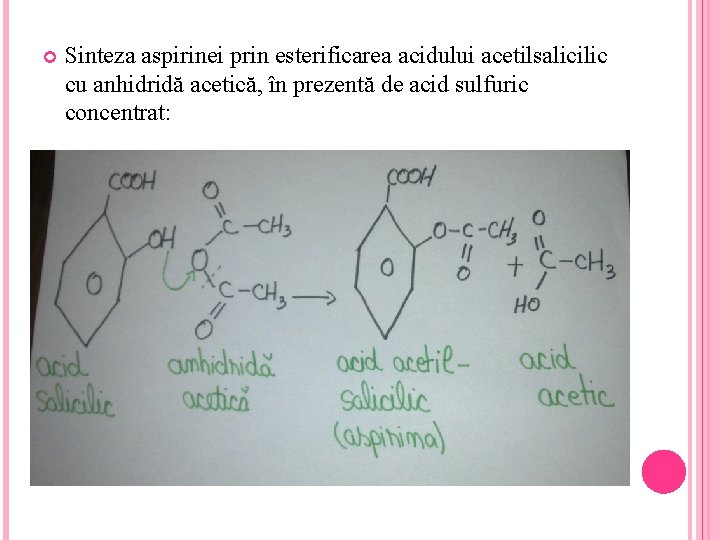
Sinteza aspirinei prin esterificarea acidului acetilsalicilic cu anhidridă acetică, în prezentă de acid sulfuric concentrat:

HIDROLIZA ACIDULUI ACETILSALICILIC Reacţia de esterificare este o reacţie de condensare. Reacţia inversă esterificări este reacţia de hidroliză. Prin hidroliza acidului acetilsalicilic se obţin acidul salicilic şi acidul acetic:

În organism, are loc hidroliza enzimatică a aspirinei. Procesul are loc sub acţiunia unei enzime.

IDENTIFICAREA ACIDULUI SALICILIC Acidul acetilsalicilic se identifică folosind ca reactiv o soluţie de Fe. Cl 3. În mediul acid se obţine o coloraţie rosu -violetă.

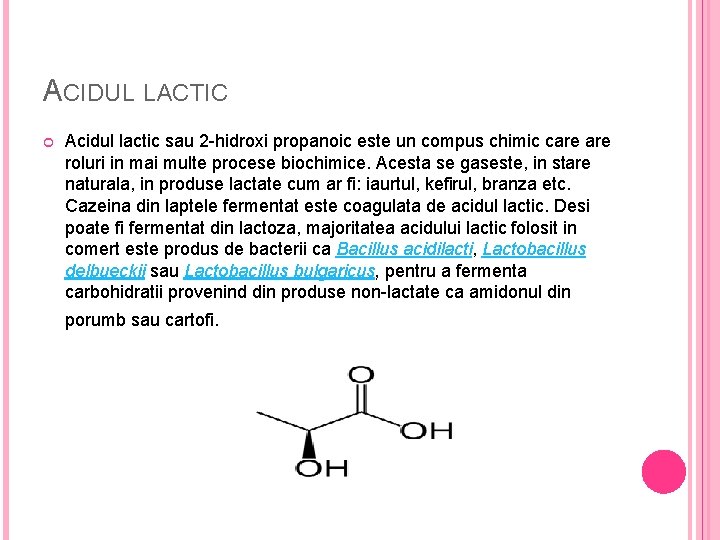
ACIDUL LACTIC Acidul lactic sau 2 -hidroxi propanoic este un compus chimic care roluri in mai multe procese biochimice. Acesta se gaseste, in stare naturala, in produse lactate cum ar fi: iaurtul, kefirul, branza etc. Cazeina din laptele fermentat este coagulata de acidul lactic. Desi poate fi fermentat din lactoza, majoritatea acidului lactic folosit in comert este produs de bacterii ca Bacillus acidilacti, Lactobacillus delbueckii sau Lactobacillus bulgaricus, pentru a fermenta carbohidratii provenind din produse non-lactate ca amidonul din porumb sau cartofi.

Acidul lactic are formula structurală CH 3 -CH-(OH)-COOH Acidul lactic este un acid carboxilic cu o formula chimica bruta de C 3 H 6 O 3 Denumire structurala: acid 2 -hidroxipropanoic, de asemenea cunoscut popular și ca acid laptic, este un acid organic slab, care joacă un anumit rol în anumite procese biochimice Unele produse care pretind a fi vegetariene au in componenta lor acidul lactic. Acidul lactic mai poate fi gasit in alte produse procesate, fie ca ingredient de reglare a p. H-ului, fie drept conservant - antioxidant sau pentru controlul patogenic microorganismelor. Mai este utilizat si la amplificarea fermentatiei la painea de secara.

STRUCTURA: Acidul lactic este un acid carboxilic cu o formulă chimică brută de C 3 H 6 O 3. Are grup auxiliar hidroxil atașat grupării carboxilice, ceea ce îl încadrează în categoria acizilor alfa-hidroxilici (uneori cunoscuți ca AAH). În soluție, ca orice acid monobazic, pierde un proton producând ionul lactat, CH 3 CH(OH)COO−. Masa molara: 90. 08 g/mol Punct de topire: 53° C Punct de fierbere: 122° C Acidul lactic are 2 izomeri optici, dintre care cel mai important fiind levogir. Este produs la animale de LDH, intr-un proces normal de fermentatie in cadrul unui metabolism normal.

ROLUL ACIDULUI LACTIC: În stare de repaus concentrația saguină a acidului lactic e de 10 mg/dl iar în timpul efortului poate crește până la 200 mg/dl. [1]. În timpul efortului acidul lactic rezultă din acid piruvic prin hidrogenare. In medicina, este folosit in resuscitarea fluidelor in urma pierderii de sange dupa traume, interventii chirurgicale sau arsuri. Acidul lactic reactioneaza cu proteinele prezente in lapte si confera iaurtului textura asemanatoare gelului. Persoanele care au intoleranta la lactoza (lapte) sunt adesea sfatuite sa consume mai degraba iaurt.