Viral Hepatitlerde Dendritik Hcre Bazl Tedaviler Prof Dr

Viral Hepatitlerde Dendritik Hücre Bazlı Tedaviler Prof. Dr. Ercüment Ovalı KTÜ-Ati Teknoloji Proje sorumlusu

Günümüzde viral ve maling hastalıkların tedavisinde çok önemli gelişmeler olmasına rağmen, Mevcut tedavilerin yeterli olduğunu söylemek mümkün değildir

Bu durumda farklı tedavi seçeneklerine gereksinim vardır Bu seçeneklerden biri immünoterapi uygulamalarıdır.

Kullanılan immünoterapi rejimlerinden biride DENDRİTİK HÜCRE bazlı uygulamalardır.

• Dentritik hücreler profesyonel antijen sunan hücrelerdir(ASH). • ASH içinde kendisine en yakın rakibinden 100 kat daha güçlü bir şekilde. T lenfositleri uyarabilmektedirler.

DH’nin Öyküsü • 19. yüzyılada Paul Langerhans LH’ni tanımladı • 1973’de Stainman bu hücreler için DH tanımını kullandı • 1990’lı yıllarda DH kök hücreden ve monositlerden üretilmeye başlandı • 2000 yılıdan sonra ilk klinik çalışmalar başladı

DH’nin kaynağı • DH’ler heterojen bir grup hücre olup kemik iliğinden Değişik büyüme faktörlerinin(flt 3 -l, GM-CSF vb) varlığında oluşurlar. • Periferik kanda ise DH’ler HLA-DR pozitif olup CD 11 c ve CD 123 varlığına göre iki ayrı gruba ayrılırlar – – Myeloit DH : CD 11 c pozitif CD 123 negatif (DC 1) Plazmasitoit DH: CD 11 c negatif CD 123 pozitif(DC 2). Yung JW. ASH Education program book. San Francisco, California December 1 -5. p: 361 -366: 2000 Osada T et al. Rev. Immunol. 25: 377 -413: 2006

Morfolojik Karakterleri • İsimlerinin tanımladığı gibi tüyümsü çıkıntıları olan , oval çekirdekli iyi gelişmiş ER’ye sahip hücrelerdir. • Plazmastoit tipi ise plazma hücresine benzer

Fonksiyonel Karakterleri • 3 farklı fonksiyonel karaktere sahiptirler: – T hücre uyarımı – İmmün toleransın indüklenmesi – B hücre fonksiyonlarının düzenlenmesi

Dendritik Hücre Bazlı tedaviler • Bir çok olguda immün sistem tümörü/viral yükü eradike edemez. Buda tümörün yayılması ile sonuçlanır. Çünkü:

Tümör İmmün Kontrolden saklanmaktadır. A-Tümörün gizlenmesi 1 - Costimulatuar molekül ekspresyonunu azaltırlar 2 - MHC I ve II eksp. azaltır. 3 - Target antijen genlerini baskılarlar B-İmmün supresyon indüksiyonu 1 - IL-10 sekresyonunu artırırlar Th 3 tip yanıt(Treg) 2 - TGF beta sekresyonunu artırırlar 3 - Solubıl ihibitörleri artırırlar)(i. NOS, ARG-1). 4 - Fas-L salgısını artırırlar. 5 - Hızlı proliferasyonla toleransı indüklerler

Viral yükün eradike edilememe nedenleri • Yetersiz immün yanıt(özellikle akut fazın semptomatik geçtiği hastalarda viral yük daha yüksek olmaktadır) (Thimme et al. , 2001) • T lenfosit epitoplarında mutasyonlar (Erickson et al. , 2001; Weiner et al. , 1995); • Viral proteinlerle immün yanıtın baskılanması (Gale et al. , 1997; Keskinen et al. , 2002; Kittlesen et al. , 2000). • APC, Hücresel yanıtın bozuk olması (Cooper et al. , 1999; Thimme et al. , 2002);
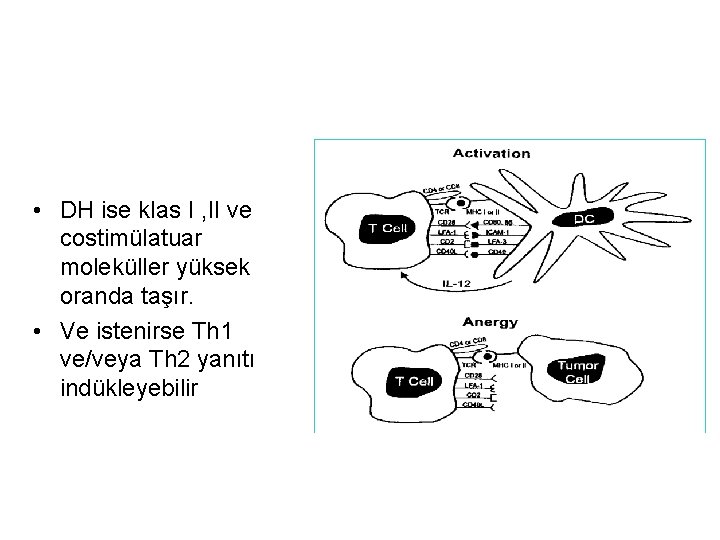
• DH ise klas I , II ve costimülatuar moleküller yüksek oranda taşır. • Ve istenirse Th 1 ve/veya Th 2 yanıtı indükleyebilir

DH’lerin elde edilmesi • Üretim • İzolasyon

Üretim • CD 34 kök hücrelerden DH Üretimi: – • Monositlerden DH üretimi: – • Flt 3 L, IL-3 and IL-6, ile 14 günlük bir inkübasyon sonrası IL-4 and GM-CSF 3 günlük yeni besleme süreci En popüler olan bu metot da hücreler IL-4, GM-CSF ile 7 gün inkübe edilirler. Neoplastik Hücrelerden DH üretimi: – Neoplastic DH’ler ALL, AML, KML hücrelerinden GM-CSF, IL-4, TNF-α ve CD 40 L varlığında üretilebilmektedir. Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413) Curti A, et al. J Immunol. 2001; 166: 848– 854. Ovalı E, et al. Haematologica. 2000; 85: 464– 469

DH İzolasyonu • Periferik kanda 3 x 106 to 17 x 106/litre • Lokoferezis ile 1 x 106 to 10 x 106 toplanabilir • Ancak yeterli olmadığından G-CSF, GMCSF, progenipoetin bu amaçla kullanılabilir Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413) Pullarkat V, et al. Clin Cancer Res. 2003; 9: 1301– 1312 Lonial S, et al. Biol Blood Marrow Transplant 2004; 10: 848– 857

Kültür özellikleri • Başlangıçta fetal calf serum (FCS) kullanılmış yaşanan sorunlar nedeniyle otolog seruma(OS) dönülmüştür. – Ancak hasta serumlarının IL-10, TGF-β gibi solubıl inhibitörleri barındırmaları olasıdır • Bu nedenle serum free media kullanımı önerilmektedir. Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413)

Yüklemede Kullanılan Antijenler • Tanımlanmış antijenler: Peptitler, proteinler, c. DNA, • Tanımlanmamış antijenler : Tumor hücreleri, tumor lysates, heat-shock proteins, tumor / DC fusions and m. RNAs, İnaktive Virüsler. • Yardımcı epitoplar: Keyhold limpet haemocyanin (KLH), tuberculosis purified protein derivate (PPD), Pan-HLA-DR binding protein (PADRE) Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413) Schnurr M, et al. Cancer Res 2001; 61: 6445– 6450 Wierecky J, Cancer Res 2006; 66: 5910– 5918. Ovali E, et al. J Exp Clin Cancer Res 2007; 26: 209– 214

DH Maturasyonu • Aşılar için mutlaka matür DH ler kullanılmalıdır. • TNFα, IL 1β, IL-6 ve PGE 2 standart maturasyon reagentlarıdır. Ama? ? ? • Hepatocyte growth factor (HGF)Hem CD 34 pozitif hücrelerden hemde monositlerden oluşan DH lerin maturasyonunda katkıda bulunabilmektedir. Schuler-Thurner B, et al. J Exp Med 2002; 195: 1279– 1288 Ovali E, et al. Haematologica. 2000; 85: 464– 469 Mc. Ilroy D, Gregoire M: Cancer Immunol Immunother 2003; 52: 583– 591 Sonmez M, et al. Saudi Med J 2007; 28: 688– 695 Ovali E, et al. J Exp Clin Cancer Res 2007; 26: 209– 214

Otoriteler İşlem - Kemik iliği nakli - Kan, Kİ, GKK hemopoietik kök hücre - Hücre tedavileri için hücrelere yapılacak her türlü işlem: Çok Kan bankacılığı, Tüp bebek uygulamaları, İmmunoterapi uygulamaları Diğer hücre tedavi ürünleri - Gen tedavi ürünleri Asgari şart Aseptik teknikler yeterli P P M M G c. G

Release Tests of DCs based vaccine products (Hinz T, et al. J Immunother 2006; 29: 472– 476, Brent M. Annual Somatic Cell Therapy Symposium, 9/25 -27/2006. Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413) Purity(as measured by flow cytometry) : >50 %HLA DR , CD 86, CD 11 c/CD 123 positive Viability: >% 70 by trypan blue exclusion or Propidium iodide stain Sterilty: Bacteria, fungus, mycoplasma negative Pyrogenitiy: Endotoxin negative by LAL Differentiation/Maturation(optional): Linage negative and CD 80, CD 83 positive (as measured by flow cytometry). Potency testings( To be developed and defined by product manufacturer): High level of target protein expression (Threshold is yet to be determined) CD 45 positivity * Mixed lymphocyte reaction Costim assay. Stability assay To be defined by product manufacturer. Functional assays (Late phase clinical development) Delayed type hypersensitivity reaction(DTH) ELISPOT Tetramer staining by flow cytometry

DH Bazlı Aşı Uygulaması • Optimal doz ve uygulama sıklığı : – Bilinmemektedir. • Önerilen ilk dozların 15 günde bir olmasıdır • En az 5 milyon hücre önerilmekte olup ilk veriler 20 Milyon hücrenin optimal olacağını işaret etmektedir – Uzamış uygulamaların etkinliği artıracağı gösterilmiştir • Uygulama şekli – SC, İD, İN uygulamalar: T hücre uyarımı için – İV uygulamalar ise B hücreleri uyarmak için tercih edilmektedir Ovali E, et al. J Exp Clin Cancer Res 2007; 26: 209– 214 Osada T, et al. Inter Rev Immunol 2006; 25: 377– 413

Yapılan Araştırmalar • Bugün değişik türdeki kanser aşılarının tamamlanmış 7 adet Faz III çalışması vardır • Ancak DH aşıları ile ilgili 100 den fazla faz I/II bir adette Faz III çalışma mevcuttur. Hepsinin ortak sonucu: – Kanser aşıları emniyetli bir uygulamadır. Dünya literatüründe bir çalışmada Grade III toksite rapor edilmiş diğer tüm çalışmalarda sadece Grade I toksite rapor edilmektedir – Objektif klinik cevap oranları %2. 6 -%32 arasında rapor edilmektedir. Freda K. Stevenson Curr Opin Oncol 17: 573— 577. 2005

Faz III Çalışmalar Doehn Ch, Richter A, Lehmacher W, Jocham D. Adjuvant autologous tumour cell-lysate vaccine versus no adjuvant treatment in patients with M 0 renal cell carcinoma after radical nephrectomy: 3 -year interim analysis of a German multicentre phase-III trial. Folia Biol (Praha). 2003; 49(2): 69 -73. Schadendorf D, Ugurel S, Schuler-Thurner B, Nestle FO, DC study group of the De. COG. Dacarbazine (DTIC) versus vaccination with autologous peptide-pulsed dendritic cells (DC) in first-line treatment of patients with metastatic melanoma: a randomized phase III trial of the DC study group of the De. COG. Ann Oncol. 2006 Apr; 17(4): 563 -70. Epub 2006 Jan 17. Hanna MG Jr, Hoover HC Jr, Vermorken JB, Harris JE, Pinedo et al, Adjuvant active specific immunotherapy of stage II and stage III colon cancer with an autologous tumor cell vaccine: first randomized phase III trials show promise. Vaccine. 2001 Mar 21; 19(1719): 2576 -82. Jocham D, Richter A, Hoffmann L, Iwig K, Fahlenkamp D, et al. Adjuvant autologous renal tumour cell vaccine and risk of tumour progression in patients with renal-cell carcinoma after radical nephrectomy: Phase III, Randomised controlled trial. Lancet. 2004; 363(9409): 594 -9.
![• [No authors listed] Phase III randomized study of autologous lymphoma-derived idiotype specific • [No authors listed] Phase III randomized study of autologous lymphoma-derived idiotype specific](http://slidetodoc.com/presentation_image_h/374663463500eea7eb2a8f32ae72d384/image-25.jpg)
• [No authors listed] Phase III randomized study of autologous lymphoma-derived idiotype specific vaccination plus GM-CSF in patients with follicular lymphoma in first complete remission. Clin Adv Hematol Oncol. 2003 Jan; 1(1): 67. • O'Brien ME, Anderson H, Kaukel E, O'Byrne K, Pawlicki M, Von Pawel J, Reck M; SR-ON-12 Study Group. SRL 172 (killed Mycobacterium vaccae) in addition to standard chemotherapy improves quality of life without affecting survival, in patients with advanced non-small-cell lung cancer: phase III results. Ann Oncol. 2004 Jun; 15(6): 906 -14. • Wallack MK, Sivanandham M, Ditaranto K, Shaw P, Balch CM, Urist MM, Bland KI, Murray D, Robinson WA, Flaherty L, Richards JM, Rosen L, Bartolucci AA. Increased survival of patients treated with a vaccinia melanoma oncolysate vaccine: second interim analysis of data from a phase III, multi-institutional trial. Ann Surg. 1997 Aug; 226(2): 198 -206.


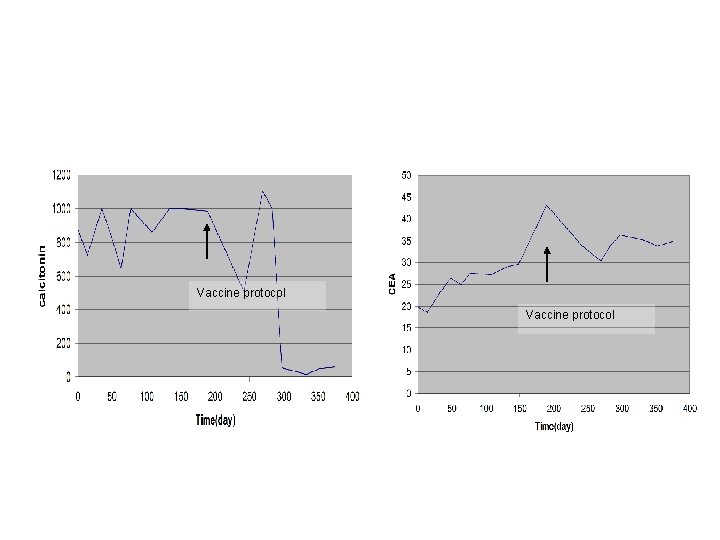
Vaccine protocol


Enfeksiyon - DH tedavisi ?

DH’lerin mikroorganizmalara karşı konak savunmasını güçlendirme veya kronik tabiatlı (HIV, HBV, HCV, papilloma, CMV gibi) mevcut bir enfeksiyonun tedavisinde kullanılabilir mi?

İlk DH aşısı örneği: spiroketlere karşı uygulanmış; B. burgdorferi yüklenmiş DH’ler farelerde spesifik koruyucu bağışık yanıt oluşturmuştur (Mbow et al. 1997) LCMV peptid-yüklü DH’ler Farelerde; çok kısa bir sürede (2 gün) güçlü ve uzun (>60 gün) süreli bir antiviral yanıt oluşturmuştur (Ludewig ve ark. (1998) influenza ve HSV-2 proteinleri ile yüklenmiş DH aşılarının (Schon et al. 2001) spesifik T hücre ve koruyucu yanıt oluşturdukları gösterilmiştir. (Lopez et al. 2000)
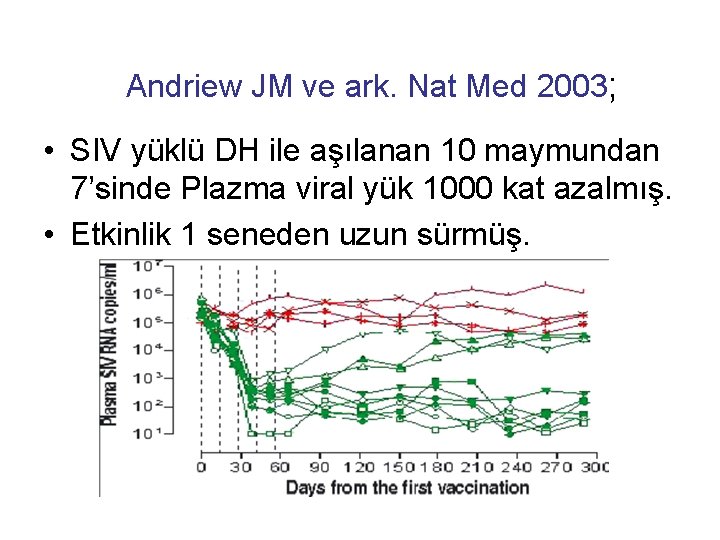
Andriew JM ve ark. Nat Med 2003; • SIV yüklü DH ile aşılanan 10 maymundan 7’sinde Plazma viral yük 1000 kat azalmış. • Etkinlik 1 seneden uzun sürmüş.
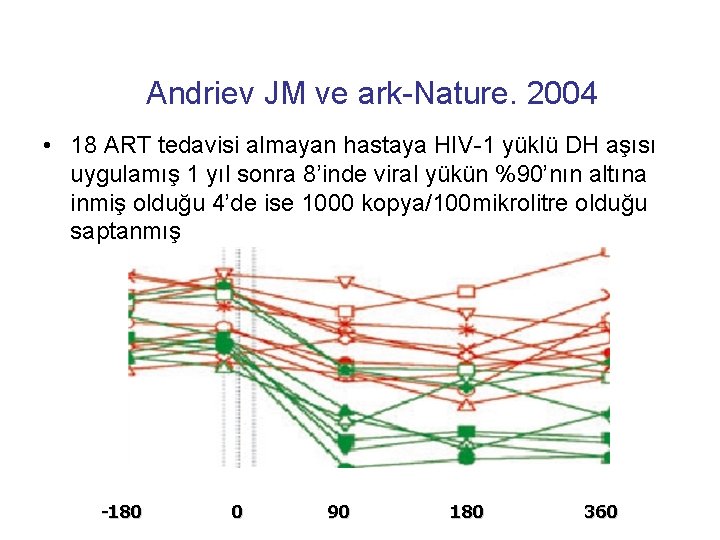
Andriev JM ve ark-Nature. 2004 • 18 ART tedavisi almayan hastaya HIV-1 yüklü DH aşısı uygulamış 1 yıl sonra 8’inde viral yükün %90’nın altına inmiş olduğu 4’de ise 1000 kopya/100 mikrolitre olduğu saptanmış -180 0 90 180 360

kronik HIV enfeksiyonunda HIVgag yüklü DH aşısı, DHpeptid aşısı insanlarda; HAART kullanılan emniyetli hastalardabulunmuş, viral reboundu baskılamada yetersiz kalsa dagüçlü spesifik oluşturduğu, çoğu hastada bir Tyanıt hücre yanıtı ve virus/DH viral. Iİİ yükte düşüşçalışmasında sağlamıştır (Luise et al. 2004). spesifik hücresel yanıtın zayıf ve geçici olduğu bildirilmiştir. İki farklı grup tarafından; HIV-1 gag, env veilepol peptid yüklü DHyüklenerek aşısı biri HIVgag peptidleri diğerinde Iİİ virus HIV-1+ hastalarda; hazırlanmış DH’ler, iyi tolere edildiği ve ayrıca kısa uygulanmış; sürede HAART tedavisi altındaki hastalara HIV spesifikiyi. IFNg+ oluşturmuştur (Connoly et al. 2007) aşılarının tolerelenfosit edildiği yanıtı belirtilmiştir (Garcia et al. 2005; Ide et al. 2006).

HCV enfeksiyonunda, HCV proteinleri ile yüklenmiş DH aşılar kullanarak HCV spesifik hücresel yanıt oluşturulabileceği ileri sürülmektedir Örneğin; r. HCV core protein ve peptidleri ile yüklenmiş DH’lerle güçlü bir humoral ve hücresel yanıt elde edilmiş (Encke et al. 2005) bir diğer çalışmada, HCV NS 3 protein geni taşıyan adenovirus ile transfekte DH’lerin farklı fare türlerinde CD 4 Th 1 ve CD 8 T hücre yanıtı oluşturulduğu gösterilmiştir (Zabelata et al. 2007).

Kronik HBV enfeksiyonunda, HBs. Ag-yüklü DH aşısının sağlıklı gönüllülerde güvenli olduğu, bazı deneklerde anti-HBs + oluşturduğu (Akbar 2004). HBV-HCC hasta DH’leri HBc. Ag ve HBs. Ag ile yüklendiklerine Kronik HBV hastalarında güçlü bir CD 40, 80 ve 86 sentezi sağladıkları, HBs. Ag-yüklü DH aşısının; T hücre proliferasyon ve IFNg salınışını güçlü bir şekilde HBV replikasyonunu baskıladığı, uyardıkları; serum viral yükü azaltdığı, HBe-Ag’nin kaybolduğu ve anti-HBe geliştiği (Chen et al. 2005). DH aşısının HBV HCC hastaları için yeni bir tedavi Kronik yöntemi HBV’de olabileceği yetersiz DHbildirilmektedir aktivitesinin, (Shi et al. 2006). HBc. Ag ve HBs. Ag-DH aşısı ile yeniden kazandırılabileceği; T lenfosit proliferasyon ve antijen spesifik IFNg üretiminin artırılabildiği bildirilmiştir (Duan et al. 2006).

Akbar ve ark. Journal of Hepatology 2007 • HB aşısına cevapsız 6 hastada HBs. Ag ve HBc. Ag yüklü DH aşılaması ile 28 gün sonra güçlü serokonverisyon elde edilmiş

DH aşı yönteminin C. trachomatis M. tuberculosis parazit ve mantar enfeksiyon modellerinde başarılı bir şekilde uygulandığı bildirilmektedir.

Sonuç DH aşı yönteminin daha çok kanser alanında potansiyeli araştırılmakta, yüzlerce çalışma yürütülmektedir. Diğer taraftan, DH’lerin enfeksiyon hastalıklarındaki rolünün daha da iyi anlaşılmasına paralel olarak, deneysel/klinik şartlarda Ag-yüklü DH aşılarının özellikle kronik viral enfeksiyonlar için de hızla değerlendirildiğini görmekteyiz. 100 hastalık AT 2 ile inaktive HIV-1 yüklü DH aşılaması ile ilgili faz III çalışma 2007 sonunda başlamıştır.

tartışılan deneysel Kanserde çalışmalarda sorun teşkil DH aşı yöntemi sorunlarının etmemekle beraber, enfeksiyon hastalıkları için de geçerli olduğu düşünülmektedir. klinik uygulamalar için en uygun DH kaynağının seçimi, DH’lerin en uygun antijenlerin belirlenmesi ve uygun şekilde DH’lere yüklemesi, yasal mevzuat gereği antijen yüklü DH’lerin en uygun şekilde, GMP şartlarında hangi sayıda ve hazırlanmış olmaları hangi yoldan gereği de enjekte edilmesi unutulmamalıdır. gibi temel konuların kapsamlı bir şekilde çalışılmasına ihtiyaç vardır.

- Slides: 42