Universita degli Studi Corsi di Laurea in Scienze















































- Slides: 55

Universita’ degli Studi Corsi di Laurea in Scienze Chimiche e dell’Insubria Chimica Industriale Chimica Fisica 1 Modulo A Termochimica dario. bressanini@uninsubria. it http: //scienze-como. uninsubria. it/bressanini

© Dario Bressanini 2

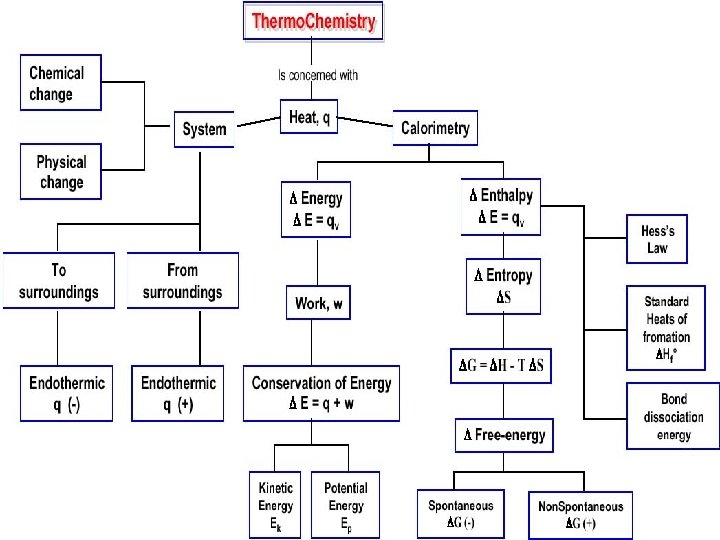
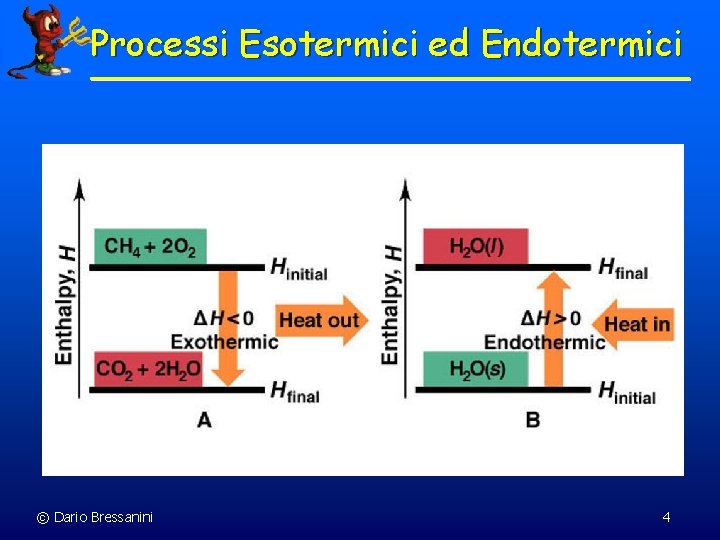
Entalpia H = U + p. V n L’Entalpia è una funzione di stato, dipende solo dallo stato iniziale e da quello finale n A pressione costante, il H di un processo, o calore di reazione, è pari al calore scambiato. ´ H < 0 : processo esotermico ´ H > 0 : processo endotermico © Dario Bressanini 3

Processi Esotermici ed Endotermici © Dario Bressanini 4

Reazioni Esotermiche © Dario Bressanini 5

NH 4 Cr 2 O 7(s) Cr 2 O 3(s) + N 2(g) + 4 H 2 O(g) © Dario Bressanini 6

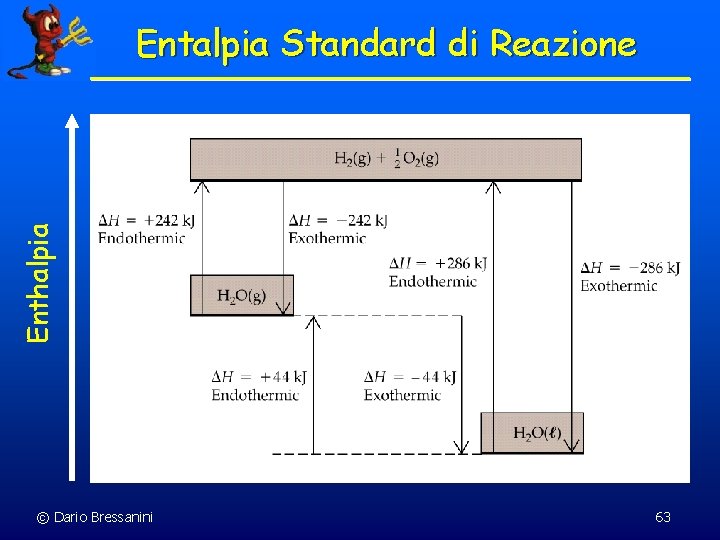
Entalpia n HA B = HB A n H 2 O(g) H 2(g) + 1/2 O 2(g) ´ n H = +241. 8 k. J H 2(g) + 1/2 O 2(g) H 2 O(g) ´ H = 241. 8 k. J © Dario Bressanini 7

Entalpia n Il H è proporzionale alla quantità di sostanza. n H 2 O(g) H 2(g) + 1/2 O 2(g) ´ n H = +241. 8 k. J 2 H 2 O(g) 2 H 2(g) + 1 O 2(g) ´ H = +483. 6 k. J © Dario Bressanini 8

Entalpia n La fase dei reagenti e dei prodotti è importante n H 2 O(g) H 2(g) + 1/2 O 2(g) ´ n H = +241. 8 k. J H 2 O(l) H 2(g) + 1/2 O 2(g) ´ H = +285. 8 k. J © Dario Bressanini 9

H e U n A pressione costante H = U + p V n Se il cambiamento di volume è molto piccolo: p V 0 © Dario Bressanini H U

Variazioni di Entalpia Standard

Stati Standard n n n E’ comodo considerare le variazioni di entalpia di un processo, riferite ad un insieme di condizioni standard. Si e’ deciso di considerare una pressione standard di 1 bar. Mentre per la temperatura NON si è fissato uno standard, ma convenzionalmente si usa 25 °C (298. 15 K) Lo stato standard di una sostanza ad una certa temperatura, è la sua forma pura alla pressione di 1 bar © Dario Bressanini

Stati Standard e H Standard n n Ad esempio, lo stato standard dell’etanolo a 298 K è etanolo liquido puro a 298 K e 1 bar. Lo stato standard del ferro a 500 K è ferro puro solido ad 1 bar. Si deve considerare la fase più stabile. Una variazione di entalpia standard, è il H di un processo dove sia lo stato iniziale che quello finale sono stati standard. © Dario Bressanini 13

H Standard H tipo Tipo di Processo © Dario Bressanini Reagenti e prodotti in stati standard: 1 bar e 25 °C H 2 O(l) H 2 O(g) vap. H° (373 K) = +44 k. J mol-1 14

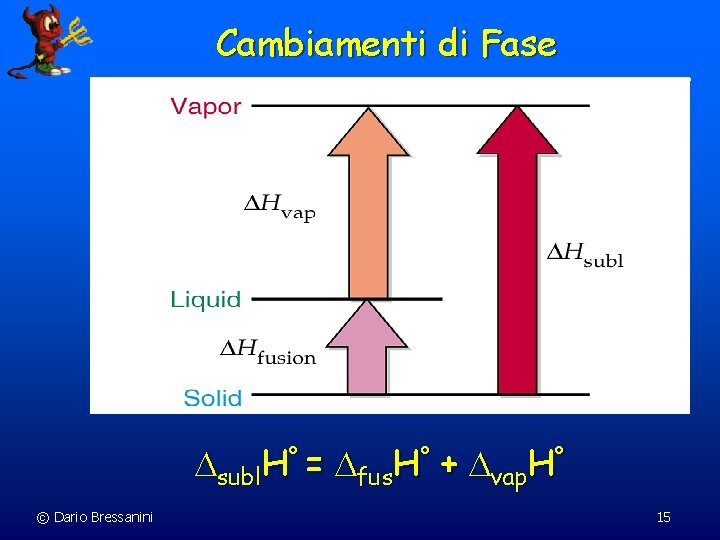
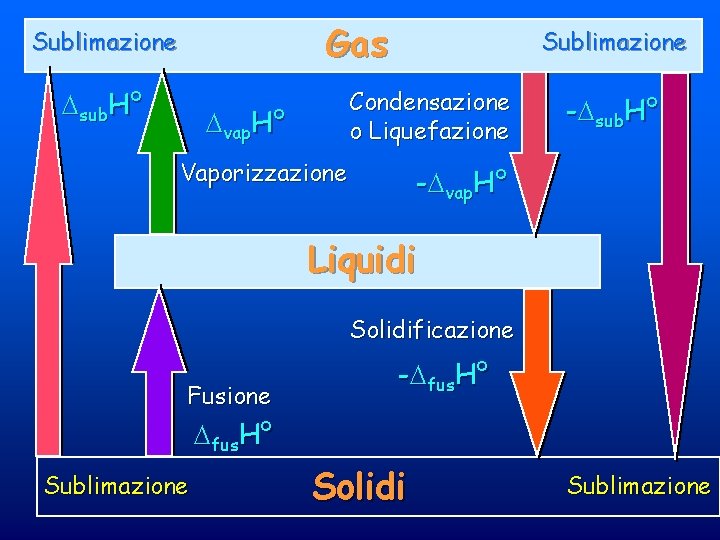
Cambiamenti di Fase subl. H° = fus. H° + vap. H° © Dario Bressanini 15

Gas Sublimazione sub. H° Sublimazione Condensazione o Liquefazione vap. H° Vaporizzazione - sub. H° - vap. H° Liquidi Solidificazione Fusione - fus. H° Sublimazione Solidi Sublimazione

Altri H Standard n Combustione n Ionizzazione n Idratazione n Miscelazione n E altri…vedi tabella sull’Atkins n c. H° ion. H° hyd. H° mix. H° Il H° delle transizioni di fase è comodo riportarlo alla temperatura a cui avviene la transizione © Dario Bressanini 17

Mistero Watson: Dottor Holmes, come funzionano le confezioni di freddo e caldo istantaneo? Sherlock Holmes: DH , mio caro Watson !!! © Dario Bressanini 18

Elementare Watson L’acetato di sodio ha un sol. H° positivo Na. CH 3 CO 2 (s) + calore Na+(aq) + CH 3 CO 2 -(aq) Quindi la formazione di acetato di sodio solido dai suoi ioni e’ una reazione esotermica © Dario Bressanini 19

Entalpia di Combustione n L’entalpia standard di combustione c. H° è l’entalpia standard per una ossidazione completa con O 2(g) di un composto organico, a dare H 2 O(l) e CO 2(g). C 3 H 8(g) + 5 O 2(g) 3 CO 2(g) + 4 H 2 O(l) © Dario Bressanini 20

Equazioni Termochimiche

Entalpia di Reazione n La variazione di Entalpia per una reazione chimica è definita come H = Hprodotti - Hreagenti. n Una Equazione Termochimica include il valore di H e le fasi in cui sono presenti i reagenti e i prodotti CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) © Dario Bressanini H= -802 k. J

Equazioni Termochimiche N 2(g) + 3 H 2(g) 2 NH 3(g) Notate che per reagenti e prodotti vengono specificate le fasi H = -92. 38 k. J Il segno < 0 indica una reazione esotermica Avendo solamente 1. 5 moli di H 2 come calcolo l’entalpia di reazione? Divido l’equazione per 2 incluso il H H = - 92. 38 k. J/2 = - 46. 19 k. J © Dario Bressanini 23

Etalpia Standard di Reazione n Un diverso modo di descrivere la variazione di entalpia in una reazione chimica, è riportare l’Entalpia standard di reazione r. H° CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) r. H°= -802 k. J mol-1 n Notate che è un’entalpia molare © Dario Bressanini 24

Entalpia di Reazione

Diagrammi di Entalpia n n Un diagramma di entalpia mostra H per lo stato iniziale e finale del processo A pressione costante q = H = -802 k. J. H H 1 CH 4(g) + 2 O 2(g) H = -802 k. J H 2 © Dario Bressanini CO 2(g) + 2 H 2 O(g)

Entalpie di Reazione n n La variazione di entalpia dipende dalla fase dei reagenti e dei prodotti CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(l) H= -890 k. J H CH 4(g) + 2 O 2(g) -802 k. J CO 2(g) + 2 H 2 O(g) CO 2(g) + 2 H 2 O(l) © Dario Bressanini H = -890 k. J

Entalpie di Reazione n Invertendo la reazione, il H si inverte di segno n CO 2(g) + 2 H 2 O(g) CH 4(g) + 2 O 2(g) H H 2 H = +802 k. J CH 4(g) + 2 O 2(g) H = +802 k. J H 1 © Dario Bressanini CO 2(g) + 2 H 2 O(g)

Entalpie di Reazione n n H è una proprietà estensiva, quindi il H dipende dalla quantità di reagenti e di prodotti Qual’è il H per la combustione di 11. 0 g di CH 4 in eccesso di ossigeno? CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) 11. 0 g CH 4 © Dario Bressanini H = -802 k. J = -550 k. J

Entalpie di Reazione Quanto butano deve bruciare per produrre 100 k. J di calore? 2 C 4 H 10(g) + 13 O 2(g) 8 CO 2(g) + 10 H 2 O(g) H = -5317 k. J 100 k. J © Dario Bressanini = 2. 19 g C 4 H 10

Legge di Hess

Legge di Hess Consideriamo una reazione in due stadi Qual’è il H? C(s) + ½ O 2(g) CO(g) H 1 = -110 k. J H 2 = -283 k. J __________ CO(g) + ½ O 2(g) CO 2(g) C(s) + O 2(g) CO 2(g) H = -393 k. J Legge di Hess: per una reazione suddivisa in più stadi, il H totale è la somma delle variazioni di entalpia dei singoli stadi © Dario Bressanini

Legge di Hess La legge di Hess si basa sul fatto che l’Entalpia è una funzione di stato H C(g) + O 2(g) -110 k. J CO(g) + ½ O 2(g) H = -393 k. J -283 k. J CO 2(g) © Dario Bressanini

Legge di Hess n La Legge di Hess è semplicemente una applicazione del primo principio della termodinamica a processi a pressione costante. Ha solamente una importanza storica, essendo stata formulata prima del primo principio della termodinamica, da cui discende. © Dario Bressanini

La Legge di Hess in azione n Date due reazioni chimiche (#1 and #2) e il loro H #1: Fe 2 O 3 + 3 CO(g) 2 Fe(s) + 3 CO 2(g) H =-26. 7 k. J #2: CO(g) + 1/2 O 2(g) CO 2(g) H =-283. 0 k. J calcolare il H della seguente reazione: 2 Fe(s) + 3/2 O 2(g) Fe 2 O 3(s) © Dario Bressanini H = ? 35

Passo 1 Cominciamo controllando la posizione di reagenti e prodotti nella reazione desiderata e in quelle date. 2 Fe(s) + 3/2 O 2(g) Fe 2 O 3(s) H = ? #1: Fe 2 O 3 + 3 CO(g) 2 Fe(s) + 3 CO 2(g) H =-26. 7 k. J Obiettivo: Osserviamo che il Ferro appare a destra nella reazione obiettivo e a sinistra nella #1 Soluzione: invertiamo la reazione #1, e cambiamo segno alla sua entalpia © Dario Bressanini 36

Passo 2 n Ci devono essere 3/2 O 2 a sinistra, e dobbiamo cancellare 3 CO 2 quando sommiamo le equazioni. Moltiplichiamo per 3 la seconda reazione, e il suo H #2: 3 [CO(g) + 1/2 O 2(g) CO 2(g) ] H = 3*(-283. 0 k. J) = -849. 0 k. J © Dario Bressanini 37

Passo 3 n Ora sommiamo assieme le due equazioni e cancelliamo ciò che appare sia a destra che a sinistra (se anche la fase è identica) 2 Fe(s) + 3 CO 2(g) Fe 2 O 3(s) + 3 CO(g) H = + 26. 7 k. J 3 CO(g) + 3/2 O 2(g) 3 CO 2(g) H = - 849. 0 k. J 2 Fe(s) +3 CO 2(g) +3 CO(g) + 3/2 O 2(g) Fe 2 O 3(s) + 3 CO(g)+ 3 CO 2(g) 2 Fe(s) + 3/2 O 2(g) Fe 2 O 3(s) © Dario Bressanini H = - 822. 3 k. J 38

Esercizio n Calcolare il H° per la reazione S(s) + O 2(g) SO 2(g) n Dati 2 SO 2(g) + O 2(g) 2 SO 3(g) 2 S(s) + 3 O 2(g) 2 SO 3(g) © Dario Bressanini H = 196 k. J H = 790 k. J 39

Entalpia di Formazione

Reazione di Formazione n n Reazione di Formazione: è la reazione di formazione di una mole di una sostanza dai suoi elementi nei loro stati standard (forma e fase più stabile a 25° e 1 bar) As esempio, la reazione di formazione di Ca. CO 3(s) Ca(s) + C(grafite) + 3/2 O 2(g) Ca. CO 3(s) © Dario Bressanini

Entalpia Standard di Formazione L’ Entalpia Standard di Formazione, f. Hº, di una sostanza è il H della sua reazione di formazione. Ca(s) + C(grafite) + 3/2 O 2(g) Ca. CO 3(s) f. H°(Ca. CO 3, s) = -1207 k. J Ca(s) + ½ O 2(g) Ca. O(s) f. H°(Ca. O, s) = -636 k. J C(grafite) + O 2(g) CO 2(g) f. H°(CO 2, g) = -394 k. J © Dario Bressanini

Entalpia Standard di Formazione n Qual è il f. H°(O 2, g)? O 2(g) Qual è il f. H °(C, diamante)? C(grafite) C(diamante) Qual è il f. H °(Cl, g)? © Dario Bressanini ½ Cl 2(g) Cl(g) f H = 0 f. H = 1. 9 k. J f. H = 122 k. J

Entalpia Standard di Formazione n n n f. H (Diamante) = 1. 9 k. J. Come si trova? La conversione diretta dalla grafite al diamante non e’ semplice (altrimenti lo faremmo tutti ) e quindi non lo possiamo misurare direttamente. Possiamo tuttavia bruciare della grafite e del diamante , misurare i calori di combustione, e usare le legge di Hess C(grafite) + O 2(g) CO 2(g) f. H° = -393. 5 k. J C(diamante) + O 2(g) CO 2(g) f. H° = -395. 4 k. J © Dario Bressanini 58

© Dario Bressanini 59

Mistero H 0 f (C, graphite) = 0 H 0 f (C, diamond) = 1. 90 k. J/mol Watson: Dottor Holmes, La Grafite e’ piu’ stabile del Diamante. Perche’ gli anelli non si trasformano in carbone ? Sherlock Holmes: Ma certo che si trasformano, caro Watson !!! Solo che lo fanno moooolto lentamente! © Dario Bressanini 60

Termodinamica e Cinetica n n La Grafite e’ termodinamicamente piu’ stabile del Diamante. Tuttavia, la termodinamica non dice nulla sul tempo perche’ avvengano i processi. Questo riguarda invece la Cinetica Chimica. Si puo’ dimostrare che la velocita’ della reazione di trasformazione dalla grafite al diamante e’ estremamente lenta. © Dario Bressanini

Entalpia Standard di Reazione n n Possiamo considerare una reazione come una decomposizione dei reagenti negli elementi, e nella formazione dei prodotti a partire dagli elementi Quindi il r. H è esprimibile come: r. H = å n f. H°(prodotti) - å m f. H°(reagenti) n Reagenti e prodotti devono essere alla stessa temperatura © Dario Bressanini

Enthalpia Entalpia Standard di Reazione © Dario Bressanini 63

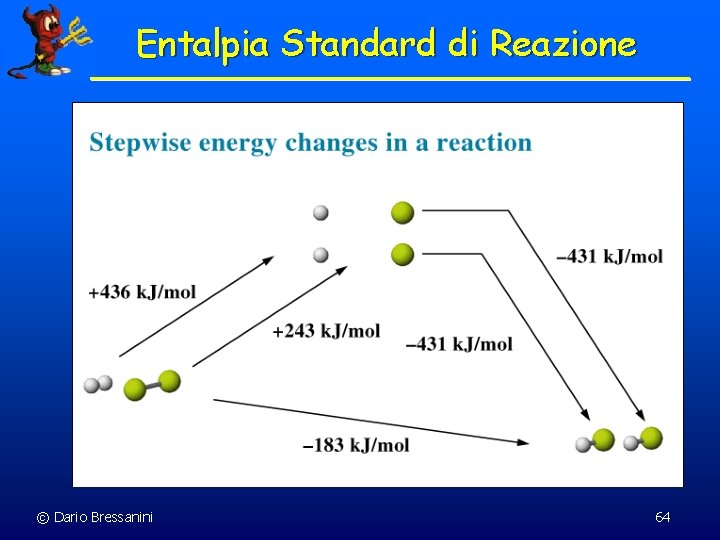
Entalpia Standard di Reazione © Dario Bressanini 64

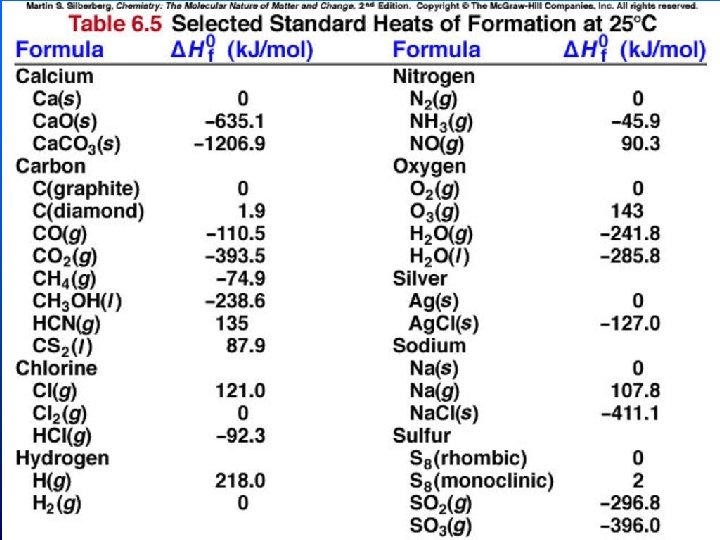
r. H° a partire dai f. H° n I f. H in k. J/mol sono tabulati Sostanza Al(s) Ba. CO 3(s) CO(g) CO 2(g) CS 2(g) f. H 0 -1219 -110 -394 +117 Sostanza Cl 2(g) H 2 O(l) H 2 O(g) Na. HCO 3(s) Na 2 CO 3(s) f. H 0 -286 -242 -947. 7 -1131 Ricordate che i f. H per gli elementi nei loro stati standard è 0 © Dario Bressanini 65

Entalpia Standard di Reazione Calcoliamo il r. Hº della reazione Ca. CO 3(s) Ca. O(s) + CO 2(g) H Ca(s) + C(s) + 3/2 O 2(g) 1207 k. J Ca. CO 3(s) -636 + -394 k. J Ca. O(s) + CO 2(g) 177 k. J Hº = f. H°(Ca. O, s) + f. H°(CO 2, g) - f. H°(Ca. CO 3, s) © Dario Bressanini

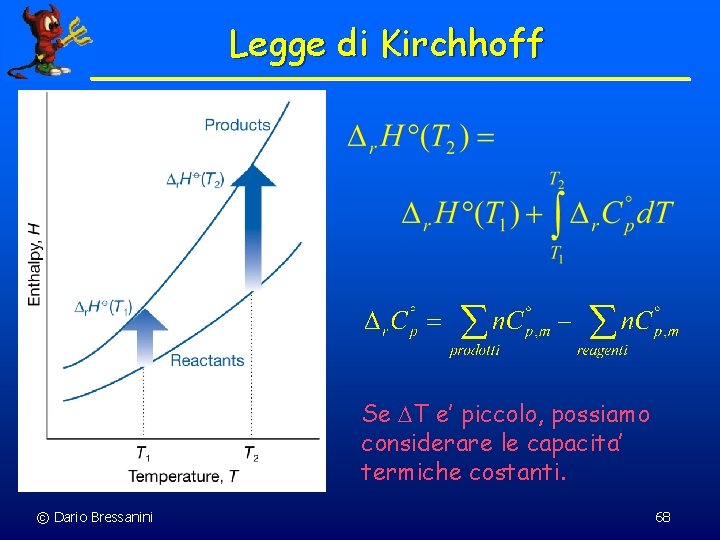
Variazione del r. H° con la Temperatura n n n Le Entalpie standard di molte importanti reazioni sono state misurate a varie temperature. In mancanza di informazioni, possiamo calcolare in modo approssimato r. H°(T) Ricordiamo l’espressione della variazione di entalpia © Dario Bressanini 67

Legge di Kirchhoff Se T e’ piccolo, possiamo considerare le capacita’ termiche costanti. © Dario Bressanini 68

Esercizio n La Nitroglicerina e’ un potente esplosivo che produce 4 gas differenti durante la detonazione 2 C 3 H 5(NO 3)3(l) 3 N 2(g) + ½ O 2(g) + 6 CO 2(g) + 5 H 2 O(g) Calcolare, usando le tabelle, l’entalpia di formazione della nitroglicerina, e calcolare l’energia liberata quando 10. 0 g vengono detonati n © Dario Bressanini 69