Jay Phelan Maria Cristina Pignocchino Le scienze naturali






















- Slides: 28


Jay Phelan, Maria Cristina Pignocchino Le scienze naturali I modelli della chimica e della genetica 2

Capitolo 1 Un modello per l’atomo 3 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

Lezione 1 Dall’osservazione ai modelli 4 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

1. La scienza indaga: macromondo e micromondo Per studiare le relazioni tra micromondo e macromondo è necessario elaborare metodi e strumenti capaci di superare i limiti dell’osservazione diretta e costruire modelli per rappresentare i fenomeni. 5 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

2. I modelli sono utili ma non definitivi I modelli sono rappresentazioni semplificate e provvisorie di fenomeni complessi. Devono essere sottoposti a verifica sperimentale e non sono mai definitivi: possono essere modificati, corretti o abbandonati. 6 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

Lezione 2 La sorprendente natura dell’atomo 7 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

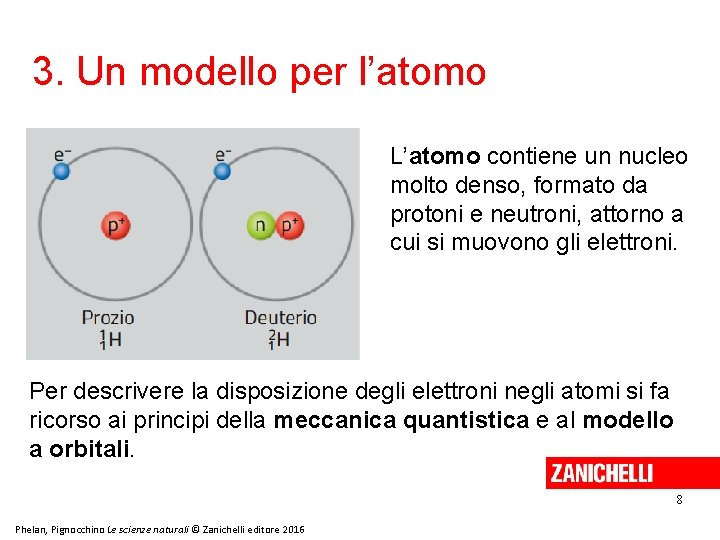
3. Un modello per l’atomo L’atomo contiene un nucleo molto denso, formato da protoni e neutroni, attorno a cui si muovono gli elettroni. Per descrivere la disposizione degli elettroni negli atomi si fa ricorso ai principi della meccanica quantistica e al modello a orbitali. 8 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

4. Una logica nuova: non si può determinare la traiettoria di un elettrone Secondo il principio di indeterminazione, è impossibile misurare precisamente e contemporaneamente sia la posizione sia la velocità di una particella piccola e leggera come l’elettrone. Infatti è impossibile studiare l’elettrone senza fornirgli energia, alterando di conseguenza la sua velocità o la sua posizione. 9 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

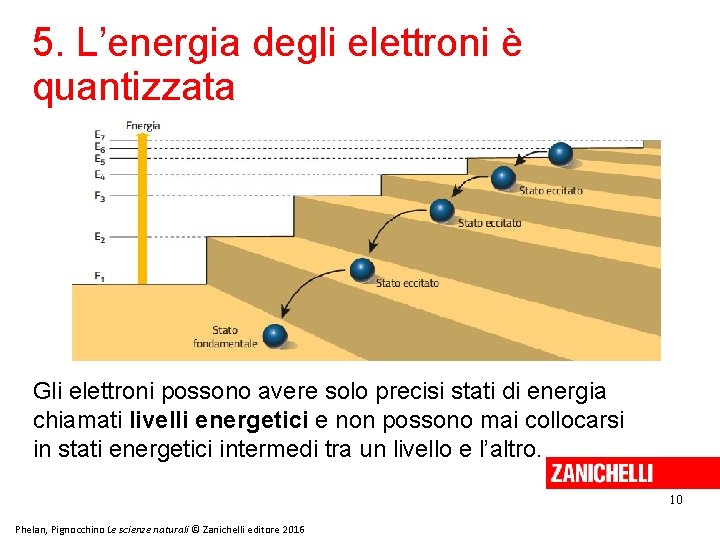
5. L’energia degli elettroni è quantizzata Gli elettroni possono avere solo precisi stati di energia chiamati livelli energetici e non possono mai collocarsi in stati energetici intermedi tra un livello e l’altro. 10 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

Lezione 3 Dagli orbitali alle configurazioni elettroniche 11 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

6. L’orbitale: dove è probabile trovare l’elettrone Ogni elettrone nell’atomo può essere descritto da un modello matematico, chiamato orbitale. L’orbitale rappresenta uno stato energetico possibile dell’elettrone e identifica la regione dello spazio entro cui si ha una probabilità del 90% di trovare l’elettrone stesso. 12 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

7. Ogni orbitale è identificato da tre numeri quantici /1 Il numero quantico principale (n) definisce il livello energetico a cui appartiene l’orbitale; n può assumere solo un valore intero positivo: 1, 2, 3… Chiamiamo livello energetico l’insieme di tutti gli elettroni che hanno il medesimo valore di n. 13 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

7. Ogni orbitale è identificato da tre numeri quantici /2 Il numero quantico secondario (l) definisce la forma dell’orbitale e il sottolivello energetico; l assume solo valori interi, positivi, compresi tra 0 e (n-1). 14 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

7. Ogni orbitale è identificato da tre numeri quantici /3 Il numero quantico magnetico (m) definisce il diverso orientamento nello spazio degli orbitali con lo stesso valore di l; m assume tutti i valori interi compresi tra –l e +l (zero incluso). 15 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

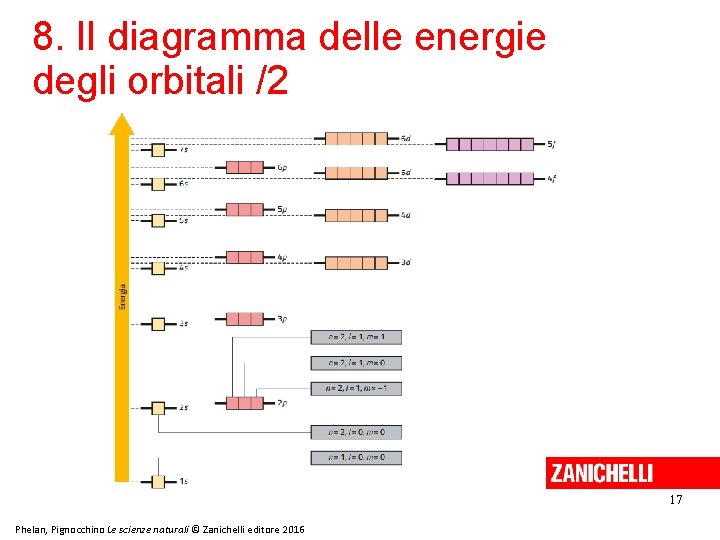
8. Il diagramma delle energie degli orbitali /1 È possibile costruire un diagramma in cui gli orbitali siano disposti in ordine crescente. Questo diagramma segue l’ordine dei livelli energetici fino al sottolivello 3 p. 16 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

8. Il diagramma delle energie degli orbitali /2 17 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

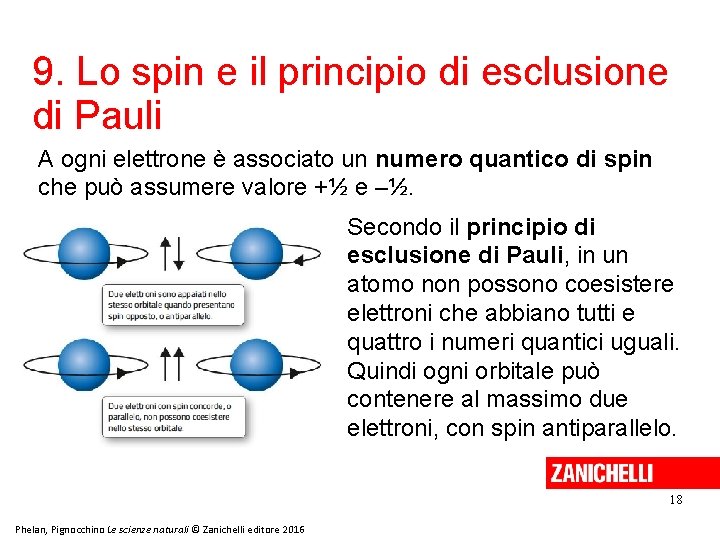
9. Lo spin e il principio di esclusione di Pauli A ogni elettrone è associato un numero quantico di spin che può assumere valore +½ e –½. Secondo il principio di esclusione di Pauli, in un atomo non possono coesistere elettroni che abbiano tutti e quattro i numeri quantici uguali. Quindi ogni orbitale può contenere al massimo due elettroni, con spin antiparallelo. 18 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

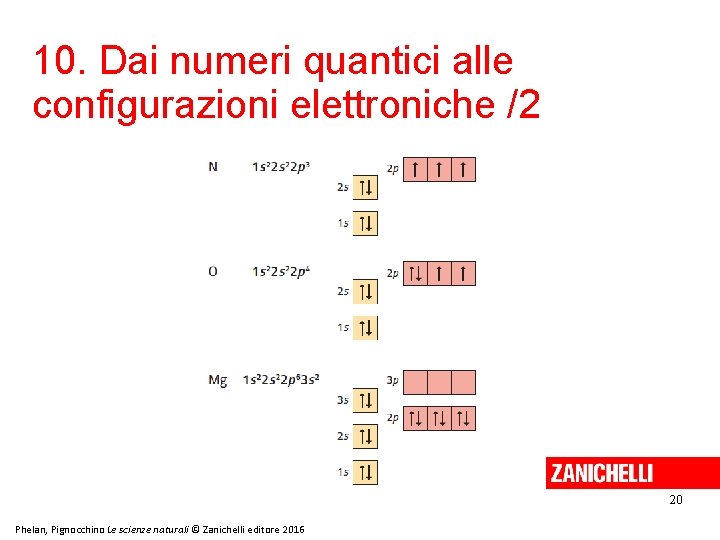
10. Dai numeri quantici alle configurazioni elettroniche /1 La configurazione elettronica di un atomo si scrive tenendo conto che: 1. gli orbitali si riempiono in ordine di energia crescente; 2. ogni orbitale può essere occupato al massimo da due elettroni con spin antiparallelo; 3. in ogni sottolivello gli elettroni si dispongono in modo da occupare il maggior numero possibile di orbitali e tendono, se non accoppiati, ad avere spin parallelo. 19 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

10. Dai numeri quantici alle configurazioni elettroniche /2 20 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

Lezione 4 Gli elettroni di valenza e le proprietà degli elementi 21 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

11. Ogni atomo ha un core e un livello di valenza Gli elettroni del livello più esterno di un atomo sono detti elettroni di valenza; tutti gli altri costituiscono il suo core. La distribuzione degli elettroni nel livello più esterno è chiamata configurazione elettronica esterna. Gli elementi di un gruppo hanno la medesima configurazione elettronica esterna. 22 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

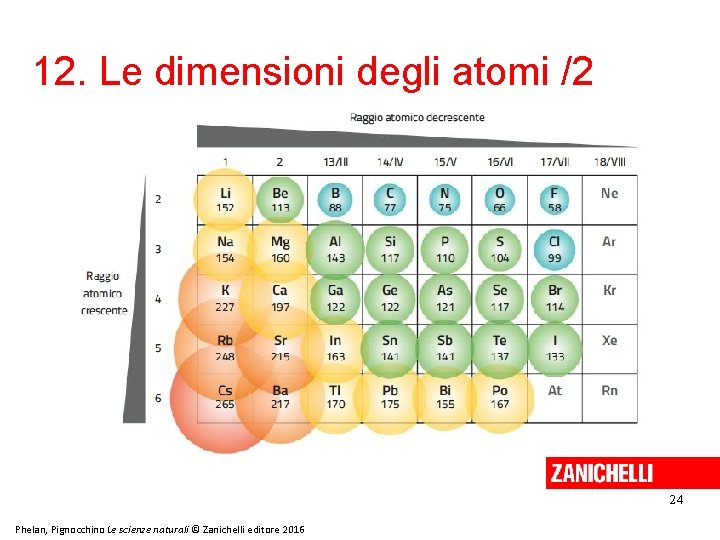
12. Le dimensioni degli atomi /1 Il raggio atomico misura la distanza media di un nucleo dagli elettroni più esterni ed è la metà della distanza tra due nuclei di atomi uguali legati tra loro. Nella tavola periodica, in modo non sempre regolare il raggio atomico diminuisce nei periodi da sinistra verso destra e aumenta lungo i gruppi dall’alto verso il basso. 23 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

12. Le dimensioni degli atomi /2 24 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

13. Energia di ionizzazione e affinità elettronica /1 L’energia di prima ionizzazione è l’energia necessaria per allontanare un elettrone da un atomo neutro allo stato gassoso, espressa in k. J/mol. Nella tavola periodica, i valori di questa grandezza crescono lungo ogni periodo e decrescono in ogni gruppo. 25 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

13. Energia di ionizzazione e affinità elettronica /2 L’affinità elettronica è l’energia emessa o assorbita quando si aggiunge un elettrone a un atomo neutro allo stato gassoso, trasformandolo in uno ione negativo. Nella tavola periodica, i valori di questa grandezza crescono lungo ogni periodo e decrescono in ogni gruppo. 26 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

13. Energia di ionizzazione e affinità elettronica /3 27 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016

14. Dagli atomi agli ioni Gli atomi dei gas nobili hanno una configurazione elettronica particolarmente stabile, che li rende inerti dal punto di vista della reattività chimica. I metalli formano facilmente cationi con la configurazione elettronica del gas nobile che li precede nella tavola periodica. I non metalli formano facilmente anioni con la configurazione elettronica del gas nobile che li segue. 28 Phelan, Pignocchino Le scienze naturali © Zanichelli editore 2016