Universita degli Studi Corsi di Laurea in Scienze



























![Quiz Co. Cl 4 -2 + 6 H 2 O [Co(H 2 O)6]+2 + Quiz Co. Cl 4 -2 + 6 H 2 O [Co(H 2 O)6]+2 +](https://slidetodoc.com/presentation_image/4b471a957e31432ed29ebb5783f98411/image-30.jpg)










- Slides: 43

Universita’ degli Studi Corsi di Laurea in Scienze Chimiche e dell’Insubria Chimica Industriale Termodinamica Chimica Equilibrio Chimico dario. bressanini@uninsubria. it http: //scienze-como. uninsubria. it/bressanini

Potenziale Chimico

Il Potenziale Chimico n Il potenziale chimico è n Per una sostanza pura n Per un gas ideale © Dario Bressanini 3

Reazioni di Equilibrio

Equilibrio A B HCN HNC H 2 O(l) H 2 O(g) n Nessuna reazione va a completamento n Tutte le reazioni raggiungono un equilibrio n All’equilibrio la velocità con cui B si trasforma in A è identica alla velocità con cui A si trasforma in B Qual’è la composizione all’Equilibrio? © Dario Bressanini 5

Equilibrio A B n Consideriamo separatamente le due reazioni A B n n Calcolando i Dr. G (uno l’opposto dell’altro) possiamo stabilire quale delle due è spontanea Supponiamo che la prima reazione sia spontanea ´ n B A Dr. G = GB, m – GA, m = m. B – m. A < 0 Allora la seconda non lo è. Come è possibile che avvenga e che si instauri un equilibrio? © Dario Bressanini 6

Grado di Avanzamento n n n Consideriamo ancora la reazione A B Supponiamo che una quantità infinitesima dx di A si trasformi in B Allora ´ ´ n dn. A = -dx (negativo perché si consuma) dn. B = dx (positivo perché si crea) x è il grado di avanzamento della reazione (e si misura ovviamente in moli) © Dario Bressanini 7

d. G n Calcoliamo ora la variazione infinitesima di energia di Gibbs, tenendo conto che ora G è anche funzione della composizione p e T costanti © Dario Bressanini m. A m. B 8

Grado di Avanzamento e d. G n n A pressione e Temperatura costanti, la variazione infinitesima di G è Sostituendo dn. A = -dx e dn. B = dx © Dario Bressanini 9

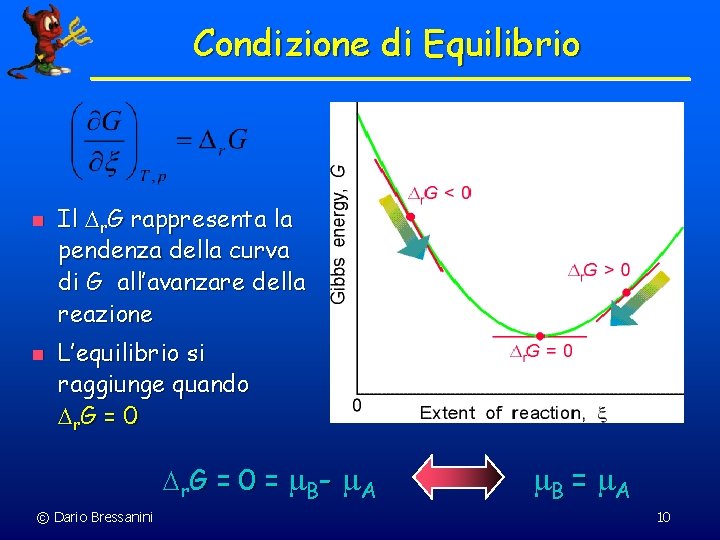
Condizione di Equilibrio n n Il Dr. G rappresenta la pendenza della curva di G all’avanzare della reazione L’equilibrio si raggiunge quando D r. G = 0 D r G = 0 = m. B - m. A © Dario Bressanini m. B = m. A 10

Condizione di Equilibrio m. B = m. A n Tenendo conto che il potenziale chimico dipende dalla composizione, dalla pressione e dalla temperatura, possiamo calcolare la composizione all’equilibrio n Dr. G > 0 reazione Endoergonica n Dr. G < 0 reazione Esoergonica © Dario Bressanini 11

Equilibrio di gas Ideali n Consideriamo un equilibrio tra due gas ideali n Per un gas ideale (con p = p/p°) © Dario Bressanini 12

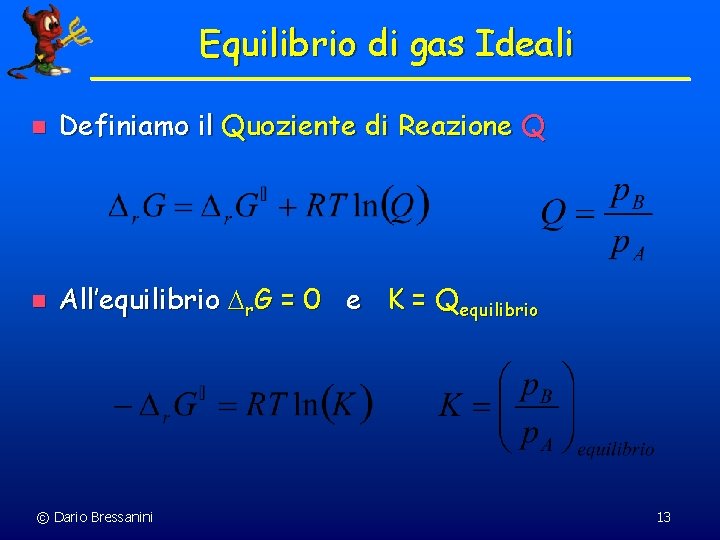
Equilibrio di gas Ideali n Definiamo il Quoziente di Reazione Q n All’equilibrio Dr. G = 0 e K = Qequilibrio © Dario Bressanini 13

K

Costante di Equilibrio n n All’equilibrio, il rapporto tra le pressioni ha un valore fisso, denominato K (Costante di Equilibrio) Abbiamo derivato questa espressione per dei gas ideali. Tuttavia, ha una validità generale. © Dario Bressanini 15

Costante di Equilibrio Termodinamica n K è la Costante di Equilibrio Termodinamica n K è un numero puro, senza dimensioni n K < 1 : reagenti favoriti n K > 1 : prodotti favoriti © Dario Bressanini 16

Reazioni tra Gas Ideali n Generalizziamo la reazione tra gas Ideali a. A(g) + b. B(g) c. C(g) + d. D(g) px = Pressione parziale di x all’equilibrio A(g) + 2 B(g) © Dario Bressanini 4 C(g) 17

Reazioni Generiche n Se abbiamo una soluzione, o un gas reale, il potenziale chimico non è più esprimibile con Che Fare? © Dario Bressanini 18

Reazioni Generiche n n n Il potenziale Chimico è una funzione di stato, ma per un gas reale o un soluto, non ne conosciamo l’espressione analitica. Per un gas reale o un soluto, definiamo la attività a come quella grandezza che rende esatta l’espressione Per un gas reale, l’attività si chiama fugacità f © Dario Bressanini 19

Attività e Fugacità n n n Per un gas reale: Se la pressione tende a zero, l’attività (fugacità f ) tende alla pressione Per un soluto: Se la concentrazione tende a zero, l’attività tende alla concentrazione D’ora in poi approssimeremo le attività con pressioni o concentrazioni. © Dario Bressanini 20

Costante di Equilibrio n Consideriamo la sintesi dell’Ammoniaca N 2(g) + 3 H 2(g) n 2 NH 3(g) La costante di equilibrio termodinamica è © Dario Bressanini 21

Costante di Equilibrio n n Se approssimiamo le fugacità con le pressioni A volte la costante approssimata con le pressioni viene chiamata Kp © Dario Bressanini 22

Equilibrio e concentrazioni n Consideriamo la reazione COCl 2 (g) CO (g) + Cl 2 (g) n Riscriviamola usando le concentrazioni ´ p = n. RT/V = [ ] RT © Dario Bressanini 23

Quoziente di Reazione n Per una reazione in soluzione a. A + b. B c. C + d. D Quoziente di Reazione Definito per un sistema non necessariamente all’equilibrio All’equilibrio: © Dario Bressanini 24

Esercizio 2 SO 3(g) 2 SO 2(g) + O 2(g) n Inizialmente abbiamo 0. 060 mol di SO 3 in 1. 0 l a 1000 K; all’equilibrio troviamo che il 36. 7% della SO 3 e’ dissociata. Calcolare la Kc Soluzione: n Chiamiamo x la concentrazione (in moli/l) di O 2 all’equilibrio n La concentrazione di SO 2 all’equilibrio e’ 2 x n Costruiamo una tabellina … © Dario Bressanini 25

Esercizio 2 SO 3(g) 2 SO 2(g) + O 2(g) Concentrazioni: Iniziali : Equilibrio : Valori : 0. 060 – 2 x 0. 038 0 2 x 0. 022 0 x 0. 011 Calcolo di 2 x : 36. 7% di SO 3 = 2 x = 0. 060 36. 7/100 = 0. 022 M © Dario Bressanini 26

Principio di Le Chatelier

Perturbando l’Equilibrio n n Supponiamo di avere un sistema all’equilibrio Disturbiamo ora l’equilibrio ´ ´ n Aggiungendo o sottraendo reagenti e/o prodotti Variando le dimensioni del contenitore Variando la pressione Variando la Temperatura Come reagisce il sistema? © Dario Bressanini 28

Principio di Le Chatelier Un sistema all’equilibrio, soggetto ad una perturbazione, risponde in modo da minimizzare l’effetto della perturbazione n Henri Le Chatelier (1850 - 1936) © Dario Bressanini Si puo’ razionalizzare considerando l’espressione della costante di equilibrio e di come varia cambiando p e T 29
![Quiz Co Cl 4 2 6 H 2 O CoH 2 O62 Quiz Co. Cl 4 -2 + 6 H 2 O [Co(H 2 O)6]+2 +](https://slidetodoc.com/presentation_image/4b471a957e31432ed29ebb5783f98411/image-30.jpg)
Quiz Co. Cl 4 -2 + 6 H 2 O [Co(H 2 O)6]+2 + 4 Cln Vi dice nulla questo equilibrio? Co. Cl 4 -2 + 6 H 2 O [Co(H 2 O)6]+2 + 4 Cl. Le (orride) statuette Segnatempo! © Dario Bressanini 30

Keq e Pressione

Variazioni di Pressione n n n La costante di equilibrio e’ definita ad una singola pressione standard Questo significa che la Keq non varia al variare della pressione Questo pero’ NON significa che la composizione all’equilibrio rimane invariata! © Dario Bressanini 32

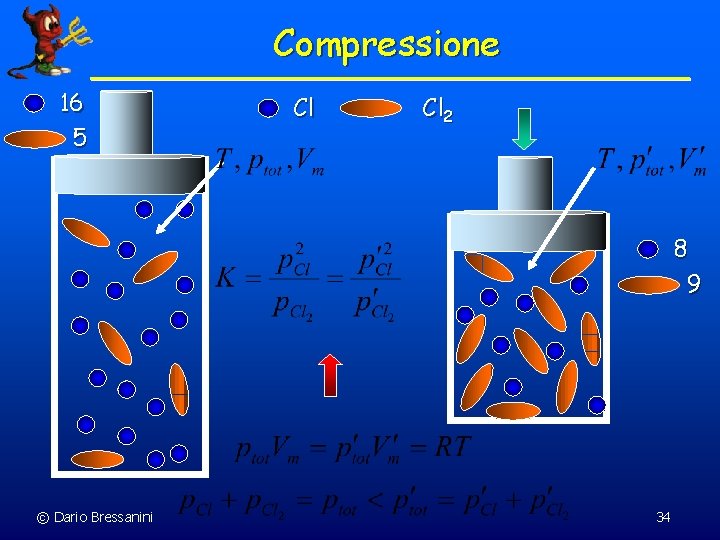
Variazioni di Pressione Cl 2(g) 2 Cl(g) n n Supponiamo di comprimere il sistema. Le pressioni parziali di Cl 2 e Cl aumentano Il numeratore aumenta di piu’ del denominatore ´ n n (p. Cl)2 contro p. Cl 2 Per mantenere costante il rapporto, l’equilibrio si sposta verso sinistra, diminuendo il numero di moli di Cl Questo e’ in accordo con il principio di Le Chatelier © Dario Bressanini 33

Compressione 16 5 Cl Cl 2 8 9 © Dario Bressanini 34

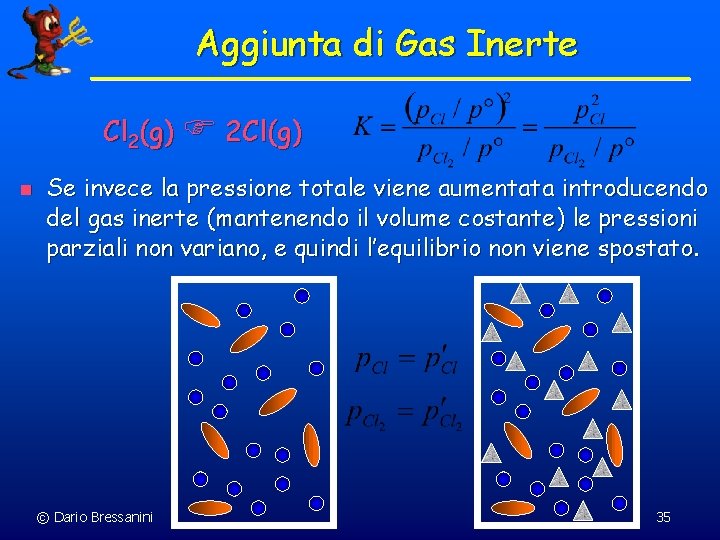
Aggiunta di Gas Inerte Cl 2(g) 2 Cl(g) n Se invece la pressione totale viene aumentata introducendo del gas inerte (mantenendo il volume costante) le pressioni parziali non variano, e quindi l’equilibrio non viene spostato. © Dario Bressanini 35

Equazione di Van’t Hoff

Variazione di Temperatura n Secondo il principio di Le Chatelier ´ ´ n aumentando la temperatura, l’equilibrio si sposta verso la reazione endotermica Diminuendo la temperatura, l’equilibrio si sposta verso la reazione esotermica Vediamo come possiamo razionalizzare questa osservazione © Dario Bressanini 37

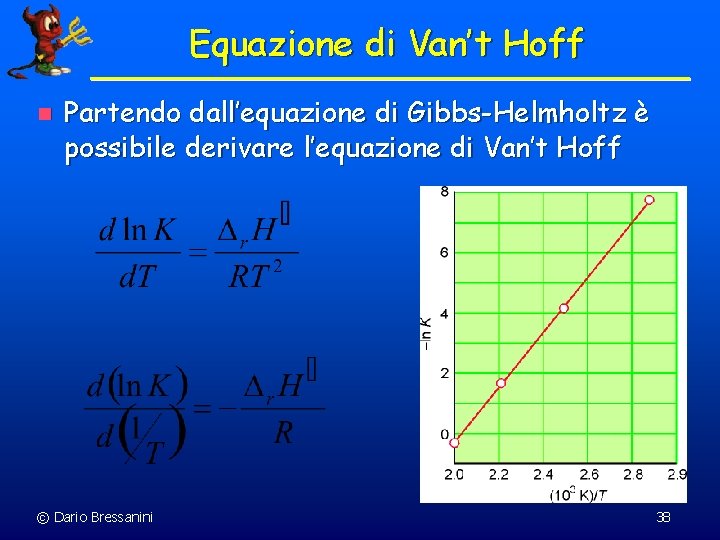
Equazione di Van’t Hoff n Partendo dall’equazione di Gibbs-Helmholtz è possibile derivare l’equazione di Van’t Hoff © Dario Bressanini 38

Equazione di Van’t Hoff n n L’equazione di Van’t Hoff permette di calcolare la costante di equilibrio a diverse temperature Assumendo che l’Entalpia di reazione non vari con la temperatura, possiamo ricavare © Dario Bressanini 39

Haber, NH 3

Ottimizzazione di Reazioni n n Le considerazioni precedenti permettono di ottimizzare la resa di una reazione chimica Prendiamo ad esempio la sintesi dell’ammoniaca N 2(g) + 3 H 2(g) 2 NH 3(g) DH = -92. 22 k. J mol-1 © Dario Bressanini 41

Ottimizzazione di Reazioni N 2(g) + 3 H 2(g) 2 NH 3(g) DH = -92. 22 k. J mol-1 La reazione è esotermica, quindi i prodotti sono favoriti a basse temperature… n Tuttavia a basse temperature la velocità delle reazioni è molto bassa n Aumentando la pressione, l’equilibrio di sposta verso destra, diminuendo il numero di moli n Possiamo poi sottrarre NH 3 dall’equilibrio ad esempio liquefandola © Dario Bressanini 42 n

Processo Haber-Bosch n Questa studio delle condizioni di reazione, e l’uso di un catalizzatore, è stata effettuata da Fritz Haber e ottimizzato da Carl Bosch © Dario Bressanini 43