Prvky I A skupiny alkalick kovy charakteristika zsadotvorn












































- Slides: 45

Prvky I. A skupiny - alkalické kovy • charakteristika: • zásadotvorné kovy • elektropozitivní prvky – jejich atomy mají nízké hodnoty elektronegativit • s – prvky – valenční elektron(y) v orbitalech s

vodík (1 H) • výskyt: • nejrozšířenější prvek ve vesmíru a třetí nejrozšířenější prvek na Zemi • volný vodík se nachází např. v plynném obalu hvězd • na Zemi se volný vodík za běžných podmínek nevyskytuje • významný biogenní prvek

Slunce

• laboratorní příprava: • reakcí elektropozitivních kovů s vodou: 2 Na + 2 H 2 O → Na. OH + H 2 • reakcí zředěných kyselin s elektropozitivními kovy: Mg + 2 HCl → H 2 + Mg. Cl 2 • elektrolýzou okyselené vody s platinovými elektrodami: (katoda – H 2, anoda – O 2)

• průmyslová výroba: • reakcí vodní páry s koksem nebo methanem: H 2 O + C → CO + H 2 (t = 1000°C) CH 4 + H 2 O → CO + H 2 (t = 1100°C) • vedlejší produkt při výrobě chlóru a hydroxidu sodného

• fyzikální vlastnosti: • v přírodě se vyskytuje jako směs tří izotopů: 1 H, 2 H, 3 H • bezbarvý plyn, bez chuti a zápachu, 14, 4 x lehčí než vzduch • obtížně se zkapalňuje a přeměňuje na pevnou látku, uchovává se v tlakových lahvích s červeným pruhem

• chemické vlastnosti: • molekulový vodík je málo reaktivní - vysoká vazebná energie • zapálen na vzduchu shoří - reaguje se vzdušným kyslíkem za vzniku vody - exotermická reakce: 2 H 2(g) + O 2(g) → 2 H 2 O(l) • při laboratorní teplotě oba plyny spolu nereagují (bez iniciace)

• při teplotě větší než 600°C probíhá slučování explozivně, tím prudčeji, čím je směs H 2 a O 2 blíže poměru 2: 1, (třaskavý plyn) • redukční vlastnosti - výroba kovů: Cu. O + H 2 → H 2 O + Cu

• elektrickým výbojem vzniká atomární vodík (H) (vodík ve stavu zrodu, nascentní vodík) – velmi reaktivní – nestálý - existuje velmi krátkou dobu a slučuje se na molekulární vodík

1 H • využití • • • výroba amoniaku, methanolu, chlorovodíku hydrogenace olejů redukční činidlo - výroba kovů řezání kovů raketové palivo

motocykl využívající vodík jako palivo

2 H • využití - výroba těžké vody pro jaderné reaktory 3 H – vzniká působením kosmického záření na vzdušný dusík • využití - sledování pohybu spodních vod, tritiová barva (displeje hodinek)

využití tritia

sodík (11 Na) - alkalický kov • výskyt: • • kamenná sůl - Na. Cl chilský ledek - Na. NO 3 kryolit – Na 3 Al. F 6 borax - Na 2 B 4 O 7· 10 H 2 O glauberit - Na 2 SO 4·Ca. SO 4 Glauberova sůl - Na 2 SO 4· 10 H 2 O mořská voda (Na. Cl)

• průmyslová výroba: • elektrolýzou roztavené směsi 40% Na. Cl a 60% Ca. Cl 2 při teplotě 580 °C (Ca. Cl 2 snižuje teplotu tání) • katoda: Na + + e- Na • anoda: Cl- - e- Cl (Cl 2)

• fyzikální vlastnosti: • měkký, nízkotající, stříbrolesklý kov, lze jej krájet nožem • krystalizuje v kubické soustavě

sodík

• chemické vlastnosti: • uchovává se pod vrstvou petroleje • s kyslíkem reaguje za vzniku oxidu (Na 2 O) a peroxidu sodného (Na 2 O 2) • reaguje s vodou: 2 Na + 2 H 2 O → 2 Na. OH + H 2

• má redukční vlastnosti: Al 2 O 3 + 6 Na → Al + 3 Na 2 O • barví plamen žlutě

reakce sodíku s vodou


hoření sodíku v chlóru – vzniká chlorid sodný

• sloučeniny: • halogenidy – bezbarvé, krystalické látky – mají vysokou teplotu tání

• chlorid sodný – získává se z přírodního materiálu – kamenná sůl (dolování) nebo vyluhováním některých ložisek vodou – mořská sůl (odpařování) – kuchyňská sůl vlhne (obsahuje malé množství nečistot, které jsou hygroskopické - hlavně Mg. Cl 2)

krystal halitu na jílovci

• využití: • výchozí látka pro přípravu řady anorganických sloučenin, např. hydroxidu sodného, sody, chlóru, sodíku

• sulfid sodný – bílá krystalická látka, činidlo v analytické chemii

• hydroxid sodný – výroba elektrolýzou roztoku chloridu sodného a) amalgámovým způsobem: od tohoto postupu se v současné době již upouští Na. Cl → Na+ + Cl. K : Na+ + e- → Na Na + Hg → Na. Hg 2 Na. Hg + 2 H 2 O → 2 Na. OH(aq) + 2 Hg + H 2 A : Cl- - e- → Cl 2 Cl → Cl 2

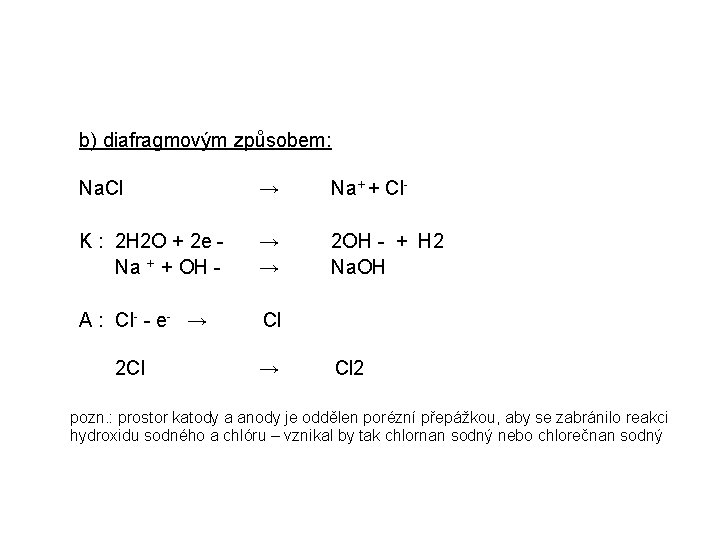
b) diafragmovým způsobem: Na. Cl → Na+ + Cl- K : 2 H 2 O + 2 e Na + + OH - → → 2 OH - + H 2 Na. OH A : Cl- - e- → Cl 2 Cl → Cl 2 pozn. : prostor katody a anody je oddělen porézní přepážkou, aby se zabránilo reakci hydroxidu sodného a chlóru – vznikal by tak chlornan sodný nebo chlorečnan sodný

– bezbarvá krystalická látka, dobře rozpustná ve vodě, hygroskopická, silná zásada – absorbuje oxid uhličitý: 2 Na. OH + CO 2 → Na 2 CO 3 + H 2 O – absorbuje sulfan: 2 Na. OH + H 2 S →Na 2 S + H 2 O • thiosíran sodný – ve vodě dobře rozpustný – bezvodý nebo pentahydrát (Na 2 S 2 O 3· 5 H 2 O) – využívá se v analytické chemii (odměrná analýza)

• uhličitan sodný (bezvodá soda) – výroba – E. Solvay: NH 3 + CO 2 + H 2 O + Na. Cl → Na. HCO 3 + NH 4 Cl 2 Na. HCO 3 → Na 2 CO 3 + H 2 O + CO 2, t = 150 C (v pecích) – bezvodá soda – bílý prášek, dobře rozpustný ve vodě – krystalová soda – krystalický dekahydrát (Na 2 CO 3· 10 H 2 O), na vzduchu větrá – heptahydrát (Na 2 CO 3· 7 H 2 O) až monohydrát (Na 2 CO 3·H 2 O) • využití - výroba mýdel, skla

• hydrogenuhličitan sodný (jedlá soda) • využití - šumivé prášky k přípravě limonád, lékařství (proti překyselení žaludku)

• dusičnan sodný • získává se z přírodních ložisek – chilský ledek • využití - hnojivo • dusitan sodný – příprava tepelným rozkladem dusičnanu sodného – bílá krystalická látka, dobře rozpustná ve vodě • využití – výroba azobarviv

• síran sodný – vedlejší produkt při výrobě kyseliny chlorovodíkové: 2 Na. Cl + H 2 SO 4 → Na 2 SO 4 + HCl

draslík (19 K) • výskyt: • sylvín - KCl • mořská voda (0, 06 % KCl)

sylvín

draslík

• fyzikální vlastnosti: • stříbrobílý, měkký kov • dobře vede teplo a elektrický proud • krystalizuje v kubické soustavě • chemické vlastnosti: • reaktivnější než sodík, s vodou prudce reaguje: • 2 K + 2 H 2 O → H 2 + 2 KOH

• barví plamen fialově, redukční vlastnosti • sloučeniny: • hydroxid draselný – bezbarvá krystalická látka, dobře rozpustná ve vodě, hygroskopická, silná zásada – vyrábí se elektrolýzou roztoku chloridu draselného

– absorbuje oxid uhličitý: 2 KOH + CO 2 → K 2 CO 3 + H 2 O – absorbuje sulfan: 2 KOH + H 2 S → K 2 S + H 2 O

• uhličitan draselný (potaš) – bílá hygroskopická látka • využití - výroba tabulového skla

potaš

• dusičnan draselný • využití - silné oxidační činidlo (střelný prach, pyrotechnika)

• chlorečnan draselný – příprava zaváděním chloru za tepla do roztoku hydroxidu draselného: 6 KOH + 3 Cl 2 → KCl. O 3 + 5 KCl +3 H 2 O – bílá hygroskopická látka • využití - v malém množství v zápalkách a výbušninách

• síran draselný – bílá, hygroskopická látka – dobře rozpustná ve vodě • využití - hnojivo