HALOGENIDY Prvky 7 skupiny Prvky 7 skupiny VII



















- Slides: 20

HALOGENIDY Prvky 7. skupiny

Prvky 7. skupiny (VII. A) jiný název = halogeny jsou reaktivní tvoří dvouatomové molekuly „barevné“ jsou jedovaté Mají 7 valenčních elektronů – skupina VII. A.

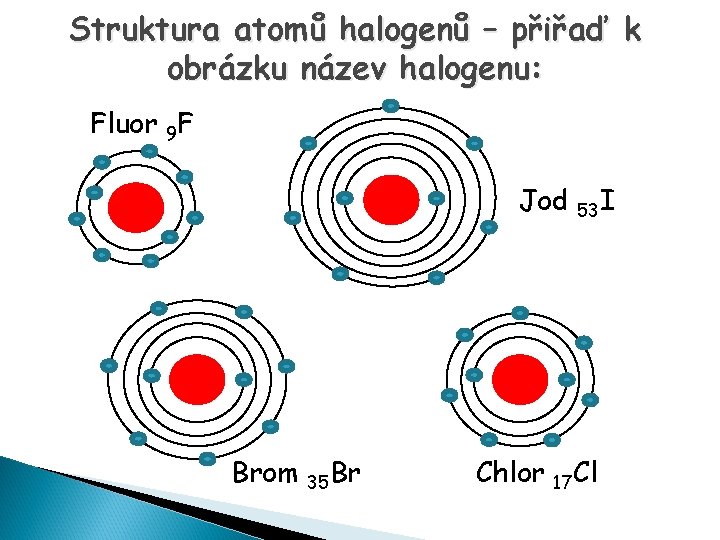
Struktura atomů halogenů – přiřaď k obrázku název halogenu: Fluor 9 F Jod Brom 35 Br Chlor 53 I 17 Cl

HALOGENIDY Dvouprvkové sloučeniny halogenů s jinými prvky (kovy). Připomeň si halogeny - doplň značky prvků a protonové číslo. • • Fluor Chlor Brom Jod ___ F ___ Cl ___ Br ___ I 9 17 35 53 ÚKOL: Z daných sloučenin vyber a podtrhni halogenidy: Na. Cl, Na. OH, K 2 O, SCl 4, Ca. F 2, Pb. S, Al. Cl 3

Oxidační číslo prvků udává zdánlivý náboj prvku ve sloučenině může nabývat hodnoty kladné nebo záporné u volných atomů nebo víceatomových molekul prvku má hodnotu 0! jeho velikost ve sloučenině závisí na elektronegativitě daného prvku (čím vyšší – záporné, čím nižší – kladné) zapisuje se římskými číslicemi od I – VIII ÚKOL: Zjisti v PSP elektronegativitu těchto prvků: Na ……. . , 1, 01 F. ……. . , 4, 10 Ca ………. . , 1, 04 Cl ……. . 2, 83. Na základě zjištění urči znaménko oxidačního čísla + 2 -. ve sloučeninách Na. Cl + -a Ca. F

Křížové pravidlo 1) Pro tvorbu vzorců i názvů platí v chemii obecně tzv. křížové pravidlo, tj. co je v názvu na prvním místě, je ve vzorci na místě druhém a naopak. 2) Pro psaní vzorců je důležité oxidační číslo prvků, které zapisujeme vpravo nahoře. 3) Ve vzorcích dvouprvkových sloučenin má jeden prvek kladné a druhý záporné oxidační číslo. 4) Součet oxidačních čísel ve vzorci = 0. 5) Oxidační číslo halogenů v halogenidu je vždy –I (F-I, Cl-I, Br-I, I-I). 6) Oxidační číslo druhého prvku se řídí koncovkou přídavného jména.

Vzorový příklad – tvoření vzorce Chlorid vápenatý Ca Cl Ca +II Cl-I Ca +II Cl 2 -I Ca. Cl 2 Název halogenidu je tvořen podstatným jménem fluorid, chlorid, bromid, jodid a přídavným jménem odvozeným od druhého prvku.

Procvičování Fluorid vápenatý Chlorid draselný Bromid hlinitý Jodid arseničný Fluorid sírový Jodid olovnatý Řešení

FLUOR – F 2 nažloutlý plyn prudce reaktivní (reaguje téměř se všemi prvky) ve starším českém názvosloví – „kazík“ (protože ochotně reaguje s každou látkou a tím ji „kazí“) ve sloučeninách pevně drží, např. snižuje kazivost zubů (jeho sloučenina je součást zubní skloviny) Použití: součást zubních past, výroba teflonu

Minerály obsahující fluorit (kazivec) Obr. 1 apatit Obr. 2

CHLOR – Cl 2 žlutozelený plyn je těžší než vzduch je silně jedovatý Použití: dezinfekce pitné vody výroba plastů(PVC), kyseliny chlorovodíkové bělení látek a papíru Zneužití: bojový plyn (1. svět. válka) – yperit (1915 – Belgie - Yprés – popsal E. M. Remarque – Na západní frontě klid)

Obr. 3

BROM – Br 2 hnědá kapalina rychle se vypařuje poškozuje oči a pokožku Použití: - chemická výroba - léčiva - jeho sloučenina se stříbrem se používá při výrobě fotografií (negativ x pozitiv)

JOD –I 2 pevná látka barva - černá, s kovovým leskem sublimuje (při zahřívání se mění přímo v páru) je nezbytný pro správný vývoj člověka (funkce štítné žlázy – jeho nedostatek může způsobit duševní poruchy) Použití: přidává se do kuchyňské soli, dezinfekce (jodová tinktura)

Obr. 4

Procvičování Doplň značky halogenů a přiřaď jim vlastnosti: fluor jod brom chlor F …. . I …. . Br …. . Cl …. . 1, 4 ………. . 3, 7 ………. . 2, 6 ………. . 1, 5 ………. . 1) plynná látka 2) kapalina 3) pevná látka 4) nažloutlá barva 5) žlutozelená barva 6) hnědá barva 7) černá barva

Sůl kamenná (halit) (Na. Cl) má krystaly tvaru krychle obsažena v solných jezerech (až 30 %), v mořích (3, 5 %) čirá nebo zbarvená do šeda průsvitná, dokonale štěpná váže vzdušnou vlhkost do ČR se dováží z Polska

využití soli kamenné Solný důl ve městě Wieliczka v Polsku posypový materiál na vozovky chemický průmysl (výroba sodíku, chlóru, jedlé soli) sklářství keramický a kožedělný průmysl obarvená koupelová sůl římští legionáři dostávali část peněz „v soli“ nejstarší hlubinný solný důl je v Polsku – město

fluorit (kazivec) (ca. F 2) fluorid vápenatý dobře štěpný, křehký zbarvení: fialový, žlutý, hnědý, zelený Využití: hutnictví (urychluje tavení rud) výroba teflonu výroba fluorovodíku (HF) výroba leptaných skel získává se z něj fluor (fluoridace pitné vody)

Citace a zdroje: Obr. 1: Soubor: USDA Mineral Flourite 93 c 3962. jpg. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 -2005 [cit. 2013 -11 -13]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: USDA_Mineral_Flourite_93 c 3962. jpg Obr. 2: Soubor: Apatite crystals. jpg. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 -2006 [cit. 2013 -11 -13]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: Apatite_crystals. jpg Obr. 3: Soubor: Chlorine. jpg. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 -2007 [cit. 2013 -11 -13]. Dostupné z: http: //cs. wikipedia. org/wiki/Soubor: Chlorine. jpg Obr. 4: File: Iodine-sample. jpg. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 -2007 [cit. 2013 -11 -13]. Dostupné z: http: //commons. wikimedia. org/wiki/File: Iodine-sample. jpg