METODI DI OTTENIMENTO DI EPC RISOLUZIONE CLASSICA CINETICA









- Slides: 48

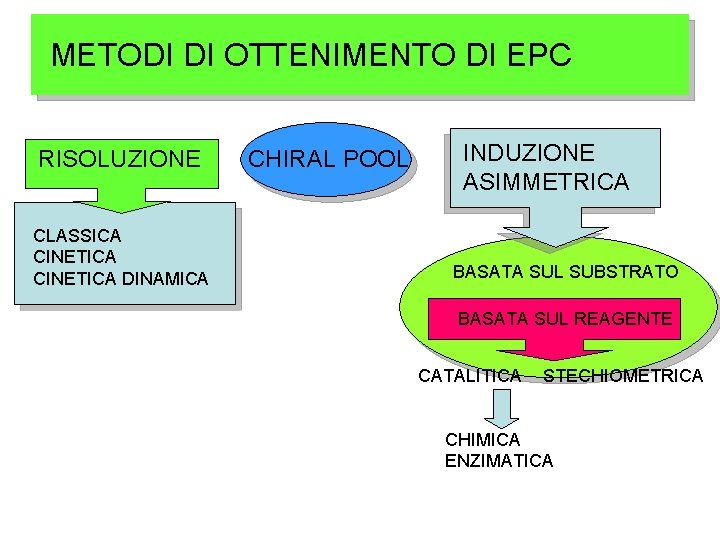
METODI DI OTTENIMENTO DI EPC RISOLUZIONE CLASSICA CINETICA DINAMICA CHIRAL POOL INDUZIONE ASIMMETRICA BASATA SUL SUBSTRATO BASATA SUL REAGENTE CATALITICA STECHIOMETRICA CHIMICA ENZIMATICA

RISOLUZIONE DI RACEMI

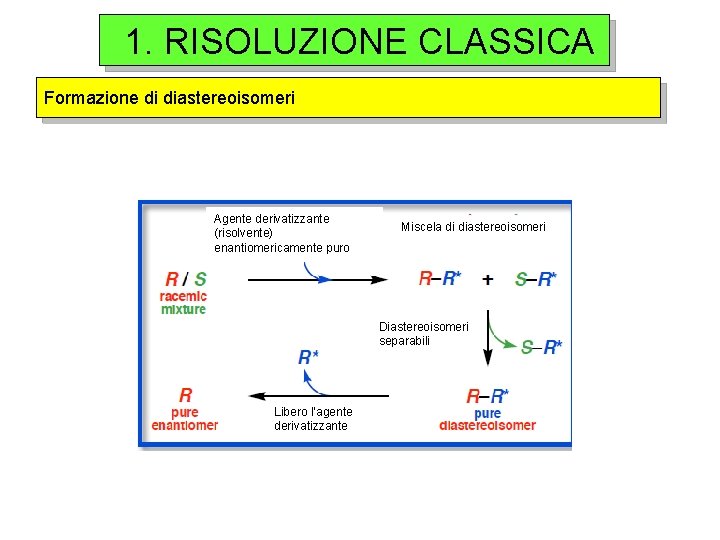
1. RISOLUZIONE CLASSICA Formazione di diastereoisomeri Agente derivatizzante (risolvente) enantiomericamente puro Miscela di diastereoisomeri Diastereoisomeri separabili Libero l’agente derivatizzante

1. RISOLUZIONE CLASSICA Formazione di sali diastereoisomeri

1. RISOLUZIONE CLASSICA Formazione di composti diastereoisomeri Agente derivatizzante

1. RISOLUZIONE CLASSICA Risoluzione fisica

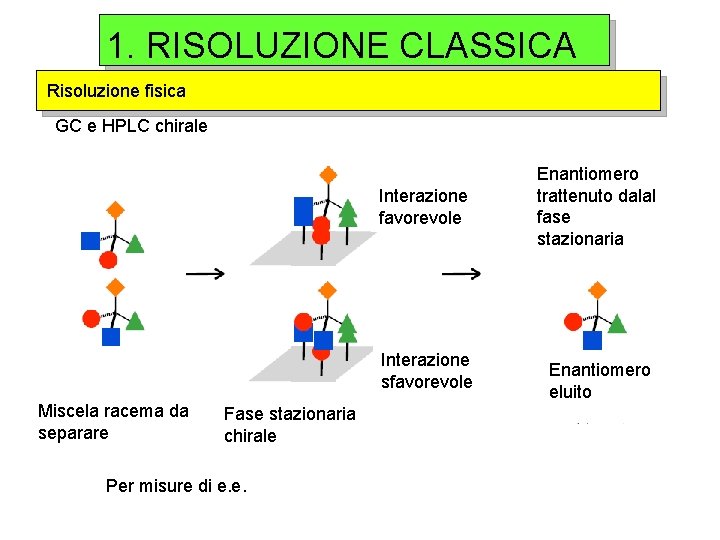
1. RISOLUZIONE CLASSICA Risoluzione fisica GC e HPLC chirale Interazione favorevole Interazione sfavorevole Miscela racema da separare Fase stazionaria chirale Per misure di e. e. Enantiomero trattenuto dalal fase stazionaria Enantiomero eluito

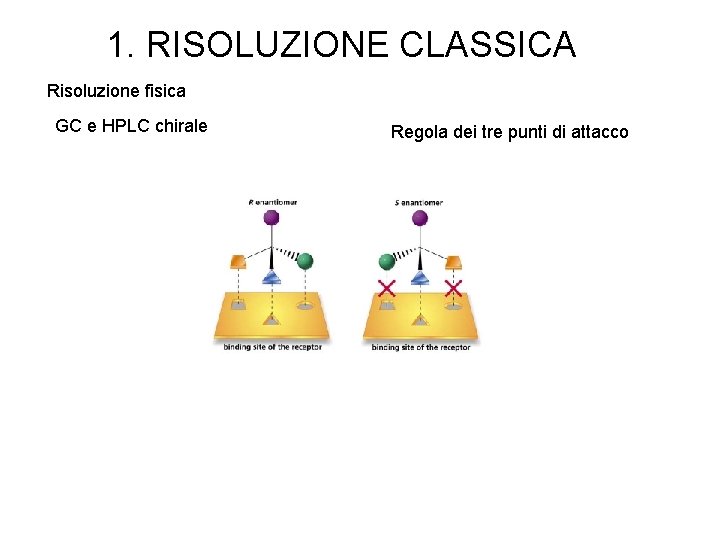
1. RISOLUZIONE CLASSICA Risoluzione fisica GC e HPLC chirale Regola dei tre punti di attacco

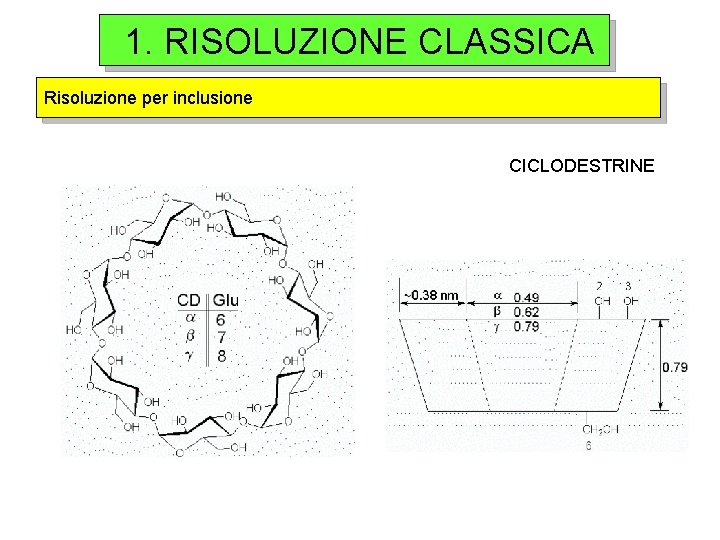
1. RISOLUZIONE CLASSICA Risoluzione per inclusione CICLODESTRINE

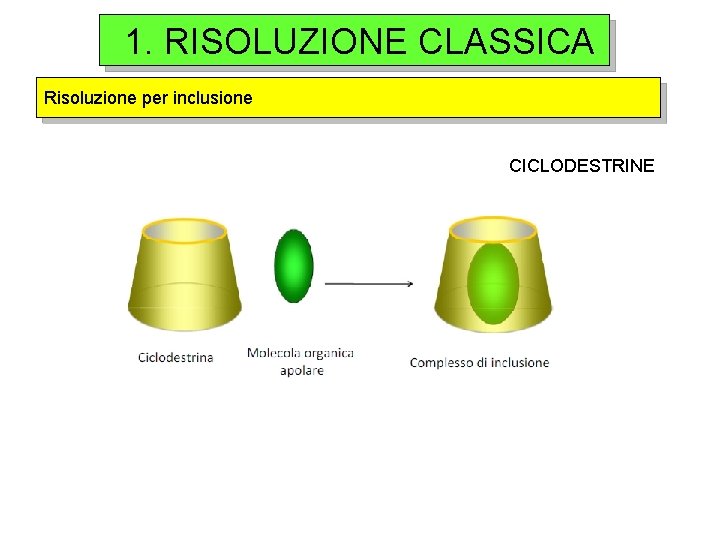
1. RISOLUZIONE CLASSICA Risoluzione per inclusione CICLODESTRINE

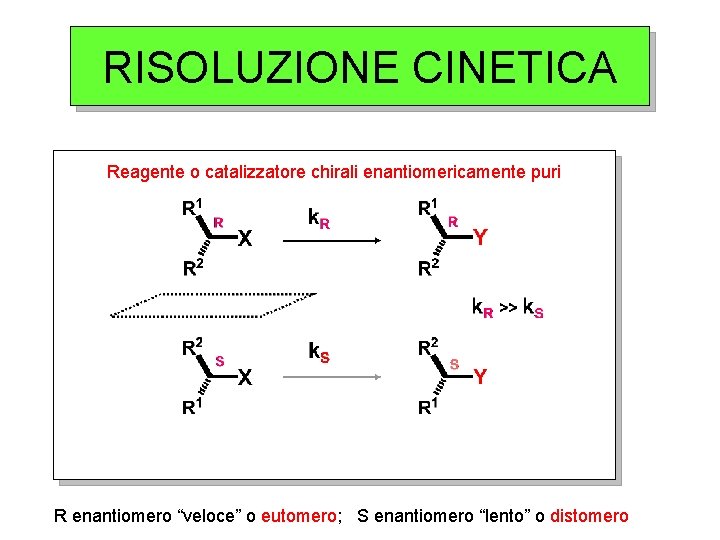
RISOLUZIONE CINETICA Reagente o catalizzatore chirali enantiomericamente puri R enantiomero “veloce” o eutomero; S enantiomero “lento” o distomero

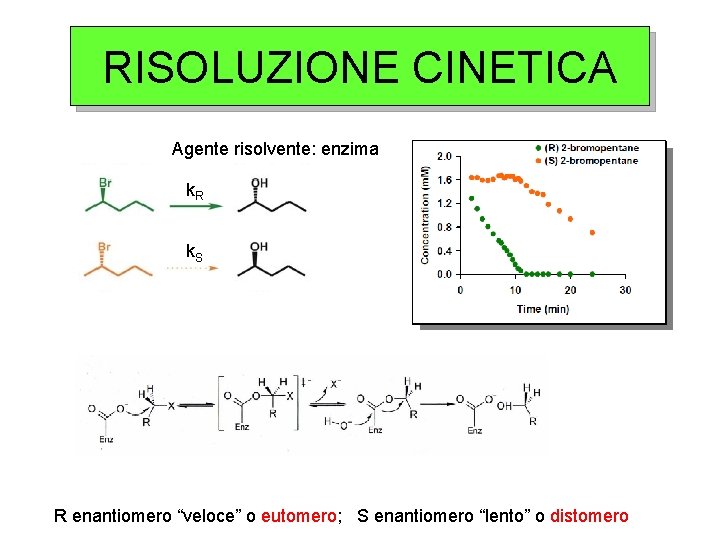
RISOLUZIONE CINETICA Agente risolvente: enzima k. R k. S R enantiomero “veloce” o eutomero; S enantiomero “lento” o distomero

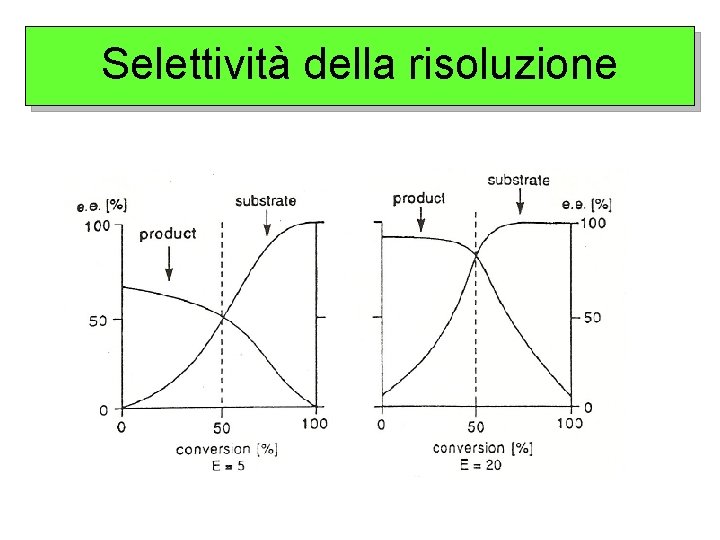
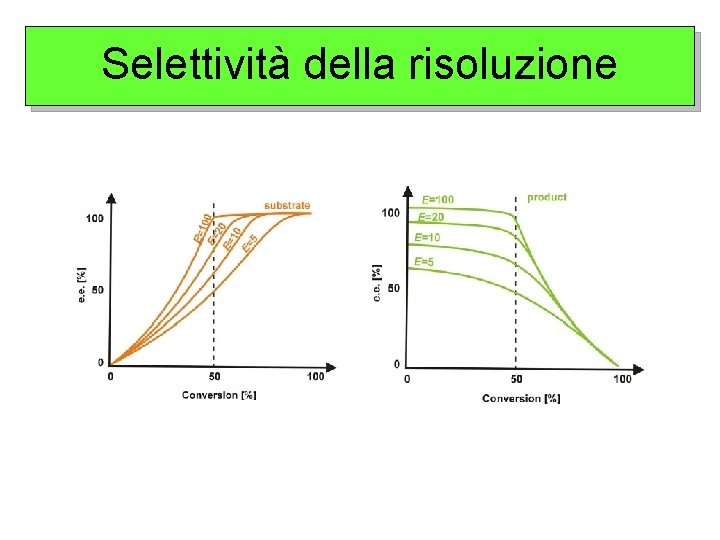
Selettività della risoluzione E= k. R Rapporto enantiomerico k. S R enantiomero “veloce”. Coincide con P (prodotto) della seconda relazione. S enantiomero “ lento”. Coincide con S (substrato non reagito) della seconda relazione. E = 1 nessuna stereoselettività E fino a 10: bassa selettività E 15 – 30 modesta – buona E > 200 eccellente

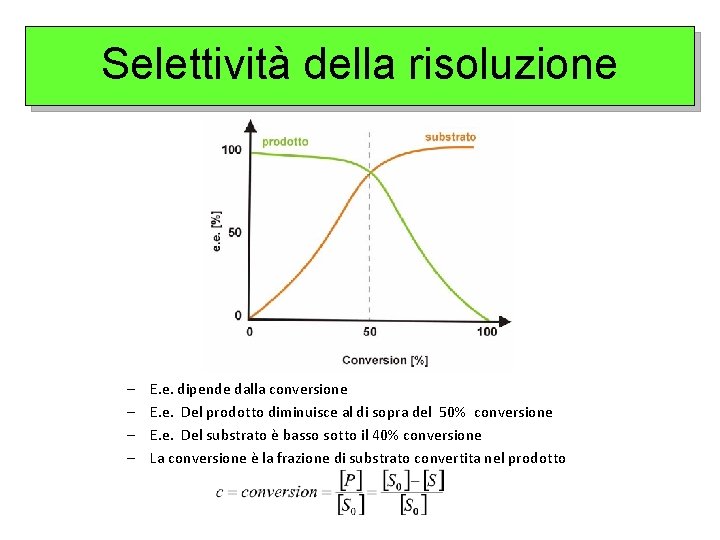
Selettività della risoluzione – – E. e. dipende dalla conversione E. e. Del prodotto diminuisce al di sopra del 50% conversione E. e. Del substrato è basso sotto il 40% conversione La conversione è la frazione di substrato convertita nel prodotto

Selettività della risoluzione

Selettività della risoluzione

Risoluzioni cinetiche (KR) Ø Resa teorica massima del 50% Ø Separazione dei prodotti necessaria Ø Eventuale smaltimento dell’enantiomero indesiderato

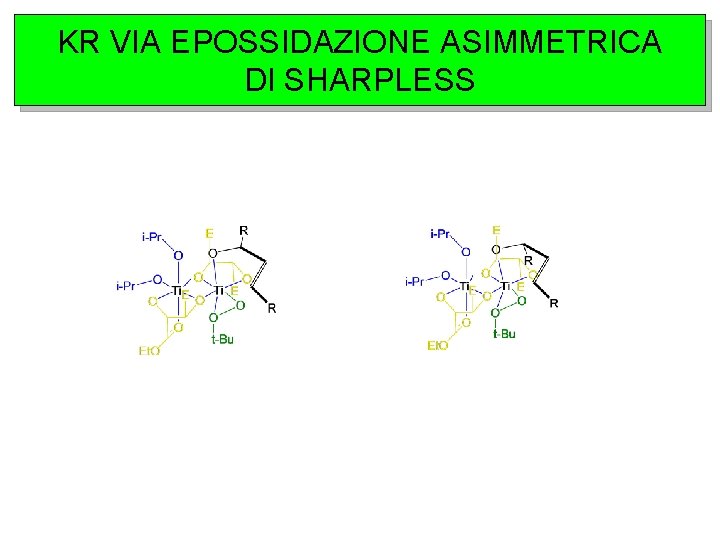
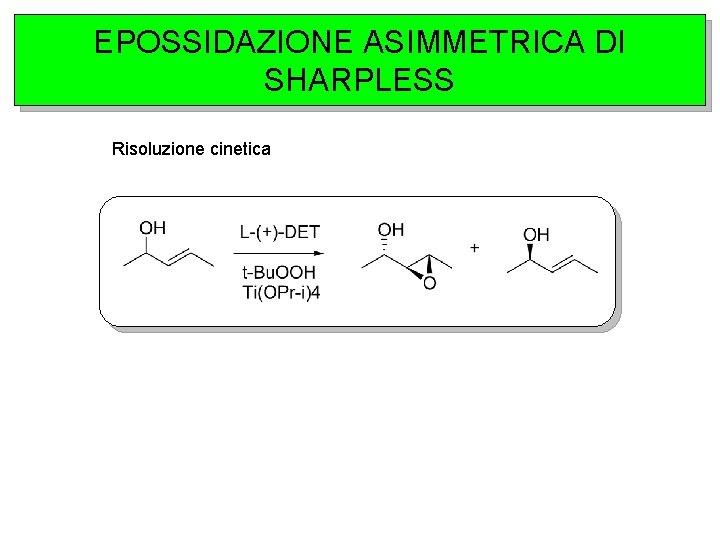
KR VIA EPOSSIDAZIONE ASIMMETRICA DI SHARPLESS Risoluzione cinetica

KR VIA EPOSSIDAZIONE ASIMMETRICA DI SHARPLESS

EPOSSIDAZIONE ASIMMETRICA DI SHARPLESS Risoluzione cinetica

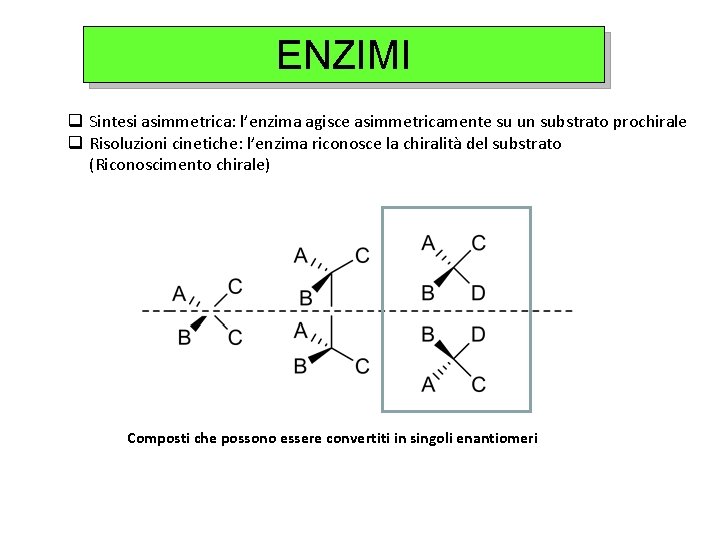
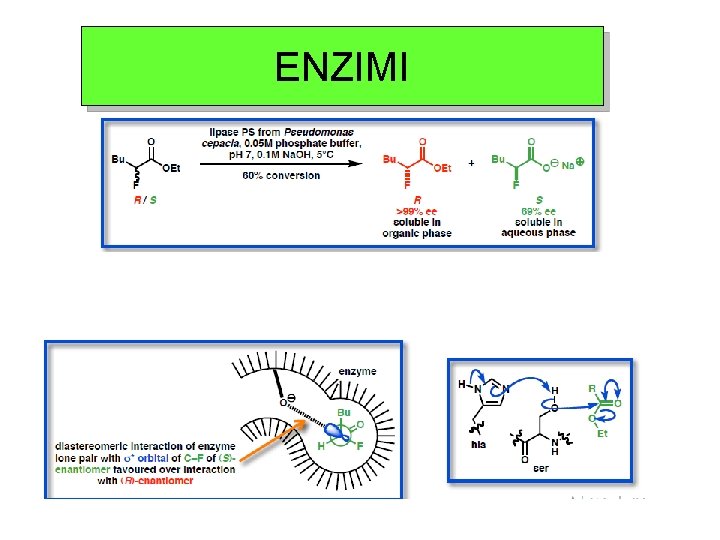
ENZIMI q Sintesi asimmetrica: l’enzima agisce asimmetricamente su un substrato prochirale q Risoluzioni cinetiche: l’enzima riconosce la chiralità del substrato (Riconoscimento chirale) Composti che possono essere convertiti in singoli enantiomeri

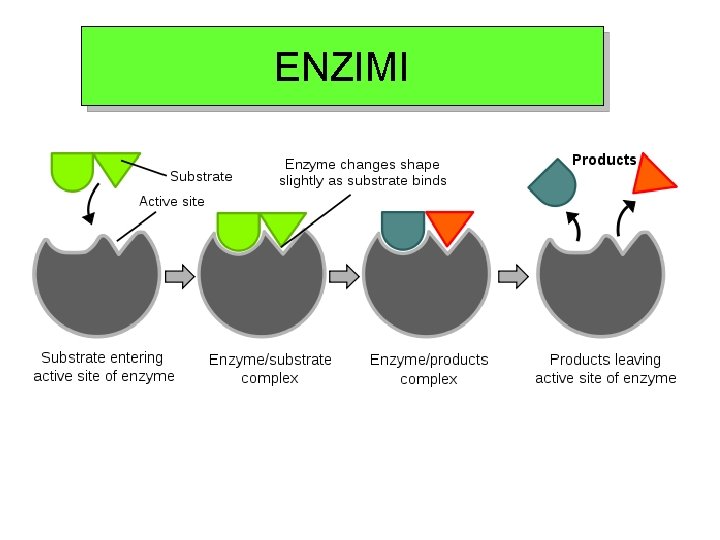
ENZIMI

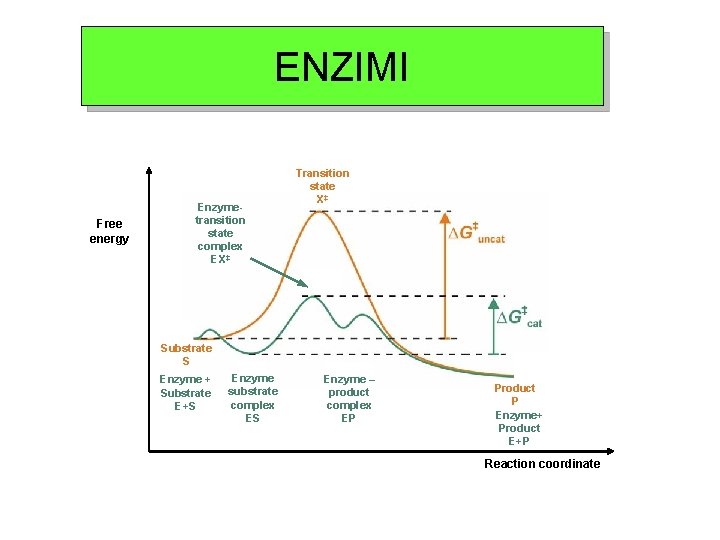
ENZIMI Free energy Enzymetransition state complex EX‡ Transition state X‡ Substrate S Enzyme + Substrate E+S Enzyme substrate complex ES Enzyme – product complex EP Product P Enzyme+ Product E+P Reaction coordinate

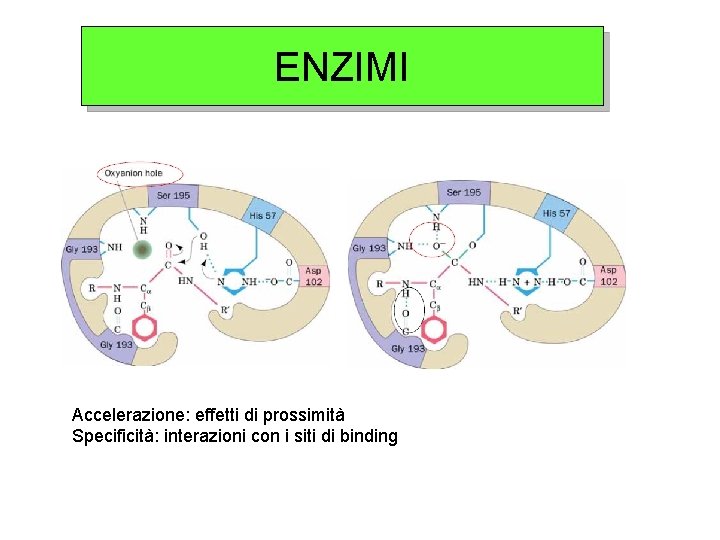
ENZIMI Accelerazione: effetti di prossimità Specificità: interazioni con i siti di binding

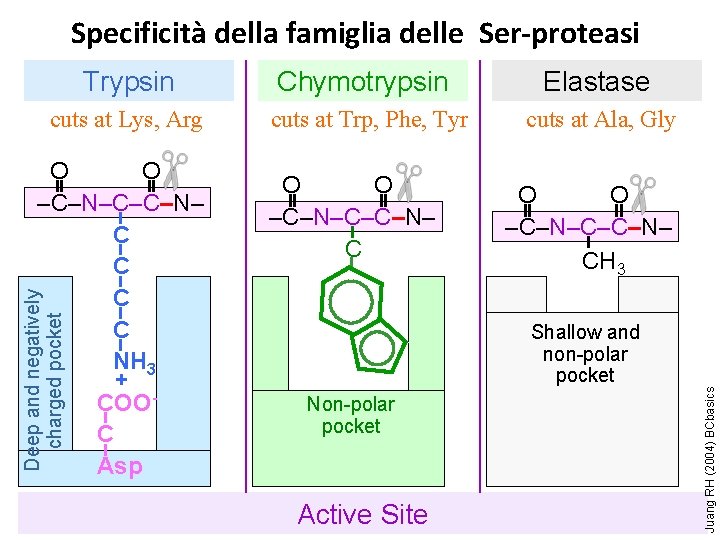
Specificità della famiglia delle Ser-proteasi Trypsin Chymotrypsin Elastase cuts at Lys, Arg cuts at Trp, Phe, Tyr cuts at Ala, Gly O O –C–N–C–C–N– CH 3 Shallow and non-polar pocket Non-polar pocket Active Site Juang RH (2004) BCbasics Deep and negatively charged pocket O O –C–N–C–C–N– C C NH 3 + COOC Asp

ENZIMI IDROLASI ESTERASI. Substrato naturale: esteri di acidi grassi. Esempi PLE (Porcine Liver Esterase), HLE (Horse Liver Esterase) LIPASI substrato naturale: trigliceridi (esteri del glicerolo e di acidi grassi). Esempi PPL (Porcine Pancreatic Lipase), PFL (Pseudomonas Fluorescens Lipase), PROTEASI substrato naturale: peptidi, proteine Esempi: a-chimotripsina

ENZIMI

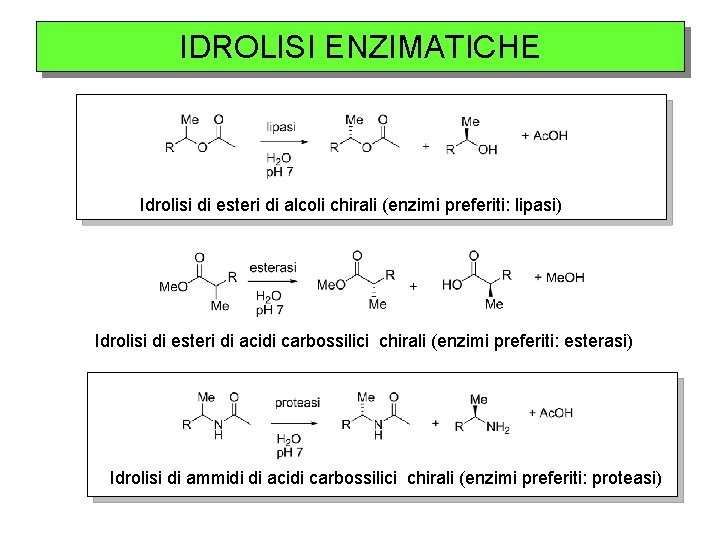
IDROLISI ENZIMATICHE Idrolisi di esteri di alcoli chirali (enzimi preferiti: lipasi) Idrolisi di esteri di acidi carbossilici chirali (enzimi preferiti: esterasi) Idrolisi di ammidi di acidi carbossilici chirali (enzimi preferiti: proteasi)

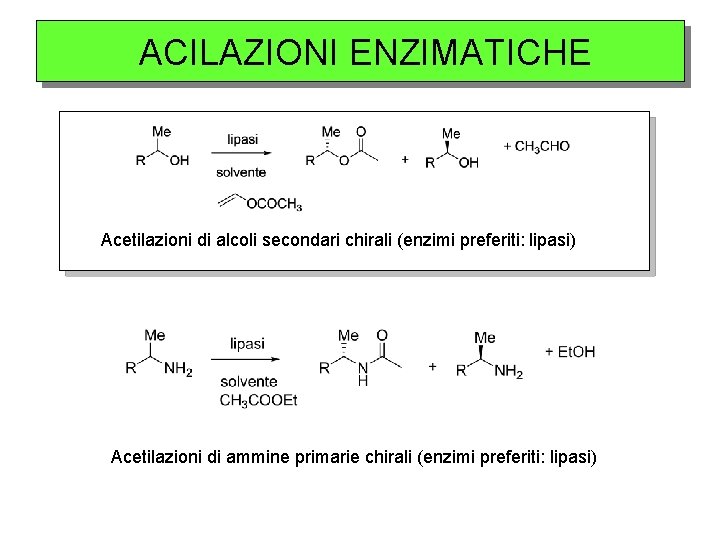
ACILAZIONI ENZIMATICHE Acetilazioni di alcoli secondari chirali (enzimi preferiti: lipasi) Acetilazioni di ammine primarie chirali (enzimi preferiti: lipasi)

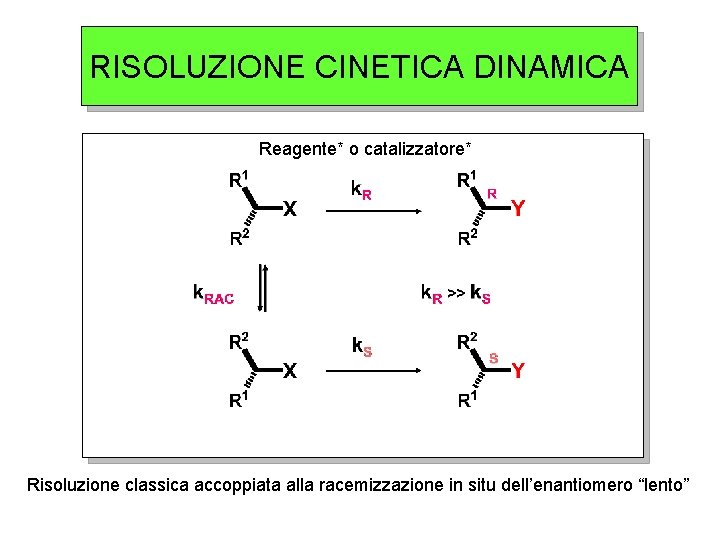
RISOLUZIONE CINETICA DINAMICA Reagente* o catalizzatore* Risoluzione classica accoppiata alla racemizzazione in situ dell’enantiomero “lento”

RISOLUZIONE CINETICA DINAMICA Per una DKR efficiente La corrispondente KR deve essere irreversibile La stereoselettività deve essere alta (k. S >> k. R o k. R>> k. S), (es. E = k. R/k. S > 20) La velocità di racemizzazione deve essere maggiore della velocità di reazione La racemizzazione del prodotto deve essere trascurabile

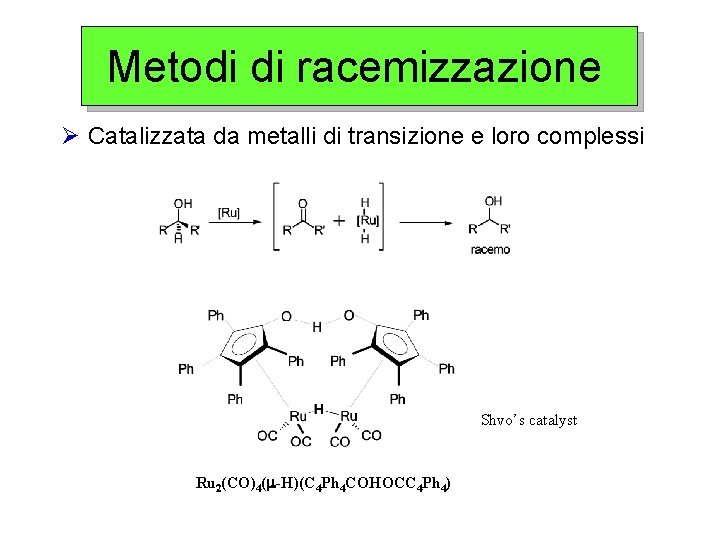
Metodi di racemizzazione Ø Catalizzata da metalli di transizione e loro complessi Shvo’s catalyst Ru 2(CO)4( -H)(C 4 Ph 4 COHOCC 4 Ph 4)

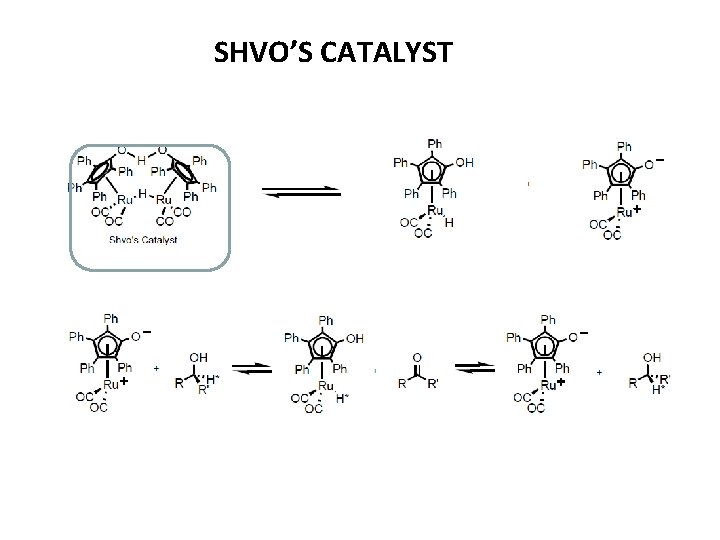
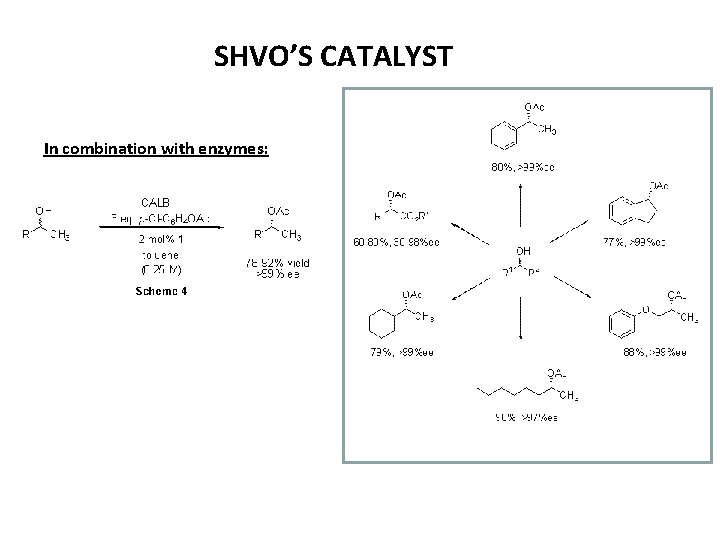
SHVO’S CATALYST

SHVO’S CATALYST In combination with enzymes:

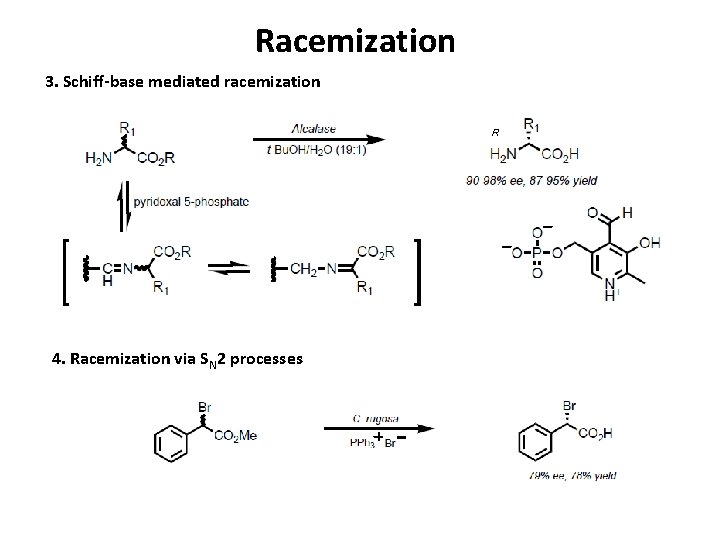
Racemization 3. Schiff-base mediated racemization R 4. Racemization via SN 2 processes

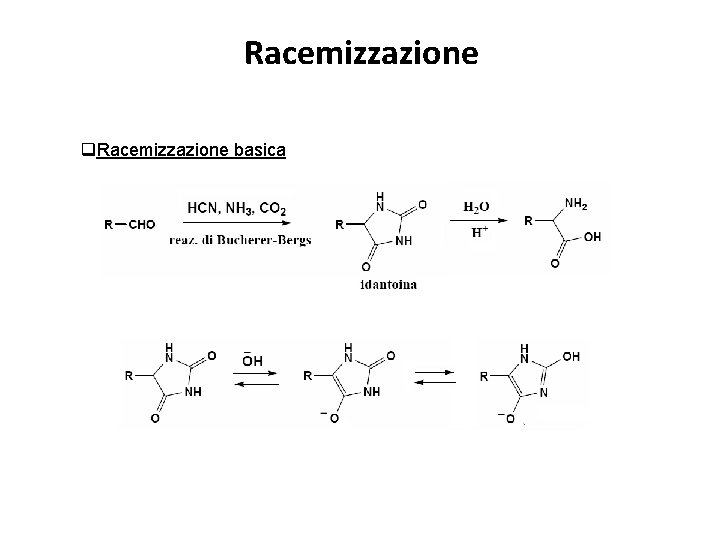
Racemizzazione q. Racemizzazione basica

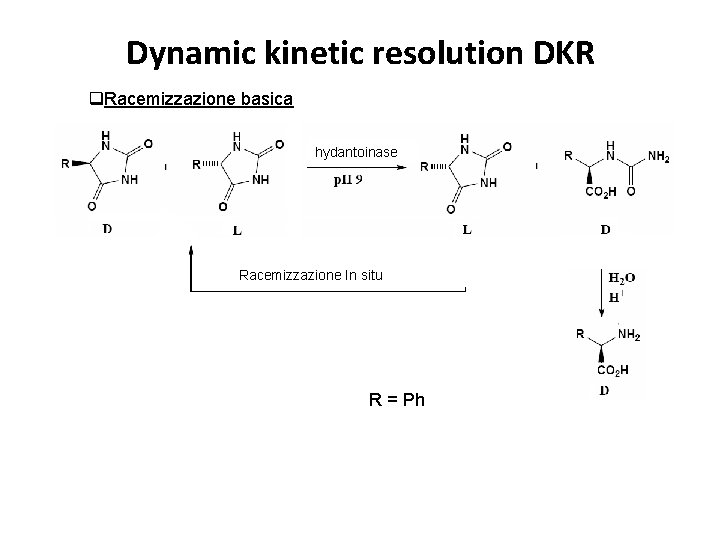
Dynamic kinetic resolution DKR q. Racemizzazione basica hydantoinase Racemizzazione In situ R = Ph

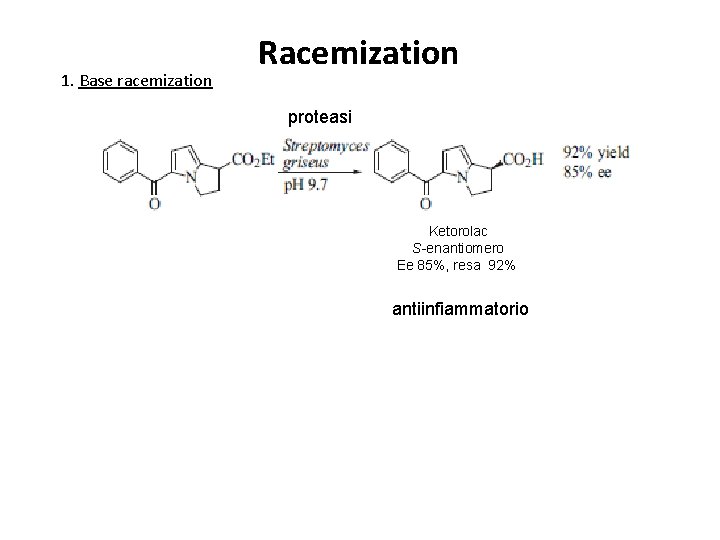
1. Base racemization Racemization proteasi Ketorolac S-enantiomero Ee 85%, resa 92% antiinfiammatorio

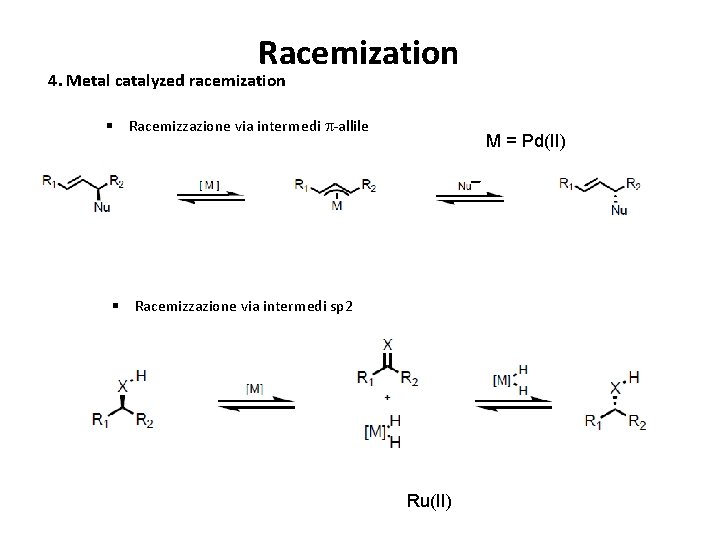
Racemization 4. Metal catalyzed racemization § Racemizzazione via intermedi p-allile M = Pd(II) § Racemizzazione via intermedi sp 2 Ru(II)

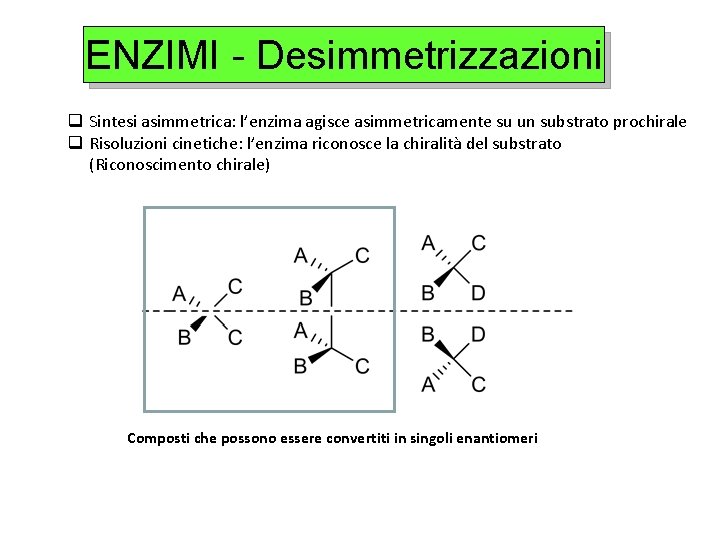
ENZIMI - Desimmetrizzazioni q Sintesi asimmetrica: l’enzima agisce asimmetricamente su un substrato prochirale q Risoluzioni cinetiche: l’enzima riconosce la chiralità del substrato (Riconoscimento chirale) Composti che possono essere convertiti in singoli enantiomeri

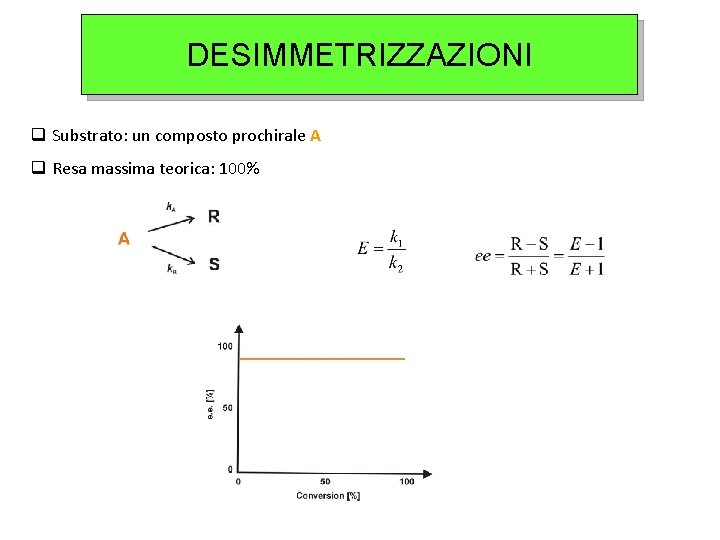
DESIMMETRIZZAZIONI q Substrato: un composto prochirale A q Resa massima teorica: 100%

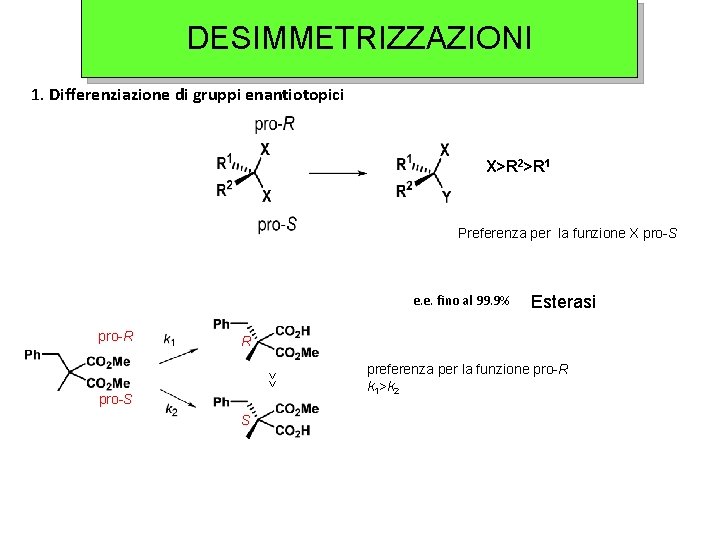
DESIMMETRIZZAZIONI 1. Differenziazione di gruppi enantiotopici X>R 2>R 1 Preferenza per la funzione X pro-S e. e. fino al 99. 9% pro-R Esterasi R >> pro-S S preferenza per la funzione pro-R k 1>k 2

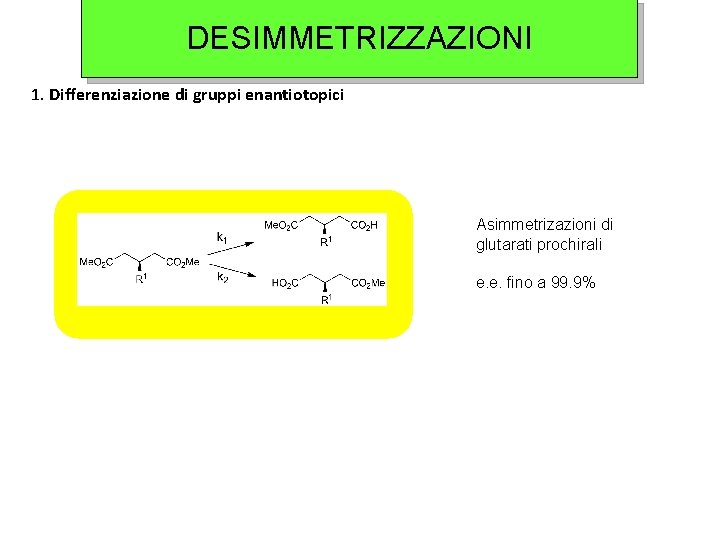
DESIMMETRIZZAZIONI 1. Differenziazione di gruppi enantiotopici Esterasi Asimmetrizazioni di glutarati prochirali e. e. fino a 99. 9%

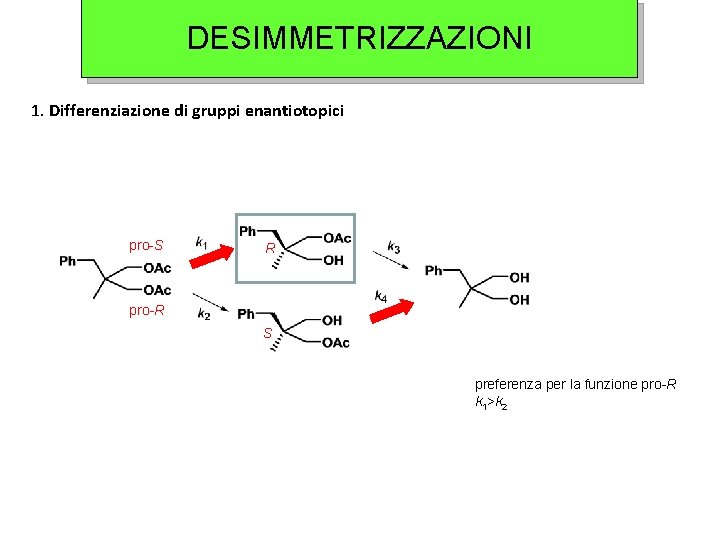
DESIMMETRIZZAZIONI 1. Differenziazione di gruppi enantiotopici pro-S R pro-R S preferenza per la funzione pro-R k 1>k 2

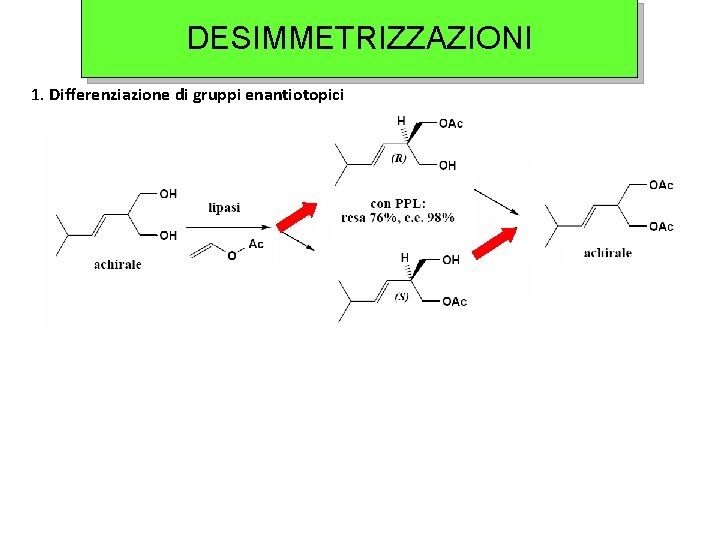
DESIMMETRIZZAZIONI 1. Differenziazione di gruppi enantiotopici

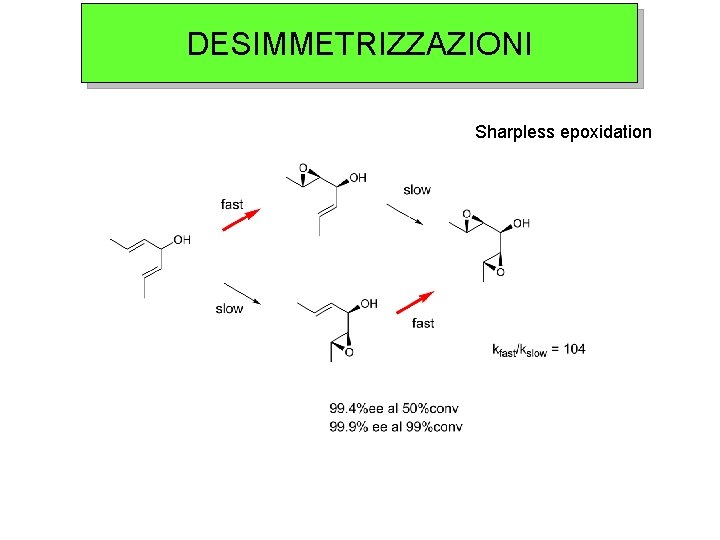
DESIMMETRIZZAZIONI Sharpless epoxidation

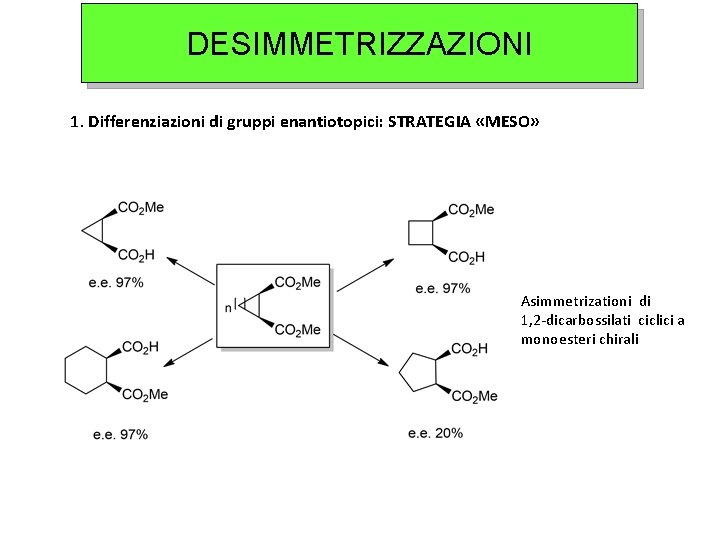
DESIMMETRIZZAZIONI 1. Differenziazioni di gruppi enantiotopici: STRATEGIA «MESO» Asimmetrizationi di 1, 2 -dicarbossilati ciclici a monoesteri chirali

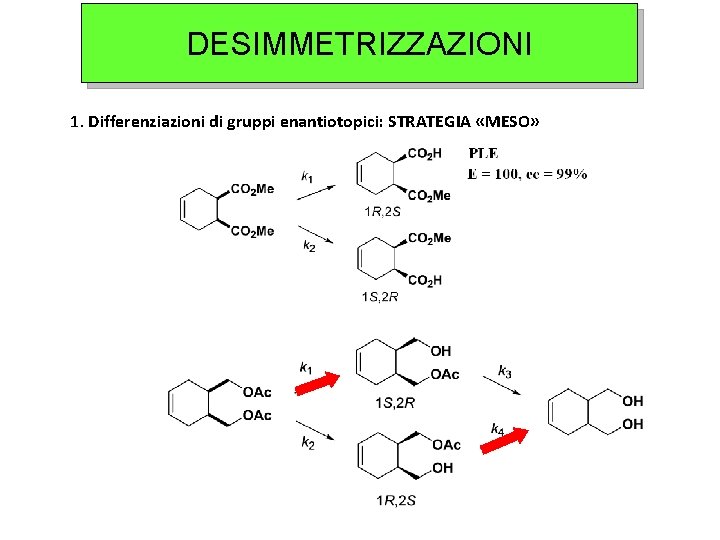
DESIMMETRIZZAZIONI 1. Differenziazioni di gruppi enantiotopici: STRATEGIA «MESO»