Hoofdstuk IX nucleofiele substitutie en eliminatie HOOFDSTUK IX

Hoofdstuk IX: nucleofiele substitutie en eliminatie HOOFDSTUK IX: nucleofiele substitutie en eliminatie Mc Murry: pagina 343 -384
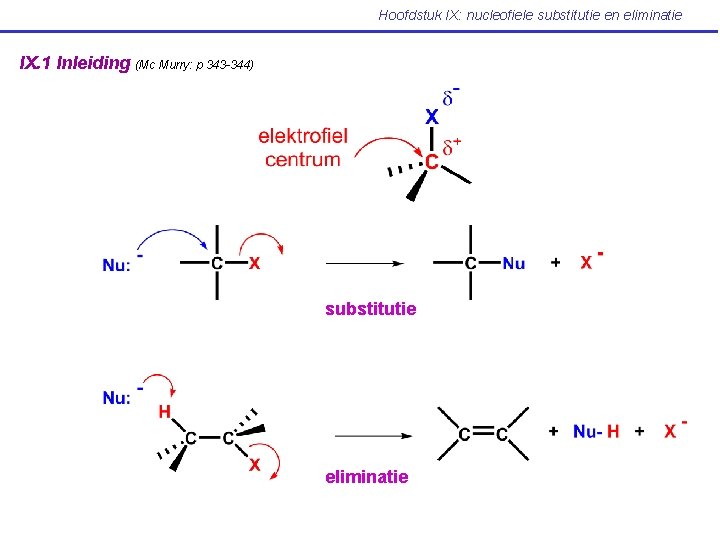
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 1 Inleiding (Mc Murry: p 343 -344) substitutie eliminatie
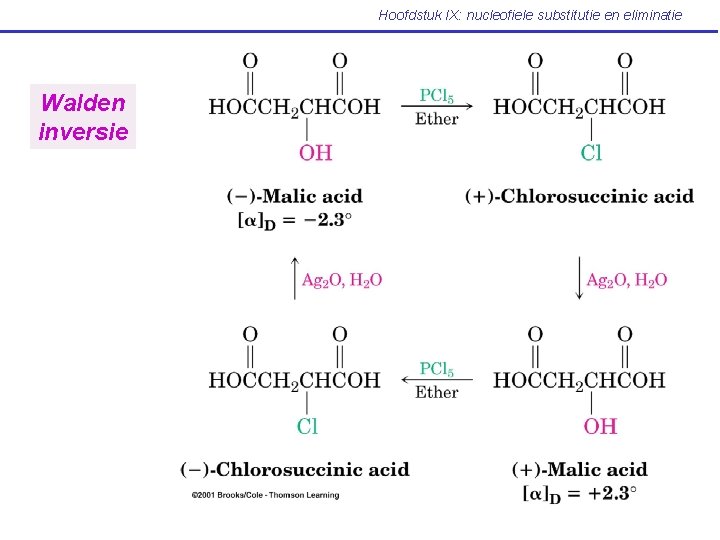
Hoofdstuk IX: nucleofiele substitutie en eliminatie Walden inversie
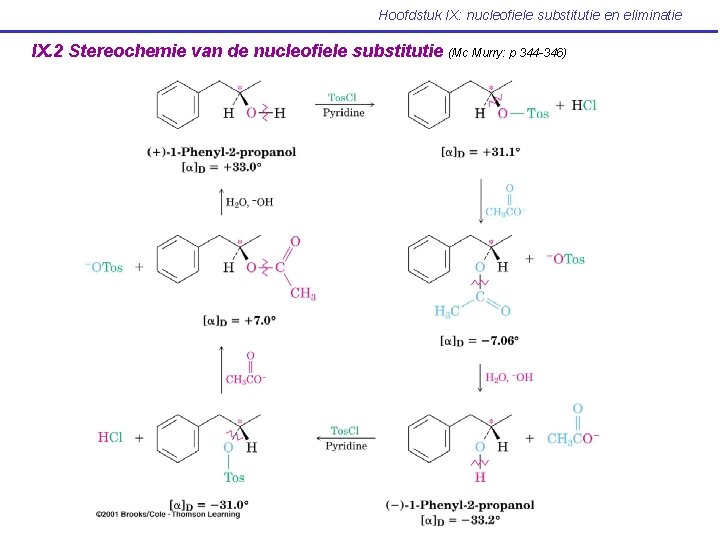
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 2 Stereochemie van de nucleofiele substitutie (Mc Murry: p 344 -346)
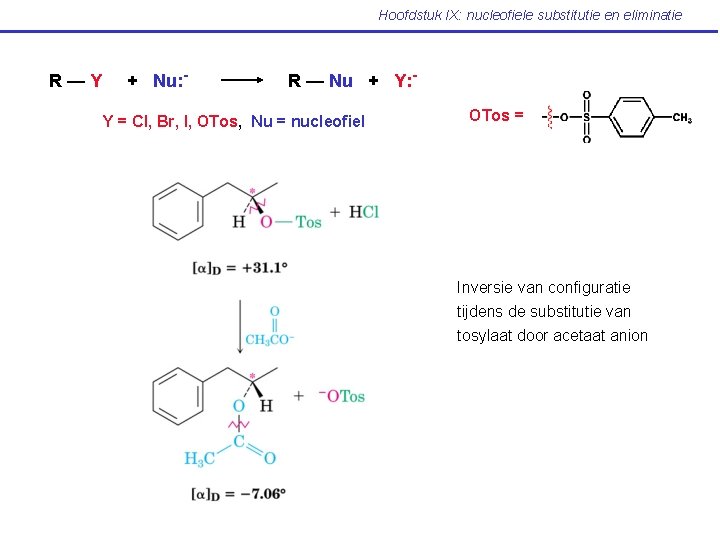
Hoofdstuk IX: nucleofiele substitutie en eliminatie R—Y + Nu: - R — Nu + Y: - Y = Cl, Br, I, OTos, Nu = nucleofiel OTos = Inversie van configuratie tijdens de substitutie van tosylaat door acetaat anion

Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 3 Kinetiek van de nucleofiele substitutie (Mc Murry: p 346 -347) Kinetiek van de reactie: relatie tussen de reactiesnelheid en de reactantconcentratie • • HO: • • + CH 3 — Br: • • • • HO — CH 3 + : Br: - Reactiesnelheid = snelheid waarmee reactant verdwijnt = k x [RX] x [-OH] met [RX] = CH 3 Br concentratie [-OH] = -OH concentratie k = snelheidsconstante (L/mol • s)
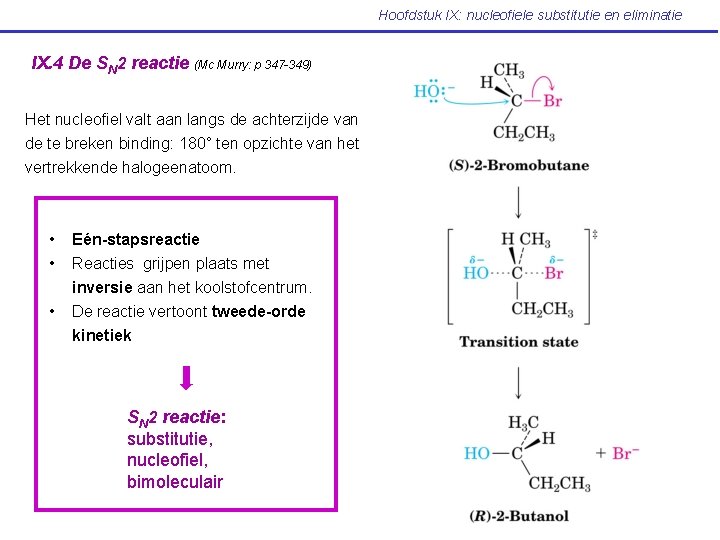
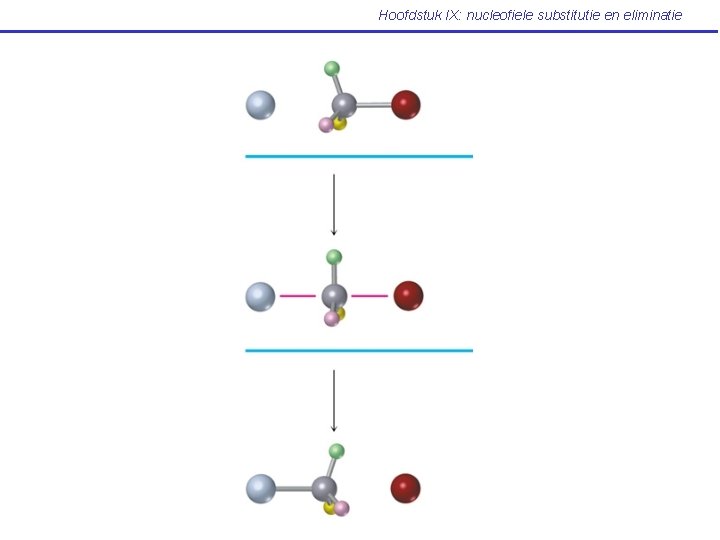
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 4 De SN 2 reactie (Mc Murry: p 347 -349) Het nucleofiel valt aan langs de achterzijde van de te breken binding: 180° ten opzichte van het vertrekkende halogeenatoom. • • Eén-stapsreactie Reacties grijpen plaats met • inversie aan het koolstofcentrum. De reactie vertoont tweede-orde kinetiek SN 2 reactie: substitutie, nucleofiel, bimoleculair
Hoofdstuk IX: nucleofiele substitutie en eliminatie
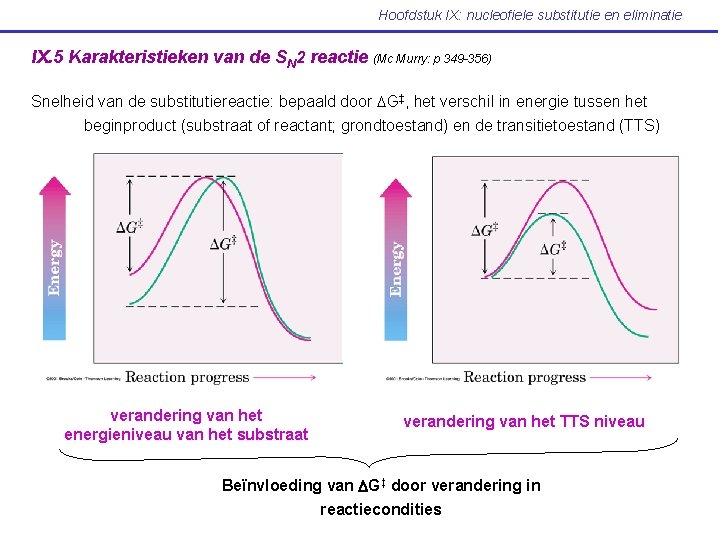
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 5 Karakteristieken van de SN 2 reactie (Mc Murry: p 349 -356) Snelheid van de substitutiereactie: bepaald door DG‡, het verschil in energie tussen het beginproduct (substraat of reactant; grondtoestand) en de transitietoestand (TTS) verandering van het energieniveau van het substraat verandering van het TTS niveau Beïnvloeding van DG‡ door verandering in reactiecondities
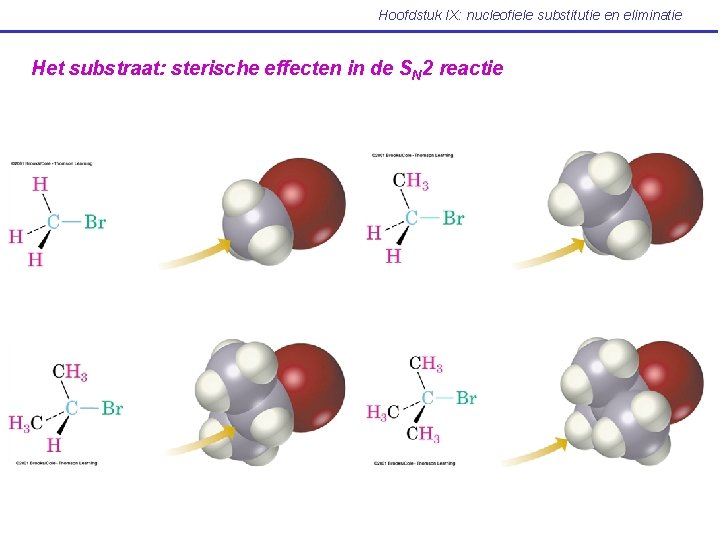
Hoofdstuk IX: nucleofiele substitutie en eliminatie Het substraat: sterische effecten in de SN 2 reactie
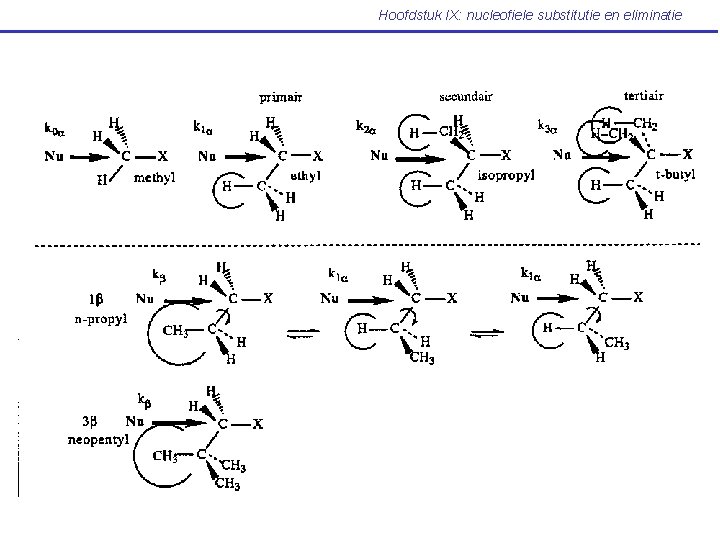
Hoofdstuk IX: nucleofiele substitutie en eliminatie
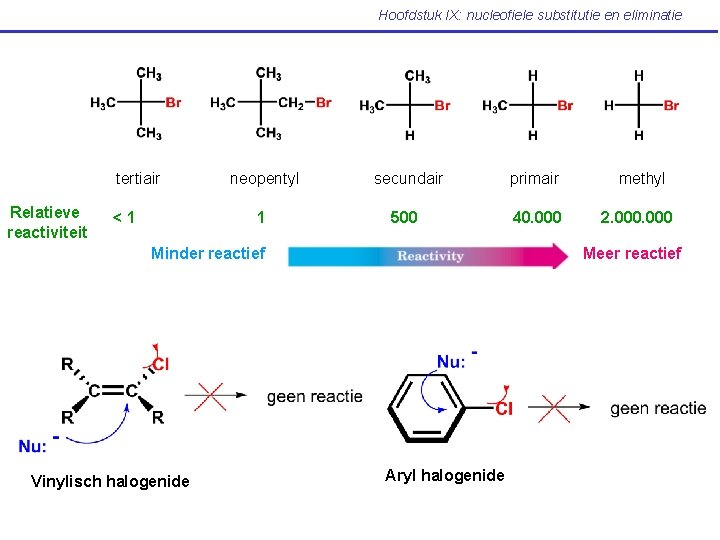
Hoofdstuk IX: nucleofiele substitutie en eliminatie tertiair Relatieve reactiviteit <1 neopentyl secundair primair 1 500 40. 000 Minder reactief Vinylisch halogenide methyl 2. 000 Meer reactief Aryl halogenide
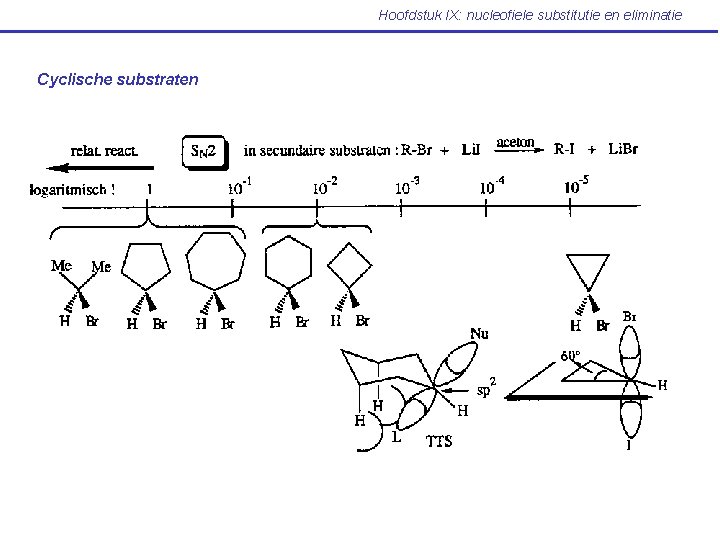
Hoofdstuk IX: nucleofiele substitutie en eliminatie Cyclische substraten
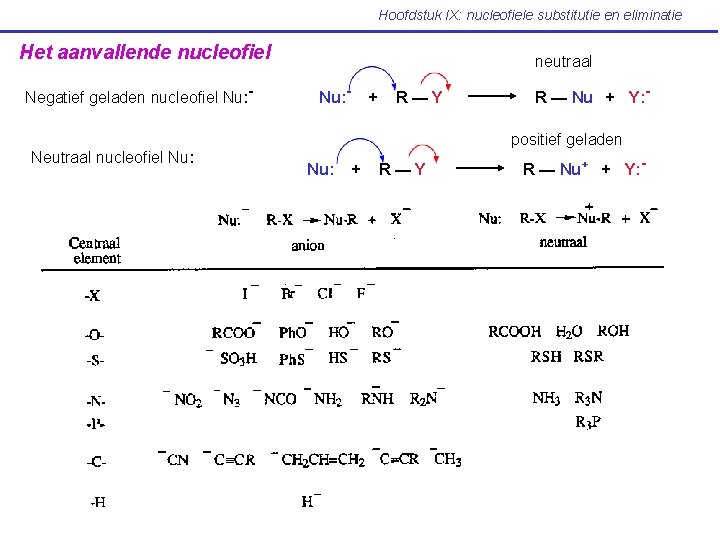
Hoofdstuk IX: nucleofiele substitutie en eliminatie Het aanvallende nucleofiel Negatief geladen nucleofiel Nu: - neutraal Nu: - + R—Y R — Nu + Y: positief geladen Neutraal nucleofiel Nu: + R—Y R — Nu+ + Y: -

Hoofdstuk IX: nucleofiele substitutie en eliminatie CH 3 — Br Nu = Relatieve reactiviteit Nu: - + H 2 O CH 3 CO 2 - NH 3 1 500 700 Minder reactief CH 3 — Nu Cl- OH- 1000 16. 000 CH 3 O 25. 000 + I- Br. CN- 100. 000 125. 000 HS 125. 000 Meer reactief Nucleofiliciteit trends: • • • Geladen nucleofielen zijn meer reactief dan niet-geladen nucleofielen nucleofiliciteit stijgt bij stijgende periode: * HS- > HO* I- > Br- > Cl. Polariseerbaarheid ! Nucleofiliciteit loopt ongeveer parallel met basiciteit

Hoofdstuk IX: nucleofiele substitutie en eliminatie
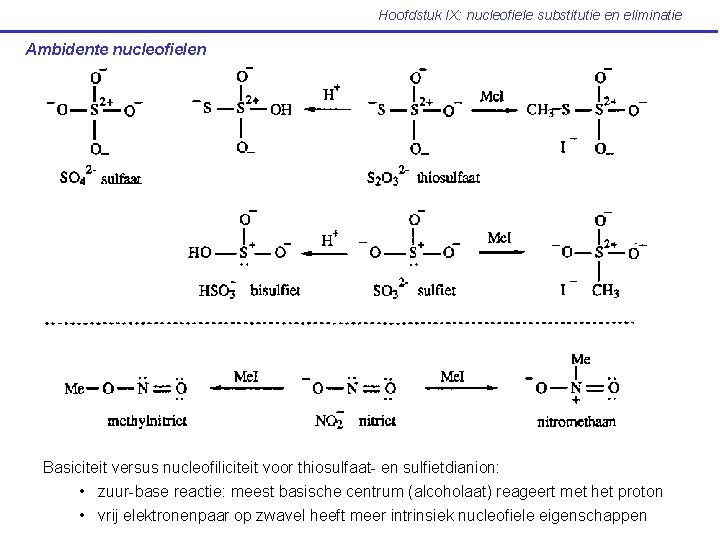
Hoofdstuk IX: nucleofiele substitutie en eliminatie Ambidente nucleofielen Basiciteit versus nucleofiliciteit voor thiosulfaat- en sulfietdianion: • zuur-base reactie: meest basische centrum (alcoholaat) reageert met het proton • vrij elektronenpaar op zwavel heeft meer intrinsiek nucleofiele eigenschappen
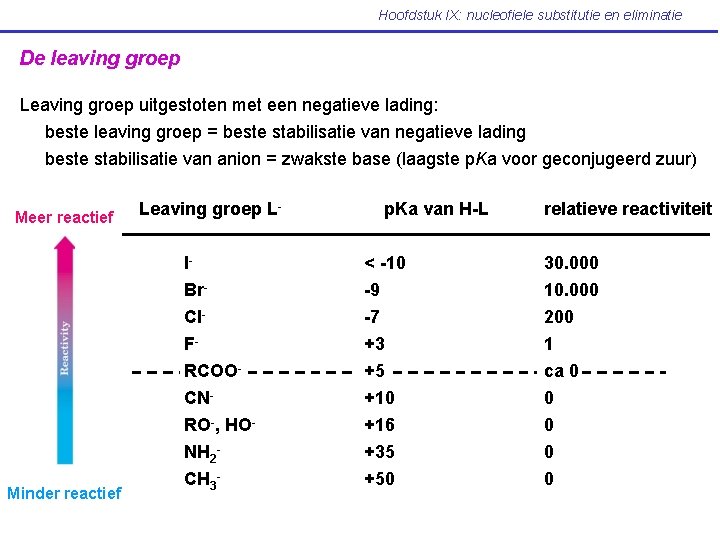
Hoofdstuk IX: nucleofiele substitutie en eliminatie De leaving groep Leaving groep uitgestoten met een negatieve lading: beste leaving groep = beste stabilisatie van negatieve lading beste stabilisatie van anion = zwakste base (laagste p. Ka voor geconjugeerd zuur) Meer reactief Minder reactief Leaving groep L- p. Ka van H-L relatieve reactiviteit I- < -10 30. 000 Br. Cl. FRCOOCNRO-, HONH 2 CH 3 - -9 -7 +3 +5 +10 +16 +35 +50 10. 000 200 1 ca 0 0 0
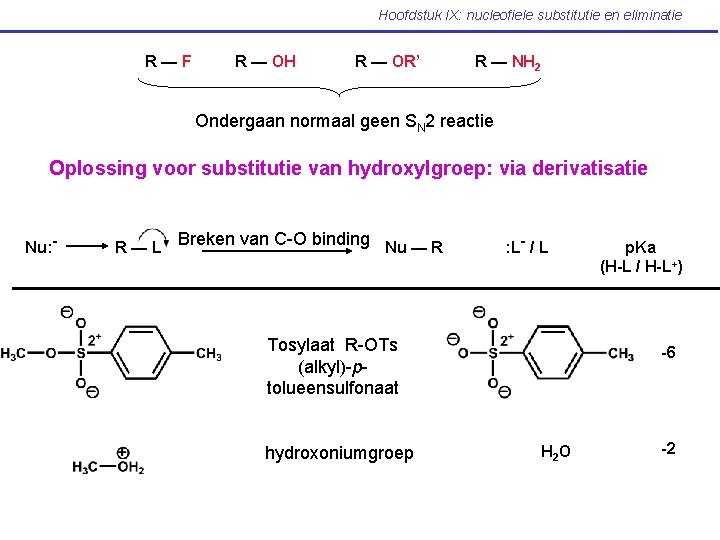
Hoofdstuk IX: nucleofiele substitutie en eliminatie R—F R — OH R — OR’ R — NH 2 Ondergaan normaal geen SN 2 reactie Oplossing voor substitutie van hydroxylgroep: via derivatisatie Nu: - R—L Breken van C-O binding Nu — R : L- / L Tosylaat R-OTs (alkyl)-ptolueensulfonaat hydroxoniumgroep p. Ka (H-L / H-L+) -6 H 2 O -2
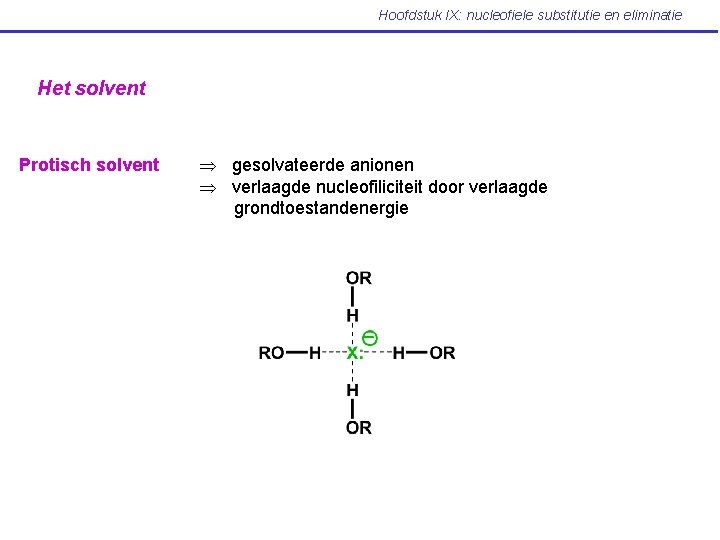
Hoofdstuk IX: nucleofiele substitutie en eliminatie Het solvent Protisch solvent gesolvateerde anionen verlaagde nucleofiliciteit door verlaagde grondtoestandenergie
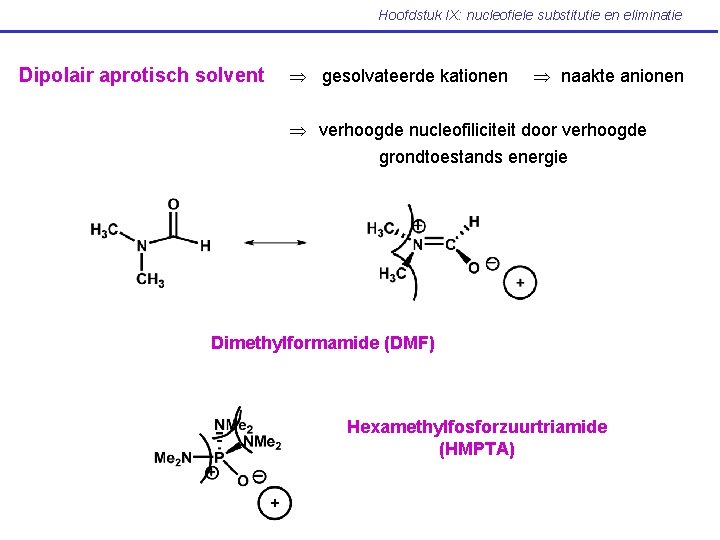
Hoofdstuk IX: nucleofiele substitutie en eliminatie Dipolair aprotisch solvent gesolvateerde kationen naakte anionen verhoogde nucleofiliciteit door verhoogde grondtoestands energie Dimethylformamide (DMF) Hexamethylfosforzuurtriamide (HMPTA)
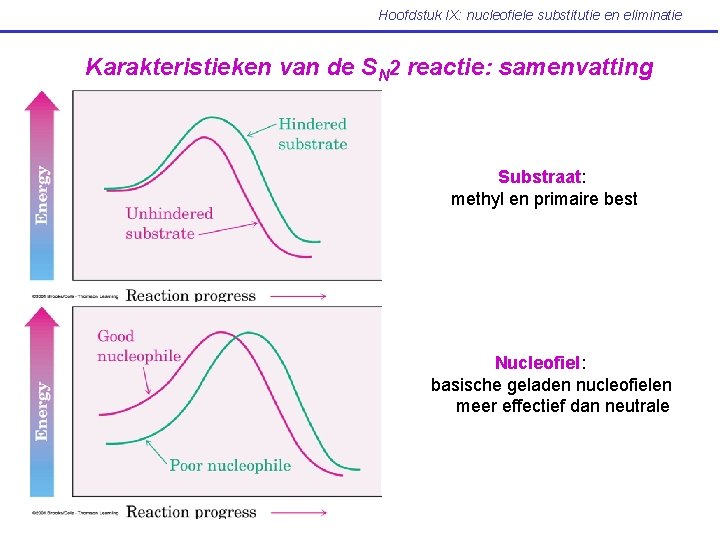
Hoofdstuk IX: nucleofiele substitutie en eliminatie Karakteristieken van de SN 2 reactie: samenvatting Substraat: methyl en primaire best Nucleofiel: basische geladen nucleofielen meer effectief dan neutrale
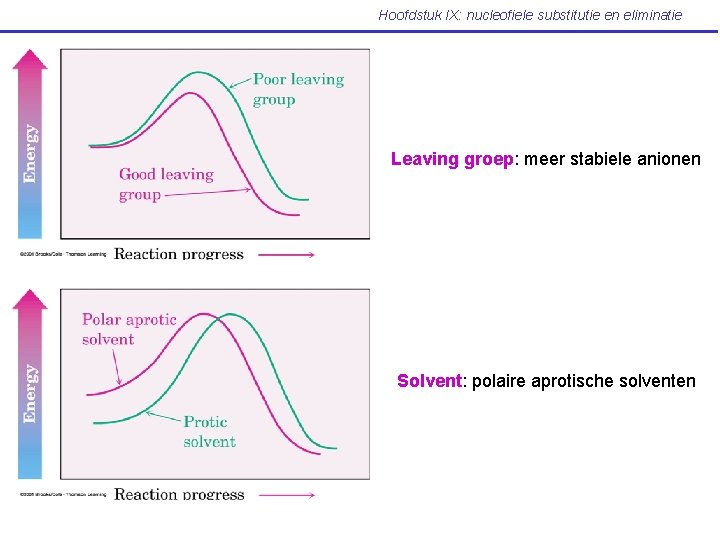
Hoofdstuk IX: nucleofiele substitutie en eliminatie Leaving groep: meer stabiele anionen Solvent: polaire aprotische solventen
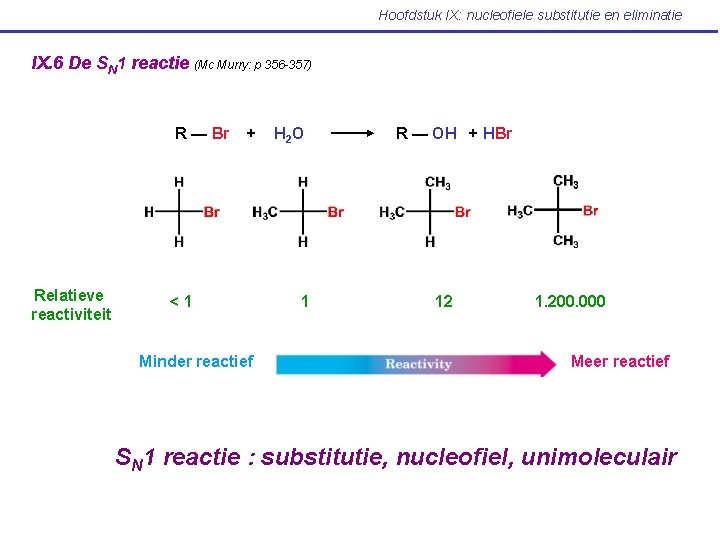
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 6 De SN 1 reactie (Mc Murry: p 356 -357) R — Br Relatieve reactiviteit + <1 Minder reactief H 2 O 1 R — OH + HBr 12 1. 200. 000 Meer reactief SN 1 reactie : substitutie, nucleofiel, unimoleculair
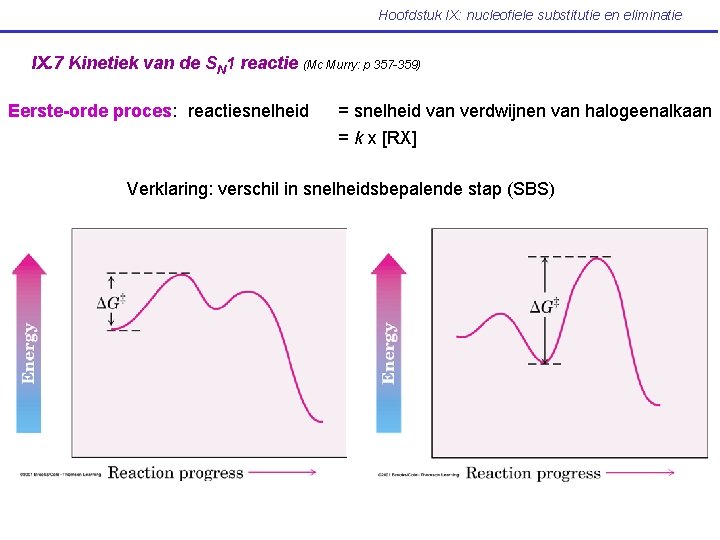
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 7 Kinetiek van de SN 1 reactie (Mc Murry: p 357 -359) Eerste-orde proces: reactiesnelheid = snelheid van verdwijnen van halogeenalkaan = k x [RX] Verklaring: verschil in snelheidsbepalende stap (SBS)
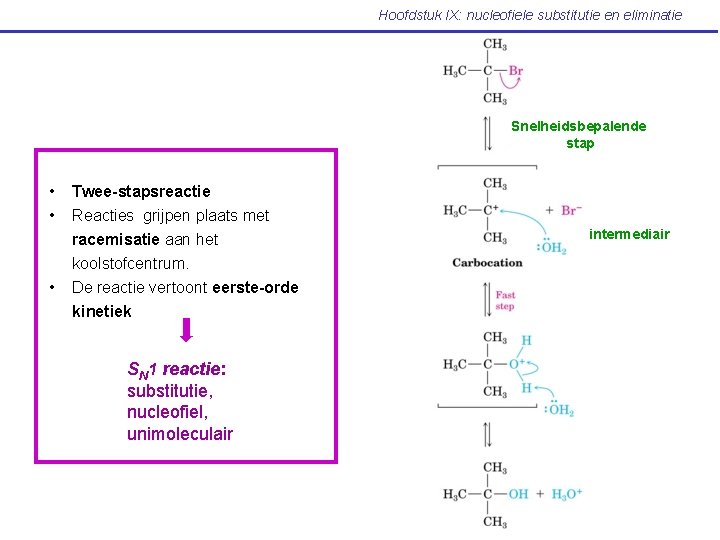
Hoofdstuk IX: nucleofiele substitutie en eliminatie Snelheidsbepalende stap • • • Twee-stapsreactie Reacties grijpen plaats met racemisatie aan het koolstofcentrum. De reactie vertoont eerste-orde kinetiek SN 1 reactie: substitutie, nucleofiel, unimoleculair intermediair
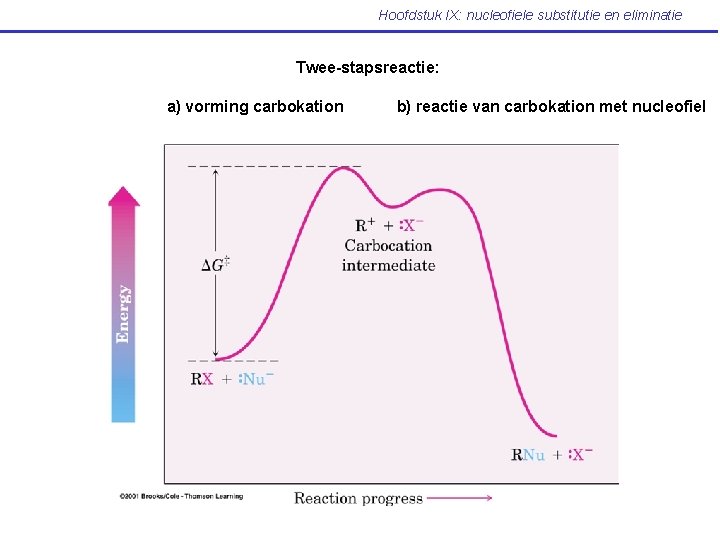
Hoofdstuk IX: nucleofiele substitutie en eliminatie Twee-stapsreactie: a) vorming carbokation b) reactie van carbokation met nucleofiel
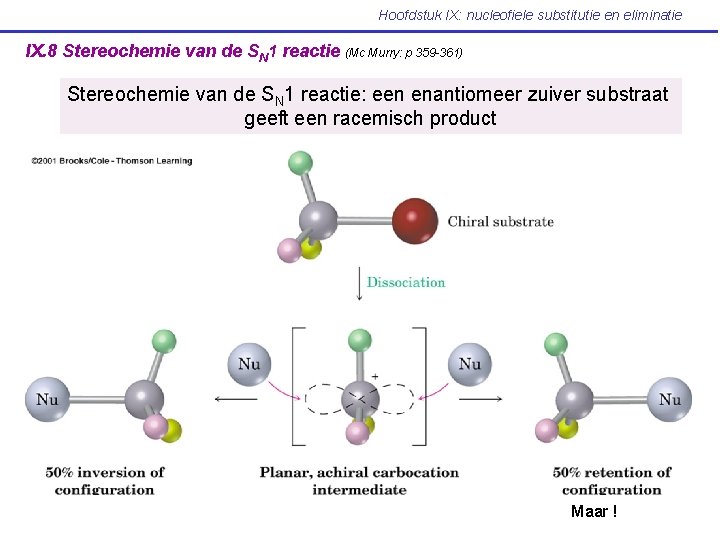
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 8 Stereochemie van de SN 1 reactie (Mc Murry: p 359 -361) Stereochemie van de SN 1 reactie: een enantiomeer zuiver substraat geeft een racemisch product Maar !
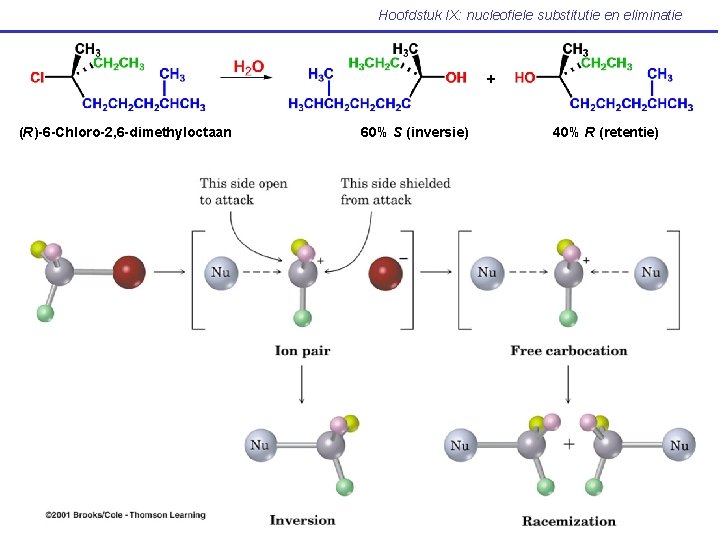
Hoofdstuk IX: nucleofiele substitutie en eliminatie + (R)-6 -Chloro-2, 6 -dimethyloctaan 60% S (inversie) 40% R (retentie)
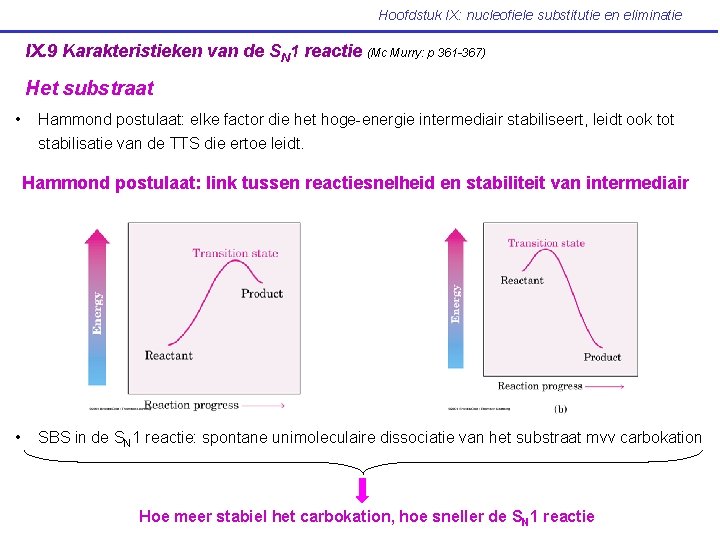
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 9 Karakteristieken van de SN 1 reactie (Mc Murry: p 361 -367) Het substraat • Hammond postulaat: elke factor die het hoge-energie intermediair stabiliseert, leidt ook tot stabilisatie van de TTS die ertoe leidt. Hammond postulaat: link tussen reactiesnelheid en stabiliteit van intermediair • SBS in de SN 1 reactie: spontane unimoleculaire dissociatie van het substraat mvv carbokation Hoe meer stabiel het carbokation, hoe sneller de SN 1 reactie
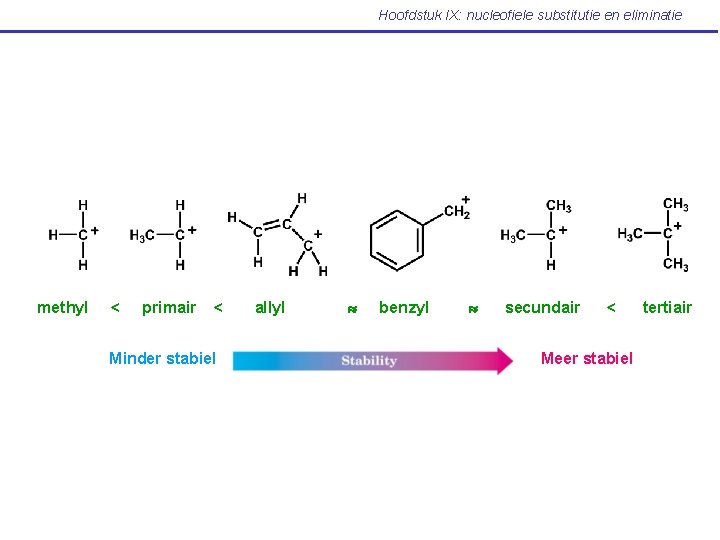
Hoofdstuk IX: nucleofiele substitutie en eliminatie methyl < primair < Minder stabiel allyl benzyl secundair < Meer stabiel tertiair
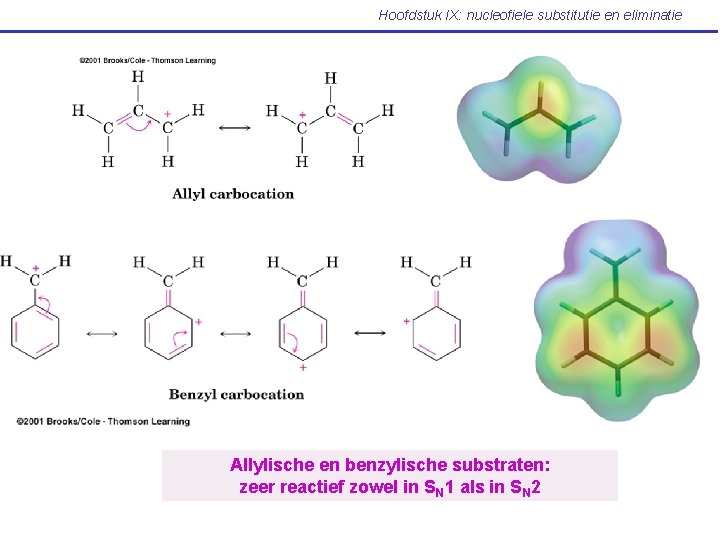
Hoofdstuk IX: nucleofiele substitutie en eliminatie Allylische en benzylische substraten: zeer reactief zowel in SN 1 als in SN 2

Hoofdstuk IX: nucleofiele substitutie en eliminatie De leaving groep H 2 O < Minder reactief Cl- < Leaving groep Br- < I- < Tos. O- Meer reactief In de SN 1 reactie: neutraal water kan optreden als leaving groep bv. bij bereiding van een halogeenalkaan uit een tertiair alcohol met HBr of HCl
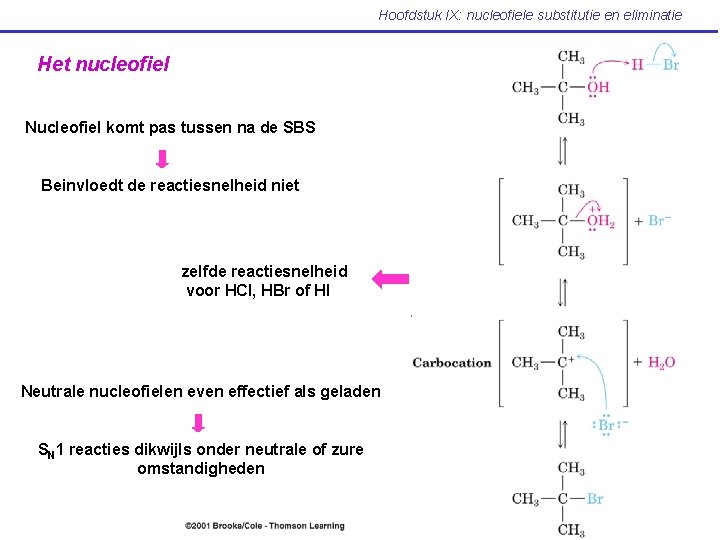
Hoofdstuk IX: nucleofiele substitutie en eliminatie Het nucleofiel Nucleofiel komt pas tussen na de SBS Beinvloedt de reactiesnelheid niet zelfde reactiesnelheid voor HCl, HBr of HI Neutrale nucleofielen even effectief als geladen SN 1 reacties dikwijls onder neutrale of zure omstandigheden
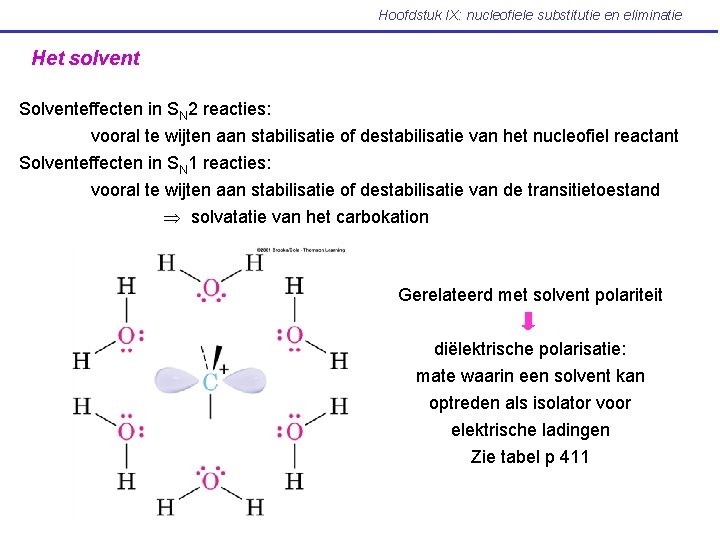
Hoofdstuk IX: nucleofiele substitutie en eliminatie Het solvent Solventeffecten in SN 2 reacties: vooral te wijten aan stabilisatie of destabilisatie van het nucleofiel reactant Solventeffecten in SN 1 reacties: vooral te wijten aan stabilisatie of destabilisatie van de transitietoestand solvatatie van het carbokation Gerelateerd met solvent polariteit diëlektrische polarisatie: mate waarin een solvent kan optreden als isolator voor elektrische ladingen Zie tabel p 411
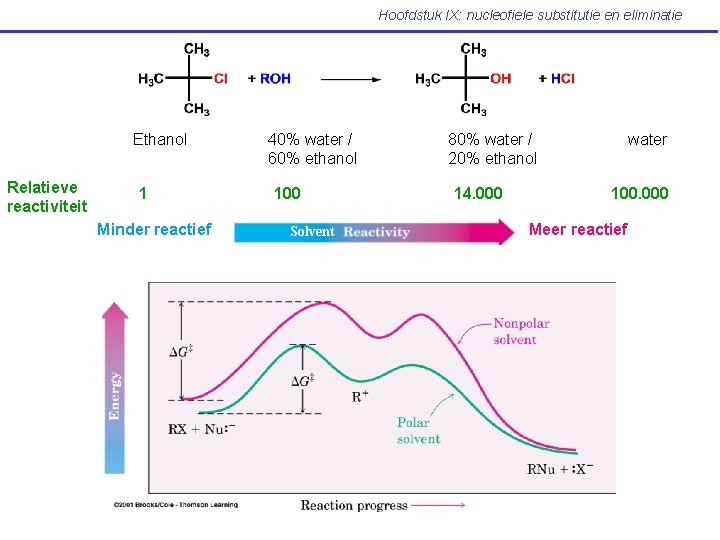
Hoofdstuk IX: nucleofiele substitutie en eliminatie Ethanol Relatieve reactiviteit 1 Minder reactief 40% water / 60% ethanol 100 Solvent 80% water / 20% ethanol 14. 000 water 100. 000 Meer reactief

Hoofdstuk IX: nucleofiele substitutie en eliminatie Karakteristieken van de SN 1 reactie: samenvatting Substraat: tertiaire, allylische en benzylische best Nucleofiel: bij voorkeur niet basisch om eliminatie te voorkomen (zie verder) neutrale nucleofielen werken goed Leaving groep: meer stabiele anionen verlagen de energie van de TTS leidend tot het carbokation Solvent: polaire solventen solvateren het carbokation en verhogen de reactiesnelheid
Hoofdstuk IX: nucleofiele substitutie en eliminatie
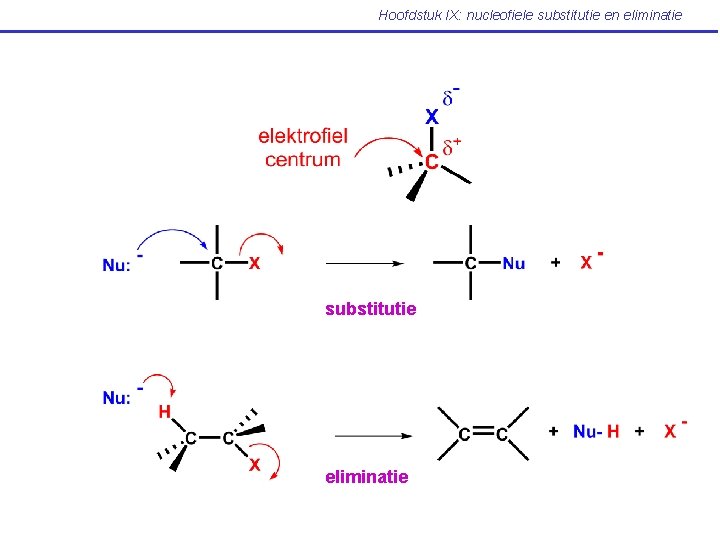
Hoofdstuk IX: nucleofiele substitutie en eliminatie substitutie eliminatie

Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 10 Eliminatiereacties van halogeenalkanen: Zaitsev regel 2 -bromobutaan 2 -buteen (81%) (Mc Murry: p 367 -369) 1 -buteen (19%) Zaitsev’s regel: Bij de eliminatie van HX uit een halogeenalkeen wordt bij voorkeur het meest gesubstitueerde alkeen gevormd. Eliminatie van HX uit een halogeenalkaan: excellente methode voor het bereiden van alkenen twee mogelijke mechanismen E 1 en E 2
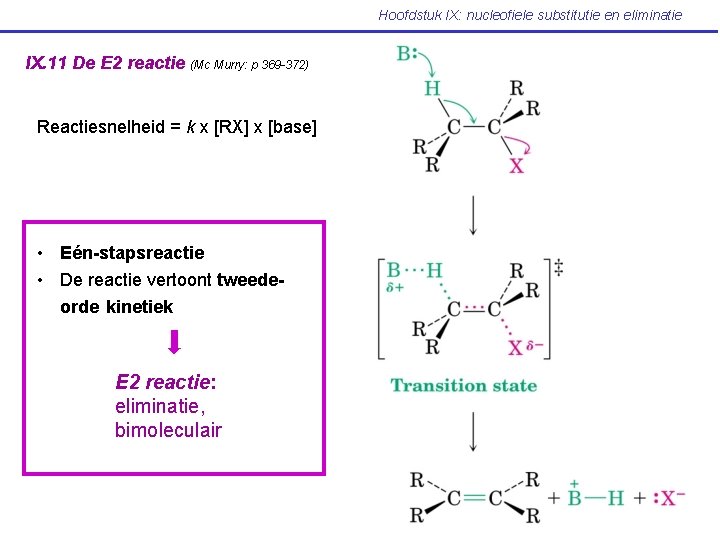
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 11 De E 2 reactie (Mc Murry: p 369 -372) Reactiesnelheid = k x [RX] x [base] • Eén-stapsreactie • De reactie vertoont tweedeorde kinetiek E 2 reactie: eliminatie, bimoleculair
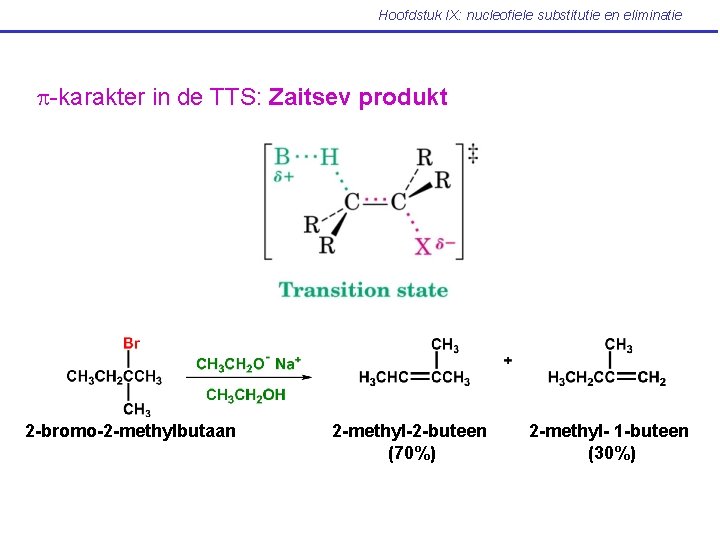
Hoofdstuk IX: nucleofiele substitutie en eliminatie p-karakter in de TTS: Zaitsev produkt 2 -bromo-2 -methylbutaan 2 -methyl-2 -buteen (70%) 2 -methyl- 1 -buteen (30%)
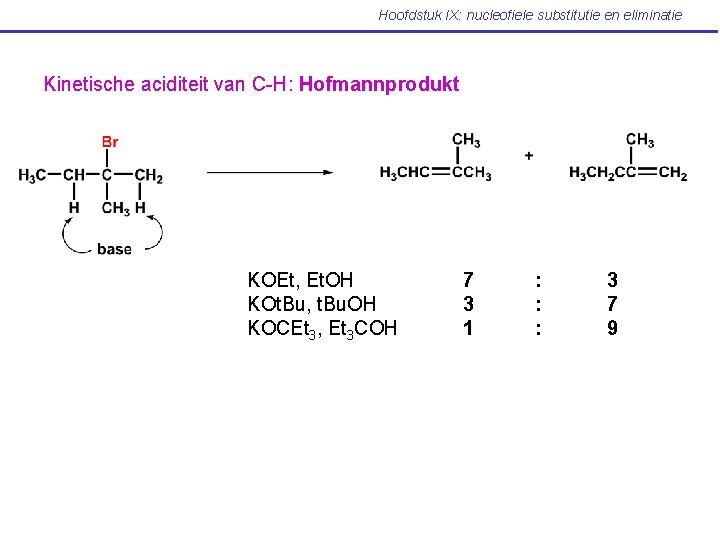
Hoofdstuk IX: nucleofiele substitutie en eliminatie Kinetische aciditeit van C-H: Hofmannprodukt KOEt, Et. OH KOt. Bu, t. Bu. OH KOCEt 3, Et 3 COH 7 3 1 : : : 3 7 9
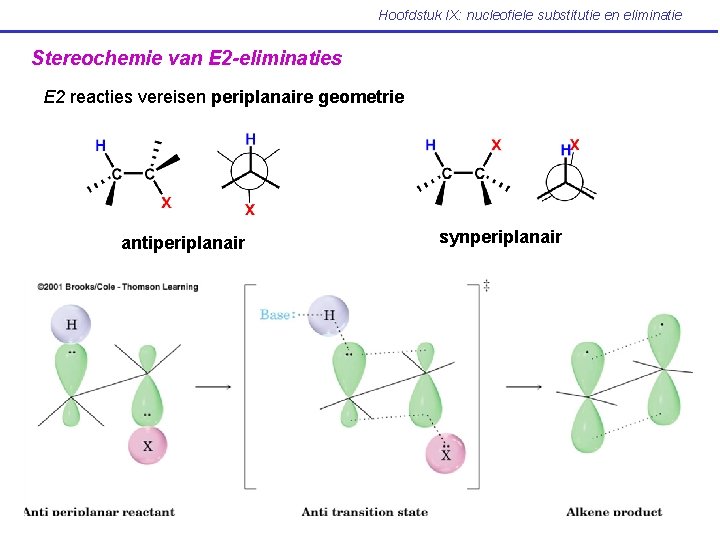
Hoofdstuk IX: nucleofiele substitutie en eliminatie Stereochemie van E 2 -eliminaties E 2 reacties vereisen periplanaire geometrie antiperiplanair synperiplanair
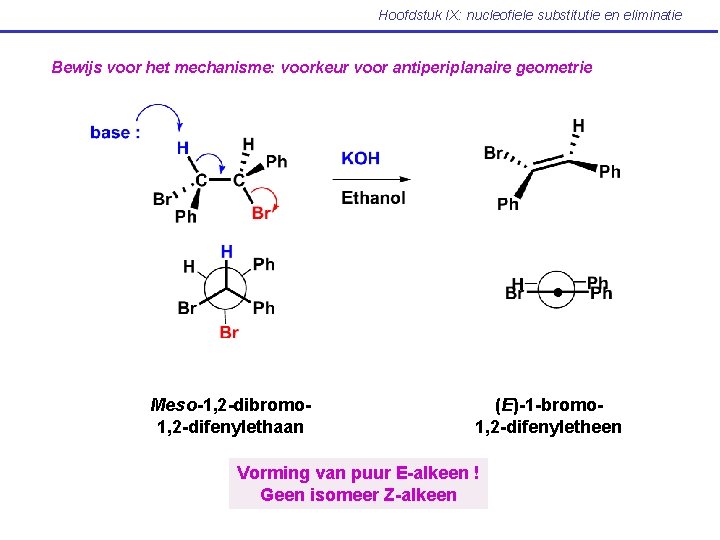
Hoofdstuk IX: nucleofiele substitutie en eliminatie Bewijs voor het mechanisme: voorkeur voor antiperiplanaire geometrie Meso-1, 2 -dibromo 1, 2 -difenylethaan (E)-1 -bromo 1, 2 -difenyletheen Vorming van puur E-alkeen ! Geen isomeer Z-alkeen
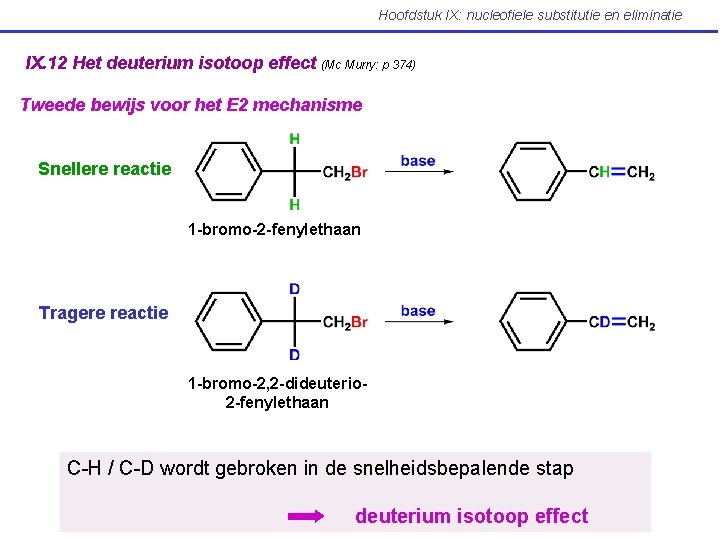
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 12 Het deuterium isotoop effect (Mc Murry: p 374) Tweede bewijs voor het E 2 mechanisme Snellere reactie 1 -bromo-2 -fenylethaan Tragere reactie 1 -bromo-2, 2 -dideuterio 2 -fenylethaan C-H / C-D wordt gebroken in de snelheidsbepalende stap deuterium isotoop effect
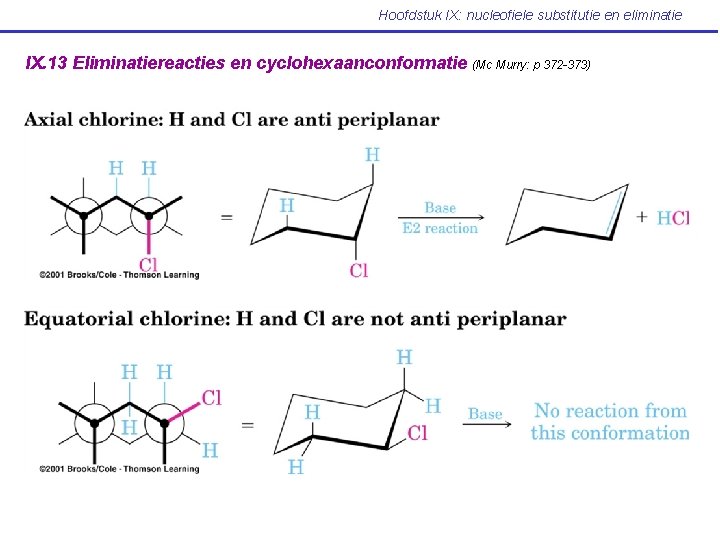
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 13 Eliminatiereacties en cyclohexaanconformatie (Mc Murry: p 372 -373)
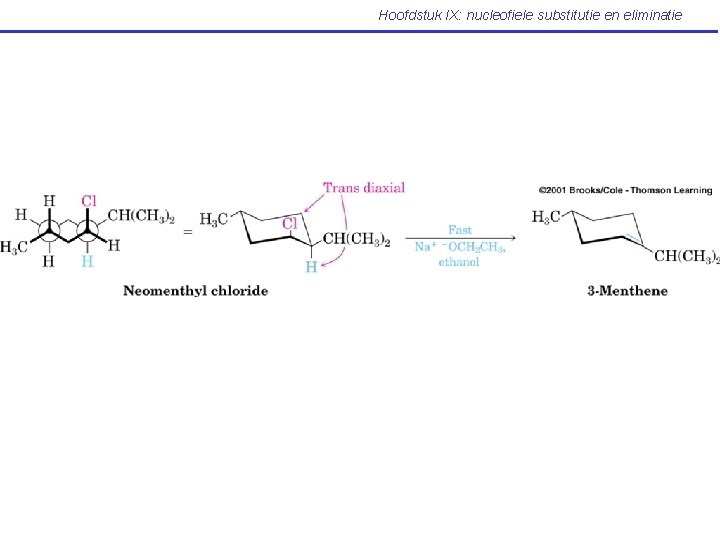
Hoofdstuk IX: nucleofiele substitutie en eliminatie
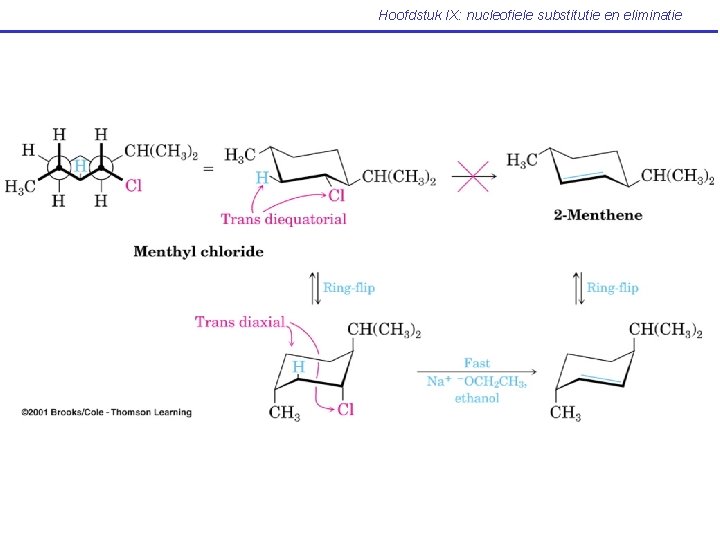
Hoofdstuk IX: nucleofiele substitutie en eliminatie
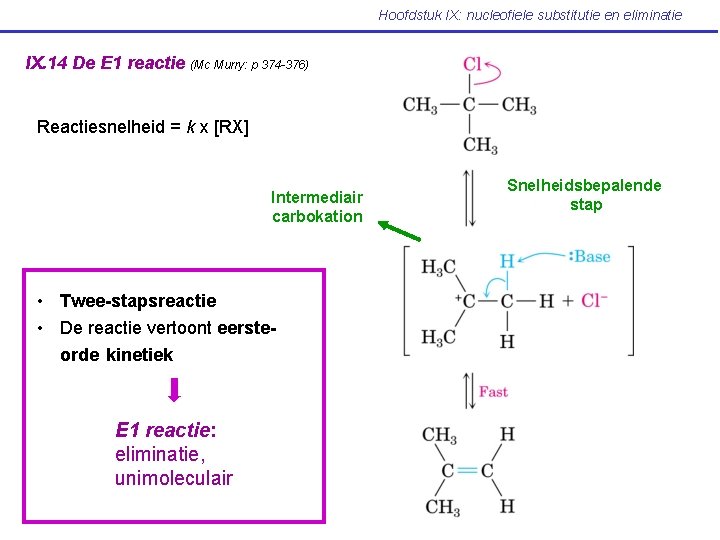
Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 14 De E 1 reactie (Mc Murry: p 374 -376) Reactiesnelheid = k x [RX] Intermediair carbokation • Twee-stapsreactie • De reactie vertoont eersteorde kinetiek E 1 reactie: eliminatie, unimoleculair Snelheidsbepalende stap
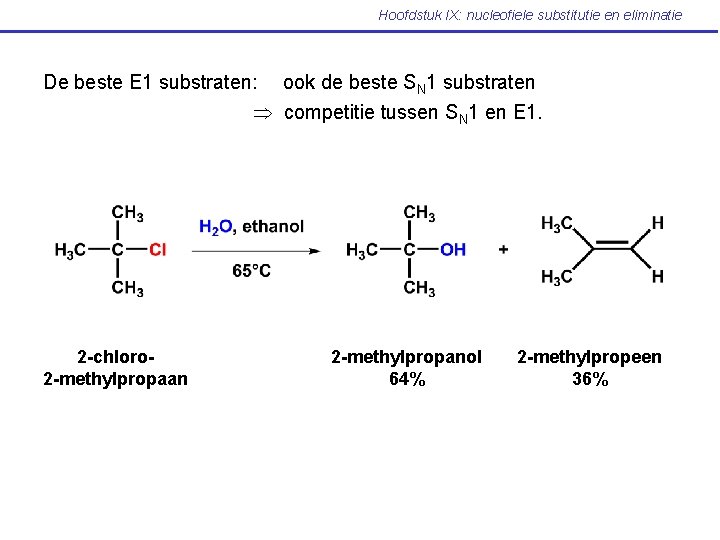
Hoofdstuk IX: nucleofiele substitutie en eliminatie De beste E 1 substraten: ook de beste SN 1 substraten competitie tussen SN 1 en E 1. 2 -chloro 2 -methylpropaan 2 -methylpropanol 64% 2 -methylpropeen 36%
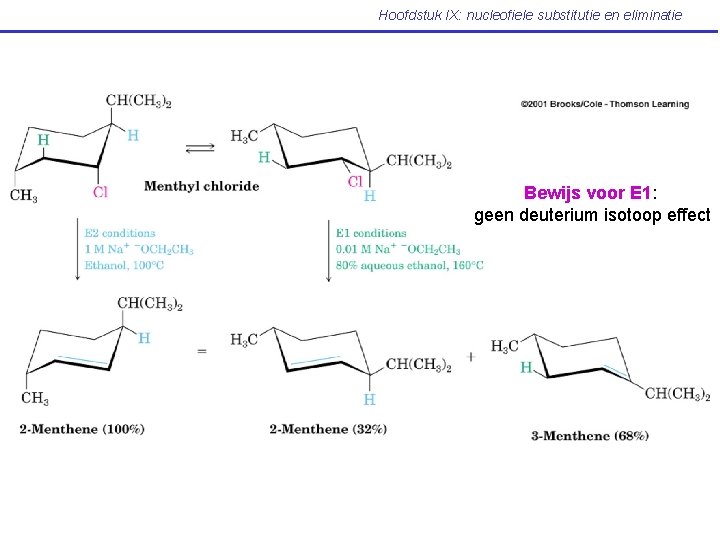
Hoofdstuk IX: nucleofiele substitutie en eliminatie Bewijs voor E 1: geen deuterium isotoop effect

Hoofdstuk IX: nucleofiele substitutie en eliminatie IX. 15 Samenvatting van reactiviteit: SN 1, SN 2, E 1, E 2 (Mc Murry: p 376 -378) Halogeenalkaan RCH 2 X SN 1 / SN 2 zeer gunstig E 1 / E 2 treedt op met sterke basen (primair) R 2 CHX (secundair) met benzylische en allylische substraten R 3 CX (tertiair) bevoordeligd in hydroxylbevattende solventen in competitie met E 2 / met benzylische en allylische substraten bevoordeligd met sterke basen treedt op in competitie met SN 1 reactie bevoordeligd met sterke basen
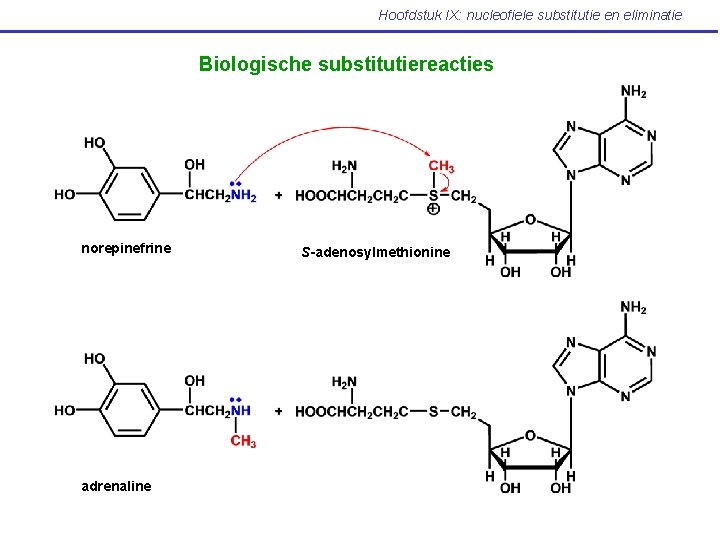
Hoofdstuk IX: nucleofiele substitutie en eliminatie Biologische substitutiereacties norepinefrine adrenaline S-adenosylmethionine
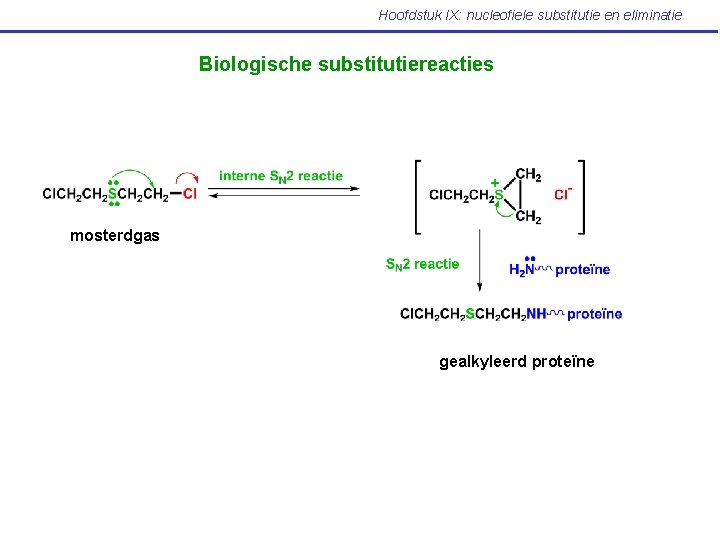
Hoofdstuk IX: nucleofiele substitutie en eliminatie Biologische substitutiereacties mosterdgas gealkyleerd proteïne
- Slides: 55