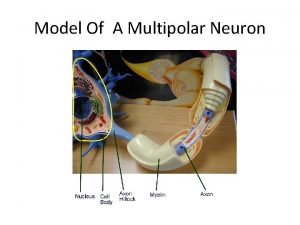
Hoofdstuk VIII halogeenalkanen en radikaalreacties HOOFDSTUK VIII halogeenalkanen


- Slides: 22

Hoofdstuk VIII: halogeenalkanen en radikaalreacties HOOFDSTUK VIII: halogeenalkanen en radikaalreacties Mc Murry: pagina 316 -337

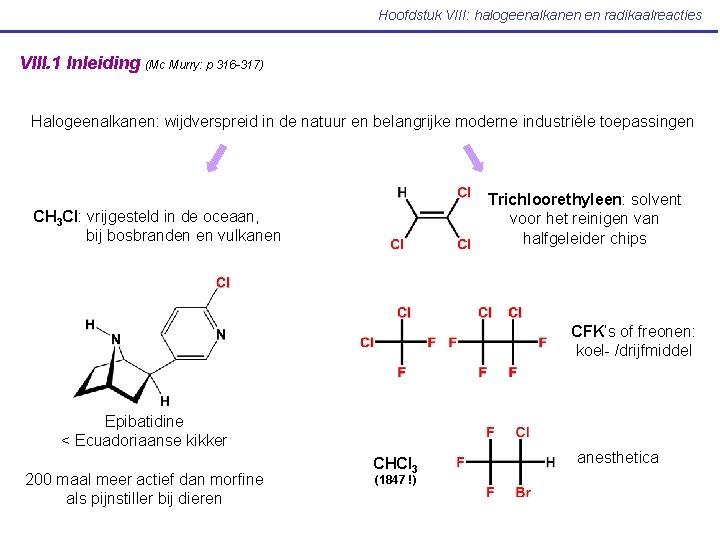
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 1 Inleiding (Mc Murry: p 316 -317) Halogeenalkanen: wijdverspreid in de natuur en belangrijke moderne industriële toepassingen Trichloorethyleen: solvent voor het reinigen van halfgeleider chips CH 3 Cl: vrijgesteld in de oceaan, bij bosbranden en vulkanen CFK’s of freonen: koel- /drijfmiddel Epibatidine < Ecuadoriaanse kikker 200 maal meer actief dan morfine als pijnstiller bij dieren CHCl 3 (1847 !) anesthetica

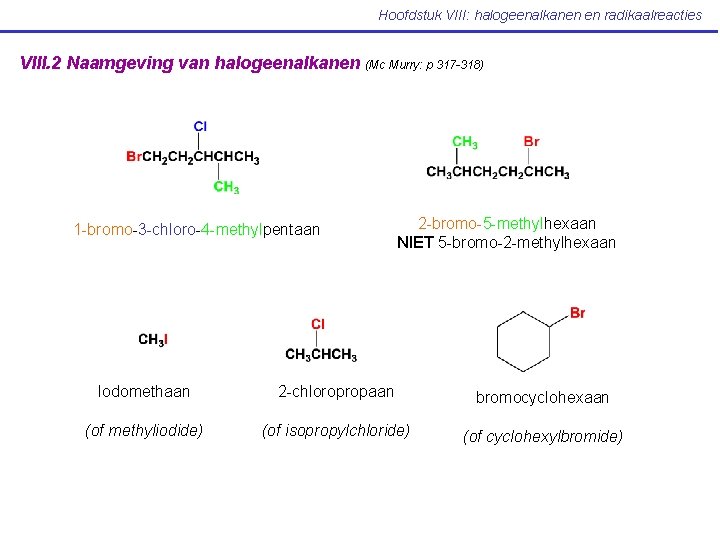
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 2 Naamgeving van halogeenalkanen (Mc Murry: p 317 -318) 1 -bromo-3 -chloro-4 -methylpentaan 2 -bromo-5 -methylhexaan NIET 5 -bromo-2 -methylhexaan Iodomethaan 2 -chloropropaan bromocyclohexaan (of methyliodide) (of isopropylchloride) (of cyclohexylbromide)

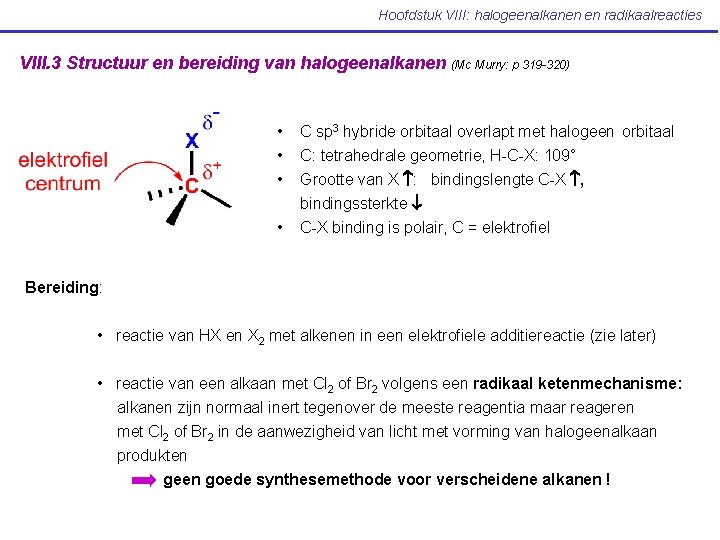
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 3 Structuur en bereiding van halogeenalkanen • • (Mc Murry: p 319 -320) C sp 3 hybride orbitaal overlapt met halogeen orbitaal C: tetrahedrale geometrie, H-C-X: 109° Grootte van X : bindingslengte C-X , bindingssterkte C-X binding is polair, C = elektrofiel Bereiding: • reactie van HX en X 2 met alkenen in een elektrofiele additiereactie (zie later) • reactie van een alkaan met Cl 2 of Br 2 volgens een radikaal ketenmechanisme: alkanen zijn normaal inert tegenover de meeste reagentia maar reageren met Cl 2 of Br 2 in de aanwezigheid van licht met vorming van halogeenalkaan produkten geen goede synthesemethode voor verscheidene alkanen !

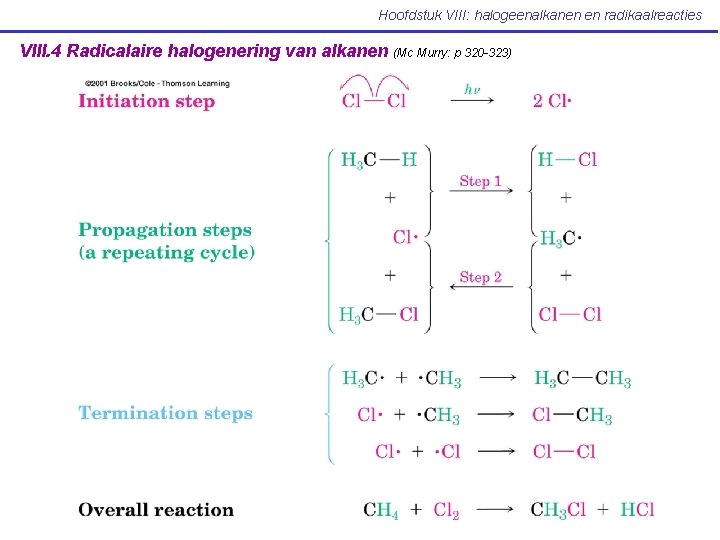
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 4 Radicalaire halogenering van alkanen (Mc Murry: p 320 -323)

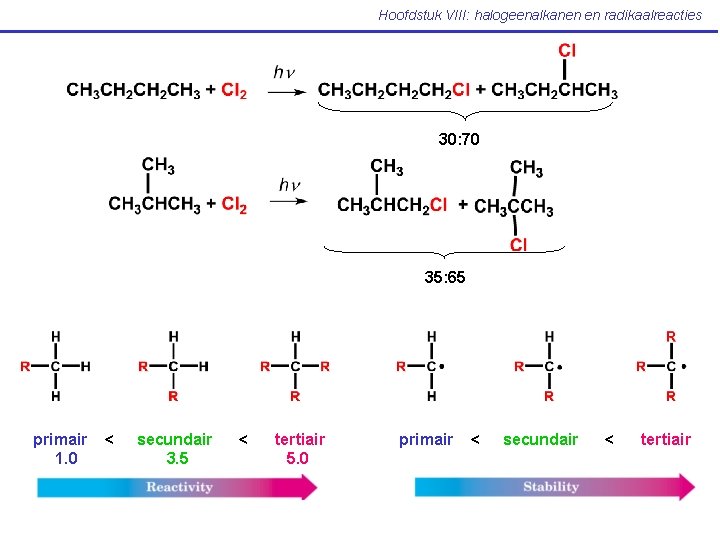
Hoofdstuk VIII: halogeenalkanen en radikaalreacties 30: 70 35: 65 primair 1. 0 < secundair 3. 5 < tertiair 5. 0 primair < secundair < tertiair

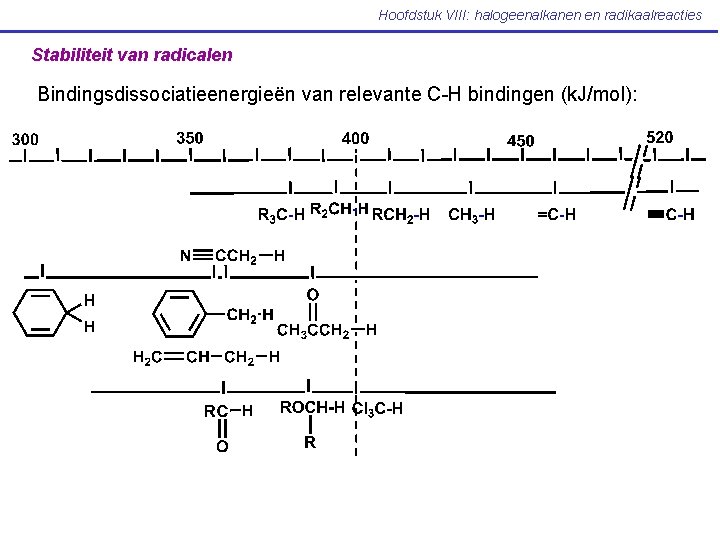
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Stabiliteit van radicalen Bindingsdissociatieenergieën van relevante C-H bindingen (k. J/mol):

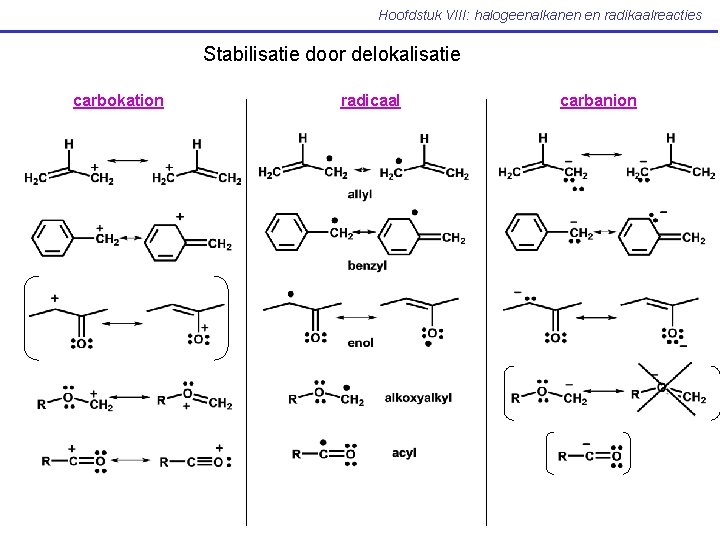
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Stabilisatie door delokalisatie carbokation radicaal carbanion

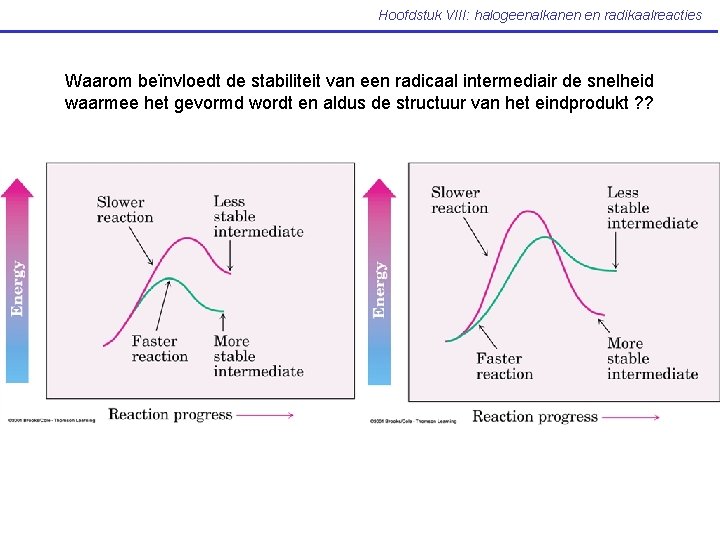
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Waarom beïnvloedt de stabiliteit van een radicaal intermediair de snelheid waarmee het gevormd wordt en aldus de structuur van het eindprodukt ? ?

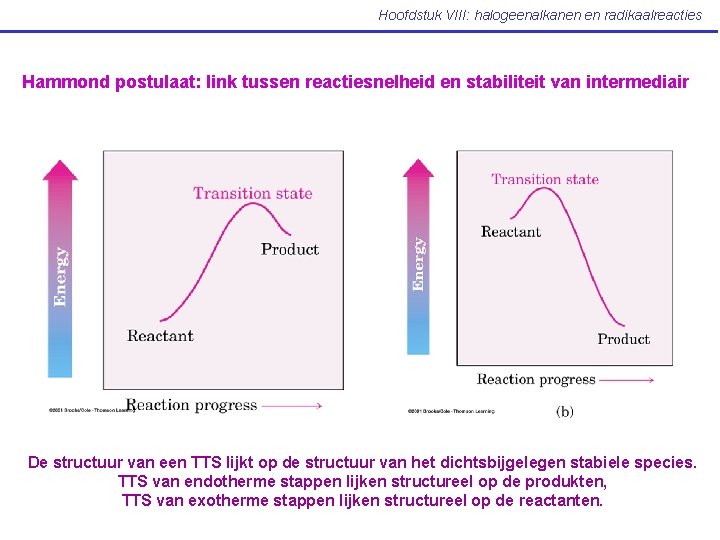
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Hammond postulaat: link tussen reactiesnelheid en stabiliteit van intermediair De structuur van een TTS lijkt op de structuur van het dichtsbijgelegen stabiele species. TTS van endotherme stappen lijken structureel op de produkten, TTS van exotherme stappen lijken structureel op de reactanten.

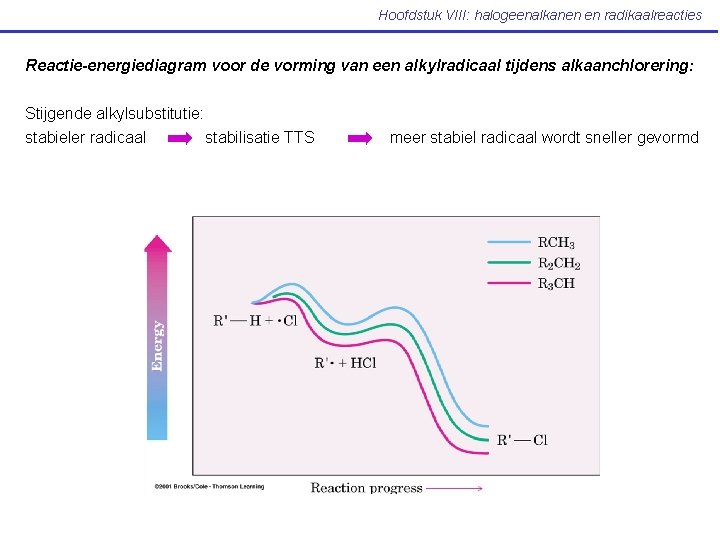
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Reactie-energiediagram voor de vorming van een alkylradicaal tijdens alkaanchlorering: Stijgende alkylsubstitutie: stabieler radicaal stabilisatie TTS meer stabiel radicaal wordt sneller gevormd

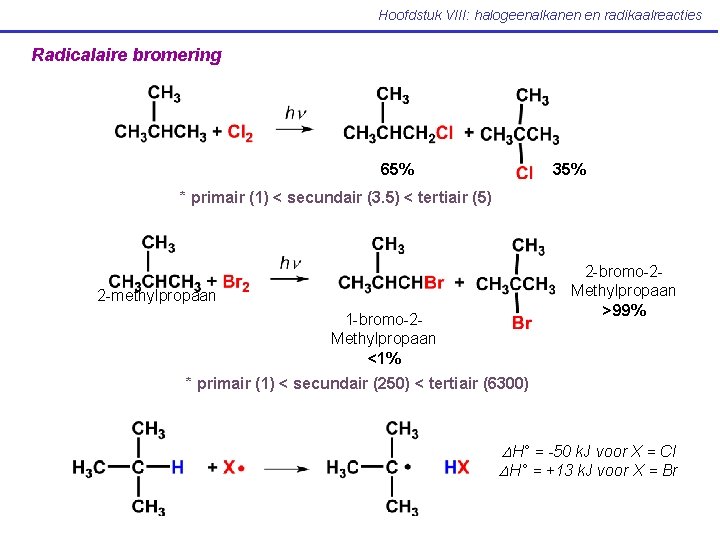
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Radicalaire bromering 65% 35% * primair (1) < secundair (3. 5) < tertiair (5) 2 -bromo-2 Methylpropaan >99% 2 -methylpropaan 1 -bromo-2 Methylpropaan <1% * primair (1) < secundair (250) < tertiair (6300) DH° = -50 k. J voor X = Cl DH° = +13 k. J voor X = Br

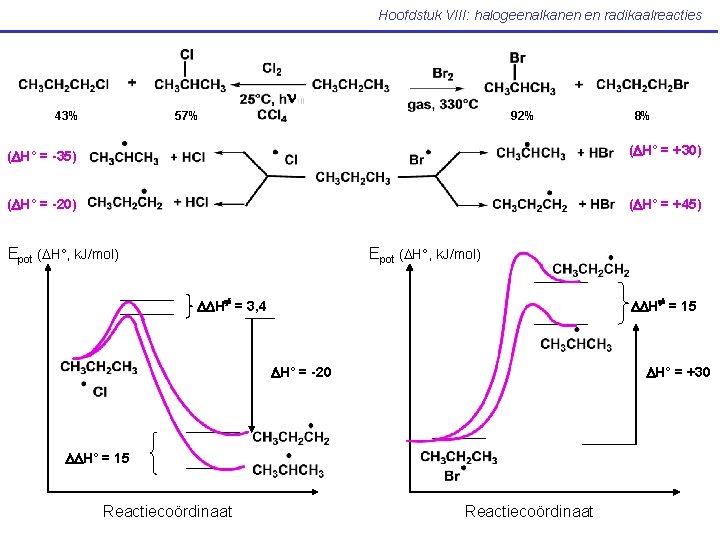
Hoofdstuk VIII: halogeenalkanen en radikaalreacties n 43% 57% 92% 8% (DH° = -35) (DH° = +30) (DH° = -20) (DH° = +45) Epot (DH°, k. J/mol) DDH = 15 DDH = 3, 4 DH° = +30 DH° = -20 DDH° = 15 Reactiecoördinaat

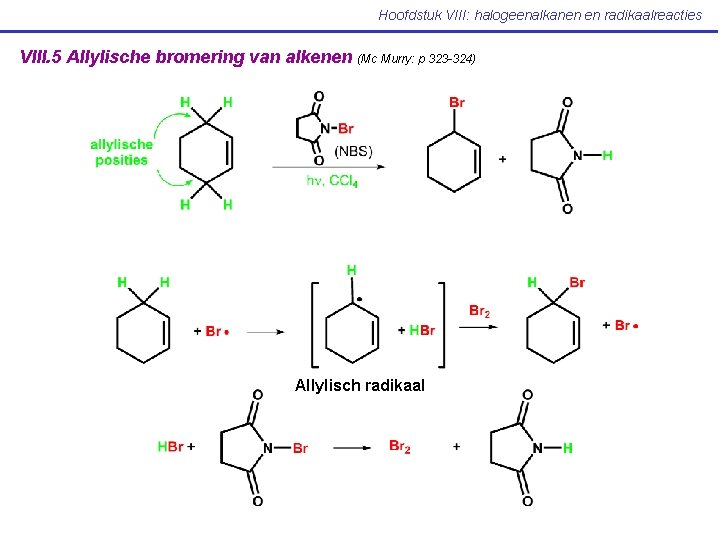
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 5 Allylische bromering van alkenen (Mc Murry: p 323 -324) Allylisch radikaal

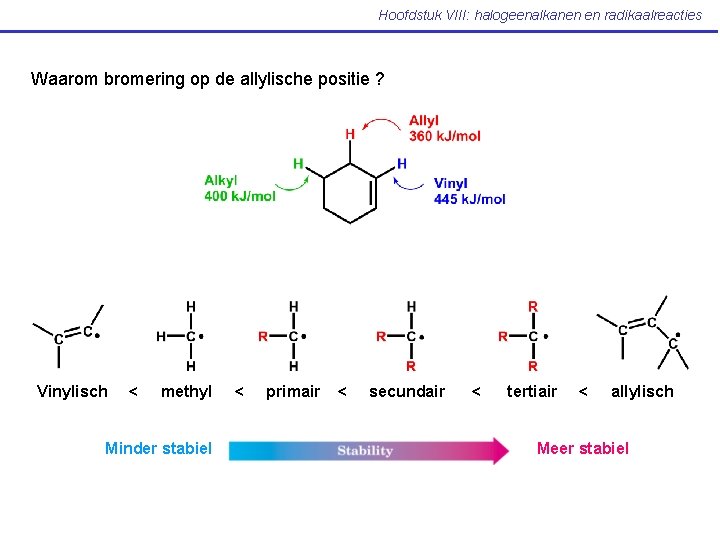
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Waarom bromering op de allylische positie ? Vinylisch < methyl Minder stabiel < primair < secundair < tertiair < allylisch Meer stabiel

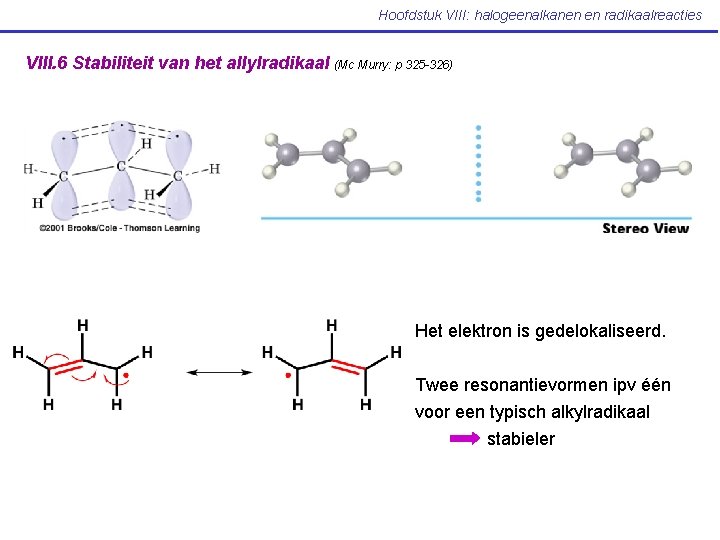
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 6 Stabiliteit van het allylradikaal (Mc Murry: p 325 -326) Het elektron is gedelokaliseerd. Twee resonantievormen ipv één voor een typisch alkylradikaal stabieler

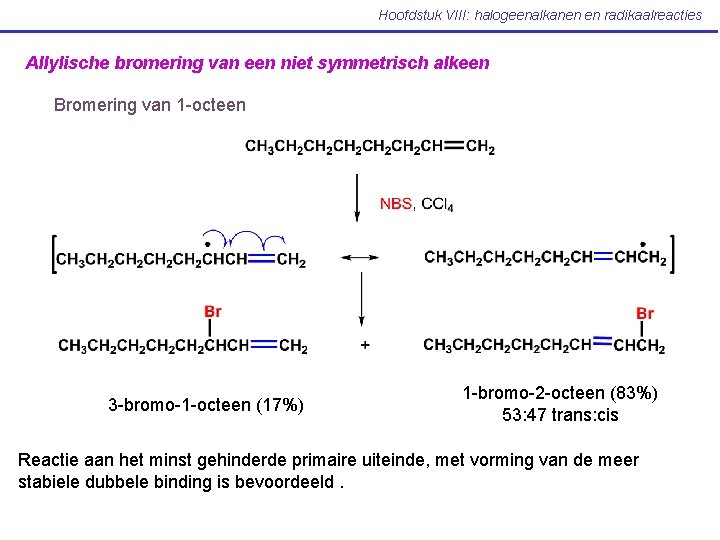
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Allylische bromering van een niet symmetrisch alkeen Bromering van 1 -octeen 3 -bromo-1 -octeen (17%) 1 -bromo-2 -octeen (83%) 53: 47 trans: cis Reactie aan het minst gehinderde primaire uiteinde, met vorming van de meer stabiele dubbele binding is bevoordeeld.

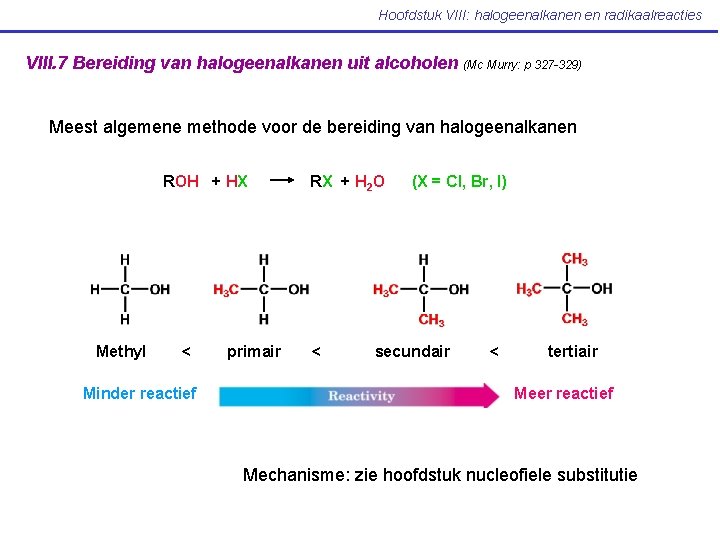
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 7 Bereiding van halogeenalkanen uit alcoholen (Mc Murry: p 327 -329) Meest algemene methode voor de bereiding van halogeenalkanen ROH + HX Methyl < Minder reactief primair RX + H 2 O < (X = Cl, Br, I) secundair < tertiair Meer reactief Mechanisme: zie hoofdstuk nucleofiele substitutie

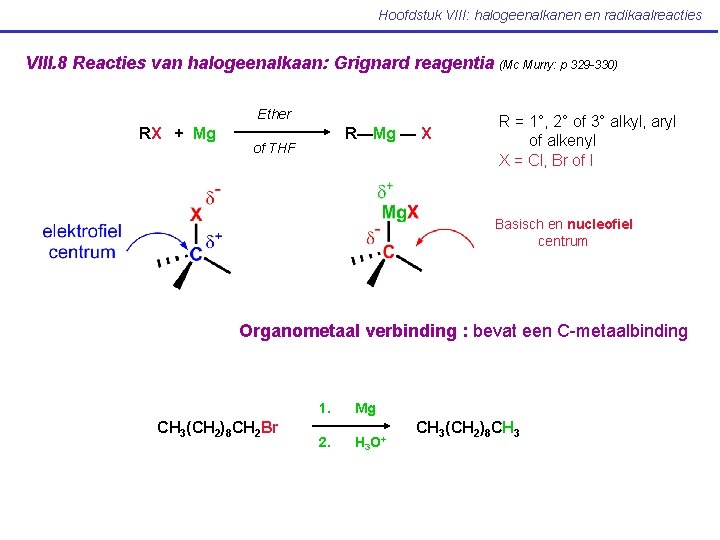
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 8 Reacties van halogeenalkaan: Grignard reagentia Ether RX + Mg R—Mg — X of THF (Mc Murry: p 329 -330) R = 1°, 2° of 3° alkyl, aryl of alkenyl X = Cl, Br of I Basisch en nucleofiel centrum Organometaal verbinding : bevat een C-metaalbinding CH 3(CH 2)8 CH 2 Br 1. Mg 2. H 3 O+ CH 3(CH 2)8 CH 3

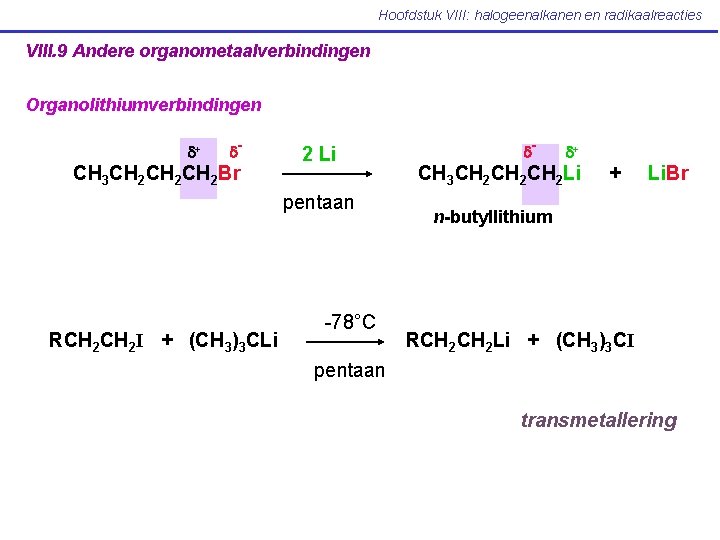
Hoofdstuk VIII: halogeenalkanen en radikaalreacties VIII. 9 Andere organometaalverbindingen Organolithiumverbindingen d+ d- CH 3 CH 2 CH 2 Br 2 Li pentaan RCH 2 I + (CH 3)3 CLi -78°C d- d+ CH 3 CH 2 CH 2 Li + Li. Br n-butyllithium RCH 2 Li + (CH 3)3 CI pentaan transmetallering

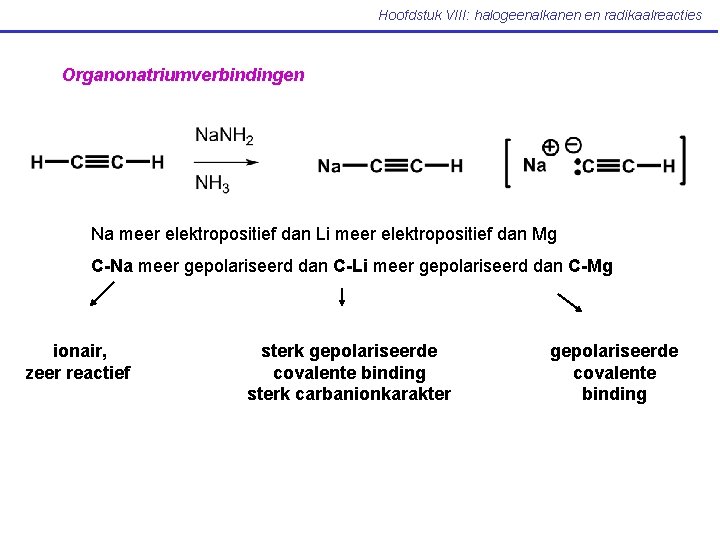
Hoofdstuk VIII: halogeenalkanen en radikaalreacties Organonatriumverbindingen Na meer elektropositief dan Li meer elektropositief dan Mg C-Na meer gepolariseerd dan C-Li meer gepolariseerd dan C-Mg ionair, zeer reactief sterk gepolariseerde covalente binding sterk carbanionkarakter gepolariseerde covalente binding

Hoofdstuk VIII: halogeenalkanen en radikaalreacties Gilman reagentia: lithium diorganokoperverbindingen ether 2 CH 3 Li + Cu. I methyllithium (CH 3)2 Cu- Li+ + Li. I Dimethylkoper lithium Cu minder elektropositief metaal Gebruik van organometaalverbindingen Worden aangewend als koolstofnucleofielen in nucleofiele substitutiereacties (zie hoofdstuk IX) en additiereacties (zie hoofdstuk XI). vorming van C-C-bindingen !!
 Vinylisch
Vinylisch Naughts and crosses chapter summary
Naughts and crosses chapter summary Begeleidingsstijlen leerling
Begeleidingsstijlen leerling Samenvatting bespiegeling hoofdstuk 9 massacultuur
Samenvatting bespiegeling hoofdstuk 9 massacultuur Handig tellen havo 4
Handig tellen havo 4 Aardrijkskunde hoofdstuk 2 havo 4
Aardrijkskunde hoofdstuk 2 havo 4 Hoofdstuk in een opera
Hoofdstuk in een opera Exploitatiebegroting betekenis
Exploitatiebegroting betekenis Wiskunde a havo 4 hoofdstuk 3
Wiskunde a havo 4 hoofdstuk 3 Symbolen elektrische stroomkring
Symbolen elektrische stroomkring Samenvatting de belofte van pisa
Samenvatting de belofte van pisa Reflexões do poeta canto viii
Reflexões do poeta canto viii Cara pembuatan xenon
Cara pembuatan xenon Henry viii beheaded wives
Henry viii beheaded wives Nn in roman numerals
Nn in roman numerals Henry viii deathbed painting
Henry viii deathbed painting Cn viii
Cn viii Gutenberg printing press ap world history
Gutenberg printing press ap world history En 13445 vs asme viii
En 13445 vs asme viii A teacher shall live with dignity
A teacher shall live with dignity Nav viii
Nav viii Viii
Viii King henry viii gardena
King henry viii gardena