ELEMENTOS DE CRISTALOQUIMICA L FUENTES CIMAV PLAN Repaso








- Slides: 25

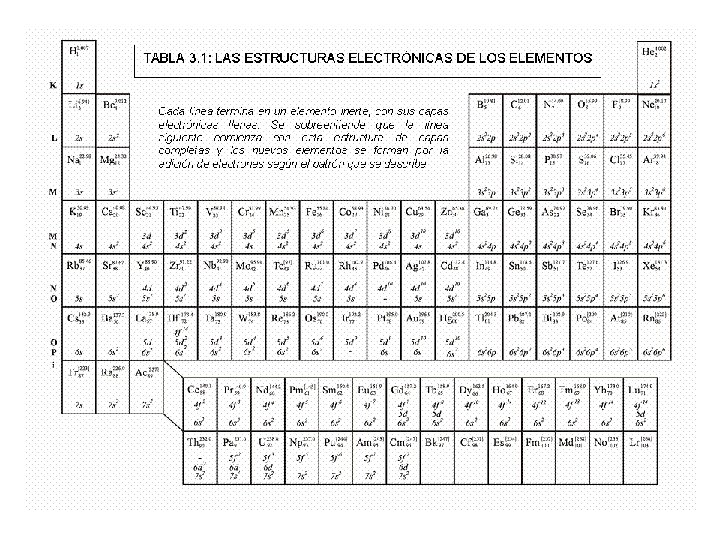
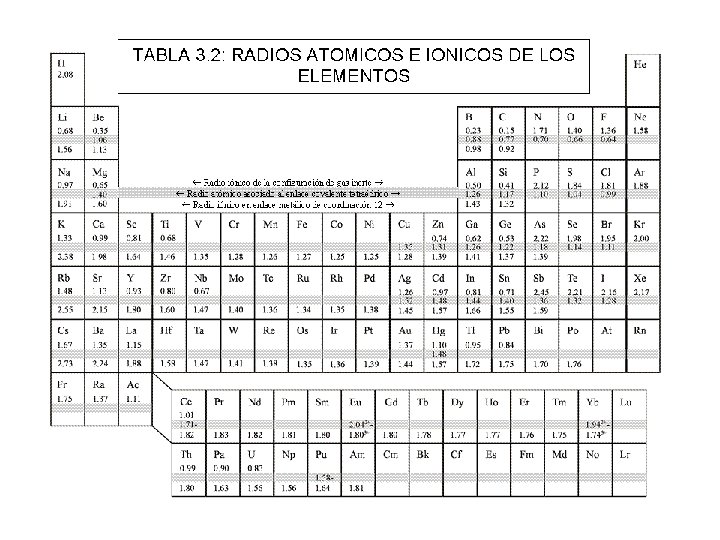
ELEMENTOS DE CRISTALOQUIMICA L. FUENTES. CIMAV PLAN ØRepaso de la Tabla Periódica -Números cuánticos, niveles de energía, llenado de las capas y subcapas. Radios atómicos e iónicos. Electronegatividades. ØEnlace iónico. Atracción y repulsión. Reglas de Pauling. Comparación Cs. Cl versus Na. Cl. ØEnlace covalente. Hibridización. Comparación diamante versus grafito. ØEnlaces de Van der Waals y de hidrógeno ØEnlace metálico. Papel del plasma electrónico.

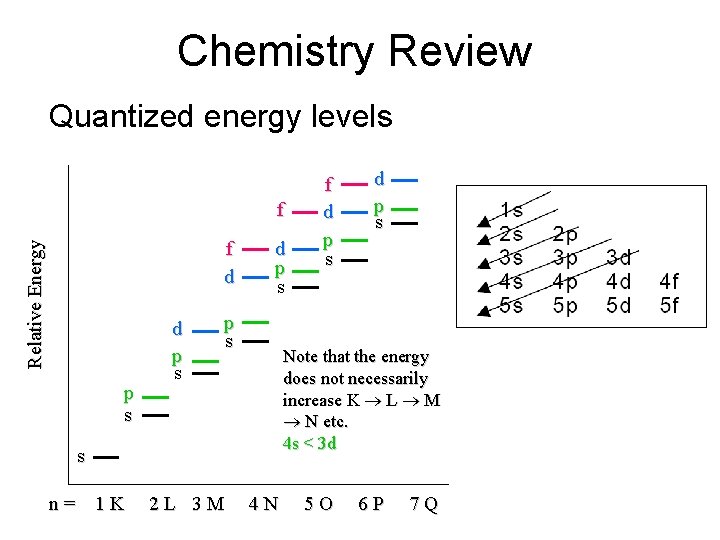
Chemistry Review Quantized energy levels f Relative Energy f d p s 2 L 3 M d p s Note that the energy does not necessarily increase K L M N etc. 4 s < 3 d s n= 1 K f d p s 4 N 5 O 6 P 7 Q

Chemistry Review Shells and Subshells innermost K (n = 1) 2 e s (lowest E) L (n = 2) 8 e s, p M (n = 3) 18 e s, p, d N (n = 4) 32 e s, p, d, f outer (generally higher E) higher levels not filled

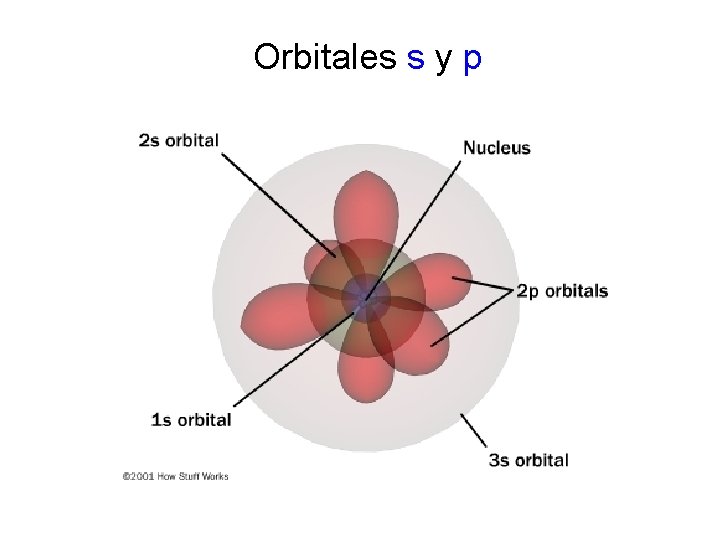
Orbitales s y p

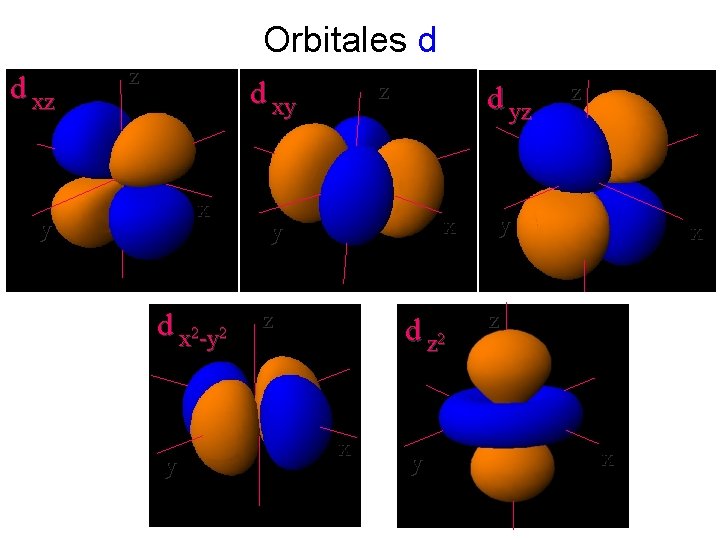
Orbitales d d xz z d xy x y d x 2 -y 2 y z d yz x y z d z 2 x y z y x z x




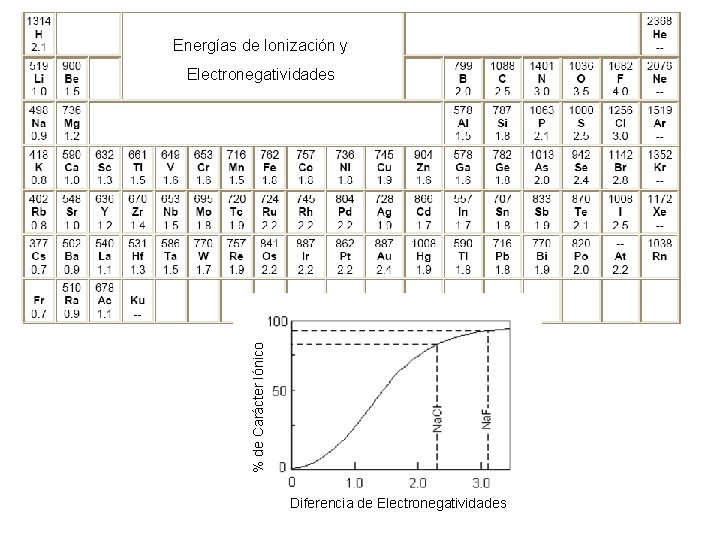
Energías de Ionización y % de Carácter Iónico Electronegatividades Diferencia de Electronegatividades

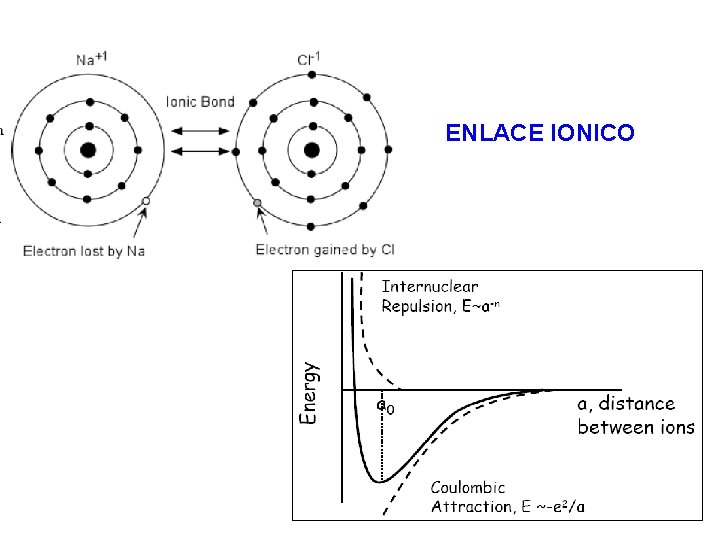
ENLACE IONICO

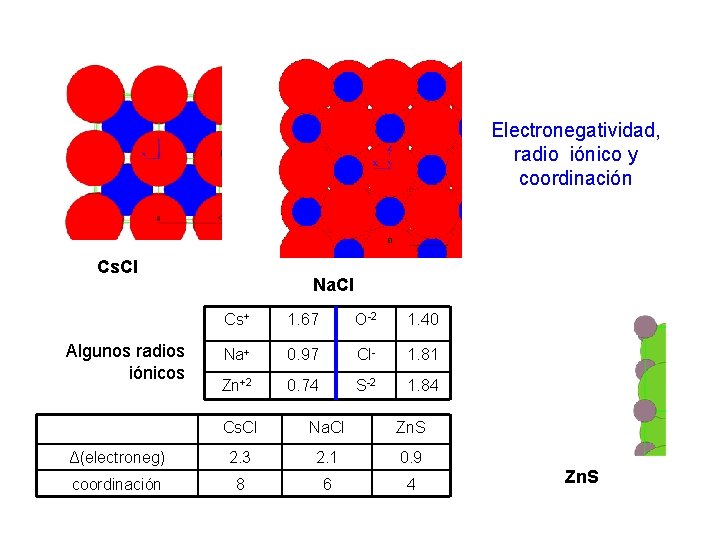
Electronegatividad, radio iónico y coordinación Cs. Cl Algunos radios iónicos Na. Cl Cs+ 1. 67 O-2 1. 40 Na+ 0. 97 Cl- 1. 81 Zn+2 0. 74 S-2 1. 84 Cs. Cl Na. Cl Zn. S Δ(electroneg) 2. 3 2. 1 0. 9 coordinación 8 6 4 Zn. S

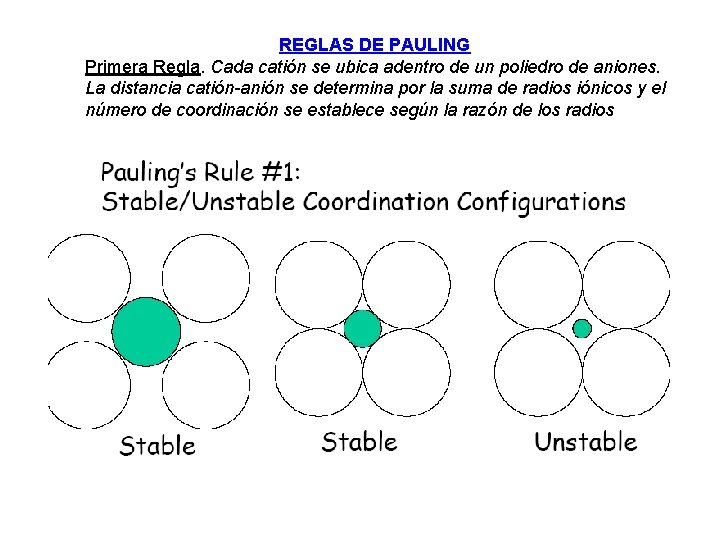
REGLAS DE PAULING Primera Regla. Cada catión se ubica adentro de un poliedro de aniones. La distancia catión anión se determina por la suma de radios iónicos y el número de coordinación se establece según la razón de los radios

Segunda Regla (Principio de Valencia Electrostática). En una estructura coordinada estable, la suma de las fortalezas de enlaces electros táticos asociados a los cationes que rodean a un anión determinado es igual a la valencia del anión. Tercera Regla. Aristas o caras comunes a dos poliedros de coordinación disminuyen la estabilidad. Cuarta Regla. En cristales que contienen diferentes cationes, los cuales comparten caras o aristas de poliedros vecinos, los cationes comunes tienden a ser aquellos de mayor valencia y menor número de coordinación. Quinta Regla. El número de motivos atómicos en un cristal tiende a ser pequeño.

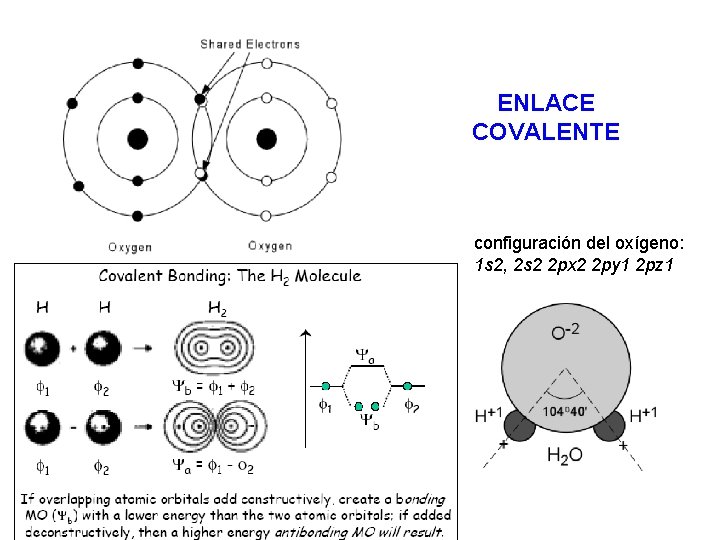
ENLACE COVALENTE configuración del oxígeno: 1 s 2, 2 s 2 2 px 2 2 py 1 2 pz 1

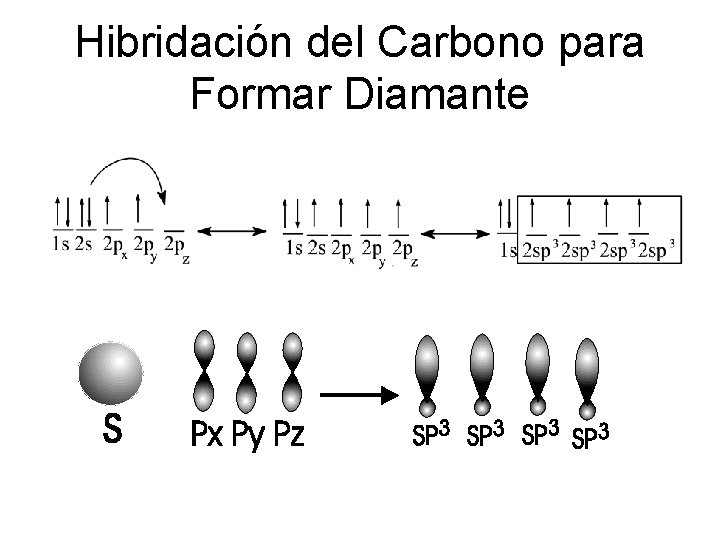
Hibridación del Carbono para Formar Diamante

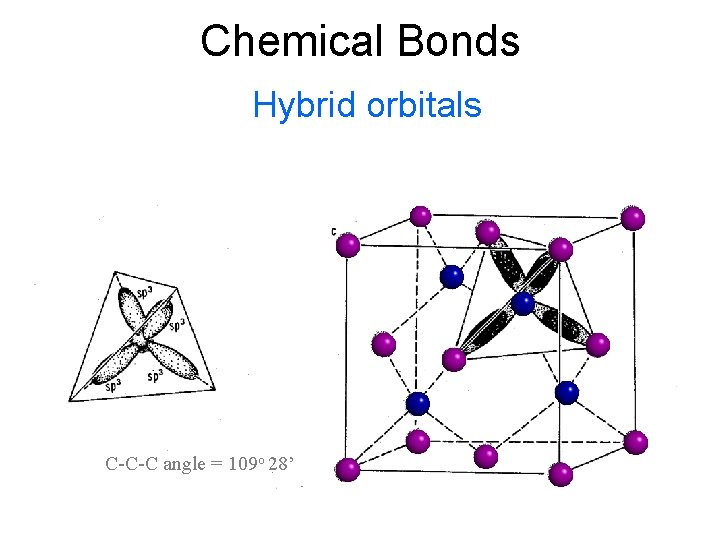
Chemical Bonds Hybrid orbitals Fig 8 -8 of Bloss, Crystallography and Crystal Chemistry. © MSA C-C-C angle = 109 o 28’

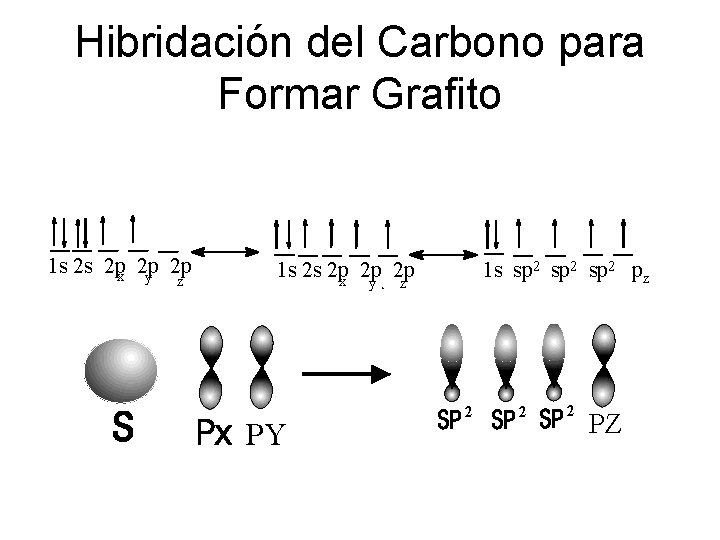
Hibridación del Carbono para Formar Grafito 1 s 2 s 2 px 2 p 2 p y z 1 s sp 2 pz z PY 2 2 2 PZ

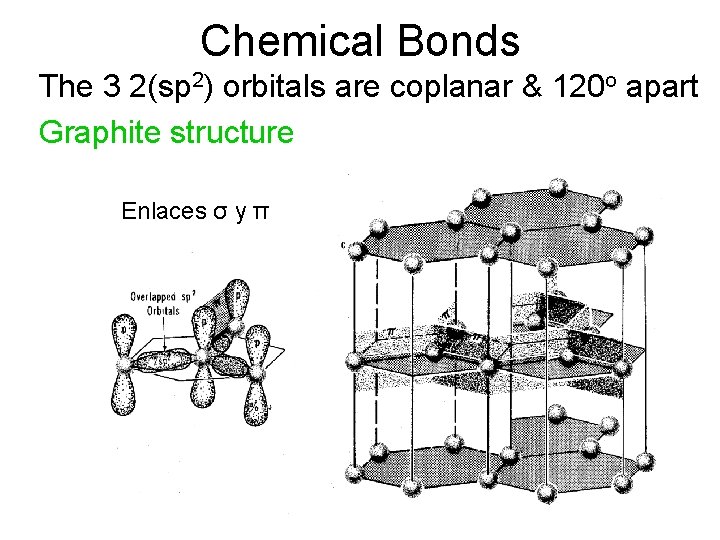
Chemical Bonds The 3 2(sp 2) orbitals are coplanar & 120 o apart Graphite structure Fig 8 -8 of Bloss, Crystallography and Crystal Chemistry. © MSA Enlaces σ y π

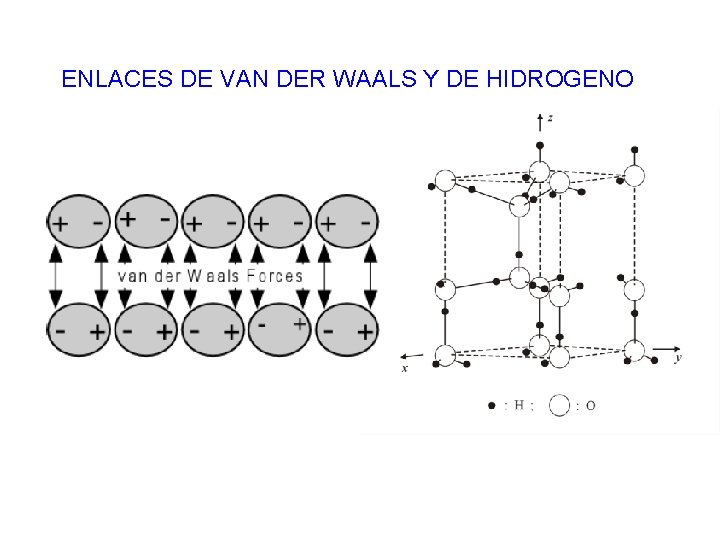
ENLACES DE VAN DER WAALS Y DE HIDROGENO

«Metales» , según el texto de Kittel

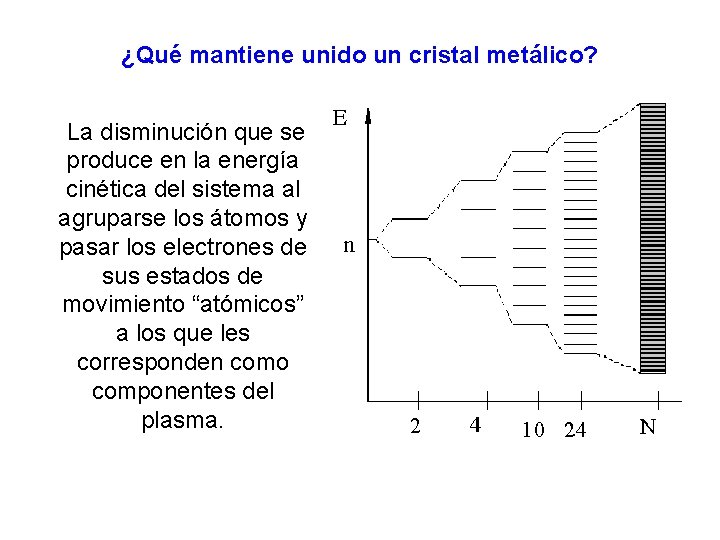
¿Qué mantiene unido un cristal metálico? La disminución que se produce en la energía cinética del sistema al agruparse los átomos y pasar los electrones de sus estados de movimiento “atómicos” a los que les corresponden como componentes del plasma.

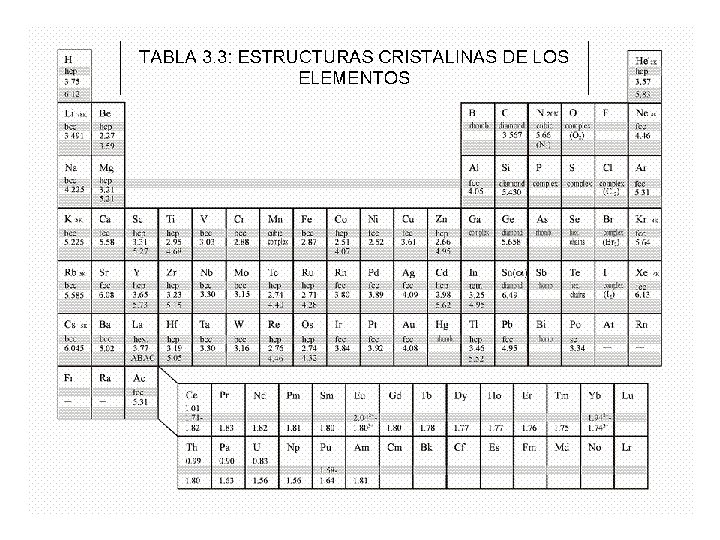
Estructuras cristalinas de los metales FCC: Ac, Ag, Al, Au, Ca, Ce, Co, Cu, Fe, Ir, La, Li, Mn, Ni, Pb, Pd, Pr, Pt, Pu, Rh, Sc, Sr, Th e Yb. HCP: Be, Cd, Ce, Dy, Er, Gd, He, Hf, Ho, Li, Lu, Mg, Na, Nd, Os, Re, Ru, Sc, Tb, Ti, Tl, Tm, Y, Zn y Zr. BCC: Ba, Be, Cr, Cs, Eu, Fe, Hf, K, Li, Mn, Mo, Na, Nb, Pu, Rb, Sr, Ta, Th, Ti, Tl, U, V, W, Y y Zr.


