Chapitre I Asthme La Lettre du Pneumologue La






- Slides: 26

Chapitre I Asthme La Lettre du Pneumologue La. La Lettre dudu Pneumologue Lettre Pneumologue

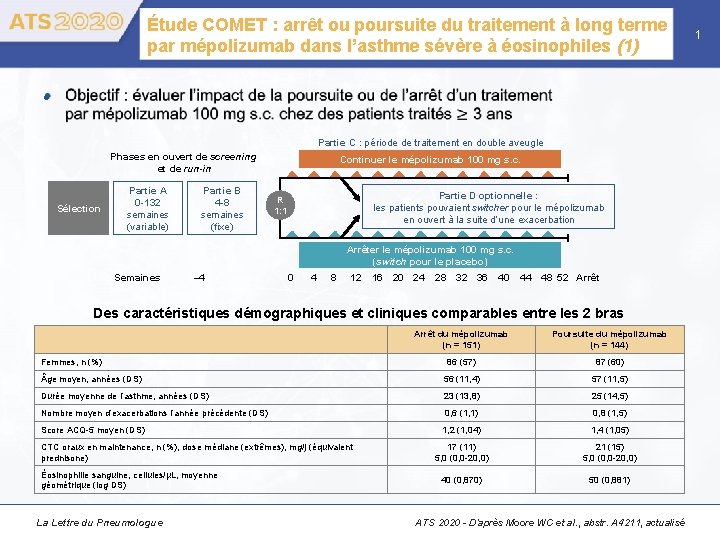
Étude COMET : arrêt ou poursuite du traitement à long terme par mépolizumab dans l’asthme sévère à éosinophiles (1) • Partie C : période de traitement en double aveugle Phases en ouvert de screening et de run-in Sélection Partie A 0 -132 semaines (variable) Partie B 4 -8 semaines (fixe) Continuer le mépolizumab 100 mg s. c. Partie D optionnelle : les patients pouvaient switcher pour le mépolizumab en ouvert à la suite d’une exacerbation R 1: 1 Arrêter le mépolizumab 100 mg s. c. (switch pour le placebo) Semaines – 4 0 4 8 12 16 20 24 28 32 36 40 44 48 52 Arrêt Des caractéristiques démographiques et cliniques comparables entre les 2 bras Arrêt du mépolizumab (n = 151) Poursuite du mépolizumab (n = 144) 86 (57) 87 (60) ge moyen, années (DS) 56 (11, 4) 57 (11, 5) Durée moyenne de l’asthme, années (DS) 23 (13, 8) 25 (14, 5) Nombre moyen d’exacerbations l’année précédente (DS) 0, 6 (1, 1) 0, 8 (1, 5) Score ACQ-5 moyen (DS) 1, 2 (1, 04) 1, 4 (1, 05) 17 (11) 5, 0 (0, 0 -20, 0) 21 (15) 5, 0 (0, 0 -20, 0) 40 (0, 870) 50 (0, 881) Femmes, n (%) CTC oraux en maintenance, n (%), dose médiane (extrêmes), mg/j (équivalent prednisone) Éosinophilie sanguine, cellules/μL, moyenne géométrique (log DS) La Lettre du Pneumologue ATS 2020 - D’après Moore WC et al. , abstr. A 4211, actualisé 1

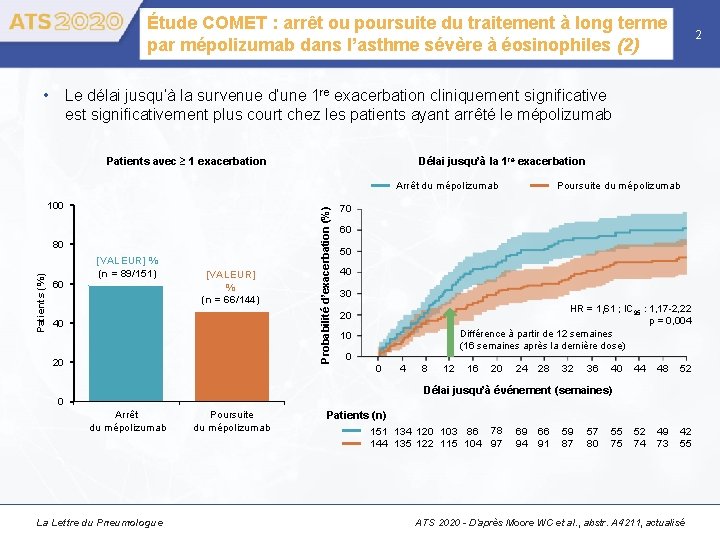
Étude COMET : arrêt ou poursuite du traitement à long terme par mépolizumab dans l’asthme sévère à éosinophiles (2) 2 • Le délai jusqu’à la survenue d’une 1 re exacerbation cliniquement significative est significativement plus court chez les patients ayant arrêté le mépolizumab Patients avec ≥ 1 exacerbation Délai jusqu’à la 1 re exacerbation 100 Patients (%) 80 60 [VALEUR] % (n = 89/151) [VALEUR] % (n = 66/144) 40 20 Probabilité d’exacerbation (%) Arrêt du mépolizumab Poursuite du mépolizumab 70 60 50 40 30 HR = 1, 61 ; IC 95 : 1, 17 -2, 22 p = 0, 004 Différence à partir de 12 semaines (16 semaines après la dernière dose) 20 10 0 0 4 8 12 16 20 24 28 32 36 40 44 48 52 52 74 49 73 42 55 Délai jusqu’à événement (semaines) 0 Arrêt du mépolizumab La Lettre du Pneumologue Poursuite du mépolizumab Patients (n) 151 134 120 103 86 78 144 135 122 115 104 97 69 94 66 91 59 87 57 80 55 75 ATS 2020 - D’après Moore WC et al. , abstr. A 4211, actualisé

Étude COMET : arrêt ou poursuite du traitement à long terme par mépolizumab dans l’asthme sévère à éosinophiles (3) • L’éosinophilie sanguine augmente chez les patients ayant arrêté le mépolizumab pour revenir aux niveaux avant traitement Arrêt du mépolizumab Ratio ajusté/inclusion 16 Poursuite du mépolizumab L’éosinophilie sanguine remonte à 270 cellules/μL à S 12 (16 semaines après la dernière dose) 8 4 Ratio S 52 (arrêt/poursuite) : 6, 19 IC 95 : 4, 89 -7, 83 p < 0, 001 2 1 0, 5 L’éosinophilie sanguine se maintient à 40 -60 cellules/μL 0 4 8 12 16 20 24 28 Semaines 32 36 40 44 48 52 145 137 136 133 121 120 103 114 84 102 79 106 75 99 68 93 66 92 60 88 60 92 Patients, n 150 141 La Lettre du Pneumologue 77 101 ATS 2020 - D’après Moore WC et al. , abstr. A 4211, actualisé 3

Étude de phase III : mépolizumab dans le syndrome hyperéosinophilique (SHE) (1) 4 • Jusqu’à 4 semaines 32 semaines Sélection R 1: 1 Jusqu’à 0 – 4 semaines Traitement SHE + mépolizumab 300 mg s. c. ou placebo Jusqu’à 8 semaines Suivi Placebo (n = 54) Mépolizumab (n = 54) 45 (15 -80) 47 (12 -82) 27 (50) 30 (56) 5, 7 (8, 04) 5, 5 (5, 08) IMC moyen 26, 20 (5, 934) 26, 38 (5, 885) Éosinophilie sanguine, moyenne géométrique (log DS) 1 350 (0, 708) 1 460 (0, 946) Caractéristiques des patients inclus ge moyen, années (extrêmes) Femmes, n (%) Durée moyenne du SHE (DS), années 4 8 12 16 20 24 28 32 Jusqu’à 40 semaines Dans le bras placebo, 70 % des patients étaient sous CTC oraux et 17 % recevaient un traitement cytotoxique/immunosuppresseur à l’inclusion La Lettre du Pneumologue Dans le bras mépolizumab, 74 % des patients étaient sous CTC oraux et 26 % recevaient un traitement cytotoxique/immunosuppresseur à l’inclusion ATS 2020 - D’après Steinfeld J et al. , abstr. A 4212, actualisé

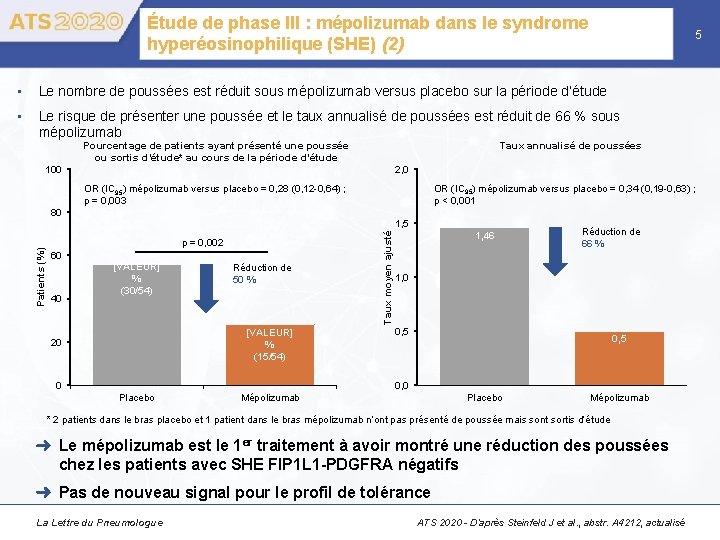
Étude de phase III : mépolizumab dans le syndrome hyperéosinophilique (SHE) (2) 5 • Le nombre de poussées est réduit sous mépolizumab versus placebo sur la période d’étude • Le risque de présenter une poussée et le taux annualisé de poussées est réduit de 66 % sous mépolizumab Pourcentage de patients ayant présenté une poussée ou sortis d’étude* au cours de la période d’étude Taux annualisé de poussées 100 2, 0 OR (IC 95) mépolizumab versus placebo = 0, 34 (0, 19 -0, 63) ; p < 0, 001 OR (IC 95) mépolizumab versus placebo = 0, 28 (0, 12 -0, 64) ; p = 0, 003 1, 5 p = 0, 002 60 40 [VALEUR] % (30/54) Réduction de 50 % [VALEUR] % (15/54) 20 0 Taux moyen ajusté Patients (%) 80 1, 46 Réduction de 66 % 1, 0 0, 5 0, 0 Placebo Mépolizumab * 2 patients dans le bras placebo et 1 patient dans le bras mépolizumab n’ont pas présenté de poussée mais sont sortis d’étude Le mépolizumab est le 1 er traitement à avoir montré une réduction des poussées chez les patients avec SHE FIP 1 L 1 -PDGFRA négatifs Pas de nouveau signal pour le profil de tolérance La Lettre du Pneumologue ATS 2020 - D’après Steinfeld J et al. , abstr. A 4212, actualisé

Le masitinib réduit les exacerbations dans l’asthme sévère non contrôlé sous corticoïdes oraux (1) • R 2: 1 Visite d’inclusion Masitinib (6 mg/kg/j) Période de traitement de 36 semaines en double aveugle Phase de run-in/placebo S Période d’extension Placebo B 2 4 6 8 10 12 16 20 24 28 32 36/F 48 60 72 Visites/semaines La Lettre du Pneumologue ATS 2020 - D’après Chanez P et al. , abstr. A 4210, actualisé 6

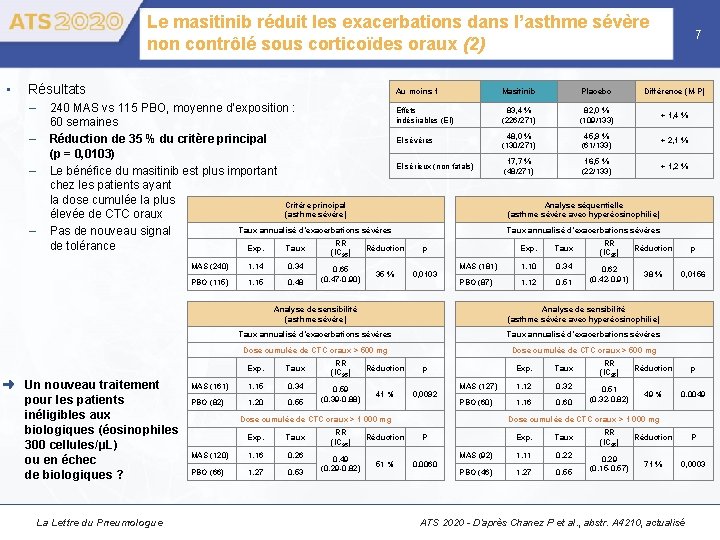
Le masitinib réduit les exacerbations dans l’asthme sévère non contrôlé sous corticoïdes oraux (2) • Résultats – – Au moins 1 240 MAS vs 115 PBO, moyenne d’exposition : Effets indésirables (EI) 60 semaines Réduction de 35 % du critère principal EI sévères (p = 0, 0103) EI sérieux (non fatals) Le bénéfice du masitinib est plus important chez les patients ayant la dose cumulée la plus Critère principal (asthme sévère) élevée de CTC oraux Taux annualisé d’exacerbations sévères Pas de nouveau signal RR de tolérance Exp. Taux Réduction p (IC ) Masitinib Placebo Différence (M-P) 83, 4 % (226/271) 82, 0 % (109/133) + 1, 4 % 48, 0 % (130/271) 45, 9 % (61/133) + 2, 1 % 17, 7 % (48/271) 16, 5 % (22/133) + 1, 2 % Analyse séquentielle (asthme sévère avec hyperéosinophilie) Taux annualisé d’exacerbations sévères Exp. Taux MAS (181) 1, 10 0, 34 PBO (87) 1, 12 0, 51 95 Un nouveau traitement pour les patients inéligibles aux biologiques (éosinophiles 300 cellules/μL) ou en échec de biologiques ? La Lettre du Pneumologue MAS (240) 1, 14 0, 34 PBO (115) 1, 15 0, 48 0, 65 (0, 47 -0, 90) 35 % 0, 0103 RR (IC 95) Réduction p 0, 62 (0, 42 -0, 91) 38 % 0, 0156 Analyse de sensibilité (asthme sévère) Analyse de sensibilité (asthme sévère avec hyperéosinophilie) Taux annualisé d’exacerbations sévères Dose cumulée de CTC oraux > 500 mg Exp. Taux MAS (161) 1, 15 0, 34 PBO (82) 1, 20 0, 55 RR (IC 95) Réduction p 0, 59 (0, 39 -0, 88) 41 % 0, 0092 Exp. Taux MAS (127) 1, 12 0, 32 PBO (60) 1, 16 0, 60 Dose cumulée de CTC oraux > 1 000 mg Exp. Taux MAS (120) 1, 16 0, 26 PBO (66) 1, 27 0, 53 7 RR (IC 95) Réduction p 0, 51 (0, 32 -0, 82) 49 % 0, 0049 Dose cumulée de CTC oraux > 1 000 mg RR (IC 95) Réduction P 0, 49 (0, 29 -0, 82) 51 % 0, 0060 Exp. Taux MAS (92) 1, 11 0, 22 PBO (46) 1, 27 0, 55 RR (IC 95) Réduction P 0, 29 (0, 15 -0, 57) 71 % 0, 0003 ATS 2020 - D’après Chanez P et al. , abstr. A 4210, actualisé

Étude de phase III IRIDIUM : IND/GLY/MF versus CSI/LABA dans l’asthme non contrôlé (1) • Période pré-randomisation Sélection (2 semaines) Run-in (2 semaines) LABA/CSI dose moyenne à élevée SAL/FU (dose moyenne) 50/250 μg x 2/j Période de traitement en double aveugle (52 semaines) Randomisation 1: 1: 1 Période de suivi, tolérance (30 jours) IND/GLY/MF* dose moyenne (150/50/80 μg)/j via Breezhaler® (n = 620) IND/GLY/MF* dose élevée (150/50/160 μg)/j via Breezhaler® (n = 619) IND/MF* dose moyenne (150/160 ug)/j via Breezhaler® (n = 617) IND/MF* dose élevée (150/320 ug)/j via Breezhaler® (n = 618) SAL/FU dose élevée 50/500 μg x 2/j via Diskus® (n = 618) Salbutamol/albutérol disponible en BD de secours au cours de l’étude Jour – 28 à – 15 Jour – 14 à – 1 Jour 1 à 365 * Traitements administrés le soir. La Lettre du Pneumologue ATS 2020 - D’après Kerstjens HAM et al. , abstr. A 3007, actualisé 8

Étude de phase III IRIDIUM : IND/GLY/MF versus CSI/LABA dans l’asthme non contrôlé (2) 9 • Amélioration du VEMS avec IND/GLY/MF versus IND/MF (critère principal à S 26) et SAL/FLU à S 26 (A) et jusqu’à S 52 (totalité de l’échantillon) (B) Variation entre l’inclusion et S 26 du VEMS (m. L) A Δ 76 m. L IC 95 : 41 -111 p < 0, 001 350 Δ 99 m. L IC 95 : 64 -133 p < 0, 001 Δ 119 m. L IC 95 : 85 -154 p < 0, 001 300 250 200 150 100 [VALEUR] n = 538 50 0 [VALEUR] n = 527 IND/MF IND/GLY/MF dose moyenne B Variation entre l’inclusion et S 52 du VEMS (m. L) Δ 65 m. L IC 95 : 31 -99 p < 0, 001 [VALEUR] n = 541 n = 527 IND/GLY/MF dose élevée [VALEUR] n = 527 IND/MF dose élevée [VALEUR] n = 538 IND/GLY/MF dose moyenne [VALEUR] n = 506 [VALEUR] n = 541 [VALEUR] n = 506 SAL/FLU dose élevée IND/GLY/MF dose élevée SAL/FLU dose élevée 400 IND/GLY/MF dose élevée 300 IND/GLY/MF dose moyenne IND/MF dose élevée IND/MF dose moyenne SAL/FLU dose élevée 200 100 0 0 Jour 2 Jour 184 Jour 365 Amélioration du score ACQ-7 avec IND/GLY/MF dose moyenne ou élevée versus SAL/FLU Taux annualisé d’exacerbations : réduit de 21 % avec IND/GLY/MF dose élevée versus IND/MF dose élevée et de 40 % versus SAL/FLU dose élevée Bon profil de tolérance comparable entre les différents bras de traitement La Lettre du Pneumologue ATS 2020 - D’après Kerstjens HAM et al. , abstr. A 3007, actualisé

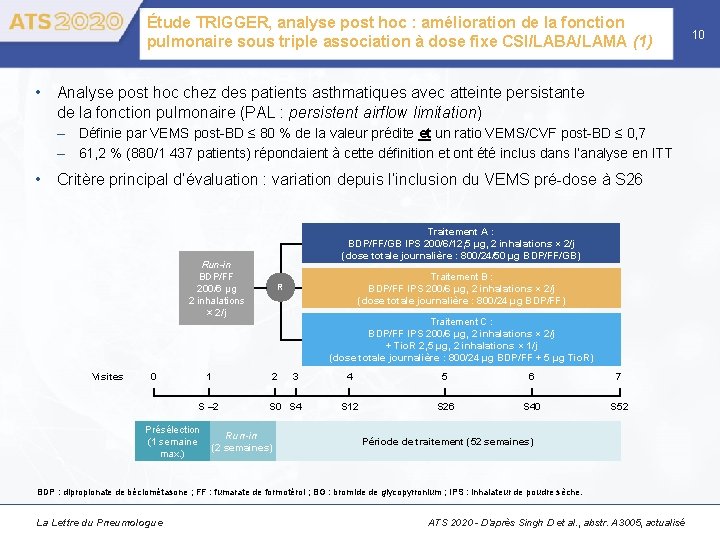
Étude TRIGGER, analyse post hoc : amélioration de la fonction pulmonaire sous triple association à dose fixe CSI/LABA/LAMA (1) • Analyse post hoc chez des patients asthmatiques avec atteinte persistante de la fonction pulmonaire (PAL : persistent airflow limitation) – Définie par VEMS post-BD ≤ 80 % de la valeur prédite et un ratio VEMS/CVF post-BD ≤ 0, 7 – 61, 2 % (880/1 437 patients) répondaient à cette définition et ont été inclus dans l’analyse en ITT • Critère principal d’évaluation : variation depuis l’inclusion du VEMS pré-dose à S 26 Traitement A : BDP/FF/GB IPS 200/6/12, 5 μg, 2 inhalations × 2/j (dose totale journalière : 800/24/50 μg BDP/FF/GB) Run-in BDP/FF 200/6 μg 2 inhalations × 2/j Visites 0 1 Présélection (1 semaine max. ) Traitement C : BDP/FF IPS 200/6 μg, 2 inhalations × 2/j + Tio. R 2, 5 μg, 2 inhalations × 1/j (dose totale journalière : 800/24 μg BDP/FF + 5 μg Tio. R) 2 S – 2 Traitement B : BDP/FF IPS 200/6 μg, 2 inhalations × 2/j (dose totale journalière : 800/24 μg BDP/FF) R 3 S 0 S 4 Run-in (2 semaines) 4 5 6 7 S 12 S 26 S 40 S 52 Période de traitement (52 semaines) BDP : dipropionate de béclométasone ; FF : fumarate de formotérol ; BG : bromide de glycopyrronium ; IPS : inhalateur de poudre sèche. La Lettre du Pneumologue ATS 2020 - D’après Singh D et al. , abstr. A 3005, actualisé 10

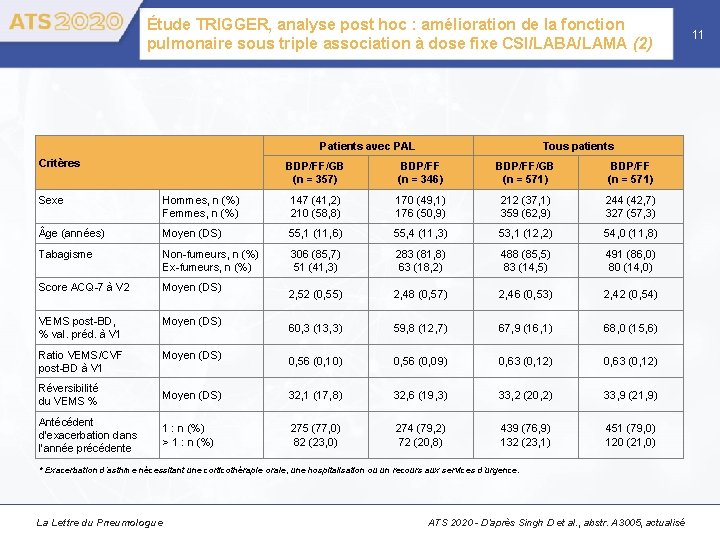
Étude TRIGGER, analyse post hoc : amélioration de la fonction pulmonaire sous triple association à dose fixe CSI/LABA/LAMA (2) Patients avec PAL Critères Tous patients BDP/FF/GB (n = 357) BDP/FF (n = 346) BDP/FF/GB (n = 571) BDP/FF (n = 571) Sexe Hommes, n (%) Femmes, n (%) 147 (41, 2) 210 (58, 8) 170 (49, 1) 176 (50, 9) 212 (37, 1) 359 (62, 9) 244 (42, 7) 327 (57, 3) ge (années) Moyen (DS) 55, 1 (11, 6) 55, 4 (11, 3) 53, 1 (12, 2) 54, 0 (11, 8) Tabagisme Non-fumeurs, n (%) Ex-fumeurs, n (%) 306 (85, 7) 51 (41, 3) 283 (81, 8) 63 (18, 2) 488 (85, 5) 83 (14, 5) 491 (86, 0) 80 (14, 0) Score ACQ-7 à V 2 Moyen (DS) 2, 52 (0, 55) 2, 48 (0, 57) 2, 46 (0, 53) 2, 42 (0, 54) VEMS post-BD, % val. préd. à V 1 Moyen (DS) 60, 3 (13, 3) 59, 8 (12, 7) 67, 9 (16, 1) 68, 0 (15, 6) Ratio VEMS/CVF post-BD à V 1 Moyen (DS) 0, 56 (0, 10) 0, 56 (0, 09) 0, 63 (0, 12) Réversibilité du VEMS % Moyen (DS) 32, 1 (17, 8) 32, 6 (19, 3) 33, 2 (20, 2) 33, 9 (21, 9) Antécédent d’exacerbation dans l’année précédente 1 : n (%) > 1 : n (%) 275 (77, 0) 82 (23, 0) 274 (79, 2) 72 (20, 8) 439 (76, 9) 132 (23, 1) 451 (79, 0) 120 (21, 0) * Exacerbation d’asthme nécessitant une corticothérapie orale, une hospitalisation ou un recours aux services d’urgence. La Lettre du Pneumologue ATS 2020 - D’après Singh D et al. , abstr. A 3005, actualisé 11

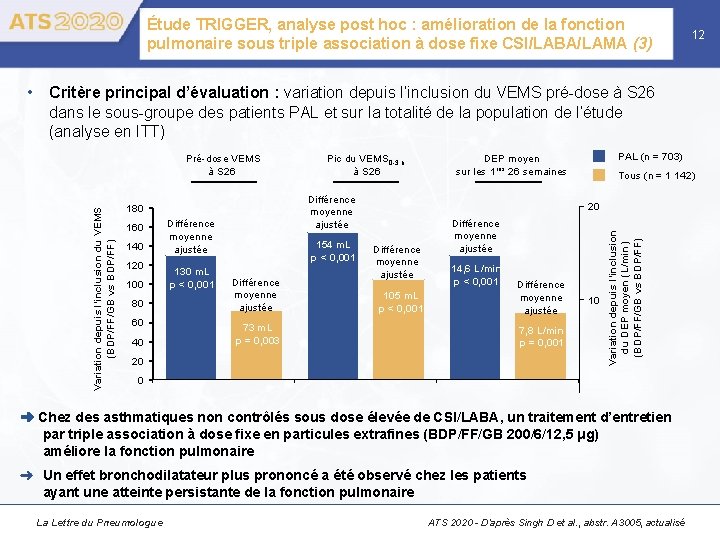
Étude TRIGGER, analyse post hoc : amélioration de la fonction pulmonaire sous triple association à dose fixe CSI/LABA/LAMA (3) 12 • Critère principal d’évaluation : variation depuis l’inclusion du VEMS pré-dose à S 26 dans le sous-groupe des patients PAL et sur la totalité de la population de l’étude (analyse en ITT) Différence moyenne ajustée 180 160 140 120 100 80 60 40 Différence moyenne ajustée 130 m. L p < 0, 001 Pic du VEMS 0 -3 h à S 26 154 m. L p < 0, 001 Différence moyenne ajustée 73 m. L p = 0, 003 PAL (n = 703) DEP moyen sur les 1 res 26 semaines Tous (n = 1 142) 20 Différence moyenne ajustée 105 m. L p < 0, 001 Différence moyenne ajustée 14, 6 L/min p < 0, 001 Différence moyenne ajustée 7, 8 L/min p = 0, 001 20 10 Variation depuis l’inclusion du DEP moyen (L/min) (BDP/FF/GB vs BDP/FF) Variation depuis l’inclusion du VEMS (BDP/FF/GB vs BDP/FF) Pré-dose VEMS à S 26 0 ➜ Chez des asthmatiques non contrôlés sous dose élevée de CSI/LABA, un traitement d’entretien par triple association à dose fixe en particules extrafines (BDP/FF/GB 200/6/12, 5 μg) améliore la fonction pulmonaire Un effet bronchodilatateur plus prononcé a été observé chez les patients ayant une atteinte persistante de la fonction pulmonaire La Lettre du Pneumologue ATS 2020 - D’après Singh D et al. , abstr. A 3005, actualisé

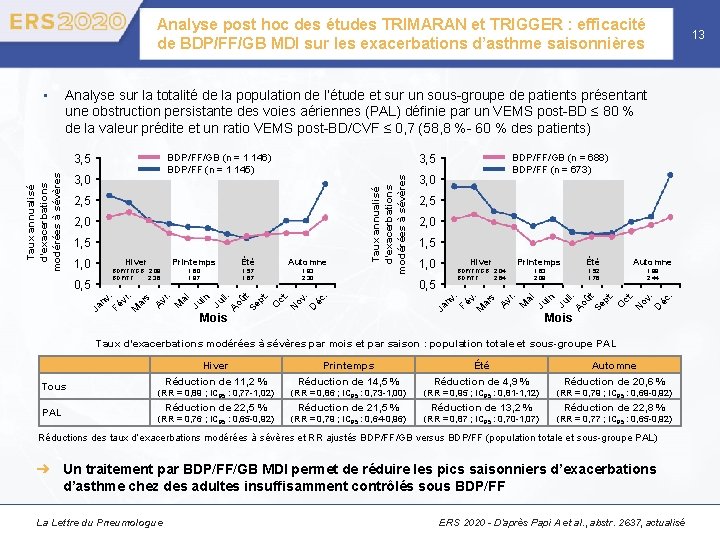
Analyse post hoc des études TRIMARAN et TRIGGER : efficacité de BDP/FF/GB MDI sur les exacerbations d’asthme saisonnières Analyse sur la totalité de la population de l’étude et sur un sous-groupe de patients présentant une obstruction persistante des voies aériennes (PAL) définie par un VEMS post-BD ≤ 80 % de la valeur prédite et un ratio VEMS post-BD/CVF ≤ 0, 7 (58, 8 %- 60 % des patients) 3, 5 2, 0 1, 5 Printemps Été Automne 1, 60 1, 87 1, 57 1, 67 1, 83 2, 30 Ja 1, 5 1, 0 0, 5 nv. Fé vr M. ar s Av r. M ai Ju in Ju il. Ao ût Se pt. O ct. N ov. D éc. 0, 5 Hiver BDP/FF/GB : 2, 09 BDP/FF : 2, 36 2, 0 Mois Hiver Printemps Été Automne BDP/FF/GB : 2, 04 BDP/FF : 2, 64 1, 63 2, 08 1, 52 1, 76 1, 88 2, 44 . 1, 0 2, 5 v M. ar s Av r. M ai Ju in Ju il. Ao ût Se pt. O ct. N ov. D éc. 2, 5 3, 0 nv 3, 0 BDP/FF/GB (n = 688) BDP/FF (n = 673) Fé BDP/FF/GB (n = 1 146) BDP/FF (n = 1 145) Ja Taux annualisé d’exacerbations modérées à sévères 3, 5 Taux annualisé d’exacerbations modérées à sévères • 13 Mois Taux d’exacerbations modérées à sévères par mois et par saison : population totale et sous-groupe PAL Hiver Tous PAL Printemps Été Automne Réduction de 11, 2 % Réduction de 14, 5 % Réduction de 4, 9 % Réduction de 20, 6 % (RR = 0, 89 ; IC 95 : 0, 77 -1, 02) (RR = 0, 86 ; IC 95 : 0, 73 -1, 00) (RR = 0, 95 ; IC 95 : 0, 81 -1, 12) (RR = 0, 79 ; IC 95 : 0, 69 -0, 92) Réduction de 22, 5 % Réduction de 21, 5 % Réduction de 13, 2 % Réduction de 22, 8 % (RR = 0, 76 ; IC 95 : 0, 65 -0, 92) (RR = 0, 79 ; IC 95 : 0, 64 -0, 96) (RR = 0, 87 ; IC 95 : 0, 70 -1, 07) (RR = 0, 77 ; IC 95 : 0, 65 -0, 92) Réductions des taux d’exacerbations modérées à sévères et RR ajustés BDP/FF/GB versus BDP/FF (population totale et sous-groupe PAL) ➜ Un traitement par BDP/FF/GB MDI permet de réduire les pics saisonniers d’exacerbations d’asthme chez des adultes insuffisamment contrôlés sous BDP/FF La Lettre du Pneumologue ERS 2020 - D’après Papi A et al. , abstr. 2637, actualisé

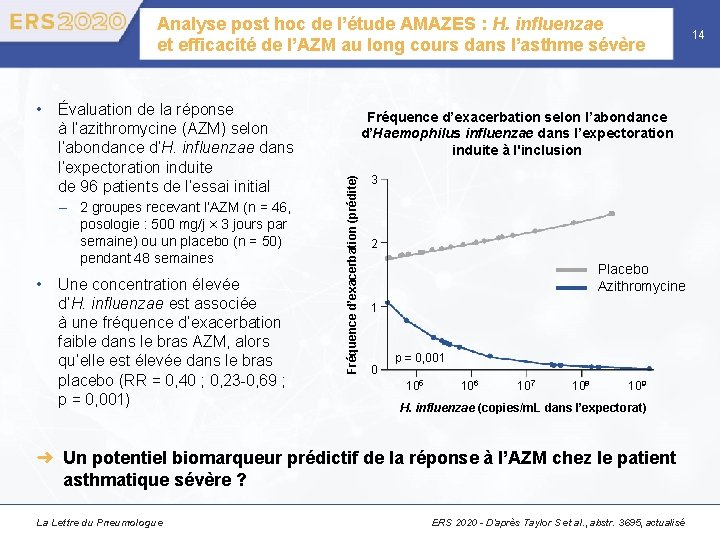
Analyse post hoc de l’étude AMAZES : H. influenzae et efficacité de l’AZM au long cours dans l’asthme sévère – 2 groupes recevant l’AZM (n = 46, posologie : 500 mg/j × 3 jours par semaine) ou un placebo (n = 50) pendant 48 semaines • Une concentration élevée d’H. influenzae est associée à une fréquence d’exacerbation faible dans le bras AZM, alors qu’elle est élevée dans le bras placebo (RR = 0, 40 ; 0, 23 -0, 69 ; p = 0, 001) Fréquence d’exacerbation selon l’abondance d’Haemophilus influenzae dans l’expectoration induite à l'inclusion Fréquence d’exacerbation (prédite) • Évaluation de la réponse à l’azithromycine (AZM) selon l’abondance d’H. influenzae dans l’expectoration induite de 96 patients de l’essai initial 3 2 Placebo Azithromycine 1 0 p = 0, 001 105 106 107 108 109 H. influenzae (copies/m. L dans l’expectorat) ➜ Un potentiel biomarqueur prédictif de la réponse à l’AZM chez le patient asthmatique sévère ? La Lettre du Pneumologue ERS 2020 - D’après Taylor S et al. , abstr. 3695, actualisé 14

Manifestations résiduelles après 2 ans d’anti-IL-5 pour asthme sévère : une étude en “vie réelle” (1) 15 • Étude de cohorte multicentrique réalisée aux Pays-Bas : objectifs – Évaluer la fréquence et les raisons du switch entre anti-IL-5 – Évaluer l’importance des manifestations résiduelles après 2 ans de traitement par anti-IL-5 Caractéristiques démographiques des patients inclus (n = 114) ge (années) 55 (46 -64) Durée de l’asthme* (années) 15 (5 -30) Hommes (%) IMC (kg/m 2) Anciens fumeurs (%) * Médiane (IQR) 54 27 (25 -31) 43 Fréquence et raisons du switch entre anti-IL-5 (n = 114) Pas de switch 59 % 1 x switch 34 % 2 x 7% Persistance des symptômes ou des exacerbations 53 % Sevrage incomplet de CSO 28 % Limitation de la persistance du débit des voies aériennes 17 % Effets indésirables 5% Autres raisons 2% ➜ Une réponse incomplète au traitement est la principale raison du switch ➜ Seuls 14 % des patients (16/114) ont présenté une réponse complète au traitement (“super-répondeurs”) La Lettre du Pneumologue ERS 2020 - D’après Eger K et al. , abstr. 5041, actualisé

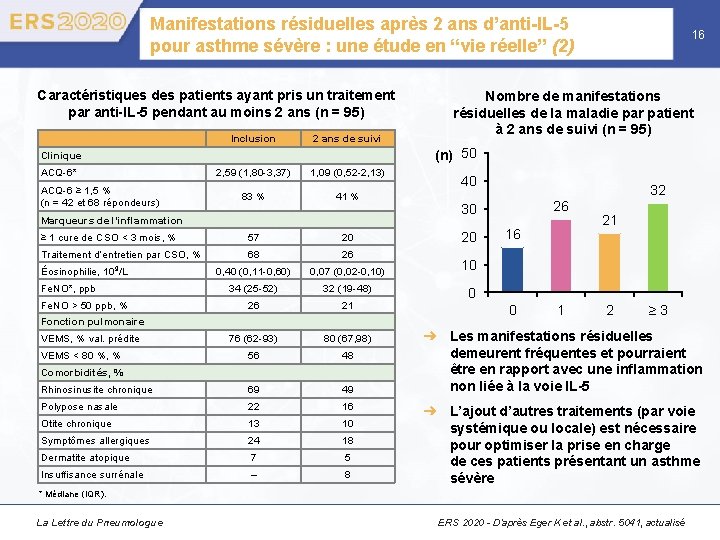
Manifestations résiduelles après 2 ans d’anti-IL-5 pour asthme sévère : une étude en “vie réelle” (2) Caractéristiques des patients ayant pris un traitement par anti-IL-5 pendant au moins 2 ans (n = 95) Inclusion 2 ans de suivi Nombre de manifestations résiduelles de la maladie par patient à 2 ans de suivi (n = 95) (n) 50 Clinique ACQ-6* ACQ-6 ≥ 1, 5 % (n = 42 et 68 répondeurs) 2, 59 (1, 80 -3, 37) 1, 09 (0, 52 -2, 13) 83 % 41 % Marqueurs de l’inflammation ≥ 1 cure de CSO < 3 mois, % 57 20 Traitement d’entretien par CSO, % 68 26 0, 40 (0, 11 -0, 60) 0, 07 (0, 02 -0, 10) 34 (25 -52) 32 (19 -48) 26 21 76 (62 -93) 80 (67, 98) 56 48 Rhinosinusite chronique 69 49 Polypose nasale 22 16 Otite chronique 13 10 Symptômes allergiques 24 18 Dermatite atopique 7 5 Insuffisance surrénale – 8 Éosinophilie, 16 10 9/L Fe. NO*, ppb Fe. NO > 50 ppb, % Fonction pulmonaire VEMS, % val. prédite VEMS < 80 %, % Comorbidités, % 40 32 26 30 20 16 21 10 0 0 1 2 ≥ 3 ➜ Les manifestations résiduelles demeurent fréquentes et pourraient être en rapport avec une inflammation non liée à la voie IL-5 ➜ L’ajout d’autres traitements (par voie systémique ou locale) est nécessaire pour optimiser la prise en charge de ces patients présentant un asthme sévère * Médiane (IQR). La Lettre du Pneumologue ERS 2020 - D’après Eger K et al. , abstr. 5041, actualisé

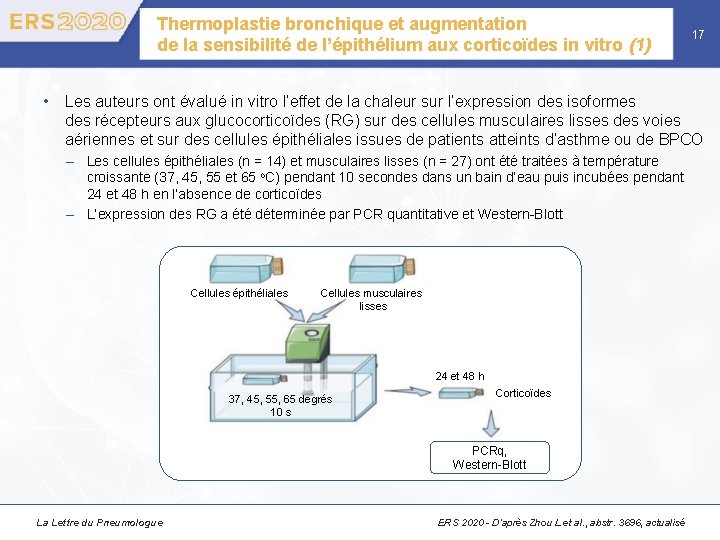
Thermoplastie bronchique et augmentation de la sensibilité de l’épithélium aux corticoïdes in vitro (1) 17 • Les auteurs ont évalué in vitro l’effet de la chaleur sur l’expression des isoformes des récepteurs aux glucocorticoïdes (RG) sur des cellules musculaires lisses des voies aériennes et sur des cellules épithéliales issues de patients atteints d’asthme ou de BPCO – Les cellules épithéliales (n = 14) et musculaires lisses (n = 27) ont été traitées à température croissante (37, 45, 55 et 65 o. C) pendant 10 secondes dans un bain d’eau puis incubées pendant 24 et 48 h en l’absence de corticoïdes – L’expression des RG a été déterminée par PCR quantitative et Western-Blott Cellules épithéliales Cellules musculaires lisses 24 et 48 h 37, 45, 55, 65 degrés 10 s Corticoïdes PCRq, Western-Blott La Lettre du Pneumologue ERS 2020 - D’après Zhou L et al. , abstr. 3696, actualisé

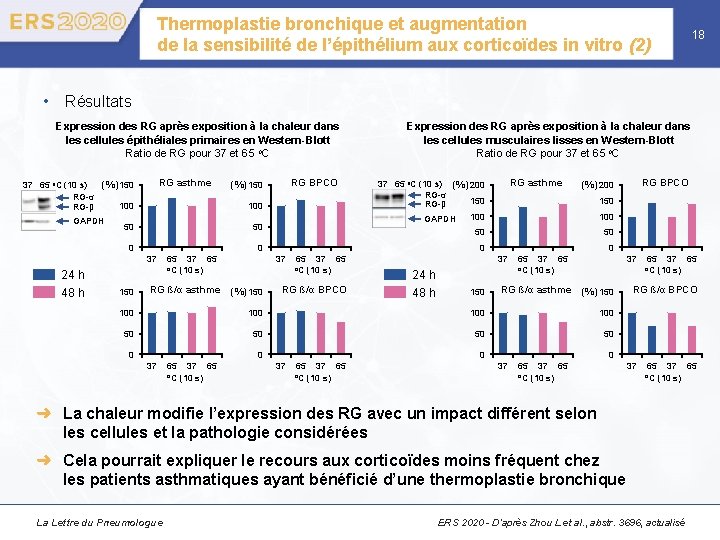
Thermoplastie bronchique et augmentation de la sensibilité de l’épithélium aux corticoïdes in vitro (2) 18 • Résultats Expression des RG après exposition à la chaleur dans les cellules épithéliales primaires en Western-Blott Ratio de RG pour 37 et 65 o. C RG asthme (%) 150 37 65 o. C (10 s) RG-α 100 RG-β GAPDH 100 50 50 0 24 h 150 65 37 65 o. C (10 s) RG ß/α asthme 150 100 50 0 65 37 65 o. C (10 s) RG ß/α BPCO 0 37 24 h 48 h 150 65 37 65 o. C (10 s) RG ß/α asthme 37 (%) 150 100 100 50 50 0 37 65 o. C (10 s) 65 o. C 100 0 RG BPCO (%) 200 50 37 (%) 150 RG asthme 37 65 o. C (10 s) (%) 200 RG-α 150 RG-β 100 GAPDH 0 37 48 h RG BPCO (%) 150 Expression des RG après exposition à la chaleur dans les cellules musculaires lisses en Western-Blott Ratio de RG pour 37 et 65 o. C 37 65 (10 s) RG ß/α BPCO 0 37 65 o. C (10 s) 37 65 o. C 37 65 (10 s) ➜ La chaleur modifie l’expression des RG avec un impact différent selon les cellules et la pathologie considérées ➜ Cela pourrait expliquer le recours aux corticoïdes moins fréquent chez les patients asthmatiques ayant bénéficié d’une thermoplastie bronchique La Lettre du Pneumologue ERS 2020 - D’après Zhou L et al. , abstr. 3696, actualisé

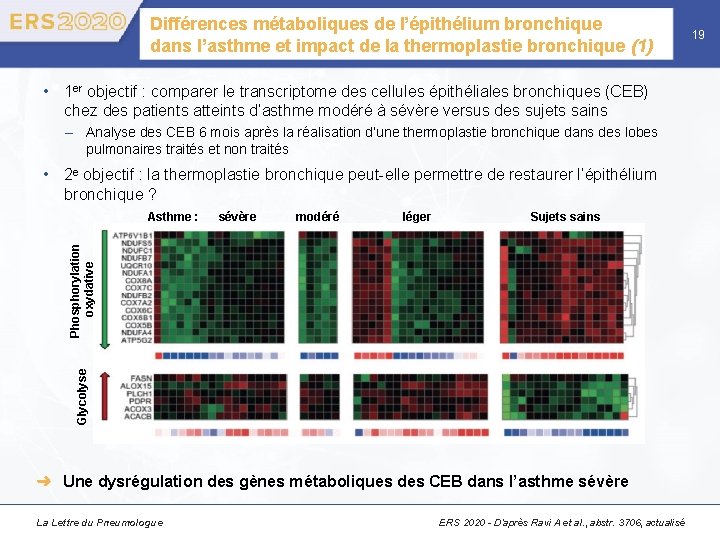
Différences métaboliques de l’épithélium bronchique dans l’asthme et impact de la thermoplastie bronchique (1) • 1 er objectif : comparer le transcriptome des cellules épithéliales bronchiques (CEB) chez des patients atteints d’asthme modéré à sévère versus des sujets sains – Analyse des CEB 6 mois après la réalisation d’une thermoplastie bronchique dans des lobes pulmonaires traités et non traités • 2 e objectif : la thermoplastie bronchique peut-elle permettre de restaurer l’épithélium bronchique ? sévère modéré léger Sujets sains Glycolyse Phosphorylation oxydative Asthme : ➜ Une dysrégulation des gènes métaboliques des CEB dans l’asthme sévère La Lettre du Pneumologue ERS 2020 - D’après Ravi A et al. , abstr. 3706, actualisé 19

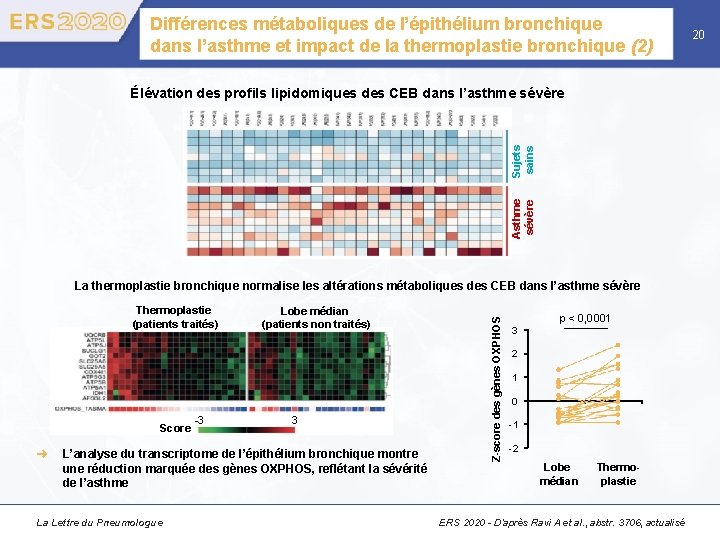
Différences métaboliques de l’épithélium bronchique dans l’asthme et impact de la thermoplastie bronchique (2) Asthme sévère Sujets sains Élévation des profils lipidomiques des CEB dans l’asthme sévère Thermoplastie (patients traités) Score ➜ -3 Lobe médian (patients non traités) 3 L’analyse du transcriptome de l’épithélium bronchique montre une réduction marquée des gènes OXPHOS, reflétant la sévérité de l’asthme La Lettre du Pneumologue Z-score des gènes OXPHOS La thermoplastie bronchique normalise les altérations métaboliques des CEB dans l’asthme sévère 3 p < 0, 0001 2 1 0 -1 -2 Lobe médian Thermoplastie ERS 2020 - D’après Ravi A et al. , abstr. 3706, actualisé 20

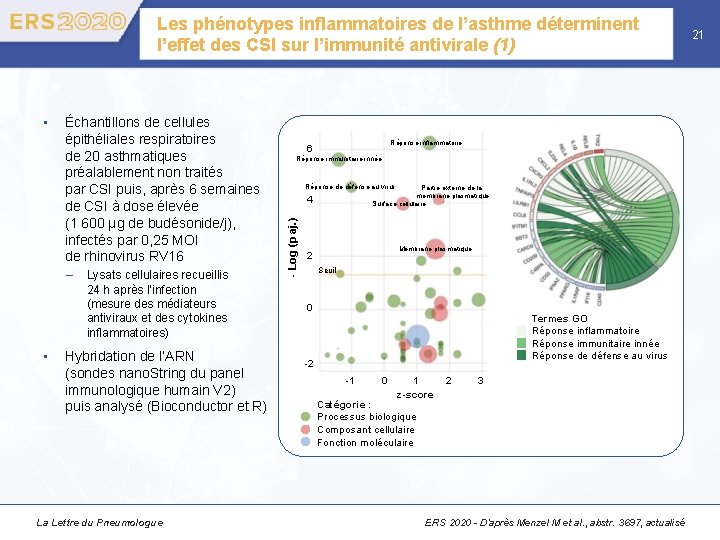
Les phénotypes inflammatoires de l’asthme déterminent l’effet des CSI sur l’immunité antivirale (1) Échantillons de cellules épithéliales respiratoires de 20 asthmatiques préalablement non traités par CSI puis, après 6 semaines de CSI à dose élevée (1 600 μg de budésonide/j), infectés par 0, 25 MOI de rhinovirus RV 16 – • Lysats cellulaires recueillis 24 h après l’infection (mesure des médiateurs antiviraux et des cytokines inflammatoires) Hybridation de l’ARN (sondes nano. String du panel immunologique humain V 2) puis analysé (Bioconductor et R) La Lettre du Pneumologue Réponse inflammatoire 6 Réponse immunitaire innée Réponse de défense au virus Partie externe de la membrane plasmatique Surface cellulaire 4 - Log (p aj. ) • Membrane plasmatique 2 Seuil 0 Termes GO Réponse inflammatoire Réponse immunitaire innée Réponse de défense au virus -2 -1 0 1 z-score 2 3 Catégorie : Processus biologique Composant cellulaire Fonction moléculaire ERS 2020 - D’après Menzel M et al. , abstr. 3697, actualisé 21

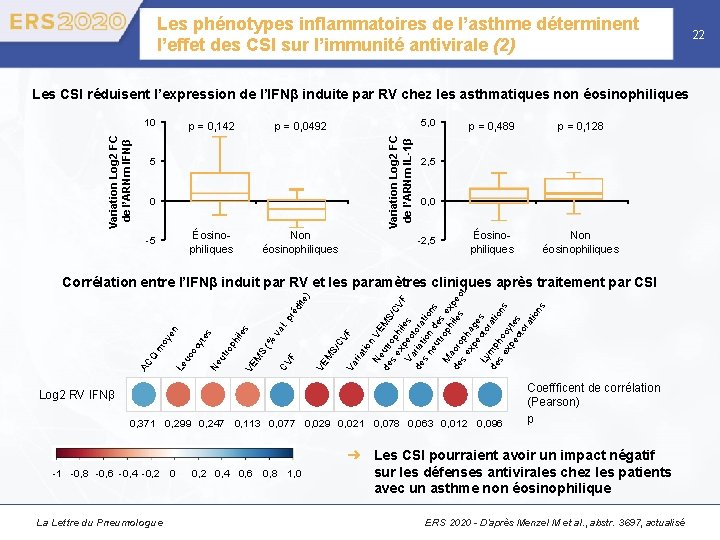
Les phénotypes inflammatoires de l’asthme déterminent l’effet des CSI sur l’immunité antivirale (2) Les CSI réduisent l’expression de l’IFNβ induite par RV chez les asthmatiques non éosinophiliques p = 0, 142 5, 0 p = 0, 0492 Variation Log 2 FC de l’ARNm IL-1β Variation Log 2 FC de l’ARNm IFNβ 10 5 0 Éosinophiliques -5 Non éosinophiliques p = 0, 489 p = 0, 128 Éosinophiliques Non éosinophiliques 2, 5 0, 0 -2, 5 F ria t CV Va VE F CV M S/ (% S M ion VE Ne M de utr s e op S/C h VF x il Va pec es t de riat ora s n ion tio eu de ns tro s M ph ex a ile pe c de ro s ct. s e ph xp ag ec es Ly to ra m de p tio h se o ns c xp yt ec es to ra tio ns l. p va es hil VE ro p ut Ne Le AC Q uc oc m oy yte s en ré dit e) Corrélation entre l’IFNβ induit par RV et les paramètres cliniques après traitement par CSI Log 2 RV IFNβ 0, 371 0, 299 0, 247 0, 113 0, 077 0, 029 0, 021 0, 078 0, 063 0, 012 0, 096 -1 -0, 8 -0, 6 -0, 4 -0, 2 0 La Lettre du Pneumologue 0, 2 0, 4 0, 6 0, 8 1, 0 Coeffficent de corrélation (Pearson) p ➜ Les CSI pourraient avoir un impact négatif sur les défenses antivirales chez les patients avec un asthme non éosinophilique ERS 2020 - D’après Menzel M et al. , abstr. 3697, actualisé 22

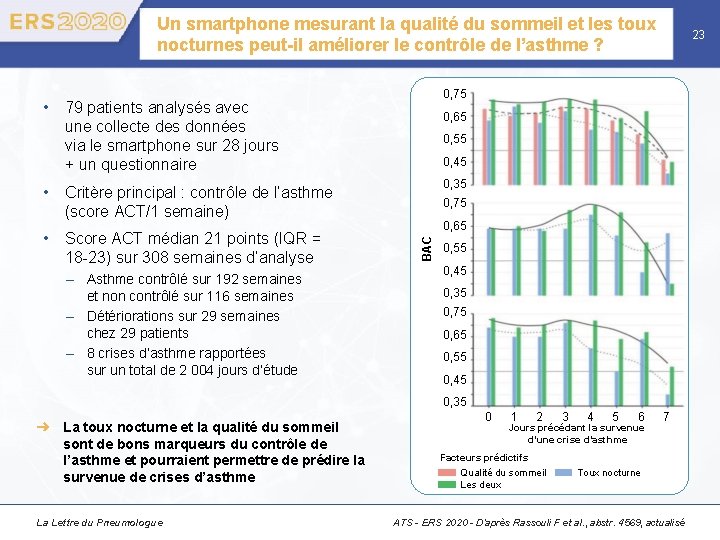
Un smartphone mesurant la qualité du sommeil et les toux nocturnes peut-il améliorer le contrôle de l’asthme ? 0, 75 • 79 patients analysés avec une collecte des données via le smartphone sur 28 jours + un questionnaire 0, 65 0, 55 0, 45 0, 35 • Critère principal : contrôle de l’asthme (score ACT/1 semaine) – Asthme contrôlé sur 192 semaines et non contrôlé sur 116 semaines – Détériorations sur 29 semaines chez 29 patients – 8 crises d’asthme rapportées sur un total de 2 004 jours d’étude 0, 75 0, 65 BAC • Score ACT médian 21 points (IQR = 18 -23) sur 308 semaines d’analyse 23 0, 55 0, 45 0, 35 0, 75 0, 65 0, 55 0, 45 0, 35 ➜ La toux nocturne et la qualité du sommeil sont de bons marqueurs du contrôle de l’asthme et pourraient permettre de prédire la survenue de crises d’asthme La Lettre du Pneumologue 0 1 2 3 4 5 6 Jours précédant la survenue d’une crise d’asthme Facteurs prédictifs Qualité du sommeil Les deux 7 Toux nocturne ATS - ERS 2020 - D’après Rassouli F et al. , abstr. 4569, actualisé

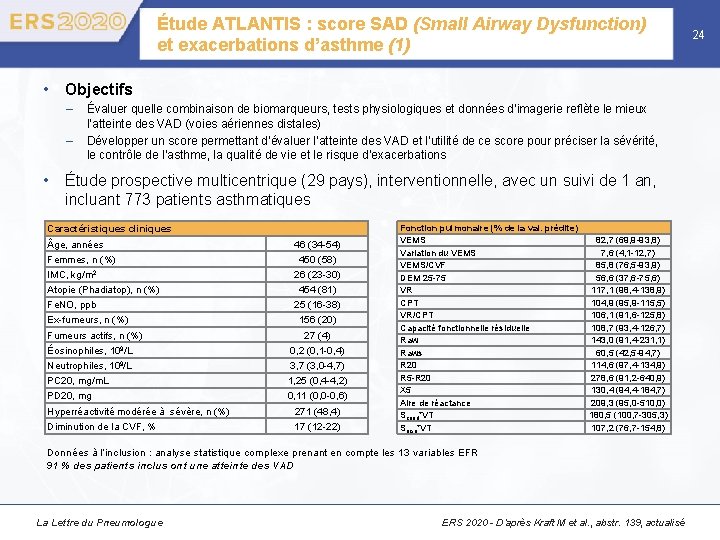
Étude ATLANTIS : score SAD (Small Airway Dysfunction) et exacerbations d’asthme (1) • Objectifs – – Évaluer quelle combinaison de biomarqueurs, tests physiologiques et données d’imagerie reflète le mieux l’atteinte des VAD (voies aériennes distales) Développer un score permettant d’évaluer l’atteinte des VAD et l’utilité de ce score pour préciser la sévérité, le contrôle de l’asthme, la qualité de vie et le risque d’exacerbations • Étude prospective multicentrique (29 pays), interventionnelle, avec un suivi de 1 an, incluant 773 patients asthmatiques Caractéristiques cliniques ge, années 46 (34 -54) Femmes, n (%) 450 (58) kg/m 2 26 (23 -30) IMC, Atopie (Phadiatop), n (%) Fe. NO, ppb 454 (81) 25 (16 -38) Ex-fumeurs, n (%) Fumeurs actifs, n (%) 156 (20) 27 (4) Éosinophiles, 109/L 0, 2 (0, 1 -0, 4) Neutrophiles, 109/L 3, 7 (3, 0 -4, 7) PC 20, mg/m. L 1, 25 (0, 4 -4, 2) PD 20, mg 0, 11 (0, 0 -0, 6) Hyperréactivité modérée à sévère, n (%) 271 (48, 4) Diminution de la CVF, % 17 (12 -22) Fonction pulmonaire (% de la val. prédite) VEMS Variation du VEMS/CVF DEM 25 -75 VR CPT VR/CPT Capacité fonctionnelle résiduelle Raws R 20 R 5 -R 20 X 5 Aire de réactance Scond*VT Sacin*VT 82, 7 (69, 9 -93, 8) 7, 6 (4, 1 -12, 7) 85, 8 (76, 5 -93, 9) 56, 6 (37, 6 -75, 6) 117, 1 (98, 4 -138, 9) 104, 9 (95, 9 -115, 5) 106, 1 (91, 6 -125, 8) 108, 7 (93, 4 -126, 7) 143, 0 (91, 4 -231, 1) 60, 5 (42, 5 -94, 7) 114, 6 (97, 4 -134, 9) 278, 6 (91, 2 -640, 9) 130, 4 (94, 4 -184, 7) 209, 3 (95, 0 -510, 0) 180, 5 (100, 7 -305, 3) 107, 2 (76, 7 -154, 8) Données à l’inclusion : analyse statistique complexe prenant en compte les 13 variables EFR 91 % des patients inclus ont une atteinte des VAD La Lettre du Pneumologue ERS 2020 - D’après Kraft M et al. , abstr. 139, actualisé 24

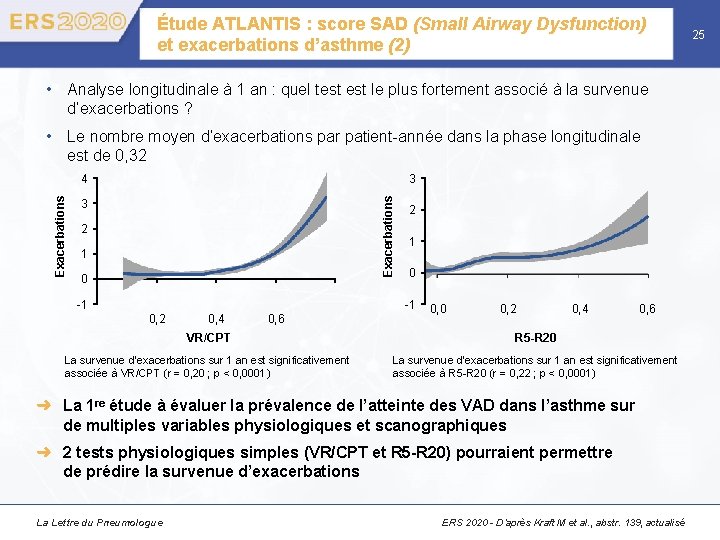
Étude ATLANTIS : score SAD (Small Airway Dysfunction) et exacerbations d’asthme (2) • Analyse longitudinale à 1 an : quel test le plus fortement associé à la survenue d’exacerbations ? • Le nombre moyen d’exacerbations par patient-année dans la phase longitudinale est de 0, 32 3 Exacerbations 4 3 2 1 0 -1 0, 2 0, 4 0, 6 0, 0 0, 2 0, 4 0, 6 VR/CPT R 5 -R 20 La survenue d’exacerbations sur 1 an est significativement associée à VR/CPT (r = 0, 20 ; p < 0, 0001) La survenue d’exacerbations sur 1 an est significativement associée à R 5 -R 20 (r = 0, 22 ; p < 0, 0001) ➜ La 1 re étude à évaluer la prévalence de l’atteinte des VAD dans l’asthme sur de multiples variables physiologiques et scanographiques ➜ 2 tests physiologiques simples (VR/CPT et R 5 -R 20) pourraient permettre de prédire la survenue d’exacerbations La Lettre du Pneumologue ERS 2020 - D’après Kraft M et al. , abstr. 139, actualisé 25