La Lettre du Cancrologue La Lettre du Pneumologue























- Slides: 49

La Lettre du Cancérologue La Lettre du Pneumologue

La Lettre du Cancérologue La Lettre du Pneumologue

La Lettre du Cancérologue La Lettre du Pneumologue CBNCP métastasique - D’après Xxxxx et al. , abstr. Xxx, actualisé

Liens d’intérêt Nicolas Girard • Liens personnels : Astra-Zeneca, Boehringer-Ingelheim, Bristol Myers Squibb, Hoffmann La Roche, Lilly, Merck Sharp Dohme, Novartis, Pfizer, Takeda • Liens institutionnels : Astra-Zeneca, Boehringer-Ingelheim, Bristol Myers Squibb, Hoffmann La Roche, Lilly, Merck Sharp Dohme, Novartis, Pfizer, Takeda Didier Debieuvre • Liens personnels : Astra. Zeneca, Chugaï, Lilly, Hoffmann La Roche, Novartis, Pfizer, Merck-Sharp Dohme, Bristol-Myers Squibb, Mundipharma, Pierre Fabre • Liens institutionnels : Astra. Zeneca, Hoffmann La Roche, Lilly, Bristol-Myers Squibb, Boehringer-Ingelheim, Chiesi, Chugaï, Janssen, Pfizer, Merck-Sharp Dohme, Novartis, Glaxo Smith Kline, Sandoz La Lettre du Cancérologue La Lettre du Pneumologue

Quelles méthodologies pour les études de vraie vie? La Lettre du Cancérologue La Lettre du Pneumologue

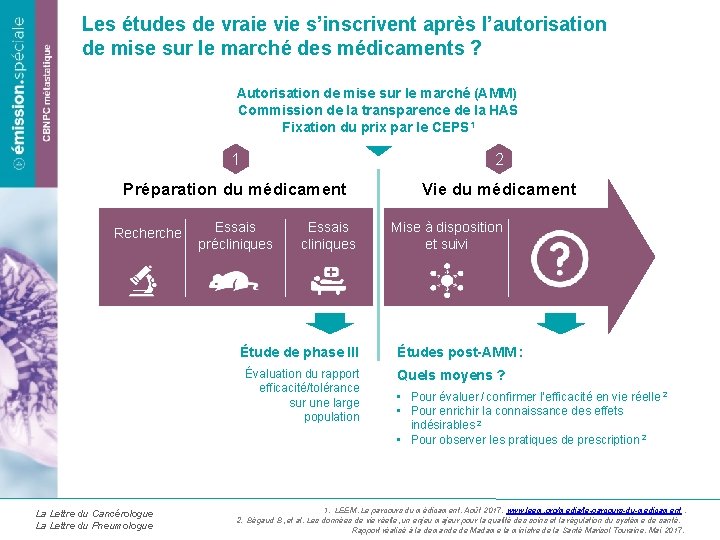
Les études de vraie vie s’inscrivent après l’autorisation de mise sur le marché des médicaments ? Autorisation de mise sur le marché (AMM) Commission de la transparence de la HAS Fixation du prix par le CEPS 1 1 2 Préparation du médicament Vie du médicament Recherche Essais précliniques Essais cliniques Étude de phase III Évaluation du rapport efficacité/tolérance sur une large population La Lettre du Cancérologue La Lettre du Pneumologue Mise à disposition et suivi Études post-AMM : Quels moyens ? • Pour évaluer / confirmer l’efficacité en vie réelle 2 • Pour enrichir la connaissance des effets indésirables 2 • Pour observer les pratiques de prescription 2 1. LEEM. Le parcours du médicament. Août 2017. www. leem. org/media/le-parcours-du-medicament. 2. Bégaud B, et al. Les données de vie réelle, un enjeu majeur pour la qualité des soins et la régulation du système de santé. Rapport réalisé à la demande de Madame la ministre de la Santé Marisol Touraine. Mai 2017.

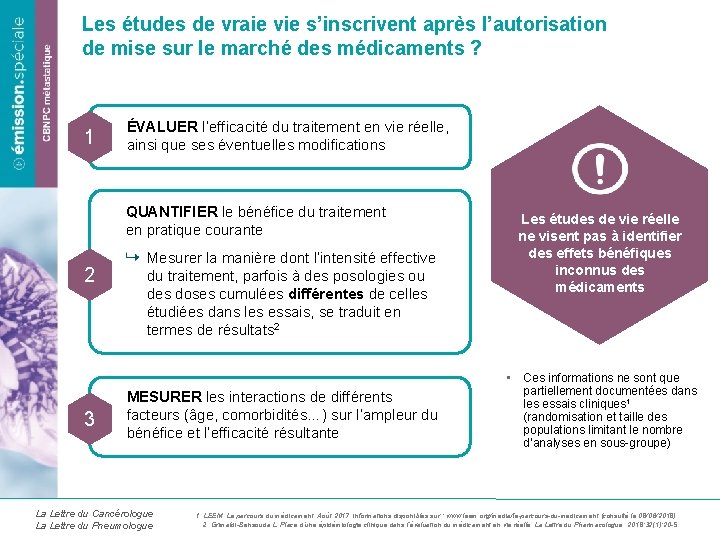
Les études de vraie vie s’inscrivent après l’autorisation de mise sur le marché des médicaments ? 1 ÉVALUER l’efficacité du traitement en vie réelle, ainsi que ses éventuelles modifications QUANTIFIER le bénéfice du traitement en pratique courante 2 3 Mesurer la manière dont l’intensité effective du traitement, parfois à des posologies ou des doses cumulées différentes de celles étudiées dans les essais, se traduit en termes de résultats 2 MESURER les interactions de différents facteurs (âge, comorbidités…) sur l’ampleur du bénéfice et l’efficacité résultante La Lettre du Cancérologue La Lettre du Pneumologue Les études de vie réelle ne visent pas à identifier des effets bénéfiques inconnus des médicaments • Ces informations ne sont que partiellement documentées dans les essais cliniques 1 (randomisation et taille des populations limitant le nombre d’analyses en sous-groupe) 1. LEEM. Le parcours du médicament. Août 2017. Informations disponibles sur : www. leem. org/media/le-parcours-du-medicament (consulté le 08/06/2018). 2. Grimaldi-Bensouda L. Place d’une épidémiologie clinique dans l’évaluation du médicament en vie réelle. La Lettre du Pharmacologue. 2018; 32(1): 20 -5.

Études en vie réelle : quelle valeur pour les autorités de santé ? (1/2) Les données de vraie vie peuvent permettre d’éclairer les décisions des régulateurs et leurs actions menées pour améliorer la qualité et l’efficience des soins 1 • Observation des effets indésirables en vie réelle 1 Surveillance de la sécurité des produits mis sur le marché • Confirmation des données de tolérance recueillies dans les essais cliniques • Détection des risques non mis en évidence • Vérification de la pertinence des prescriptions et de leur conformité aux recommandations 2 Surveillance de l’usage 3 Évaluation de l’efficacité et en vie réelle La Lettre du Cancérologue La Lettre du Pneumologue • Détection des facteurs de risques liés aux modalités d’utilisation, mais aussi des innovations d’usage profitables (pratiques sur des indications non validées) et des gains d’efficience, de qualité et d’équité • Confirmation, ou non, des résultats des essais cliniques • Vérification de la transposabilité des conditions d’efficacité observées dans les essais dans la vie réelle 1. Bégaud B, et al. Les données de vie réelle, un enjeu majeur pour la qualité des soins et la régulation du système de santé. Rapport réalisé à la demande de Madame la Ministre de la Santé Marisol Touraine. Mai 2017.

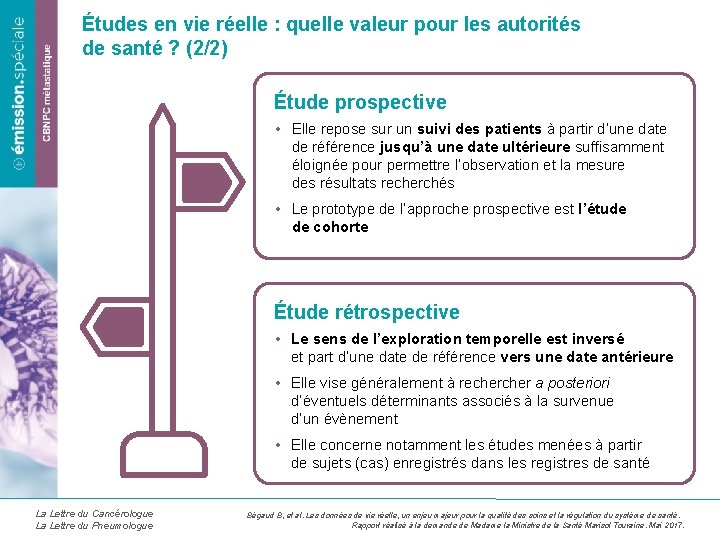
Études en vie réelle : quelle valeur pour les autorités de santé ? (2/2) Étude prospective • Elle repose sur un suivi des patients à partir d’une date de référence jusqu’à une date ultérieure suffisamment éloignée pour permettre l’observation et la mesure des résultats recherchés • Le prototype de l’approche prospective est l’étude de cohorte Étude rétrospective • Le sens de l’exploration temporelle est inversé et part d’une date de référence vers une date antérieure • Elle vise généralement à recher a posteriori d’éventuels déterminants associés à la survenue d’un évènement • Elle concerne notamment les études menées à partir de sujets (cas) enregistrés dans les registres de santé La Lettre du Cancérologue La Lettre du Pneumologue Bégaud B, et al. Les données de vie réelle, un enjeu majeur pour la qualité des soins et la régulation du système de santé. Rapport réalisé à la demande de Madame la Ministre de la Santé Marisol Touraine. Mai 2017.

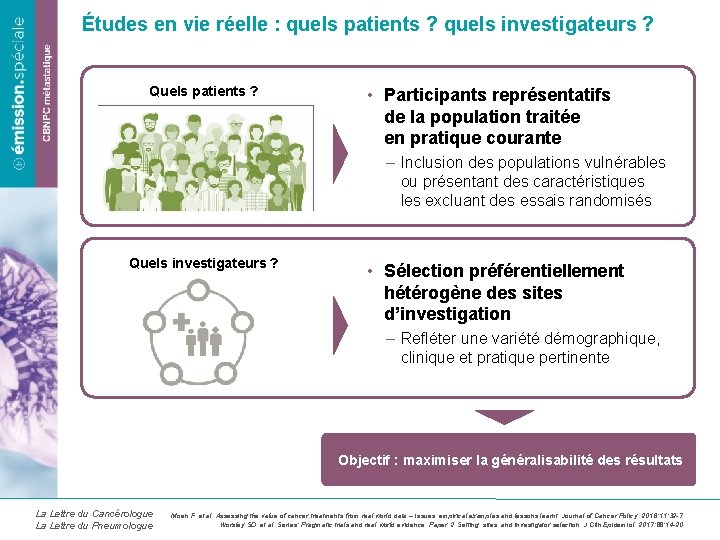
Études en vie réelle : quels patients ? quels investigateurs ? Quels patients ? • Participants représentatifs de la population traitée en pratique courante – Inclusion des populations vulnérables ou présentant des caractéristiques les excluant des essais randomisés Quels investigateurs ? • Sélection préférentiellement hétérogène des sites d’investigation – Refléter une variété démographique, clinique et pratique pertinente Objectif : maximiser la généralisabilité des résultats La Lettre du Cancérologue La Lettre du Pneumologue Moen F, et al. Assessing the value of cancer treatments from real world data – Issues, empirical examples and lessons learnt. Journal of Cancer Policy. 2016; 11: 32 -7. Worsley SD, et al. Series: Pragmatic trials and real world evidence. Paper 2. Setting, sites, and investigator selection. J Clin Epidemiol. 2017; 88: 14 -20.

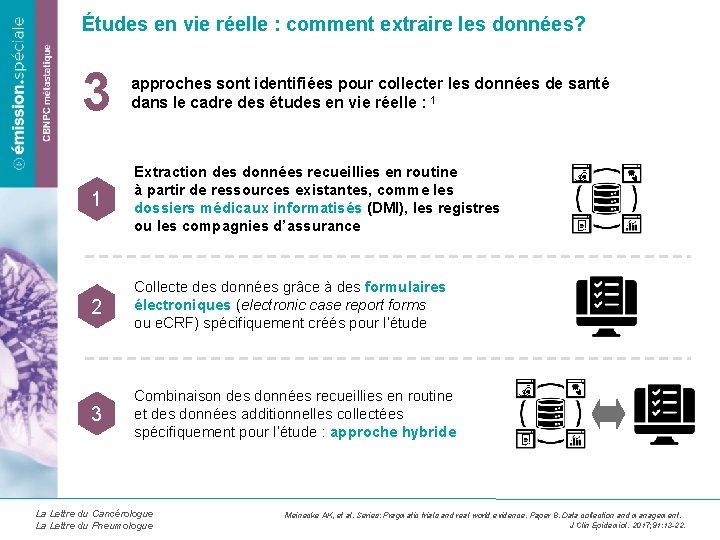
Études en vie réelle : comment extraire les données? 3 approches sont identifiées pour collecter les données de santé dans le cadre des études en vie réelle : 1 1 Extraction des données recueillies en routine à partir de ressources existantes, comme les dossiers médicaux informatisés (DMI), les registres ou les compagnies d’assurance 2 Collecte des données grâce à des formulaires électroniques (electronic case report forms ou e. CRF) spécifiquement créés pour l’étude 3 Combinaison des données recueillies en routine et des données additionnelles collectées spécifiquement pour l’étude : approche hybride La Lettre du Cancérologue La Lettre du Pneumologue Meinecke AK, et al. Series: Pragmatic trials and real world evidence. Paper 8. Data collection and management. J Clin Epidemiol. 2017; 91: 13 -22.

Études en vie réelle : quels biais possibles ? Un contrôle des sources de biais doit être réalisé afin d’assurer la validité interne des études en vie réelle Sources de biais Individu Technologie Système de prise en charge Découlent des… Dynamiques patients-soignants et caractéristiques du patient Dossiers médicaux informatisés Pratiques (DMI) ou electronic health professionnelles et records influences sur le système de santé Types de biais • Biais d’informations (enregistrement inexact des variables du patient) influençant l’exactitude de la collecte des données • Biais de confusion, liés aux caractéristiques et aux comorbidités du patient (influence des variables extrinsèques sur l’association entre le traitement et les résultats) • Biais de compliance, liés à une mauvaise adhérence du patient au traitement • Biais d’informations, liés à • Biais de sélection, des variations dans les liés à l’hétérogénéité interfaces des DMI, aux de l’accès aux soins, procédures d’entrée des influençant le cadre données ou aux méthodes d’échantillonnage de récupération des • Biais de confusion, données, compromettant la liés aux variations qualité des données régionales des • Biais de sélection standards de prise en (population non charge ou de représentative de la vraie disponibilité des distribution des patients dans traitements la population globale) découlant de l’utilisation des codes thérapeutiques et diagnostiques des DMI La Lettre du Cancérologue La Lettre du Pneumologue Khozin S, et al. Real-world Data for Clinical Evidence Generation in Oncology. J Natl Cancer Inst. 2017; 109(11): djx 187.

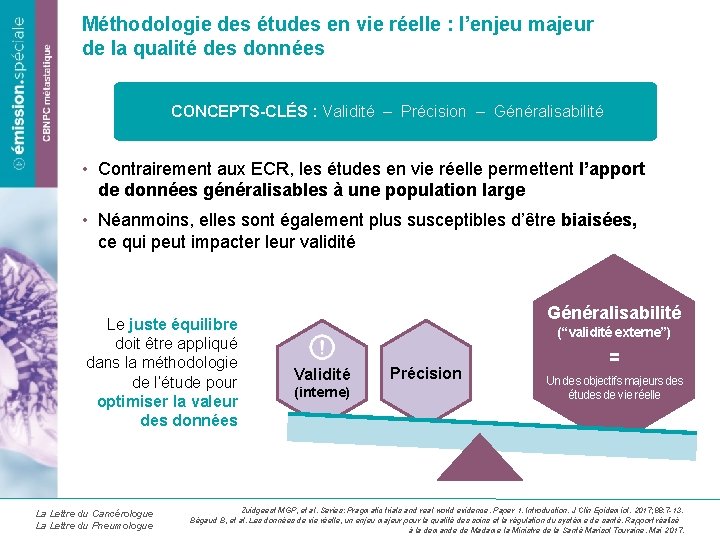
Méthodologie des études en vie réelle : l’enjeu majeur de la qualité des données CONCEPTS-CLÉS : Validité – Précision – Généralisabilité • Contrairement aux ECR, les études en vie réelle permettent l’apport de données généralisables à une population large • Néanmoins, elles sont également plus susceptibles d’être biaisées, ce qui peut impacter leur validité Le juste équilibre doit être appliqué dans la méthodologie de l’étude pour optimiser la valeur des données La Lettre du Cancérologue La Lettre du Pneumologue Généralisabilité (“validité externe”) Validité (interne) Précision = Un des objectifs majeurs des études de vie réelle Zuidgeest MGP, et al. Series: Pragmatic trials and real world evidence. Paper 1. Introduction. J Clin Epidemiol. 2017; 88: 7 -13. Bégaud B, et al. Les données de vie réelle, un enjeu majeur pour la qualité des soins et la régulation du système de santé. Rapport réalisé à la demande de Madame la Ministre de la Santé Marisol Touraine. Mai 2017.

Quelques exemples de données de vie réelle en oncologie thoracique • Sur un médicament spécifique • Sur une stratégie thérapeutique de prise en charge La Lettre du Cancérologue La Lettre du Pneumologue

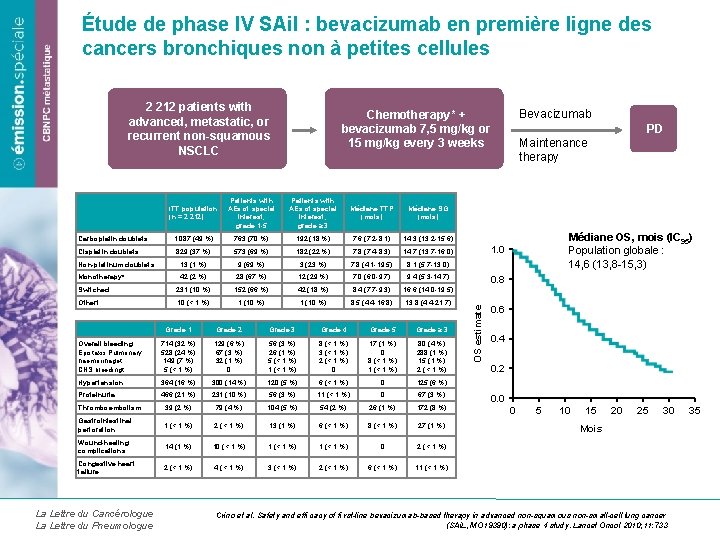
Étude de phase IV SAil : bevacizumab en première ligne des cancers bronchiques non à petites cellules 2 212 patients with advanced, metastatic, or recurrent non-squamous NSCLC Cisplatin doublets ITT population (n = 2 212) Patients with AEs of special interest, grade 1 -5 Patients with AEs of special interest, grade ≥ 3 Médiane TTP (mois) Médiane SG (mois) 1 087 (49 %) 763 (70 %) 192 (18 %) 7, 6 (7, 2 -8, 1) 14, 3 (13, 2 -15, 6) 829 (37 %) 573 (69 %) 182 (22 %) 7, 8 (7, 4 -8, 3) 14, 7 (13, 7 -16, 0) Non-platinum doublets 13 (1 %) 9 (69 %) 3 (23 %) 7, 8 (4, 1 -19, 5) 8, 1 (5, 7 -13, 0) Monotherapy* 42 (2 %) 28 (67 %) 12 (29 %) 7, 0 (6, 0 -9, 7) 9, 4 (5, 3 -14, 7) Switched 231 (10 %) 152 (66 %) 42 (18 %) 8, 4 (7, 7 -9, 3) 16, 6 (14, 0 -19, 5) Othert 10 (< 1 %) 1 (10 %) 8, 5 (4, 4 -16, 8) 13, 8 (4, 4 -21, 7) Grade 1 Grade 2 Grade 3 Grade 4 Grade 5 Grade ≥ 3 Overall bleeding Epistaxis Pulmonary haemorrhaget CNS bleedingt 714 (32 %) 528 (24 %) 149 (7 %) 5 (< 1 %) 129 (6 %) 67 (3 %) 32 (1 %) 0 56 (3 %) 26 (1 %) 5 (< 1 %) 1 (< 1 %) 8 (< 1 %) 3 (< 1 %) 2 (< 1 %) 0 17 (1 %) 0 8 (< 1 %) 1 (< 1 %) 80 (4 %) 288 (1 %) 15 (1 %) 2 (< 1 %) Hypertension 364 (16 %) 300 (14 %) 120 (5 %) 6 (< 1 %) 0 125 (6 %) Proteinuria 466 (21 %) 231 (10 %) 56 (3 %) 11 (< 1 %) 0 67 (3 %) Thromboembolism 39 (2 %) 79 (4 %) 104 (5 %) 54 (2 %) 26 (1 %) 172 (8 %) Gastrointestinal perforation 1 (< 1 %) 2 (< 1 %) 13 (1 %) 6 (< 1 %) 8 (< 1 %) 27 (1 %) Wound-healing complications 14 (1 %) 10 (< 1 %) 1 (< 1 %) 0 2 (< 1 %) Congestive heart failure 2 (< 1 %) 4 (< 1 %) 3 (< 1 %) 2 (< 1 %) 6 (< 1 %) 11 (< 1 %) La Lettre du Cancérologue La Lettre du Pneumologue PD Maintenance therapy Médiane OS, mois (IC 95) Population globale : 14, 6 (13, 8 -15, 3) 1. 0 0. 8 OS estimate Carboplatin doublets Bevacizumab Chemotherapy* + bevacizumab 7, 5 mg/kg or 15 mg/kg every 3 weeks 0. 6 0. 4 0. 2 0. 0 0 5 10 15 20 25 30 Mois Crino et al. Safety and effi cacy of fi rst-line bevacizumab-based therapy in advanced non-squamous non-small-cell lung cancer (SAi. L, MO 19390): a phase 4 study. Lancet Oncol 2010; 11: 733 35

Étude de phase IV EVIDENS : nivolumab en seconde ligne des cancers bronchiques non à petites cellules La Lettre du Cancérologue La Lettre du Pneumologue Dixmier et al. EVIDENS: An observational study of Nivolumab-treated patients in Advanced Non-Small Cell Lung Cancer (NSCLC) in a Real-world Setting: initial results on 1394 Patients (NCT 03382496, BMS sponsored). ESMO 2018, d’après 1469 P

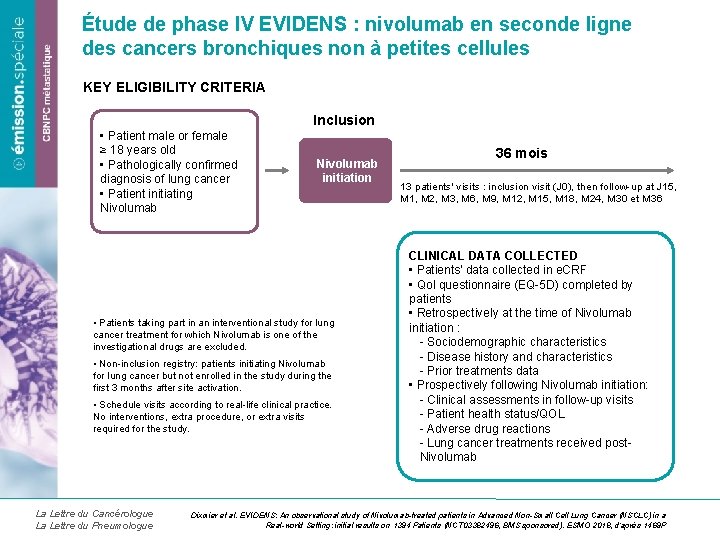
Étude de phase IV EVIDENS : nivolumab en seconde ligne des cancers bronchiques non à petites cellules KEY ELIGIBILITY CRITERIA Inclusion • Patient male or female ≥ 18 years old • Pathologically confirmed diagnosis of lung cancer • Patient initiating Nivolumab initiation • Patients taking part in an interventional study for lung cancer treatment for which Nivolumab is one of the investigational drugs are excluded. • Non-inclusion registry: patients initiating Nivolumab for lung cancer but not enrolled in the study during the first 3 months after site activation. • Schedule visits according to real-life clinical practice. No interventions, extra procedure, or extra visits required for the study. La Lettre du Cancérologue La Lettre du Pneumologue 36 mois 13 patients' visits : inclusion visit (J 0), then follow-up at J 15, M 1, M 2, M 3, M 6, M 9, M 12, M 15, M 18, M 24, M 30 et M 36 CLINICAL DATA COLLECTED • Patients' data collected in e. CRF • Qol questionnaire (EQ-5 D) completed by patients • Retrospectively at the time of Nivolumab initiation : - Sociodemographic characteristics - Disease history and characteristics - Prior treatments data • Prospectively following Nivolumab initiation: - Clinical assessments in follow-up visits - Patient health status/QOL - Adverse drug reactions - Lung cancer treatments received post. Nivolumab Dixmier et al. EVIDENS: An observational study of Nivolumab-treated patients in Advanced Non-Small Cell Lung Cancer (NSCLC) in a Real-world Setting: initial results on 1394 Patients (NCT 03382496, BMS sponsored). ESMO 2018, d’après 1469 P

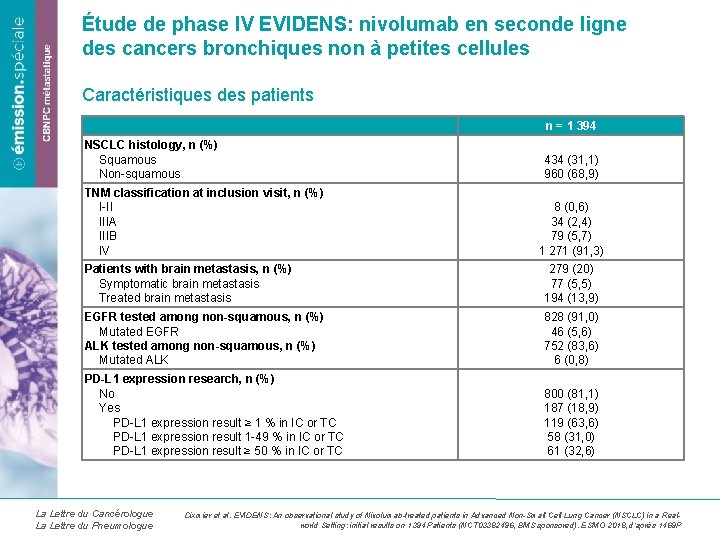
Étude de phase IV EVIDENS: nivolumab en seconde ligne des cancers bronchiques non à petites cellules Caractéristiques des patients n = 1 394 NSCLC histology, n (%) Squamous Non-squamous TNM classification at inclusion visit, n (%) I-II IIIA IIIB IV 434 (31, 1) 960 (68, 9) 8 (0, 6) 34 (2, 4) 79 (5, 7) 1 271 (91, 3) Patients with brain metastasis, n (%) Symptomatic brain metastasis Treated brain metastasis 279 (20) 77 (5, 5) 194 (13, 9) EGFR tested among non-squamous, n (%) Mutated EGFR ALK tested among non-squamous, n (%) Mutated ALK 828 (91, 0) 46 (5, 6) 752 (83, 6) 6 (0, 8) PD-L 1 expression research, n (%) No Yes PD-L 1 expression result ≥ 1 % in IC or TC PD-L 1 expression result 1 -49 % in IC or TC PD-L 1 expression result ≥ 50 % in IC or TC 800 (81, 1) 187 (18, 9) 119 (63, 6) 58 (31, 0) 61 (32, 6) La Lettre du Cancérologue La Lettre du Pneumologue Dixmier et al. EVIDENS: An observational study of Nivolumab-treated patients in Advanced Non-Small Cell Lung Cancer (NSCLC) in a Realworld Setting: initial results on 1394 Patients (NCT 03382496, BMS sponsored). ESMO 2018, d’après 1469 P

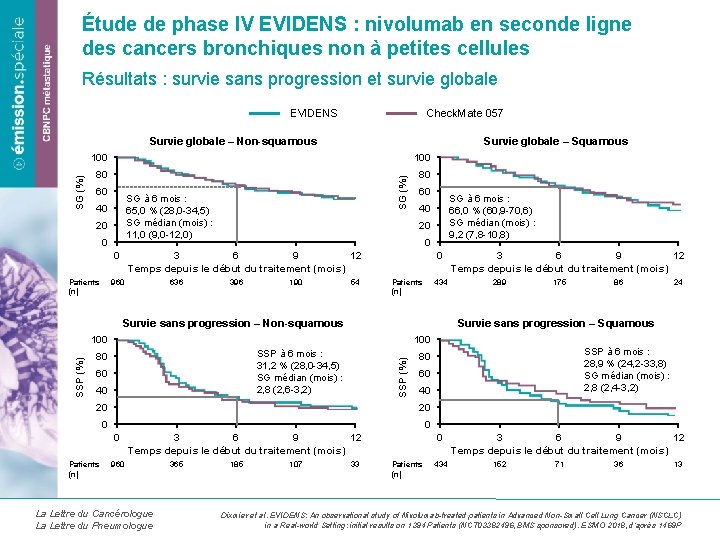
Étude de phase IV EVIDENS : nivolumab en seconde ligne des cancers bronchiques non à petites cellules Résultats : survie sans progression et survie globale EVIDENS Check. Mate 057 Survie globale – Squamous 100 80 80 60 SG à 6 mois : 65, 0 % (28, 0 -34, 5) SG médian (mois) : 11, 0 (9, 0 -12, 0) 40 20 0 0 Patients (n) SG (%) Survie globale – Non-squamous 60 20 0 3 6 9 12 Temps depuis le début du traitement (mois) 960 636 SG à 6 mois : 66, 0 % (60, 9 -70, 6) SG médian (mois) : 9, 2 (7, 8 -10, 8) 40 396 190 54 0 Patients (n) 434 Survie sans progression – Non-squamous 175 86 24 100 SSP à 6 mois : 31, 2 % (28, 0 -34, 5) SG médian (mois) : 2, 8 (2, 6 -3, 2) 80 60 40 SSP (%) 289 Survie sans progression – Squamous 100 20 SSP à 6 mois : 28, 9 % (24, 2 -33, 8) SG médian (mois) : 2, 8 (2, 4 -3, 2) 80 60 40 20 0 Patients (n) 3 6 9 12 Temps depuis le début du traitement (mois) 960 La Lettre du Cancérologue La Lettre du Pneumologue 365 185 107 33 0 Patients (n) 434 3 6 9 12 Temps depuis le début du traitement (mois) 152 71 36 13 Dixmier et al. EVIDENS: An observational study of Nivolumab-treated patients in Advanced Non-Small Cell Lung Cancer (NSCLC) in a Real-world Setting: initial results on 1394 Patients (NCT 03382496, BMS sponsored). ESMO 2018, d’après 1469 P

Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés La Lettre du Cancérologue La Lettre du Pneumologue Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

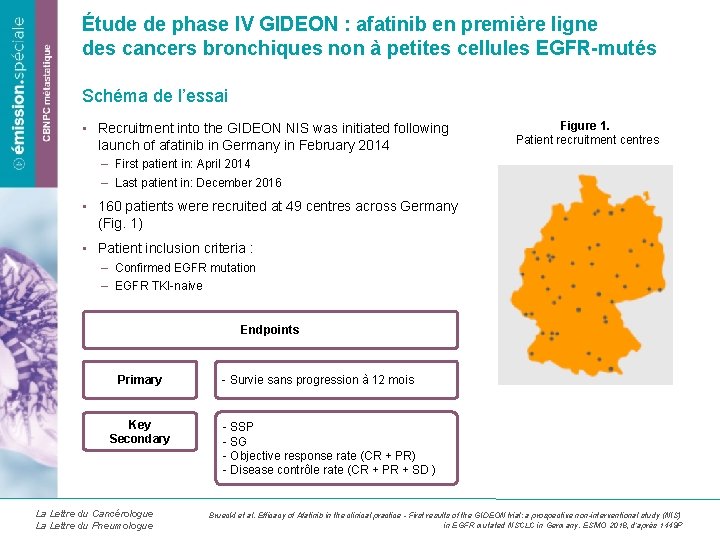
Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés Schéma de l’essai • Recruitment into the GIDEON NIS was initiated following launch of afatinib in Germany in February 2014 Figure 1. Patient recruitment centres – First patient in: April 2014 – Last patient in: December 2016 • 160 patients were recruited at 49 centres across Germany (Fig. 1) • Patient inclusion criteria : – Confirmed EGFR mutation – EGFR TKI-naive Endpoints Primary Key Secondary La Lettre du Cancérologue La Lettre du Pneumologue - Survie sans progression à 12 mois - SSP - SG - Objective response rate (CR + PR) - Disease contrôle rate (CR + PR + SD ) Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

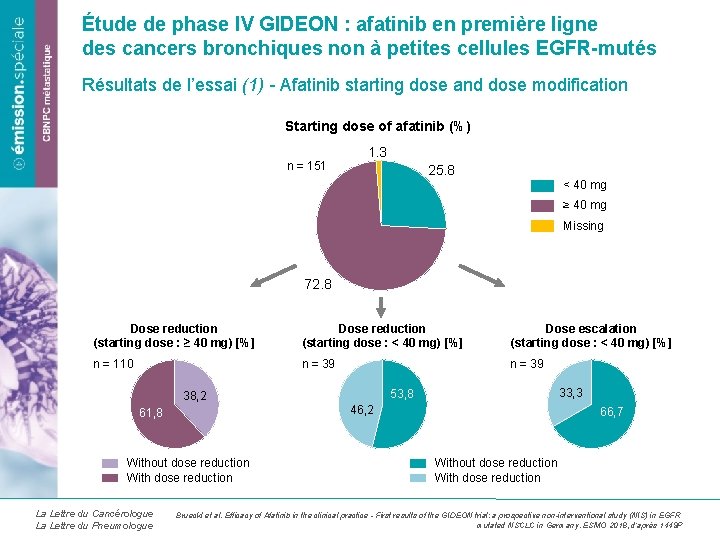
Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés Résultats de l’essai (1) - Afatinib starting dose and dose modification Starting dose of afatinib (%) n = 151 1. 3 25. 8 < 40 mg ≥ 40 mg Missing 72. 8 Dose reduction (starting dose : ≥ 40 mg) [%] Dose reduction (starting dose : < 40 mg) [%] Dose escalation (starting dose : < 40 mg) [%] n = 110 n = 39 46, 2 61, 8 Without dose reduction With dose reduction La Lettre du Cancérologue La Lettre du Pneumologue 33, 3 53, 8 38, 2 66, 7 Without dose reduction With dose reduction Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés Résultats de l’essai (2) ORR and DCR • ORR was 73 % and DCR was 90 % (Fig. 3) • There was little variability in ORR (65 -83 %) and DCR (89 -93 %) between patient subgroups – Both ORR and DCR were similar in patients with different types of mutations (Del 19, L 858 R, or uncommon), with or without baseline brain metastases, and with a starting dose of 40 mg or < 40 mg Best response to afatinib, by investigator assessment (%) 10 PR 17 CR SD 4 69 La Lettre du Cancérologue La Lettre du Pneumologue PD Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

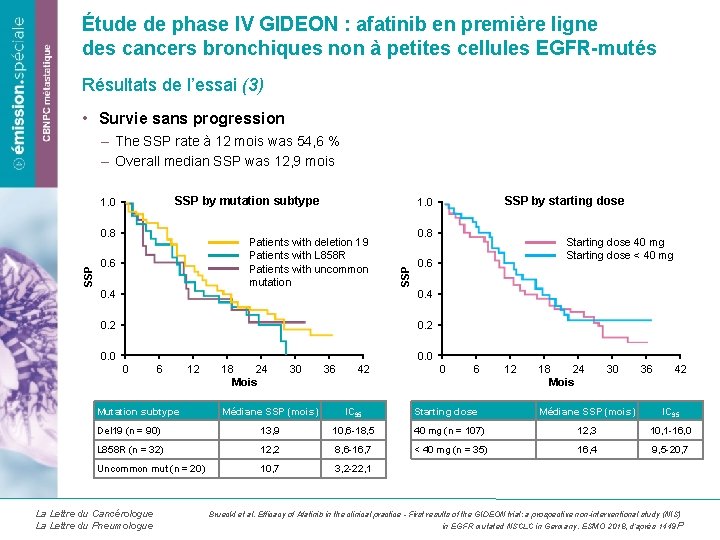
Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés Résultats de l’essai (3) • Survie sans progression – The SSP rate à 12 mois was 54, 6 % – Overall median SSP was 12, 9 mois SSP by mutation subtype SSP 0. 8 Patients with deletion 19 Patients with L 858 R Patients with uncommon mutation 0. 6 0. 8 0. 4 0. 2 0. 0 6 12 Mutation subtype 18 24 Mois 30 36 42 Médiane SSP (mois) IC 95 Del 19 (n = 90) 13, 9 10, 6 -18, 5 L 858 R (n = 32) 12, 2 8, 6 -16, 7 Uncommon mut (n = 20) 10, 7 3, 2 -22, 1 La Lettre du Cancérologue La Lettre du Pneumologue Starting dose 40 mg Starting dose < 40 mg 0. 6 0. 4 0 SSP by starting dose 1. 0 SSP 1. 0 0 6 Starting dose 12 18 24 Mois 30 36 42 Médiane SSP (mois) IC 95 40 mg (n = 107) 12, 3 10, 1 -16, 0 < 40 mg (n = 35) 16, 4 9, 5 -20, 7 Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

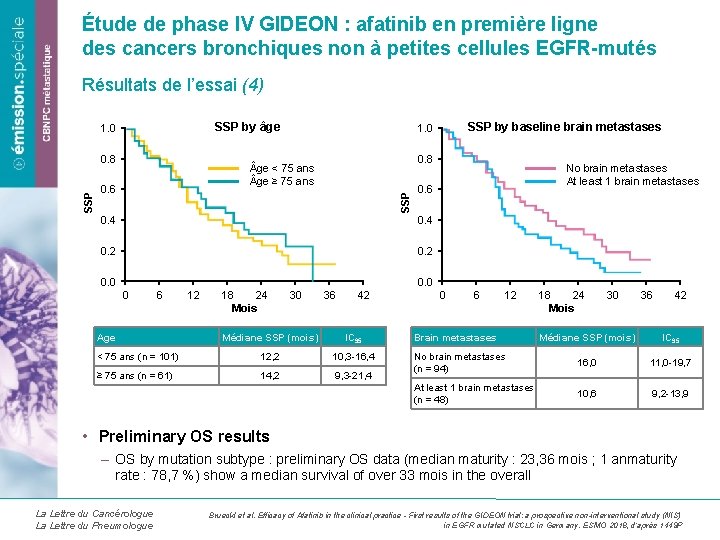
Étude de phase IV GIDEON : afatinib en première ligne des cancers bronchiques non à petites cellules EGFR-mutés Résultats de l’essai (4) SSP by âge 1. 0 0. 8 ge < 75 ans ge ≥ 75 ans 0. 6 SSP 0. 8 SSP by baseline brain metastases 1. 0 0. 6 0. 4 0. 2 0. 0 No brain metastases At least 1 brain metastases 0. 0 0 6 Age 12 18 24 Mois 30 36 42 Médiane SSP (mois) IC 95 < 75 ans (n = 101) 12, 2 10, 3 -16, 4 ≥ 75 ans (n = 61) 14, 2 9, 3 -21, 4 0 6 12 Brain metastases 18 24 Mois 30 36 42 Médiane SSP (mois) IC 95 No brain metastases (n = 94) 16, 0 11, 0 -19, 7 At least 1 brain metastases (n = 48) 10, 6 9, 2 -13, 9 • Preliminary OS results – OS by mutation subtype : preliminary OS data (median maturity : 23, 36 mois ; 1 anmaturity rate : 78, 7 %) show a median survival of over 33 mois in the overall La Lettre du Cancérologue La Lettre du Pneumologue Brueckl et al. Efficacy of Afatinib in the clinical practice - First results of the GIDEON trial: a prospective non-interventional study (NIS) in EGFR mutated NSCLC in Germany. ESMO 2018, d’après 1449 P

Quelques exemples de données de vie réelle en oncologie thoracique • Sur un médicament spécifique • Sur une stratégie thérapeutique de prise en charge La Lettre du Cancérologue La Lettre du Pneumologue

Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Schéma de l’étude Patients included in the IFCT-1502 CLINIVO study (n = 907) Ineligible (n = 5) • Opposition to data collection (n = 2) • Included in a clinical trial with nivolumab (n = 1) • Initiated nivolumab outside the inclusion period (n = 2) 902 patients included in the current analysis n = 317 Sq (35 %) ; n = 585 Non-Sq (65 %) Nivolumab discontinuation (n = 815) • Progression (n = 587 ; 72, 0 %) • Death (n = 77 ; 9, 4 %) • Toxicity (n = 73 ; 9, 0 %) • Investigator's decision (n = 50 ; 6, 1 %) • Lost sight of (n = 14 ; 1, 7 %) • Intercurrent disease (n = 8 ; 1, 0 %) • Patient's choice (n = 6 ; 0, 7 %) Ongoing nivolumab (n = 87) Median follow-up : 26, 1 mois ; IC 95 : 25, 8 -27, 1 Median tt duration : 2, 4 mois ; Min 0, Max 25, 5 La Lettre du Cancérologue La Lettre du Pneumologue n = 426 ≥ 1 post-nivolumab tt n = 319 with first post-nivolumab systemic tt Discontinuation (n = 290) • Progression (52, 8 %) • Death (16, 2 %) • Toxicity (12, 1 %) • Investigator's decision (10 %) • Lost sight of (1, 4 %) • Intercurrent disease (3, 5 %) • Patient's choice (1, 7 %) • Missing (2, 4 %) Girard N et al. IFCT‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

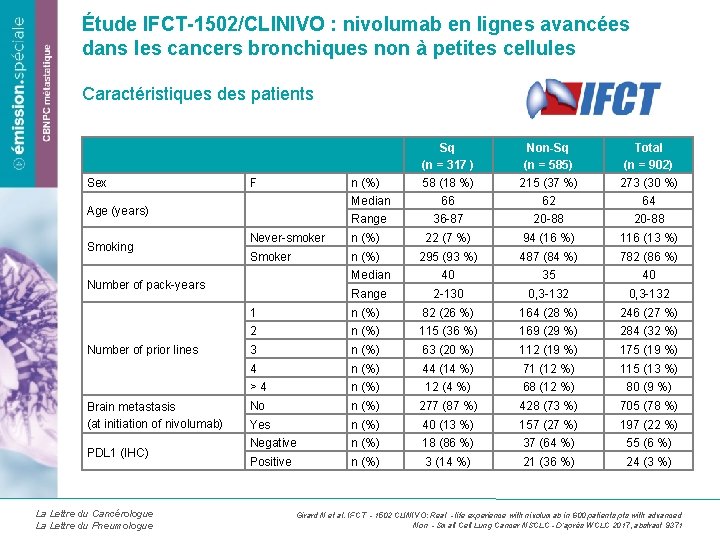
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Caractéristiques des patients Sex Brain metastasis (at initiation of nivolumab) PDL 1 (IHC) La Lettre du Cancérologue La Lettre du Pneumologue Total (n = 902) n (%) Median Range 58 (18 %) 66 36 -87 215 (37 %) 62 20 -88 273 (30 %) 64 20 -88 Never-smoker n (%) 22 (7 %) 94 (16 %) 116 (13 %) Smoker n (%) 295 (93 %) 487 (84 %) 782 (86 %) Median 40 35 40 Range 2 -130 0, 3 -132 1 n (%) 82 (26 %) 164 (28 %) 246 (27 %) 2 n (%) 115 (36 %) 169 (29 %) 284 (32 %) 3 n (%) 63 (20 %) 112 (19 %) 175 (19 %) 4 n (%) 44 (14 %) 71 (12 %) 115 (13 %) > 4 n (%) 12 (4 %) 68 (12 %) 80 (9 %) No n (%) 277 (87 %) 428 (73 %) 705 (78 %) Yes n (%) 40 (13 %) 157 (27 %) 197 (22 %) Negative n (%) 18 (86 %) 37 (64 %) 55 (6 %) Positive n (%) 3 (14 %) 21 (36 %) 24 (3 %) Number of pack-years Number of prior lines Non-Sq (n = 585) F Age (years) Smoking Sq (n = 317 ) Girard N et al. IFCT ‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

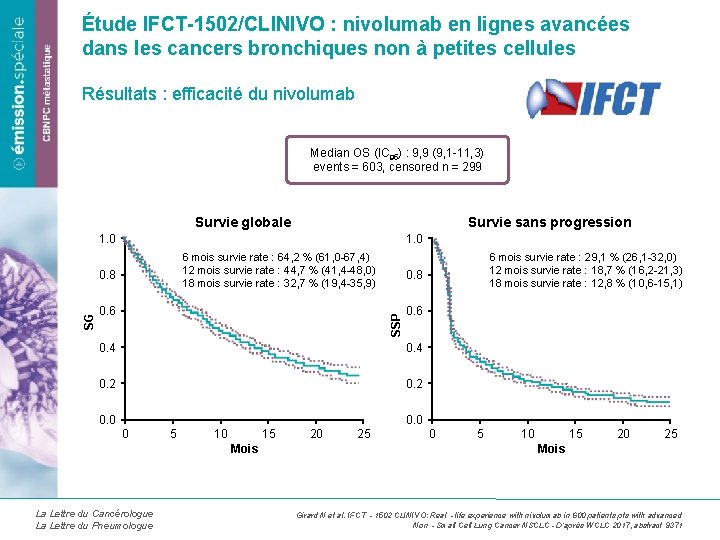
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Résultats : efficacité du nivolumab Median OS (IC 95) : 9, 9 (9, 1 -11, 3) events = 603, censored n = 299 Survie globale Survie sans progression 1. 0 6 mois survie rate : 64, 2 % (61, 0 -67, 4) 12 mois survie rate : 44, 7 % (41, 4 -48, 0) 18 mois survie rate : 32, 7 % (19, 4 -35, 9) 0. 6 0. 8 SSP SG 0. 8 0. 6 0. 4 0. 2 0. 0 6 mois survie rate : 29, 1 % (26, 1 -32, 0) 12 mois survie rate : 18, 7 % (16, 2 -21, 3) 18 mois survie rate : 12, 8 % (10, 6 -15, 1) 0. 0 0 5 10 15 Mois La Lettre du Cancérologue La Lettre du Pneumologue 20 25 0 5 10 15 20 25 Mois Girard N et al. IFCT ‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

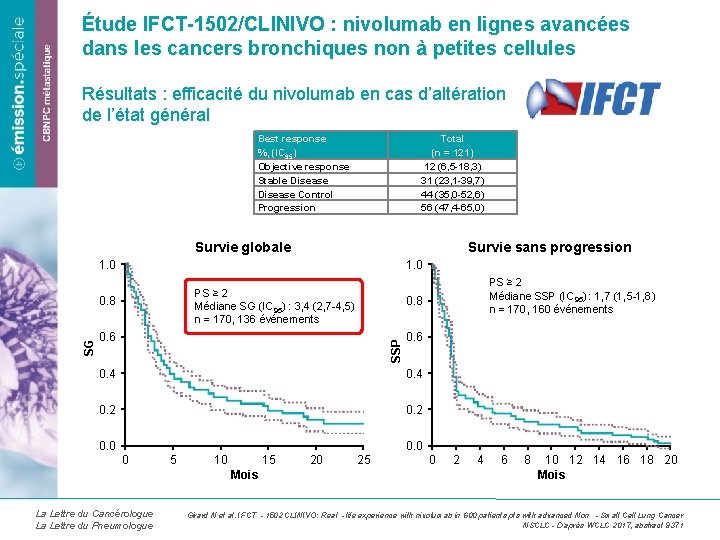
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Résultats : efficacité du nivolumab en cas d’altération de l’état général Best response Total %, (IC 95) (n = 121) Objective response 12 (6, 5 -18, 3) Stable Disease 31 (23, 1 -39, 7) Disease Control 44 (35, 0 -52, 6) Progression 56 (47, 4 -65, 0) Survie globale Survie sans progression 1. 0 PS ≥ 2 Médiane SG (IC 95) : 3, 4 (2, 7 -4, 5) n = 170, 136 événements 0. 8 0. 6 SSP SG 0. 8 0. 6 0. 4 0. 2 0. 0 0 5 10 15 Mois La Lettre du Cancérologue La Lettre du Pneumologue 20 PS ≥ 2 Médiane SSP (IC 95) : 1, 7 (1, 5 -1, 8) n = 170, 160 événements 25 0 2 4 6 8 10 12 14 16 18 20 Mois Girard N et al. IFCT ‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non ‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

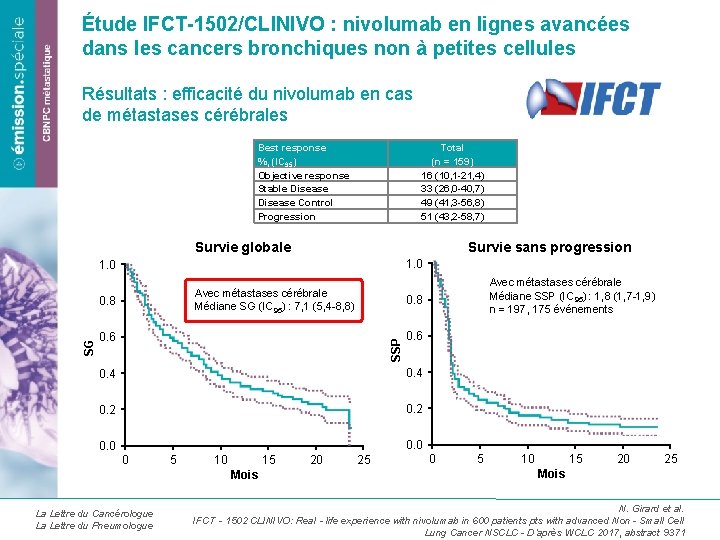
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Résultats : efficacité du nivolumab en cas de métastases cérébrales Best response Total %, (IC 95) (n = 159) Objective response 16 (10, 1 -21, 4) Stable Disease 33 (26, 0 -40, 7) Disease Control 49 (41, 3 -56, 8) Progression 51 (43, 2 -58, 7) Survie globale Survie sans progression 1. 0 Avec métastases cérébrale Médiane SG (IC 95) : 7, 1 (5, 4 -8, 8) 0. 8 0. 6 SSP SG 0. 8 0. 6 0. 4 0. 2 0. 0 0 5 10 15 Mois La Lettre du Cancérologue La Lettre du Pneumologue 20 Avec métastases cérébrale Médiane SSP (IC 95) : 1, 8 (1, 7 -1, 9) n = 197, 175 événements 25 0 5 10 15 20 25 Mois N. Girard et al. IFCT‐ 1502 CLINIVO: Real‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Schéma de l’étude Patients included in the IFCT-1502 CLINIVO study (n = 907) Ineligible (n = 5) • Opposition to data collection (n = 2) • Included in a clinical trial with nivolumab (n = 1) • Initiated nivolumab outside the inclusion period (n = 2) 902 patients included in the current analysis n = 317 Sq (35 %) ; n = 585 Non-Sq (65 %) Nivolumab discontinuation (n = 815) • Progression (n = 587 ; 72, 0 %) • Death (n = 77 ; 9, 4 %) • Toxicity (n = 73 ; 9, 0 %) • Investigator's decision (n = 50 ; 6, 1 %) • Lost sight of (n = 14 ; 1, 7 %) • Intercurrent disease (n = 8 ; 1, 0 %) • Patient's choice (n = 6 ; 0, 7 %) Ongoing nivolumab (n = 87) Median follow-up : 26, 1 mois ; IC 95 : 25, 8 -27, 1 Median tt duration : 2, 4 mois ; Min 0, Max 25, 5 La Lettre du Cancérologue La Lettre du Pneumologue n = 426 ≥ 1 post-nivolumab tt n = 319 with first post-nivolumab systemic tt Discontinuation (n = 290) • Progression (52, 8 %) • Death (16, 2 %) • Toxicity (12, 1 %) • Investigator's decision (10 %) • Lost sight of (1, 4 %) • Intercurrent disease (3, 5 %) • Patient's choice (1, 7 %) • Missing (2, 4 %) N. Girard et al. IFCT‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Résultats : description du premier traitement post-nivolumab Exclusive systemic tt Single agent chemotherapy n = 319 (75 %) n = 210 (49 %) Platin-based doublet n = 35 (8 %) Targeted therapy n = 57 (13 %) Nivolumab rechallenge Other/unknown systemic tt Surgery ± radiotherapy ± systemic tt Unknown tt n = 15 (4 %) n = 2 (0, 5 %) n = 100 (24 %) n = 7 (2 %) La Lettre du Cancérologue La Lettre du Pneumologue Docetaxel 61 (14 %) Gemcitabine 64 (15 %) Paclitacel ± bevacizumab 38 (9 %) Vinorelbine 24 (6 %) Pemetrexed 20 (5 %) Other 3 (1 %) Platin-Paclitaxel 21 (5 %) Other 14 (3 %) Erlotinib 43 (10 %) Other 14 (3%) Girard N et al. IFCT ‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

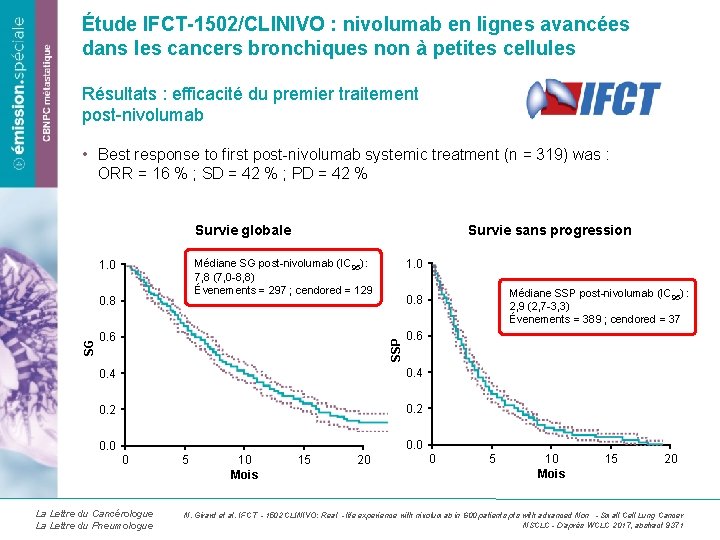
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Résultats : efficacité du premier traitement post-nivolumab • Best response to first post-nivolumab systemic treatment (n = 319) was : ORR = 16 % ; SD = 42 % ; PD = 42 % Survie globale 1. 0 Médiane SG post-nivolumab (IC 95) : 7, 8 (7, 0 -8, 8) Évenements = 297 ; cendored = 129 1. 0 0. 8 0. 6 0. 4 0. 2 0. 0 0 La Lettre du Cancérologue La Lettre du Pneumologue 5 10 Mois 15 20 Médiane SSP post-nivolumab (IC 95) : 2, 9 (2, 7 -3, 3) Évenements = 389 ; cendored = 37 0. 8 SSP SG Survie sans progression 0 5 10 Mois 15 20 N. Girard et al. IFCT‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non ‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

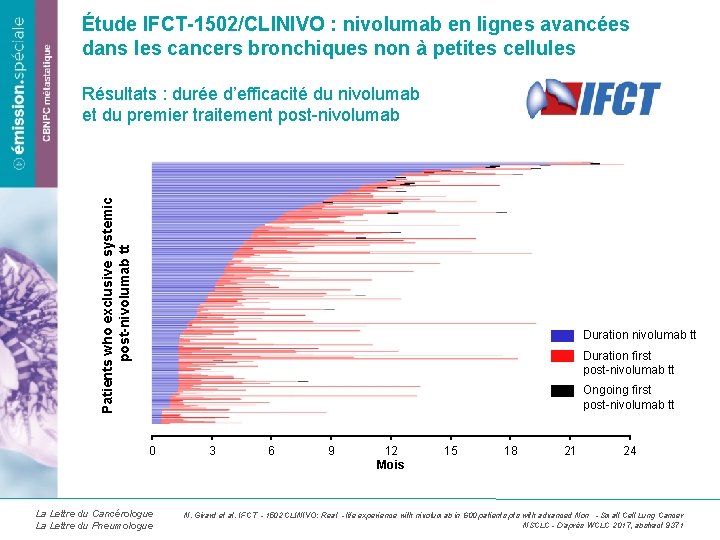
Étude IFCT-1502/CLINIVO : nivolumab en lignes avancées dans les cancers bronchiques non à petites cellules Patients who exclusive systemic post-nivolumab tt Résultats : durée d’efficacité du nivolumab et du premier traitement post-nivolumab Duration nivolumab tt Duration first post-nivolumab tt Ongoing first post-nivolumab tt 0 La Lettre du Cancérologue La Lettre du Pneumologue 3 6 9 12 Mois 15 18 21 24 N. Girard et al. IFCT‐ 1502 CLINIVO: Real ‐life experience with nivolumab in 600 patients pts with advanced Non ‐Small Cell Lung Cancer NSCLC - D’après WCLC 2017, abstract 9371

Étude Gio Tag : séquence afatinib-osimertinib dans les cancers bronchiques non à petites cellules EGFR-mutés Schéma de l’essai La Lettre du Cancérologue La Lettre du Pneumologue Hochmain MJ, et al. Future Oncol 2018; doi: 10. 2217/fon-2018 -0711

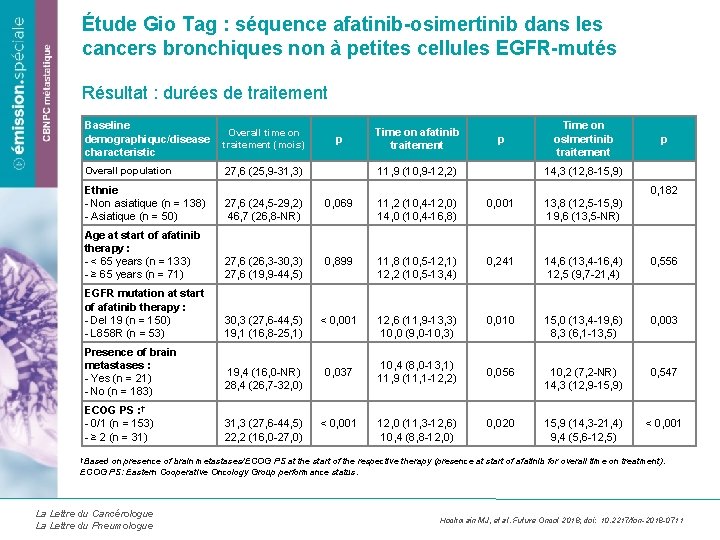
Étude Gio Tag : séquence afatinib-osimertinib dans les cancers bronchiques non à petites cellules EGFR-mutés Résultat : durées de traitement Baseline Overall time on demographiquc/disease traitement (mois) characteristic p Time on afatinib traitement p p Overall population 27, 6 (25, 9 -31, 3) Ethnie - Non asiatique (n = 138) - Asiatique (n = 50) 27, 6 (24, 5 -29, 2) 46, 7 (26, 8 -NR) 0, 069 11, 2 (10, 4 -12, 0) 14, 0 (10, 4 -16, 8) 0, 001 13, 8 (12, 5 -15, 9) 19, 6 (13, 5 -NR) Age at start of afatinib therapy : - < 65 years (n = 133) - ≥ 65 years (n = 71) 27, 6 (26, 3 -30, 3) 27, 6 (19, 9 -44, 5) 0, 899 11, 8 (10, 5 -12, 1) 12, 2 (10, 5 -13, 4) 0, 241 14, 6 (13, 4 -16, 4) 12, 5 (9, 7 -21, 4) 0, 556 EGFR mutation at start of afatinib therapy : - Del 19 (n = 150) - L 858 R (n = 53) 30, 3 (27, 6 -44, 5) 19, 1 (16, 8 -25, 1) < 0, 001 12, 6 (11, 9 -13, 3) 10, 0 (9, 0 -10, 3) 0, 010 15, 0 (13, 4 -19, 6) 8, 3 (6, 1 -13, 5) 0, 003 19, 4 (16, 0 -NR) 28, 4 (26, 7 -32, 0) 0, 037 0, 056 10, 2 (7, 2 -NR) 14, 3 (12, 9 -15, 9) 0, 547 31, 3 (27, 6 -44, 5) 22, 2 (16, 0 -27, 0) < 0, 001 0, 020 15, 9 (14, 3 -21, 4) 9, 4 (5, 6 -12, 5) < 0, 001 Presence of brain metastases : - Yes (n = 21) - No (n = 183) ECOG PS : † - 0/1 (n = 153) - ≥ 2 (n = 31) 11, 9 (10, 9 -12, 2) Time on oslmertinib traitement 14, 3 (12, 8 -15, 9) 0, 182 10, 4 (8, 0 -13, 1) 11, 9 (11, 1 -12, 2) 12, 0 (11, 3 -12, 6) 10, 4 (8, 8 -12, 0) †Based on presence of brain metastases/ECOG PS at the start of the respective therapy (presence at start of afatinib for overall time on treatment). ECOG PS: Eastern Cooperative Oncology Group performance status. La Lettre du Cancérologue La Lettre du Pneumologue Hochmain MJ, et al. Future Oncol 2018; doi: 10. 2217/fon-2018 -0711

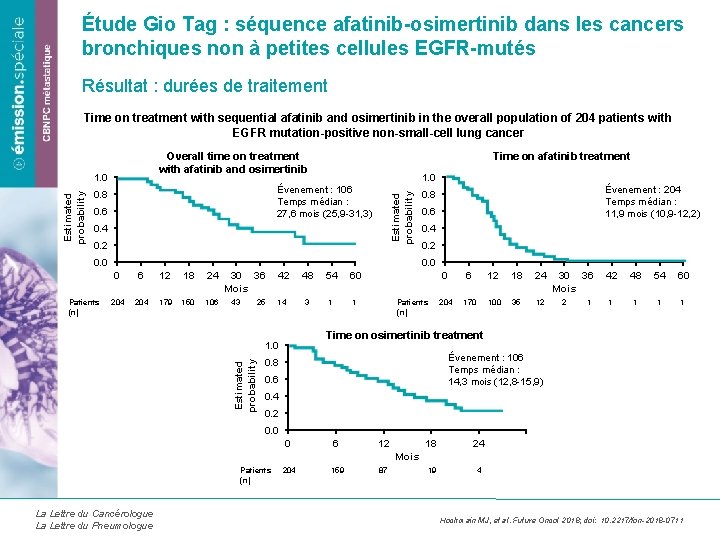
Étude Gio Tag : séquence afatinib-osimertinib dans les cancers bronchiques non à petites cellules EGFR-mutés Résultat : durées de traitement Time on treatment with sequential afatinib and osimertinib in the overall population of 204 patients with EGFR mutation-positive non-small-cell lung cancer Overall time on treatment with afatinib and osimertinib 1. 0 Évenement : 106 Temps médian : 27, 6 mois (25, 9 -31, 3) 0. 8 0. 6 Estimated probability 1. 0 Time on afatinib treatment 0. 4 0. 2 0. 0 Patients (n) Évenement : 204 Temps médian : 11, 9 mois (10, 9 -12, 2) 0. 8 0. 6 0. 4 0. 2 0. 0 0 6 12 18 24 204 179 150 106 30 36 Mois 43 25 42 14 54 60 3 1 1 Patients (n) 0 6 12 18 24 204 170 100 35 12 30 36 Mois 2 1 42 48 54 60 1 1 Time on osimertinib treatment 1. 0 Estimated probability 48 Évenement : 106 Temps médian : 14, 3 mois (12, 8 -15, 9) 0. 8 0. 6 0. 4 0. 2 0. 0 0 6 12 18 24 19 4 Mois Patients (n) La Lettre du Cancérologue La Lettre du Pneumologue 204 159 87 Hochmain MJ, et al. Future Oncol 2018; doi: 10. 2217/fon-2018 -0711

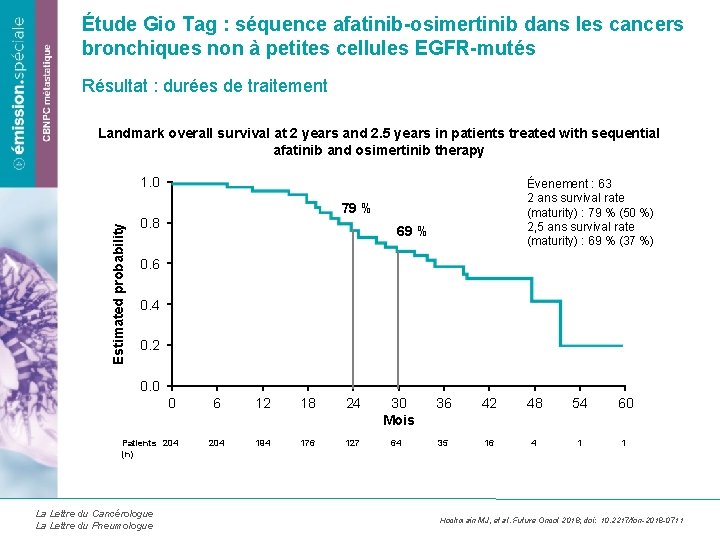
Étude Gio Tag : séquence afatinib-osimertinib dans les cancers bronchiques non à petites cellules EGFR-mutés Résultat : durées de traitement Landmark overall survival at 2 years and 2. 5 years in patients treated with sequential afatinib and osimertinib therapy Estimated probability 1. 0 Évenement : 63 2 ans survival rate (maturity) : 79 % (50 %) 2, 5 ans survival rate (maturity) : 69 % (37 %) 79 % 0. 8 69 % 0. 6 0. 4 0. 2 0. 0 0 Patients 204 (n) La Lettre du Cancérologue La Lettre du Pneumologue 6 12 18 24 30 Mois 36 42 48 54 60 204 194 176 127 64 35 16 4 1 1 Hochmain MJ, et al. Future Oncol 2018; doi: 10. 2217/fon-2018 -0711

Les grandes cohortes: expérience française des études KBP et ESCAP La Lettre du Cancérologue La Lettre du Pneumologue

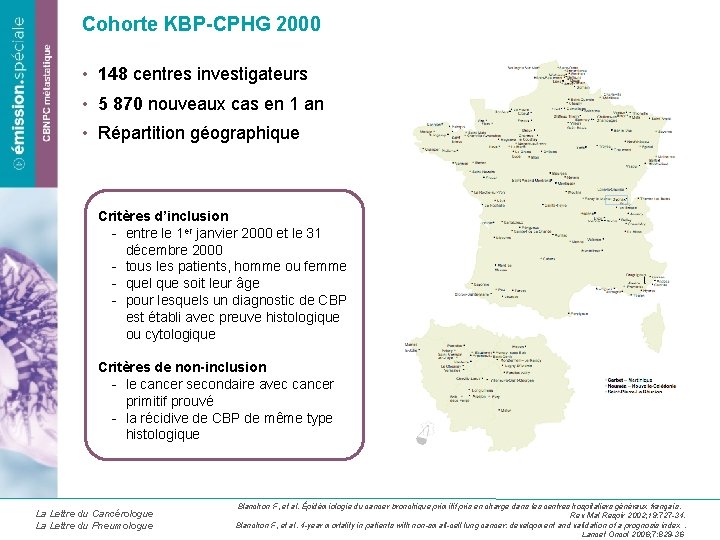
Cohorte KBP-CPHG 2000 • 148 centres investigateurs • 5 870 nouveaux cas en 1 an • Répartition géographique Critères d’inclusion - entre le 1 er janvier 2000 et le 31 décembre 2000 - tous les patients, homme ou femme - quel que soit leur âge - pour lesquels un diagnostic de CBP est établi avec preuve histologique ou cytologique Critères de non-inclusion - le cancer secondaire avec cancer primitif prouvé - la récidive de CBP de même type histologique La Lettre du Cancérologue La Lettre du Pneumologue Blanchon F, et al. Épidémiologie du cancer bronchique primitif pris en charge dans les centres hospitaliers généraux français. Rev Mal Respir 2002; 19: 727 -34. Blanchon F, et al. 4 -year mortality in patients with non-small-cell lung cancer: development and validation of a prognosis index. Lancet Oncol 2006; 7: 829 -36

Cohorte KBP-CPHG 2010 • 119 centres participants • 7 610 nouveaux cas en 1 an • Répartition géographique Critères d’inclusion - ge ≥ 18 ans - CBP primitif prouvé histologiquement ou cytologiquement entre le 1 er janvier et le 31 déc 2010 (date du prélèvement) - Suivi par un pneumologue dans un CHG - Consentement éclairé oral Critères de non-inclusion - ge < 18 ans - CBP secondaire - Récidive d’un CBP primitif de même type histologique - Inclusion antérieure dans l’étude - Patient privé de liberté à la suite d'une décision judiciaire ou administrative La Lettre du Cancérologue La Lettre du Pneumologue Locher C, Debieuvre D, Coëtmeur D et al. Major changes in lung cancer over the last 10 years in France: the KBP-CPHG Studies. Lung Cancer. 2013 Jul; 81(1): 32 -8

Cohortes KBP-CPHG 2000 et 2010 KBP-2000 -CPHG Participation Centres : 148 Patients : 5 870 Exclusion* Centres : 11 Patients : 203 Cohorte KBP-2000 -CPHG Centres : 137 Patients : 5 667 La Lettre du Cancérologue La Lettre du Pneumologue KBP-2010 -CPHG Participation Centres : 119 Patients : 7 610 Exclusion* Centres : 15 Patients : 559 Cohorte KBP-2010 -CPHG Centres : 104 Patients : 7 051 Debieuvre D, Locher C, Neidhardt A, et al. Évolution en 10 ans du cancer bronchique non à petites cellules en fonction du sexe. Résultats de l’étude KBP-2010 -CPHG du Collège des pneumologues des hôpitaux généraux. Rev Mal Respir 2014 Nov; 31(9): 805 -16. Debieuvre D, Oster J-P, Riou R et al. The new face of non-small-cell lung cancer in men: results of two French prospective epidemiological studies conducted 10 years apart. Lung Cancer. 2016 Jan; 91: 1 -6.

Cohortes KBP-CPHG 2000 et 2010 • En 10 ans : – Augmentation du nombre et du pourcentage de femmes et de non-fumeurs (notamment chez les hommes), de stades IV – Explosion du nombre et du pourcentage d’adénocarcinomes indépendante des changements survenus en termes d’âge, de sexe ou de tabagisme – Chez les hommes, le statut tabagique des hommes a significativement évolué (≈ 2 fois plus de non-fumeurs, p < 0, 0001) – La survie globale à 5 ans des patients a été légèrement améliorée, due à l’augmentation de la survie des CBNPC (11, 4 % en 2000 vs 13, 8 % en 2010 ; p < 0, 001). L’amélioration de la survie pour les CBNPC est indépendante des changements du patient et des caractéristiques de la tumeur observés en 10 ans. – La survie à 1 an s’est améliorée (≈ + 5 %) chez les hommes et les femmes, pour les CBNPC et les adénocarcinomes La Lettre du Cancérologue La Lettre du Pneumologue Grivaux M, Debieuvre D, Herman D et al. Early mortality in lung cancer: french prospective multicentre observational study. BMC Pulmonary Medicine 2016; 16(1): 45 Morel H, Raynard B, d’Arlhac M et al. Prediagnosis weight loss, a stronger factor than BMI, to predict survival in patients with lung cancer. Lung Cancer. In press.

Cohorte KBP-CPHG 2010 et développement de ESCAP Participation KBP-2010 -CPHG Centres : 119 Patients : 7 610 Exclusion Centres : 15 Patients : 203 Cohorte KBP-2010 -CPHG Centres : 104 Patients : 7 051 Participation ESCAP-2011 -CPHG Centres : 53 Patients : 4 026 Exclusion Centres : 0 Patients : 83 Cohorte ESCAP-2011 -CPHG Centres : 53 Patients : 3 943 Critères d’inclusion - Être suivi dans un centre volontaire pour participer à ESCAP-2011 -CPHG - Appartenir à la cohorte KBP-2010 -CPHG La Lettre du Cancérologue La Lettre du Pneumologue Grivaux M, Goupil F, Asselain B et al. ESCAP-2011 -CPHG : Stratégies thérapeutiques les 2 premières années après un diagnostic de cancer du poumon. Rev Mal Resp 2017; 34(9): 991 -9

Cohorte KBP-CPHG 2020 : bases du questionnaire Données sur le patient Données sur le CBP Données sur les traitements jusqu’à la 1 re progression Données sur la survie La Lettre du Cancérologue La Lettre du Pneumologue Consommation de cannabis, e-cigarette. . . TNM 8 e édition Classification anatomopathologique Mise à jour des mutations, réarrangements… Modalités diagnostiques PD-L 1, charge mutationnelle Actualisation et prise en compte des nouveaux traitements… Années de recherche de survie (encore en discussion), survie actuarielle. . .

Cohorte KBP-CPHG 2020 : bases du questionnaire • Sur la base du questionnaire ESCAP antérieur avec les adaptations et corrections tirées de l’expérience : Traitement réalisé par blocs successifs Chainage des blocs Date de début et fin, systémiques et locaux Modélisation et représentation graphique de la prise en charge sur un timeline des traitements successifs avec les motifs de début, d’arrêt, les toxicités et leur prise en charge, traitements systémiques et locaux… Données de biologie moléculaire Évolution/cinétique par bloc de traitements successifs, mutations de résistance, nouvelles mutations, nouvelles cibles… Suivi prolongé et données de survie Suivi sur 3 ans, années de recherche de survie (encore en discussion), survie actuarielle… Chainage avec les données de santé (SNDS, IRIS) Traitements associés, hospitalisations, coûts annexes, score de déprivation sociale (accès aux soins)… La Lettre du Cancérologue La Lettre du Pneumologue

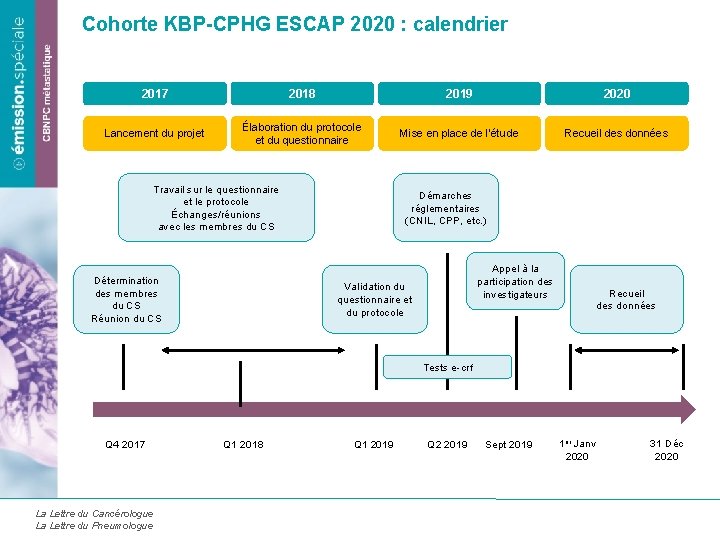
Cohorte KBP-CPHG ESCAP 2020 : calendrier 2017 2018 2019 2020 Lancement du projet Élaboration du protocole et du questionnaire Mise en place de l’étude Recueil des données Travail sur le questionnaire et le protocole Échanges/réunions avec les membres du CS Détermination des membres du CS Réunion du CS Démarches réglementaires (CNIL, CPP, etc. ) Appel à la participation des investigateurs Validation du questionnaire et du protocole Recueil des données Tests e-crf Q 4 2017 La Lettre du Cancérologue La Lettre du Pneumologue Q 1 2018 Q 1 2019 Q 2 2019 Sept 2019 1 er Janv 2020 31 Déc 2020

Conclusions : données de vie réelle • Importance de la prise en compte de la méthodologie et des populations étudiées • Objectifs variés : analyse d’un médicament spécifique et/ou étude d’une séquence thérapeutique • Intérêt des grandes cohortes La Lettre du Cancérologue La Lettre du Pneumologue