Asthme Aigu et BPCO Sergio Salmeron Service de

Asthme Aigu et BPCO Sergio Salmeron Service de Pneumologie - Allergologie Groupe Hospitalier Paris Saint Joseph Patrick Ray SAU, Hôpital Tenon et UPMC Université Paris 06 DESC MU 2012

Asthme Aigu et BPCO

Asthme en France CREDES 1998 • Prévalence cumulée de l’asthme – 8% population générale = 5 millions • Prévalence actuelle – 5% population générale – 10 à 15% chez les « jeunes » • Environ 2000 décès par an • Dépenses globales de santé – 7 Milliards de francs en 1994 (1. 1 Md Euros) – 1. 5 Milliards d’Euros, estimation 2001
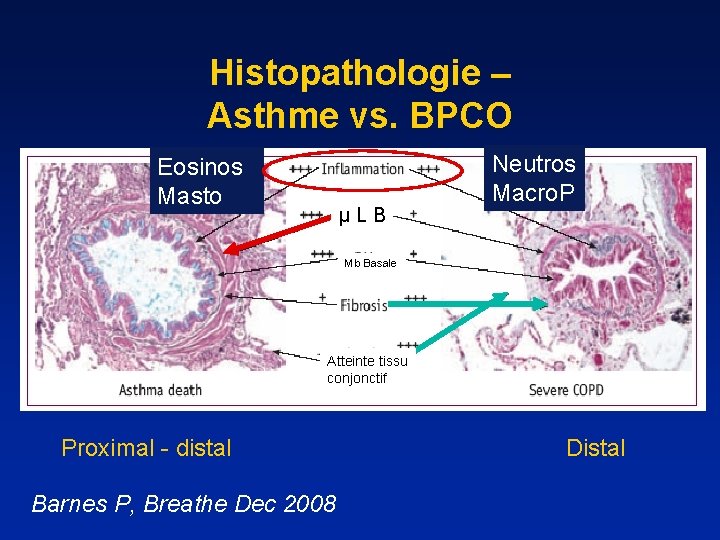
Histopathologie – Asthme vs. BPCO Eosinos Masto µ L B Neutros Macro. P Mb Basale Atteinte tissu conjonctif Proximal - distal Barnes P, Breathe Dec 2008 Distal

Asthme Syndrome caractérisé par : § Une inflammation chronique des bronches (mastocytes et éosinophiles) § Une réactivité bronchique anormalement accrue § Une obstruction bronchique diffuse réversible +++ § Décès ont diminué à ≈1000 en 2006
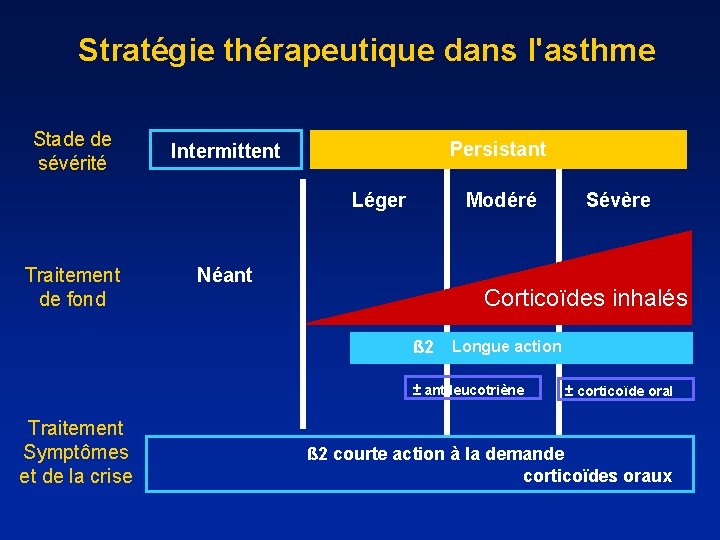
Stratégie thérapeutique dans l'asthme Stade de sévérité Persistant Intermittent Léger Traitement de fond Modéré Néant Corticoïdes inhalés ß 2 Longue action ± antileucotriène Traitement Symptômes et de la crise Sévère ± corticoïde oral ß 2 courte action à la demande corticoïdes oraux
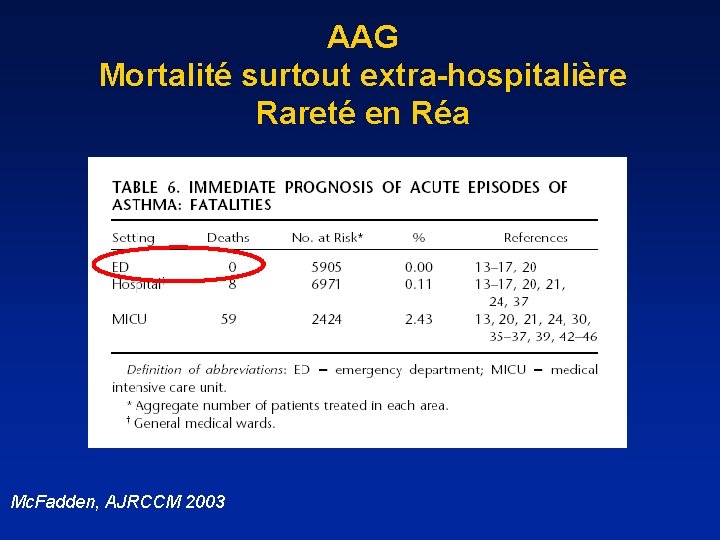
AAG Mortalité surtout extra-hospitalière Rareté en Réa Mc. Fadden, AJRCCM 2003
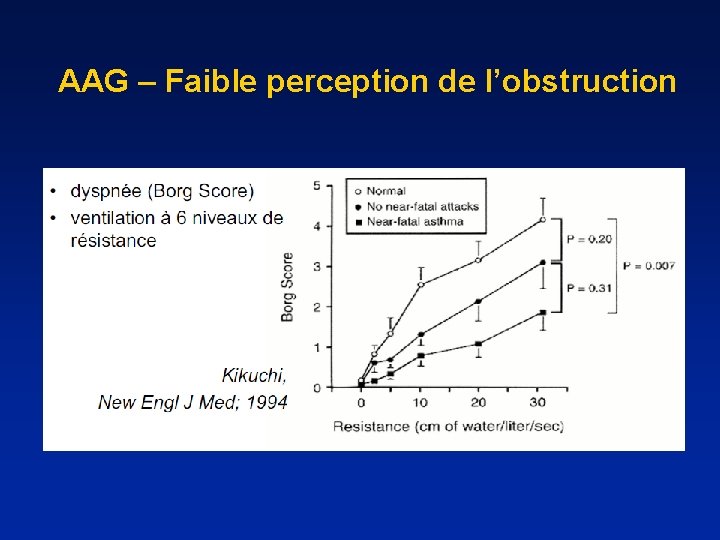
AAG – Faible perception de l’obstruction
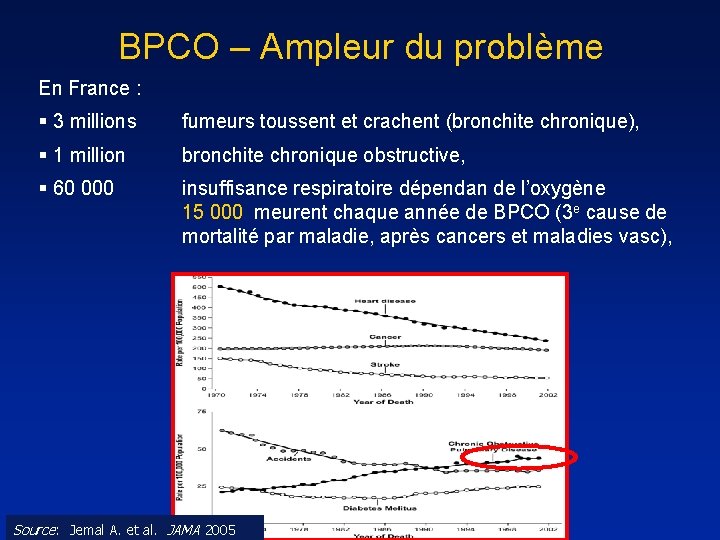
BPCO – Ampleur du problème En France : § 3 millions fumeurs toussent et crachent (bronchite chronique), § 1 million bronchite chronique obstructive, § 60 000 insuffisance respiratoire dépendan de l’oxygène 15 000 meurent chaque année de BPCO (3 e cause de mortalité par maladie, après cancers et maladies vasc), Source: Jemal A. et al. JAMA 2005
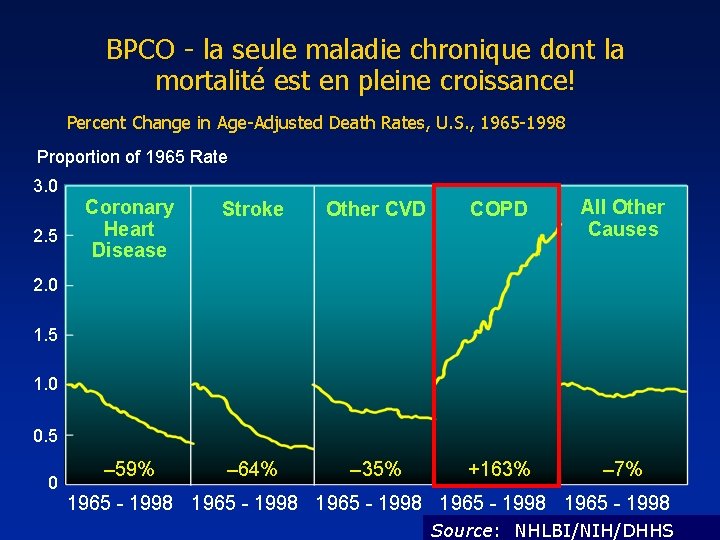
BPCO - la seule maladie chronique dont la mortalité est en pleine croissance! Percent Change in Age-Adjusted Death Rates, U. S. , 1965 -1998 Proportion of 1965 Rate 3. 0 2. 5 Coronary Heart Disease Stroke Other CVD COPD All Other Causes – 59% – 64% – 35% +163% – 7% 2. 0 1. 5 1. 0 0. 5 0 1965 - 1998 1965 - 1998 Source: NHLBI/NIH/DHHS
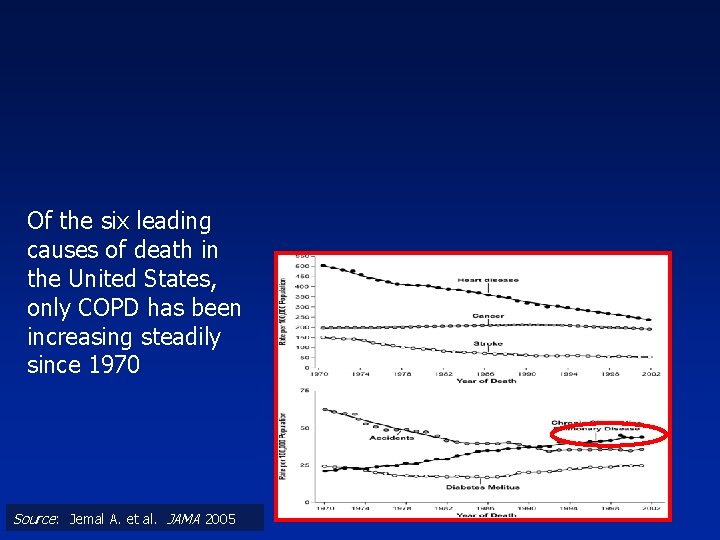
Of the six leading causes of death in the United States, only COPD has been increasing steadily since 1970 Source: Jemal A. et al. JAMA 2005
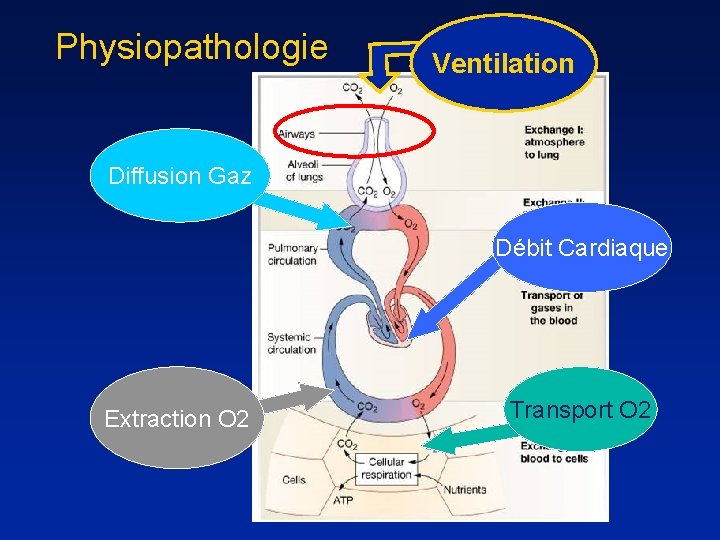
Physiopathologie Ventilation Diffusion Gaz Débit Cardiaque Extraction O 2 Transport O 2
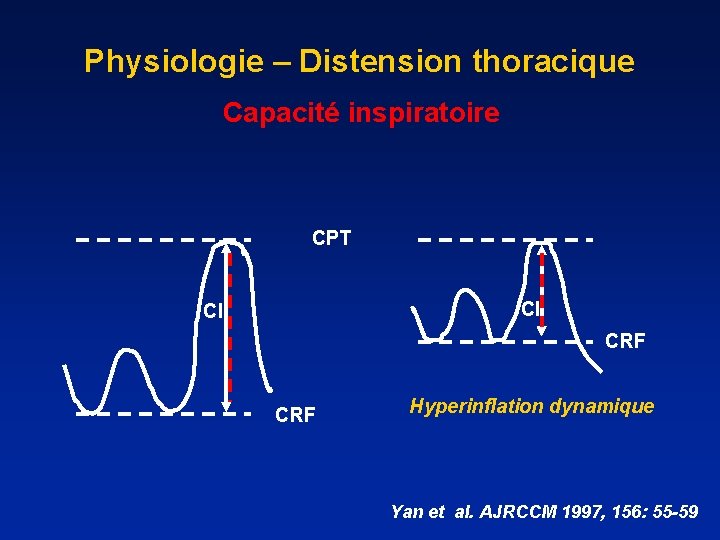
Physiologie – Distension thoracique Capacité inspiratoire CPT CI CI CRF Hyperinflation dynamique Yan et al. AJRCCM 1997, 156: 55 -59
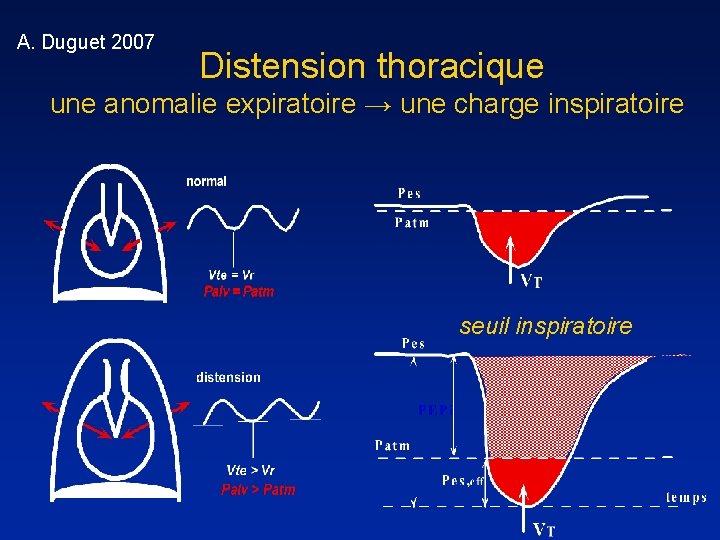
A. Duguet 2007 Distension thoracique une anomalie expiratoire → une charge inspiratoire seuil inspiratoire

BPCO - Définition § Maladie chronique, lentement progressive, bronches et poumons § Diminution non/peu réversible des débits expiratoires § Essentiellement liée au tabac § Elle englobe la bronchite chronique, l’emphysème, l’insuffisance respiratoire § Elle touche également le cœur, les muscles, le système nerveux Composante inflammatoire locale et systémique Rev Mal Respir 2003; 20: 4 S 10 -4 S 13

Stades de sévérité – SPLF 2003

Spirometric classification of COPD: Post-bronchodilator FEV 1/ FVC <0. 7 confirms the presence of airflow limitation that is not fully reversible. Severity Postbrochodilator FEV 1/FVC FEV 1 % pred >0. 7 80 Mild COPD 0. 7 80 Moderate COPD 0. 7 50– 80 Severe COPD 0. 7 30– 50 Very severe COPD 0. 7 <30 At risk Patients who: –smoke or have exposure to pollutants –have cough, sputum or dyspnoea –have family history of respiratory disease ERS/ATS COPD Guidelines 2005

TTT selon le stade de la BPCO I: Minime II: Modéré III: Sévere IV: Très Sévere FEV 1 < 30% prédite FEV 1 > 80% prédite 50% < FEV 1 < 80% prédite 30% < FEV 1 < 50% prédite ou FEV 1 < 50% prédite + chronic respiratory failure Active reduction of risk factor(s); influenza vaccination Add short-acting bronchodilator (when needed) Add regular treatment with one or more long-acting bronchodilators (when needed); Add rehabilitation Add inhaled glucocorticosteroids if repeated exacerbations GOLD COPD Guidelines 2007 Add long term oxygen if chronic respiratory failure. Consider surgical treatments

Dyspnée aiguë - Histoire clinique • Importance de l’histoire clinique – Age, maladie préexistante – Traitement en cours +++ – Présentation clinique • • • Facteur déclenchant, caractère aigu/subaigu… DE d’aggravation progressive +++ Expectoration purulente Douleur thoracique Fièvre, IVD, hémoptysie Choc

Dyspnée aiguë - Éléments d’orientation clinique Cyanose Suggère Sa. O 2 basse Pâleur Anémia, choc Polypnée superficielle Non spécifique (BPCO, restrictive, cardiopathie) Cardiovasculaire Tachycardie, arythmie, hypotension. Choc etc… Signes d’hyperinflation thorax (Hoover), lèvres pincées BPCO, asthme Sibilants… Stridor Dysfonction voies aériennes sup Wheezing, TE Asthme, BPCO « Psychogenic » hyperventilation Considérer toutes les autres causes Thrombose veineuse profonde (TVP) Évoquer embolie pulmonaire (PE)!!…

Dyspnée aiguë – Stratégie diagnostique Radio thorax souvent RAS Facteur déclencht? - maladie connue sévérité - hyperinflation BPCO, asthme - non spécifique autres investigations nécessaires Pa. O 2, Pa. CO 2, p. H, lactates Pa. O 2 Pa. CO 2 ou (parenchyme, pompe RI) p. H N ou (acidose respir et/ou métabolique) CO 2 T N ou ECG, BNP Cardiac arythmie, ischémie etc. IVG… Ddimères If (non spécifique) mais considérer EP Hb, Hyperleuco Cardiac enzymes anémie, infection Ischémie cardiaque DEP !!!

Signes de gravité - AAG Signes d’alarme Signes de gravité Troubles de vigilance Orthopnée Pauses respiratoires Contraction SC Silence auscultatoire Cyanose Sueurs Parole impossible Agitation FC ≥ 110 / min Attention discordance Clinique – DEP (jeunes) FR ≥ 30 / min DEP ≤ 30 % th Pa. CO 2 ≥ 40 mm Hg
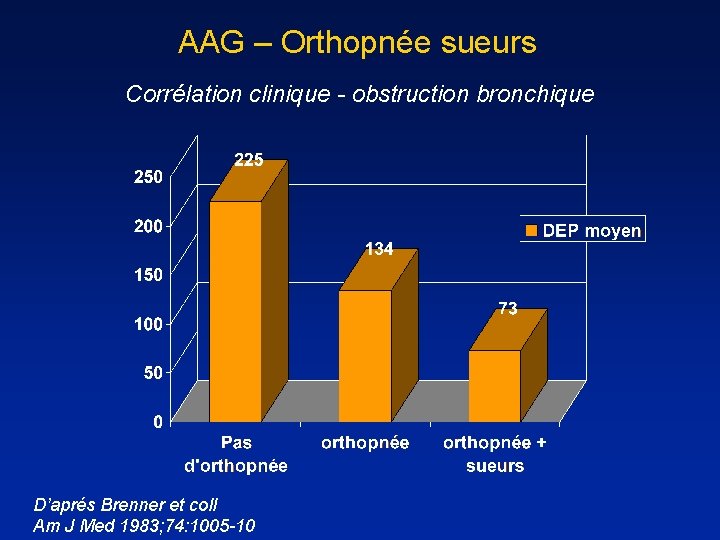
AAG – Orthopnée sueurs Corrélation clinique - obstruction bronchique D’aprés Brenner et coll Am J Med 1983; 74: 1005 -10
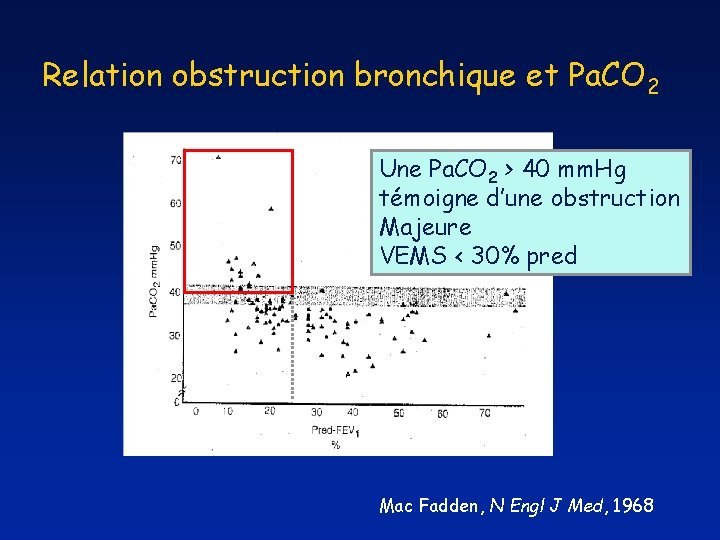
Relation obstruction bronchique et Pa. CO 2 Une Pa. CO 2 > 40 mm. Hg témoigne d’une obstruction Majeure VEMS < 30% pred Mac Fadden, N Engl J Med, 1968
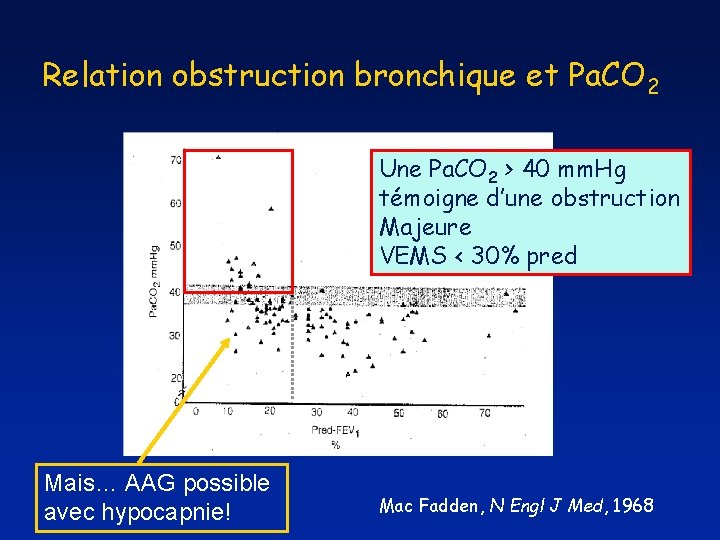
Relation obstruction bronchique et Pa. CO 2 Une Pa. CO 2 > 40 mm. Hg témoigne d’une obstruction Majeure VEMS < 30% pred Mais… AAG possible avec hypocapnie! Mac Fadden, N Engl J Med, 1968
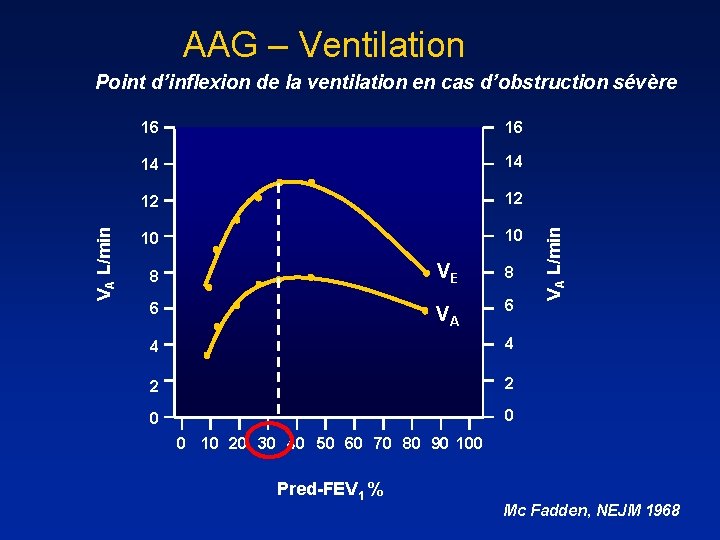
AAG – Ventilation 16 16 14 14 12 12 10 10 8 VE 8 6 VA 6 4 4 2 2 0 0 VA L/min Point d’inflexion de la ventilation en cas d’obstruction sévère 0 10 20 30 40 50 60 70 80 90 100 Pred-FEV 1 % Mc Fadden, NEJM 1968

Signes de gravité – BPCO – VNI? Signes de gravité Signes classiques Troubles de vigilance Orthopnée Pauses respiratoires Contraction SC Silence auscultatoire Respiration abdo paradoxale Sueurs Parole impossible OMI Cyanose FC ≥ 110 / min 2 Signes cliniques inhabituels fièvre choc FR ≥ 30 / min DEP ≤ 30 % th Pa. CO 2 ≥ 40 mm Hg p. H
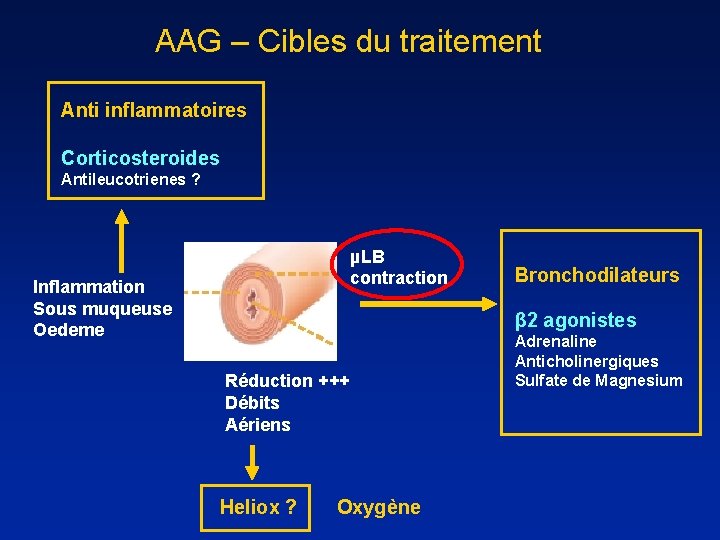
AAG – Cibles du traitement Anti inflammatoires Corticosteroides Antileucotrienes ? µLB contraction Inflammation Sous muqueuse Oedeme Bronchodilateurs β 2 agonistes Réduction +++ Débits Aériens Heliox ? Oxygène Adrenaline Anticholinergiques Sulfate de Magnesium

Traitement de l’AA aux Urgences Traitement conventionnel – Première ligne : BD inhalés β 2+, Antichol, corticoïdes, – Deuxième ligne : idem + Sulfate de Magnésium ? Traitement non conventionnel – – β 2+ IV, adré, amino… Heliox Ketamine Halogénés
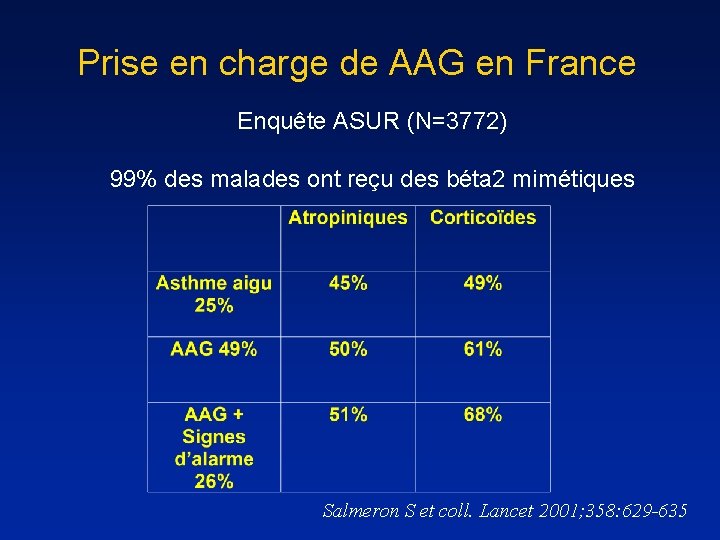
Prise en charge de AAG en France Enquête ASUR (N=3772) 99% des malades ont reçu des béta 2 mimétiques Salmeron S et coll. Lancet 2001; 358: 629 -635
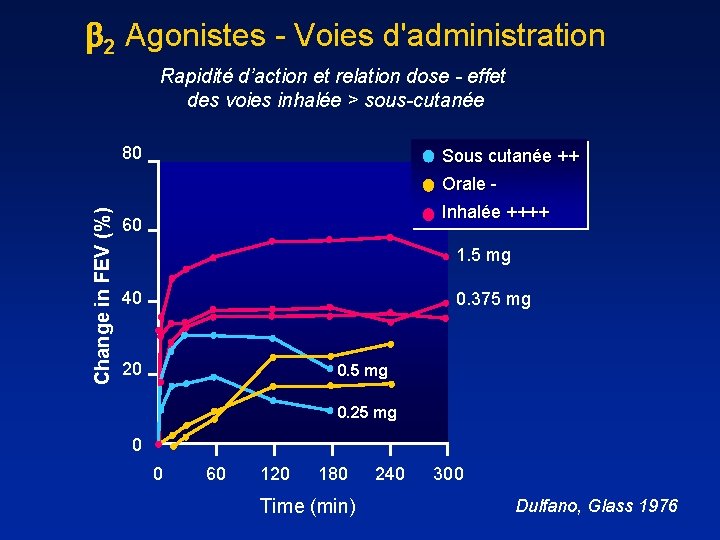
2 Agonistes - Voies d'administration Rapidité d’action et relation dose - effet des voies inhalée > sous-cutanée 80 Sous cutanée ++ Change in FEV (%) Orale Inhalée ++++ 60 1. 5 mg 40 0. 375 mg 20 0. 5 mg 0. 25 mg 0 0 60 120 180 Time (min) 240 300 Dulfano, Glass 1976
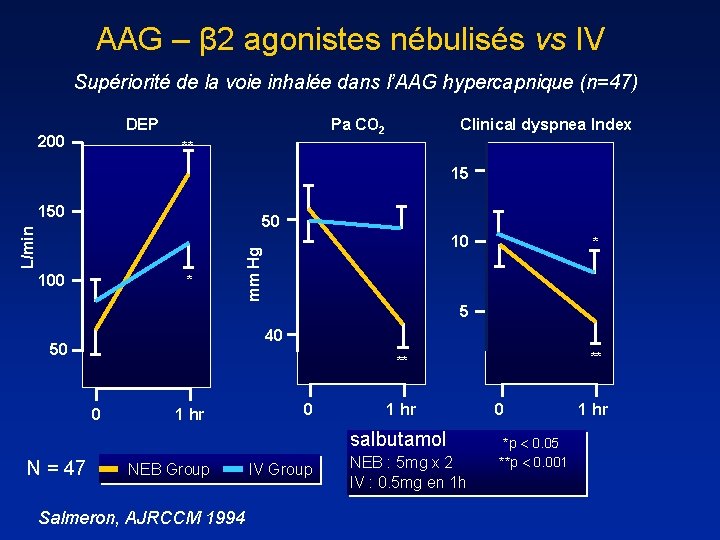
AAG – β 2 agonistes nébulisés vs IV Supériorité de la voie inhalée dans l’AAG hypercapnique (n=47) DEP 200 Pa CO 2 Clinical dyspnea Index ** 15 150 100 * 10 mm Hg L/min 50 * 5 40 50 0 1 hr salbutamol N = 47 ** ** NEB Group Salmeron, AJRCCM 1994 IV Group NEB : 5 mg x 2 IV : 0. 5 mg en 1 h 0 *p 0. 05 **p 0. 001 1 hr
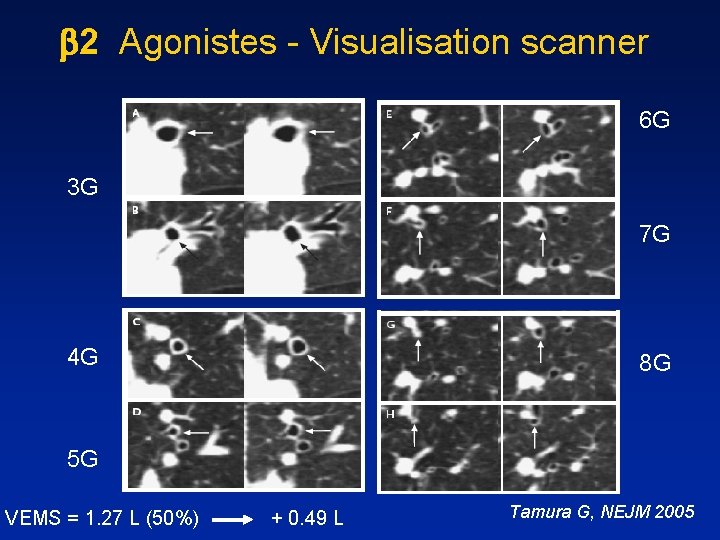
2 Agonistes - Visualisation scanner 6 G 3 G 7 G 4 G 8 G 5 G VEMS = 1. 27 L (50%) + 0. 49 L Tamura G, NEJM 2005
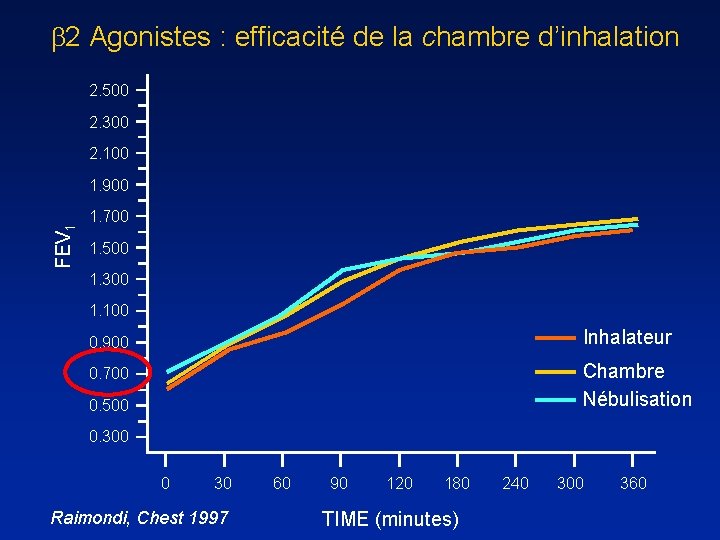
2 Agonistes : efficacité de la chambre d’inhalation 2. 500 2. 300 2. 100 FEV 1 1. 900 1. 700 1. 500 1. 300 1. 100 0. 900 Inhalateur 0. 700 Chambre Nébulisation 0. 500 0. 300 0 30 Raimondi, Chest 1997 60 90 120 180 TIME (minutes) 240 300 360

Intérêt de l’utilisation d’une chambre d’inhalation pour l’administration de salbutamol au cours des crises d’asthme sévères D’aprés Newman KB ET coll. Chest 2002; 121: 1036 -1041
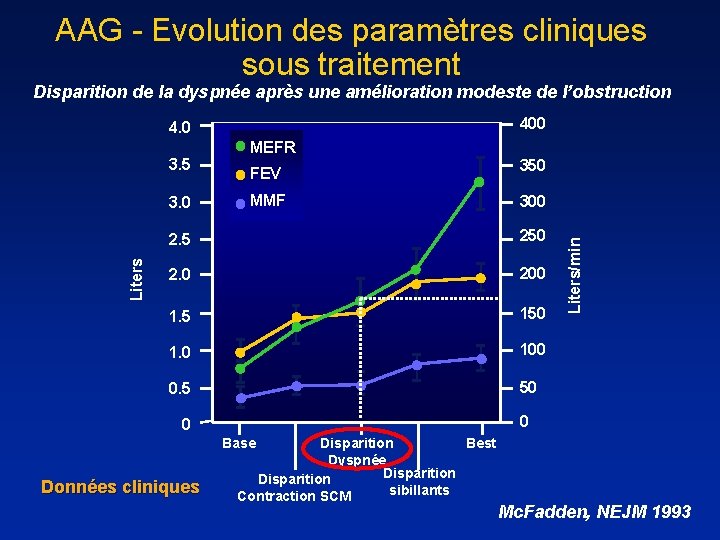
AAG - Evolution des paramètres cliniques sous traitement Disparition de la dyspnée après une amélioration modeste de l’obstruction 400 3. 5 Liters 3. 0 MEFR FEV MMF 350 300 2. 5 250 2. 0 200 1. 5 150 1. 0 100 0. 5 50 Liters/min 4. 0 0 0 Base Données cliniques Disparition Best Dyspnée Disparition sibillants Contraction SCM Mc. Fadden, NEJM 1993
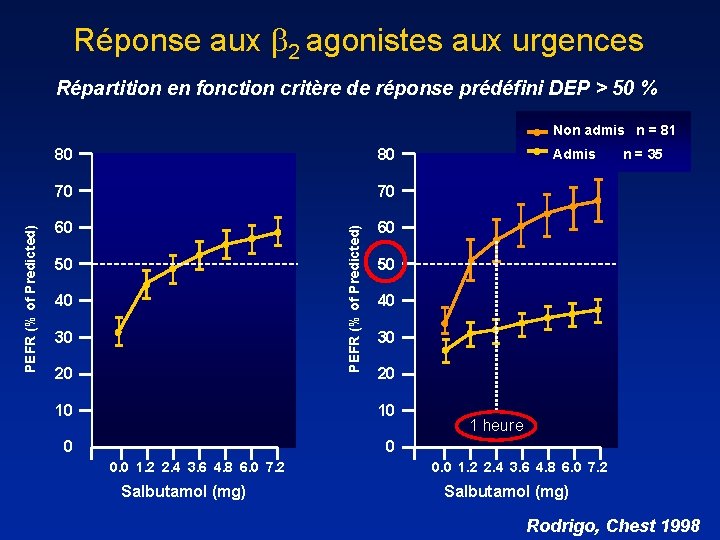
Réponse aux 2 agonistes aux urgences Répartition en fonction critère de réponse prédéfini DEP > 50 % 80 80 70 70 60 60 PEFR (% of Predicted) Non admis n = 81 50 40 30 20 10 0 0 Salbutamol (mg) n = 35 50 10 0. 0 1. 2 2. 4 3. 6 4. 8 6. 0 7. 2 Admis 1 heure 0. 0 1. 2 2. 4 3. 6 4. 8 6. 0 7. 2 Salbutamol (mg) Rodrigo, Chest 1998
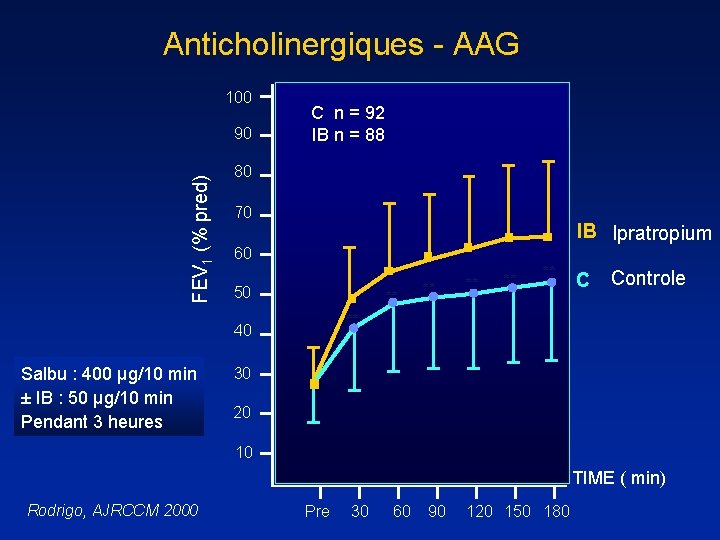
Anticholinergiques - AAG 100 FEV 1 (% pred) 90 C n = 92 IB n = 88 80 70 IB Ipratropium 60 50 ** ** ** C Controle ** 40 Salbu : 400 μg/10 min ± IB : 50 μg/10 min Pendant 3 heures ** ** 30 20 10 TIME ( min) Rodrigo, AJRCCM 2000 Pre 30 60 90 120 150 180
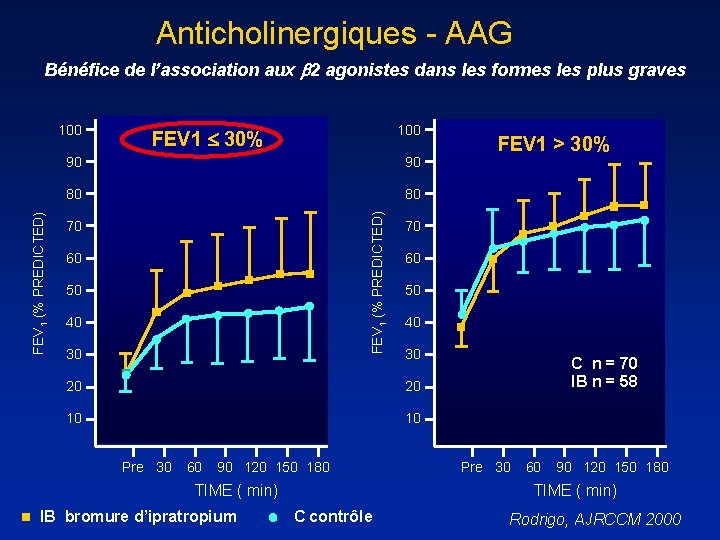
Anticholinergiques - AAG Bénéfice de l’association aux 2 agonistes dans les formes les plus graves 100 FEV 1 30% 90 90 80 80 FEV 1 (% PREDICTED) 100 70 60 50 40 30 20 20 10 10 Pre 30 60 90 120 150 180 TIME ( min) IB bromure d’ipratropium FEV 1 > 30% C n = 70 IB n = 58 Pre 30 60 90 120 150 180 TIME ( min) C contrôle Rodrigo, AJRCCM 2000
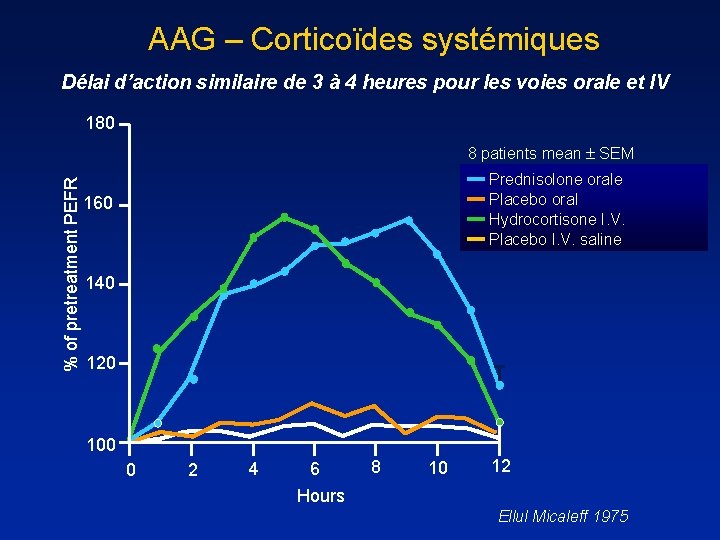
AAG – Corticoïdes systémiques Délai d’action similaire de 3 à 4 heures pour les voies orale et IV 180 % of pretreatment PEFR 8 patients mean SEM Prednisolone orale Placebo oral Hydrocortisone I. V. Placebo I. V. saline 160 140 120 100 0 2 4 6 8 10 12 Hours Ellul Micaleff 1975
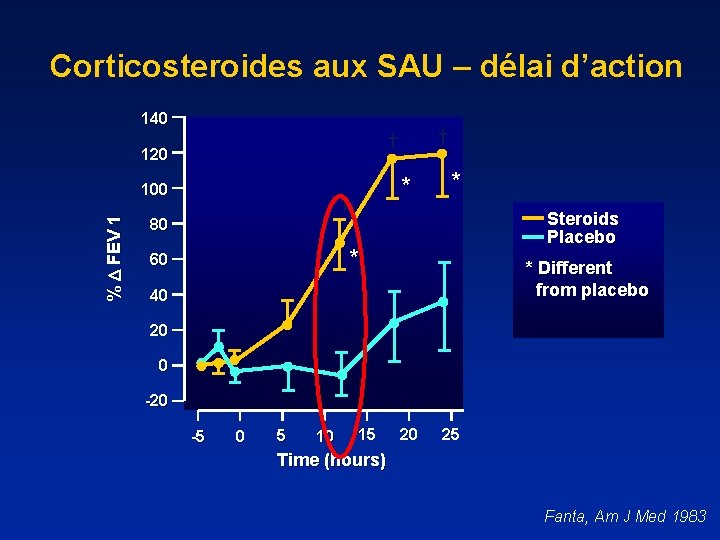
Corticosteroides aux SAU – délai d’action 140 120 100 % FEV 1 † † * Steroids Placebo 80 * 60 * Different from placebo 40 20 0 -20 -5 0 5 10 15 20 25 Time (hours) Fanta, Am J Med 1983

AAG – Doses de CTS Evolution du DEP dans les 3 groupes Pas de différence significative entre les 3 groupes Bowler S. D. Thorax 1992; 47: 584 -587
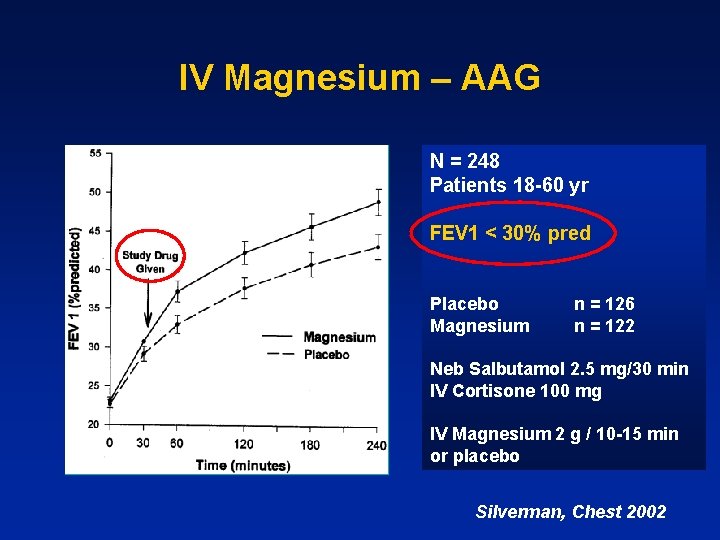
IV Magnesium – AAG N = 248 Patients 18 -60 yr FEV 1 < 30% pred Placebo Magnesium n = 126 n = 122 Neb Salbutamol 2. 5 mg/30 min IV Cortisone 100 mg IV Magnesium 2 g / 10 -15 min or placebo Silverman, Chest 2002
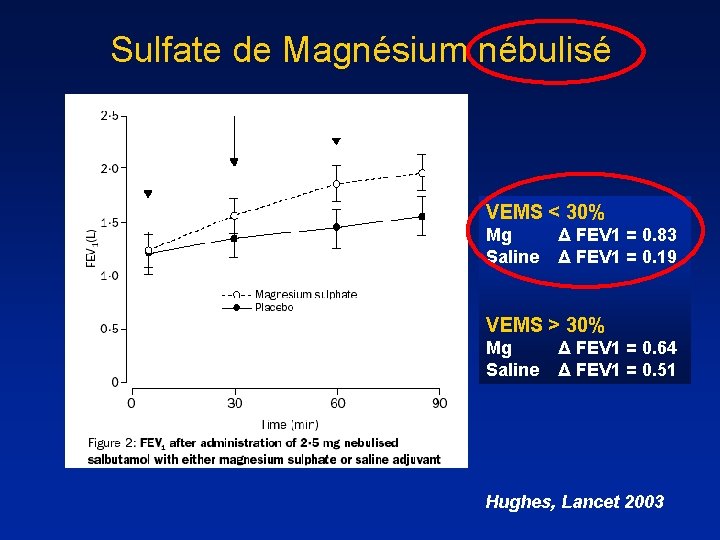
Sulfate de Magnésium nébulisé VEMS < 30% Mg Saline Δ FEV 1 = 0. 83 Δ FEV 1 = 0. 19 VEMS > 30% Mg Saline Δ FEV 1 = 0. 64 Δ FEV 1 = 0. 51 Hughes, Lancet 2003

Traitement de l’AA aux Urgences Traitement conventionnel – Première ligne : BD inhalés β 2+, Antichol, corticoïdes, – Deuxième ligne : idem + Sulfate de Magnésium – On fait mieux dans ASUR-2 > ASUR-1… Traitement non conventionnel – – – β 2+ IV Adré, amino… Heliox (en pré-Hosp. diminution de la VM ? ) Ketamine, Halogénés VNI
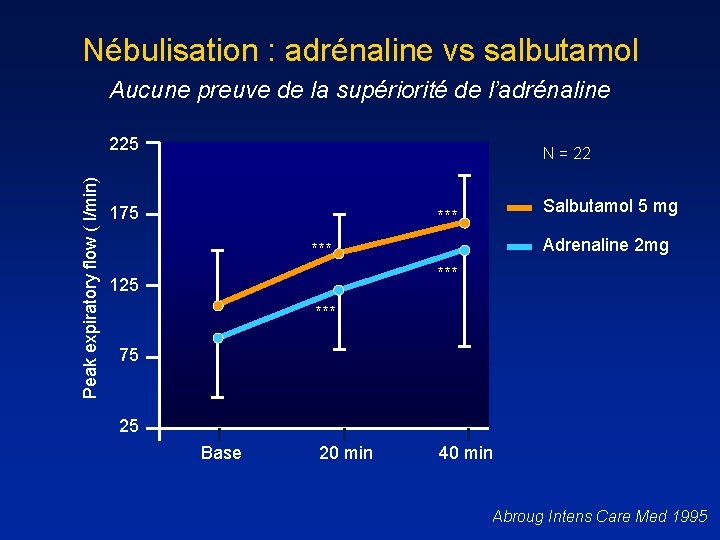
Nébulisation : adrénaline vs salbutamol Aucune preuve de la supériorité de l’adrénaline Peak expiratory flow ( l/min) 225 N = 22 175 Salbutamol 5 mg *** Adrenaline 2 mg *** 125 *** 75 25 Base 20 min 40 min Abroug Intens Care Med 1995
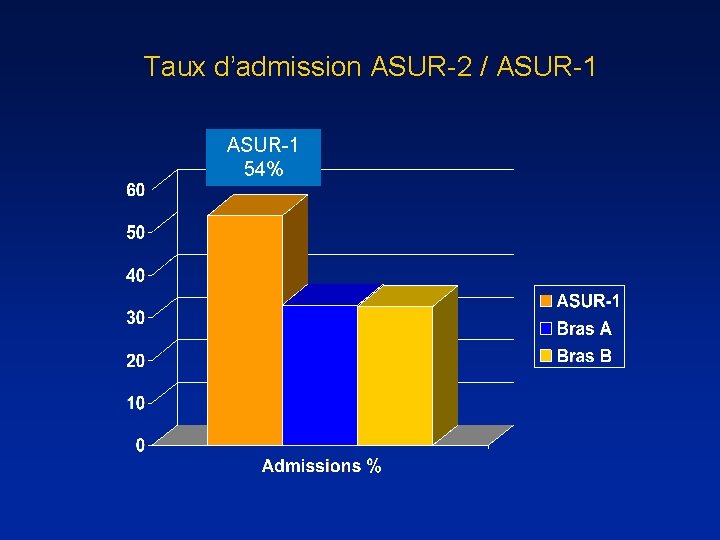
Taux d’admission ASUR-2 / ASUR-1 54%
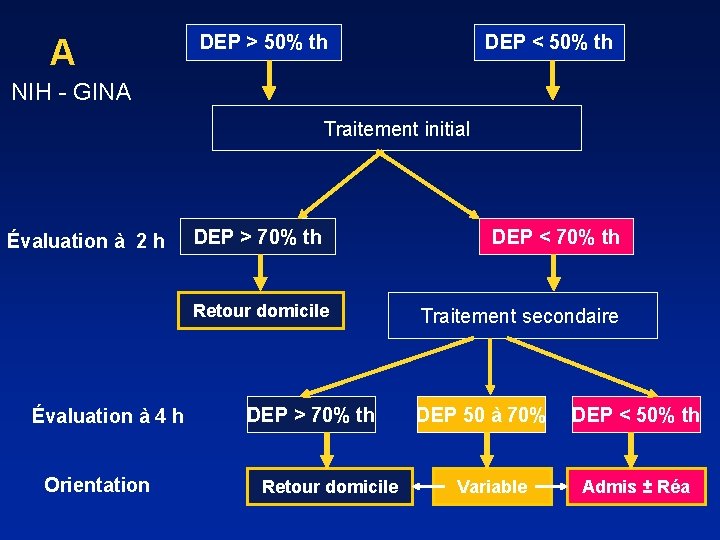
A DEP > 50% th DEP < 50% th NIH - GINA Traitement initial Évaluation à 2 h DEP > 70% th Retour domicile Évaluation à 4 h Orientation DEP > 70% th Retour domicile DEP < 70% th Traitement secondaire DEP 50 à 70% Variable DEP < 50% th Admis ± Réa
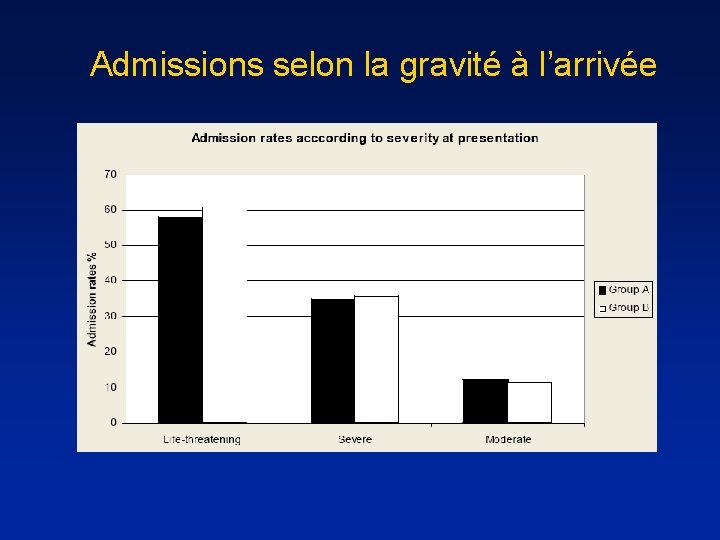
Admissions selon la gravité à l’arrivée
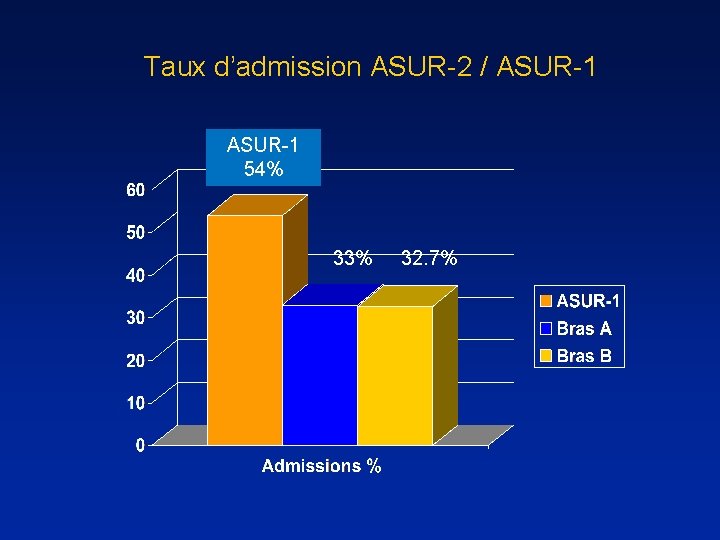
Taux d’admission ASUR-2 / ASUR-1 54% 33% 32. 7%
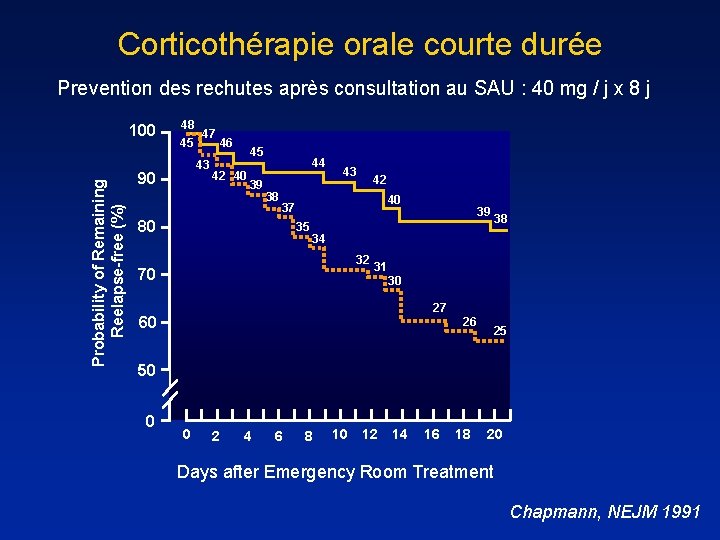
Corticothérapie orale courte durée Prevention des rechutes après consultation au SAU : 40 mg / j x 8 j Probability of Remaining Reelapse-free (%) 100 48 45 47 43 90 46 45 42 40 39 44 38 43 42 40 37 80 35 39 38 34 32 70 31 30 27 60 26 25 50 0 0 2 4 6 8 10 12 14 16 18 20 Days after Emergency Room Treatment Chapmann, NEJM 1991
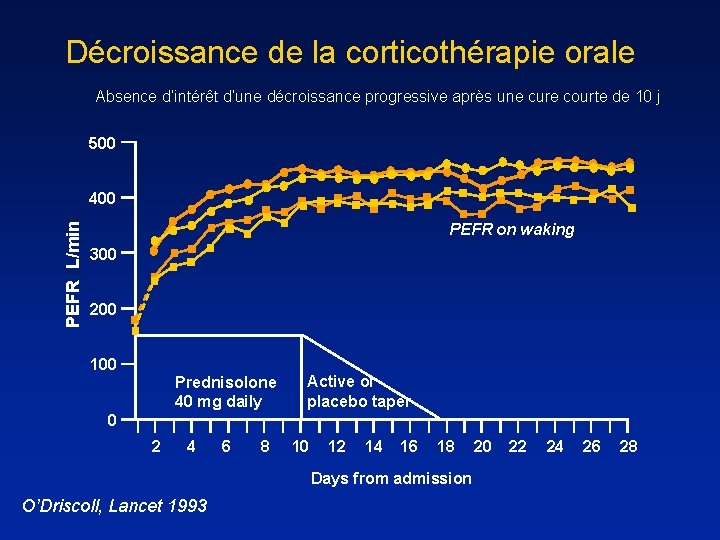
Décroissance de la corticothérapie orale Absence d’intérêt d’une décroissance progressive après une cure courte de 10 j 500 PEFR (L/min) 400 PEFR on waking 300 200 100 Prednisolone 40 mg daily Active or placebo taper 0 2 4 6 8 10 12 14 16 18 Days from admission O’Driscoll, Lancet 1993 20 22 24 26 28

Traitement au décours des Urgences Traitement – β 2+ et corticoïdes inhalés, – Cure courtes de CST (5 -7) TTT non médicamenteux – Circuit pneumo (CPU ? ) – Bilan étiologique – Education (DEP, spray, tabac…? )
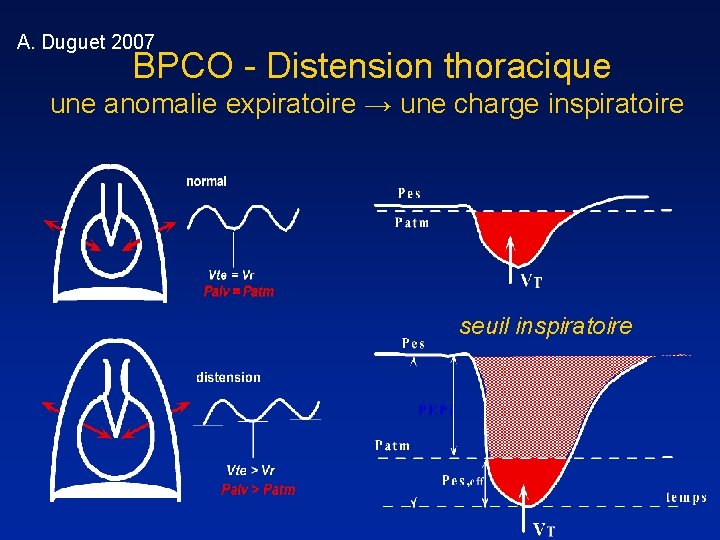
A. Duguet 2007 BPCO - Distension thoracique une anomalie expiratoire → une charge inspiratoire seuil inspiratoire


Traitement de l’AA aux Urgences (et décompensation BPCO? ) Traitement conventionnel – – – O 2 nasal BD inhalés β 2+, Antichol, corticoïdes, VNI ? ? ? Facteur déclenchant TAC préventif Cortic ? ? – Deuxième ligne : idem + β 2+ IV, adré, amino… Traitement non conventionnel – Sulfate de Magnésium – Heliox – Ketamine – Halogénés
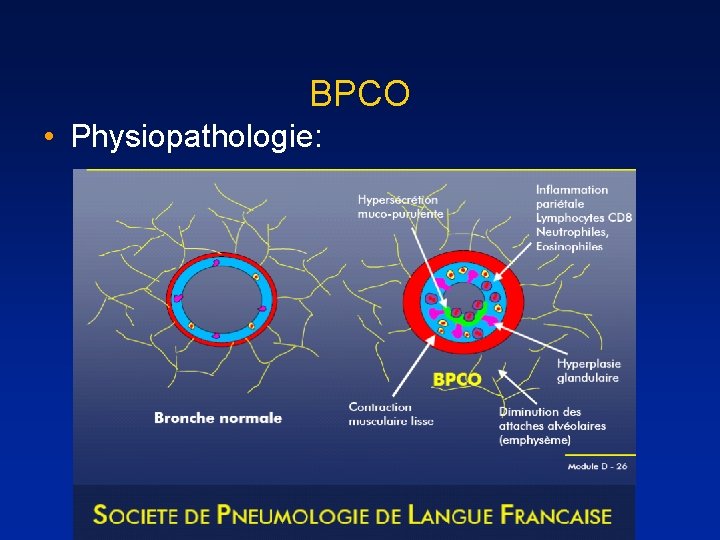
BPCO • Physiopathologie:
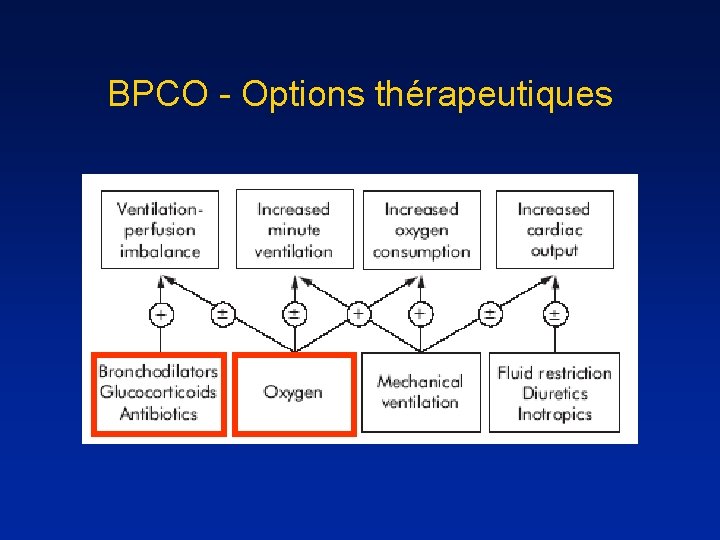
BPCO - Options thérapeutiques

Traitement BPCO aux Urgences Traitement conventionnel – Première ligne : BD inhalés β 2+, +/- Antichol ? – Deuxième ligne : Corticoïdes (45%), ATB – Comment on fait aux Urgences…

Caractéristiques au SAU • N = 780 • 72 ans, H = 70% • Tabac = 80%, BPCO connue = 84% • FR = 26/ • β 2+ = 90% aux Urgences

10% sortis du SAU 11% admis en réa 7% de décès

Les bronchodilatateurs diminuent la distension • amélioration de la dyspnée Ramirez-Venagas et al, Chest 1997 • diminution du travail respiratoire Mancebo et al. Am Rev Respir Dis 1991 • amélioration de la performance diaphragmatique Hatipoglu et al. , AJRCCM 1999 • amélioration de l’endurance à l’effort 0’Donnell et al. Am J Respir Crit Care Dis 1999 • diminution des asynchronies patientventilateur • diminution de l’insevrabilité



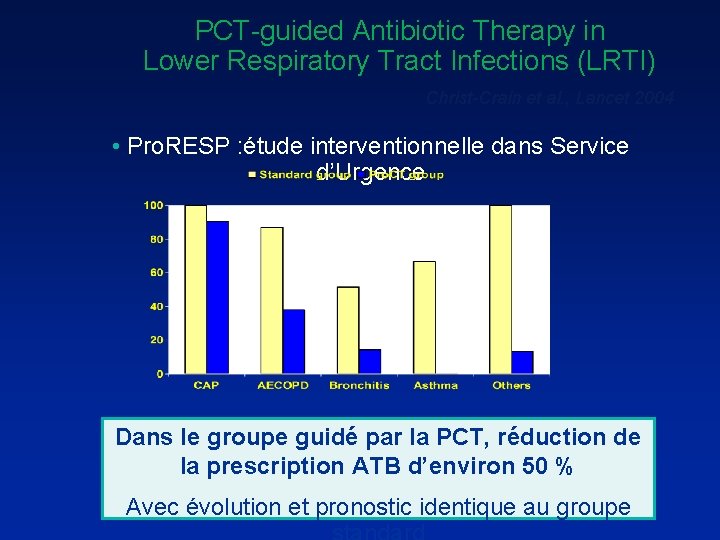
PCT-guided Antibiotic Therapy in Lower Respiratory Tract Infections (LRTI) Christ-Crain et al. , Lancet 2004 • Pro. RESP : étude interventionnelle dans Service d’Urgence Dans le groupe guidé par la PCT, réduction de la prescription ATB d’environ 50 % Avec évolution et pronostic identique au groupe


BPCO – Stéroides et ATB • Pas de niveau de preuve suffisante pour Donner dès les Urgences des CTS per os ou IV Etiologie difficile à trouver EP : 20% quand l’étiologie de l’exacerbation n’est pas évidente ou chez les patients admis pour BPCO) Infection difficile à diagnostiquer Etudes evidence based medicine encore nécessaires pour ATB

BPCO - VNI • VNI et décompensation aiguë de BPCO: - 15 essais randomisés et 4 méta-analyses Peter JV et al. Crit Care Med – 2002 – Keenan SP et al. Ann Intern Med – 2003 – Lightowlet JV et al. Br J Med – 2003 – Ram FS et al. Cockrane – 2005 - VNI – – Diminue la FR et la dyspnée Améliore le p. H Diminue l’incidence de l’intubation de 60 % Diminue la mortalité de 50%

BPCO

BPCO

BPCO • Critères associés à un risque d’échec accru de la VNI
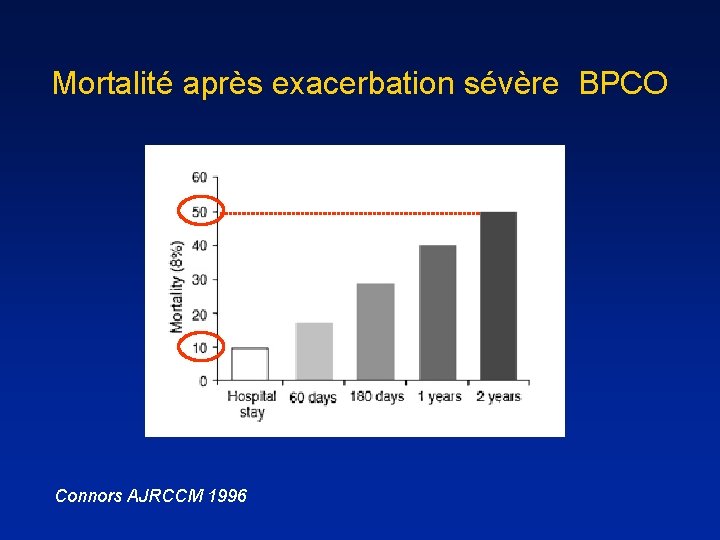
Mortalité après exacerbation sévère BPCO Connors AJRCCM 1996
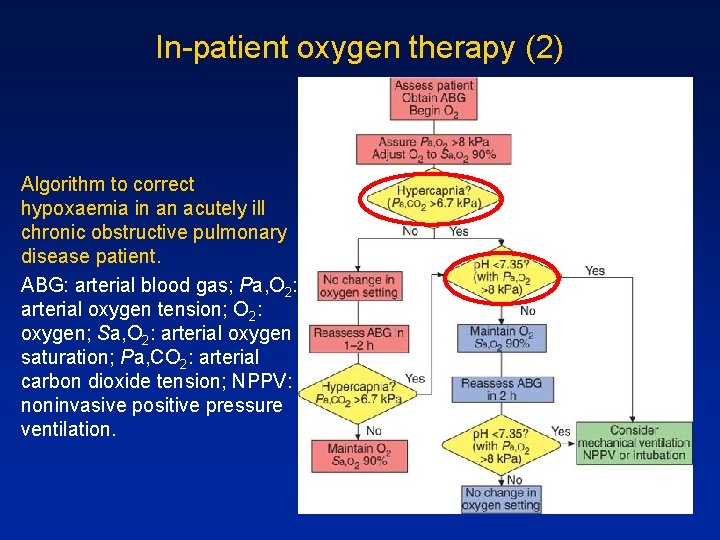
In-patient oxygen therapy (2) Algorithm to correct hypoxaemia in an acutely ill chronic obstructive pulmonary disease patient. ABG: arterial blood gas; Pa, O 2: arterial oxygen tension; O 2: oxygen; Sa, O 2: arterial oxygen saturation; Pa, CO 2: arterial carbon dioxide tension; NPPV: noninvasive positive pressure ventilation.
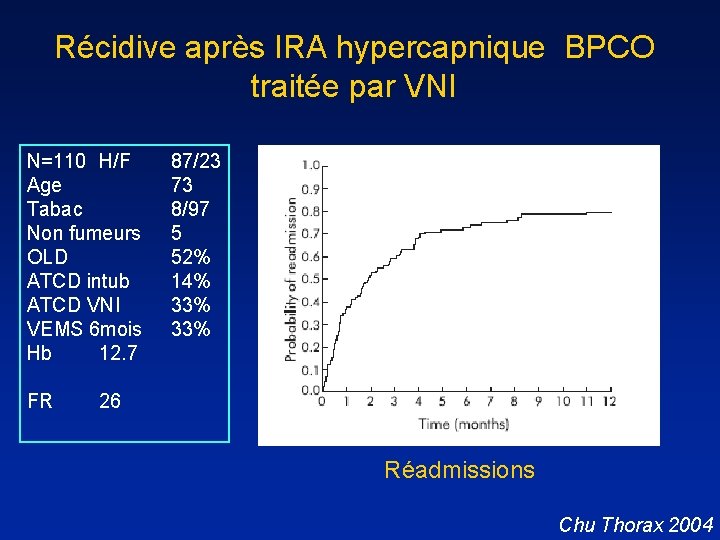
Récidive après IRA hypercapnique BPCO traitée par VNI N=110 H/F Age Tabac Non fumeurs OLD ATCD intub ATCD VNI VEMS 6 mois Hb 12. 7 FR 87/23 73 8/97 5 52% 14% 33% 26 Réadmissions Chu Thorax 2004
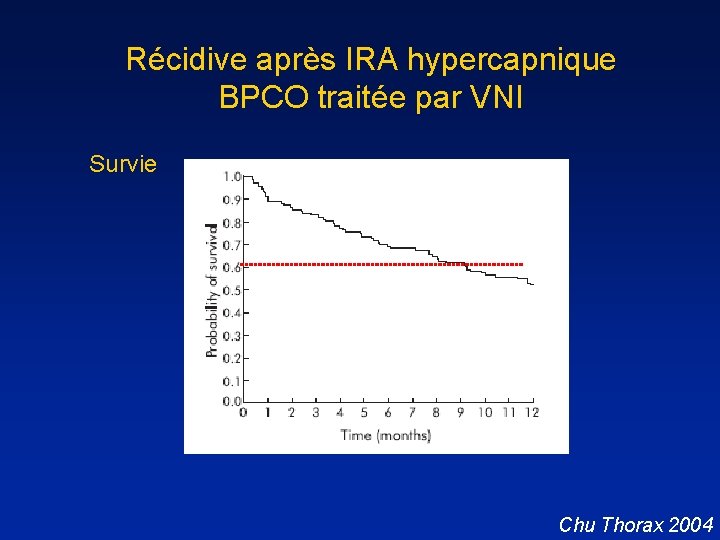
Récidive après IRA hypercapnique BPCO traitée par VNI Survie Chu Thorax 2004

Oxygénothérapie – Points clés § Objectif Sa. O 2 > 90% § Sonde nasale ou masque Venturi § GDS Pa. O 2, Pa. CO 2, p. H § Sp. O 2 oxymétrie de pouls ajustement O 2 § Prévention hypoxie tissulaire > crainte de rétention CO 2 § Si rétention CO 2 vérifier p. H § Si acidose considérer ventilation mécanique

Bronchodilatateurs inhalés prioritaires § Inhaled bronchodilators (particularly inhaled ß 2 -agonists with or without anticholinergics) and oral glucocortico-steroids are effective treatments for exacerbations of COPD (Evidence A - GOLD). § Salbutamol/terbutaline inhalés ± ipratropium § augmentation des débits § diminution de la distension +++ § amélioration travail des muscles respiratoires

Management Moderate/severe COPD exacerbations www. goldcopd. org

Traitement du Facteur déclenchant ! § The most common causes of an exacerbation are infection of the tracheobronchial tree and air pollution, but the cause of about one-third of severe exacerbations cannot be identified (Evidence B - GOLD). § 30 -40% pas de cause retrouvée § Patients experiencing COPD exacerbations with clinical signs of airway infection (e. g. , increased sputum purulence) may benefit from antibiotic treatment (Evidence B). § Antibiotiques en cas d’expectoration purulente

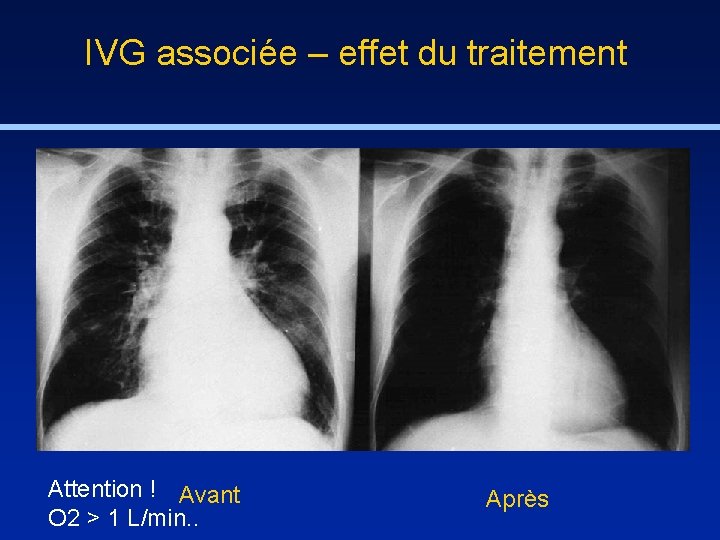
IVG associée – effet du traitement Attention ! Avant O 2 > 1 L/min. . Après
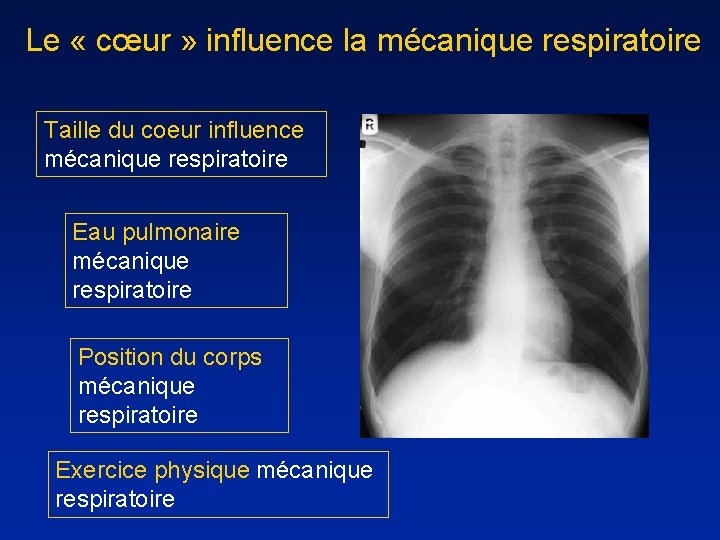
Le « cœur » influence la mécanique respiratoire Taille du coeur influence mécanique respiratoire Eau pulmonaire mécanique respiratoire Position du corps mécanique respiratoire Exercice physique mécanique respiratoire

Ventilation non invasive Le plus souvent proposée en cas d IRA avec au moins deux des trois critères suivants: • tachypnée (supérieure à 25/min. ) • hypoxémie (saturation inférieure à 90 %) • acidose p. H < 7, 35 respiratoire (Pa. CO 2 > 45 mm. Hg) contre-indiquée - gravité extrême, coma, choc (intubation trachéale) - Vomissements - dysmorphie faciale majeure elle diminue le recours secondaire à l ’intubation trachéale, l ’incidence des infections nosocomiales, la morbidité et la mortalité en réanimation et à l ’hôpital
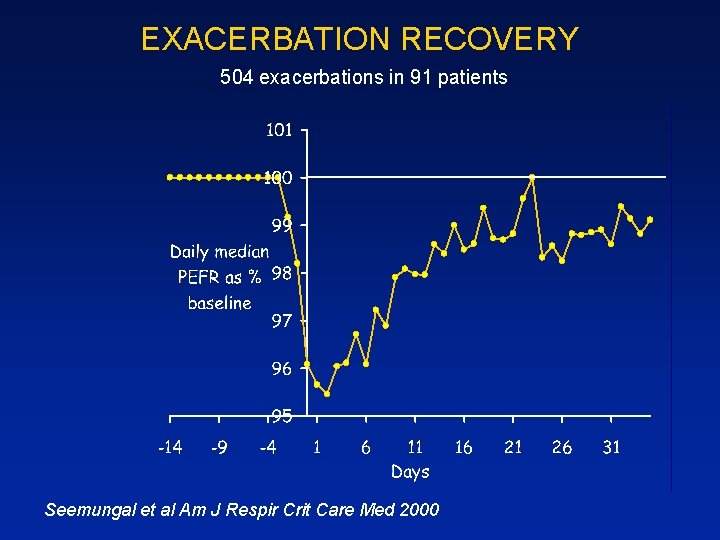
EXACERBATION RECOVERY 504 exacerbations in 91 patients Seemungal et al Am J Respir Crit Care Med 2000
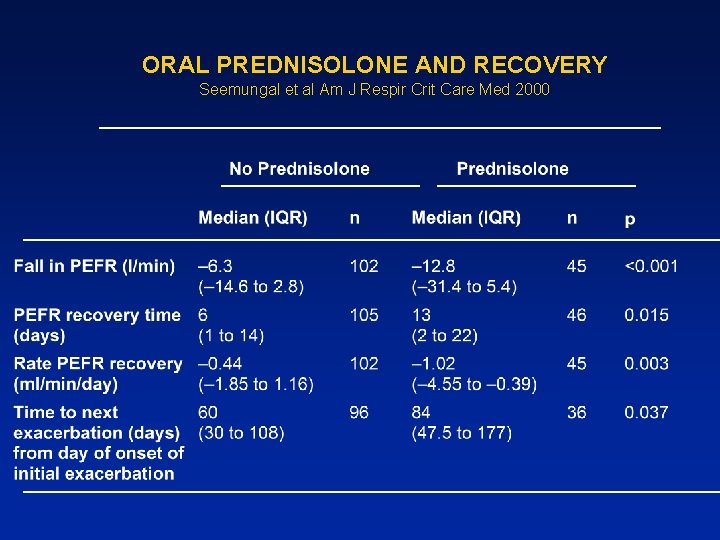
ORAL PREDNISOLONE AND RECOVERY Seemungal et al Am J Respir Crit Care Med 2000

Four Components of COPD Management 1. Assess and monitor disease 2. Reduce risk factors 3. Manage stable COPD Revised 2006 l Education l Pharmacologic l Non-pharmacologic 4. Manage exacerbations

Management COPD Exacerbations Key Points An exacerbation of COPD is defined as: “An event in the natural course of the disease characterized by a change in the patient’s baseline dyspnea, cough, and/or sputum that is beyond normal day-to-day variations, is acute in onset, and may warrant a change in regular medication in a patient with underlying COPD. ”

Management COPD Exacerbations Key Points § § Fréquent et personnes âgées +++ § § Etiologie pas évidente (EP) 20% BPCO méconnue, réseau pneumo au décours ? En dehors des B 2+, pas de stéroides ou ATB PCT utile pour guider la mise en route d’ATB VNI +++ VS en AI-PEP, mais nécessite formation

Conclusions • 2 entités cliniques avec physiopathologie ≈ proche • BPCO: VNI +++ ( effet prouvé sur mortalité) • AAG: TTT médical (nébulisation 2 agonistes corticoïdes) (+ BA + Mag) si gravité +++: IOT + VM
- Slides: 90