XENOBIOTICI Composti estranei allorganismo Contaminanti ambientali assorbiti attraverso

XENOBIOTICI Composti estranei all’organismo Contaminanti ambientali assorbiti attraverso la pelle, i polmoni o introdotti con l’alimentazione Prodotti chimici industriali (pesticidi, inquinanti) Prodotti di pirolisi della cottura dei cibi Alcaloidi (sostanze azotate prodotte nelle piante a partire da aacidi aromatici) metaboliti secondari delle piante Tossine prodotte da funghi, piante, animali Farmaci Gli xenobiotici sono SOSTANZE LIPOFILICHE
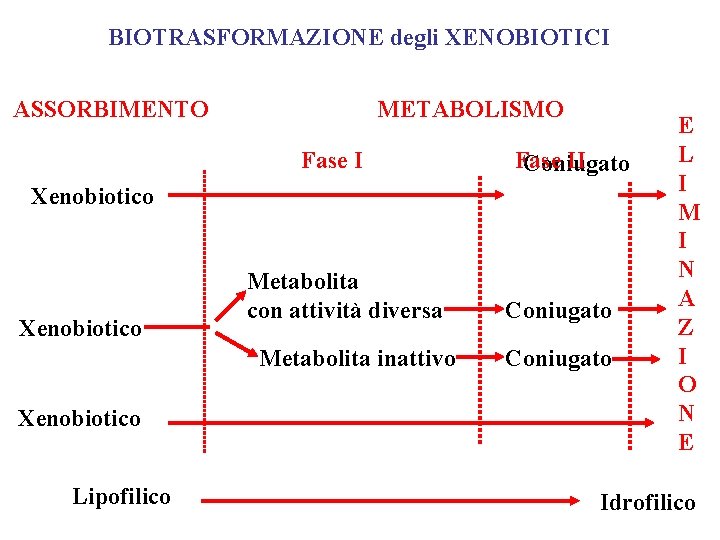
BIOTRASFORMAZIONE degli XENOBIOTICI ASSORBIMENTO METABOLISMO Fase II Coniugato Xenobiotico Metabolita con attività diversa Metabolita inattivo Xenobiotico Lipofilico Coniugato E L I M I N A Z I O N E Idrofilico

Enzimi del metabolismo degli xenobiotici Tipi di reazioni Enzima Fase I Ossidazione Citocromo P 450 Alcol deidrogenasi Aldeide deidrogenasi Monossigenasi flaviniche Monoaminossidasi Riduzione Chinone reduttasi (DT diaforasi) Citocromo P 450 reduttasi Idrolisi Epossido idrolasi Fase II Coniugazione UDP glucuronil transferasi Solfotransferasi N-acetil transferasi Metiltransferasi Coniugazione con amminoacidi Glutatione transferasi
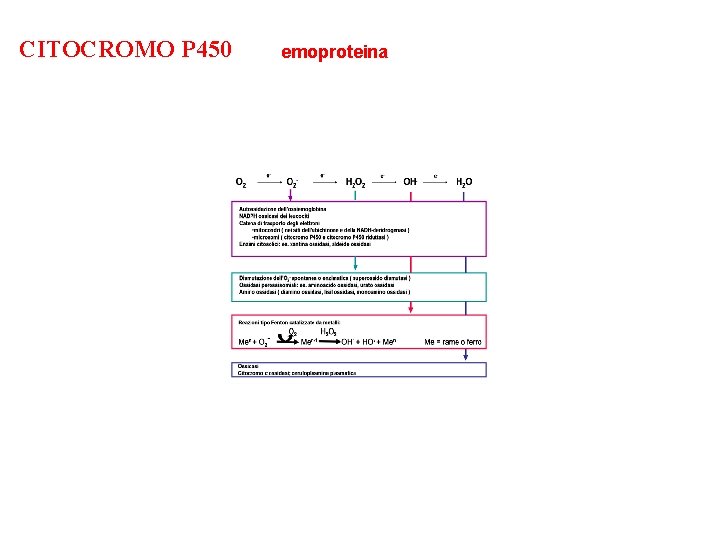
CITOCROMO P 450 emoproteina
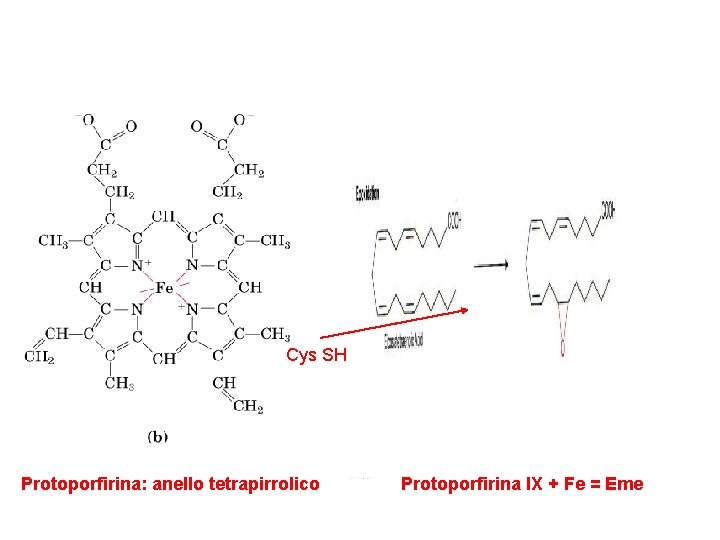
Cys SH Protoporfirina: anello tetrapirrolico Protoporfirina IX + Fe = Eme


Il Cyt P 450 assorbe a 450 nm quando il Ferro è nello stato ridotto (Fe 2+) e legato al CO (monossido di carbonio)
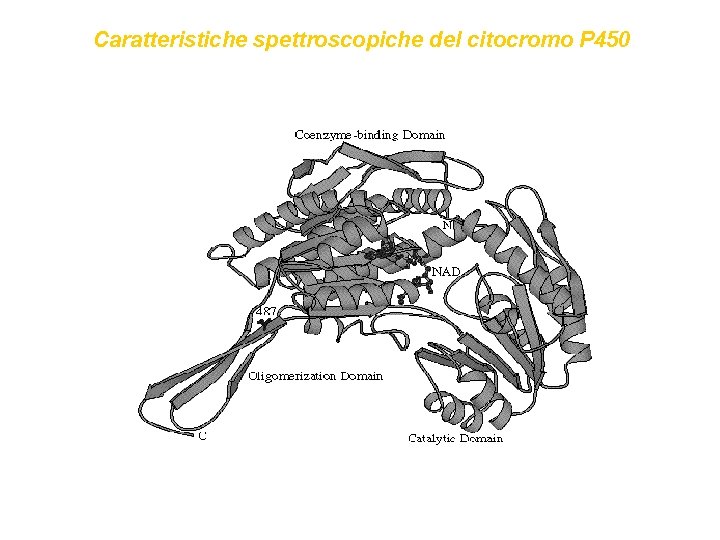
Caratteristiche spettroscopiche del citocromo P 450

Localizzazione intracellulare Il citocromo P 450 degli eucarioti è ancorato alle membrane Microsomiale e mitocondriale Gli enzimi P 450 predisposti al metabolismo degli xenobiotici si trovano soprattutto nel reticol endoplasmatico del fegato Il citocromo P 450 microsomiale è legato alla membrana del reticolo endoplasmatico tramite la regione N-term idrofobica che genera un’elica transmembrana.

Reazione catalizzata dal P 450 Il citocromo P 450 è una ossidasi a funzione mista (monossigenasi) XH + O 2 + NAD(P)H + H+ XOH + NAD(P)+ + H 2 O X = Substrato

SUBSTRATI DEL CITOCROMO P 450 Xenobiotici Farmaci, inclusi antibiotici Carcinogeni Antiossidanti Solventi Anestetici Coloranti Pesticidi Derivanti del petrolio Alcol Odori Composti di origine fisiologica Colesterolo, Steroidi Eicosanoidi (leucotrieni, prostaglandine) Acidi grassi Idroperossidi dei lipidi Retinoidi (vitamina A) Acetone
Sistema di trasporto degli elettroni del citocromo P 450 • Uno dei problemi : il ferro-eme del gruppo prostetico può accettare un elettrone alla volta mentre l’NADPH trasferisce generalmente due elettroni • Per cui è necessaria una proteina che prende due elettroni dall’NADPH e ne trasferisce uno al citocromo P 450 • Questa funzione è svolta da una flavoproteina NADPH-dipendente • Il sistema di trasporto degli elettroni dall’ NADPH al citocromo P 450 si trova associato con le membrane mitocondriali o del reticolo endoplasmatico

Sistema di trasporto microsomiale del citocromo P 450 • Nel reticolo endoplasmatico l’NADPH dona gli elettroni ad una flavoproteina denominata NADPH-citocromo P 450 reduttasi • Peso molecolare di 78 k. Da • Contiene sia il FAD che l’FMN come gruppi prostetici • N-terminale contiene numerosi residui idrofobici ed è la parte associata alla membrana 1. Il FAD prende elettroni dall’NADPH 2. L’FMN li dona al ferro 3. Gli elettroni possono derivare dal citocromo b 5 4. Il citocromo b 5 è ridotto: - NADPH-citocromo P 450 red - NADH-citocromo b 5 red
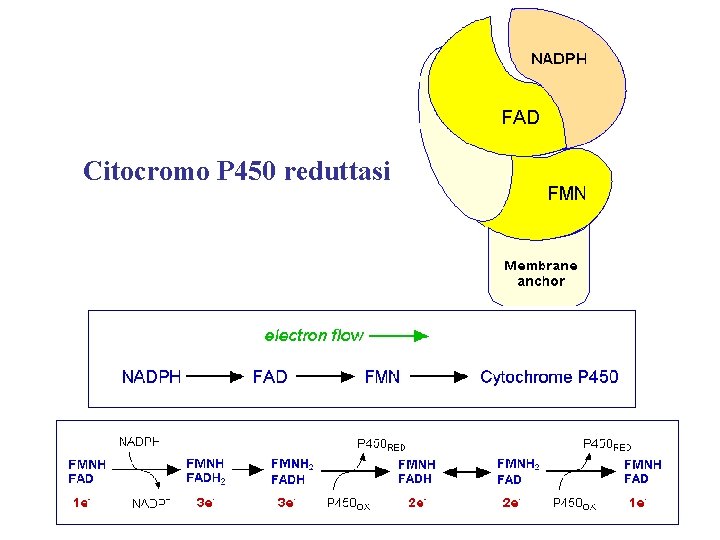
Citocromo P 450 reduttasi

Sistema di trasporto microsomiale del citocromo P 450 S SOH Non si conosce la ragione dell’esistenza delle due vie
H 2 O 2 O 2. S.
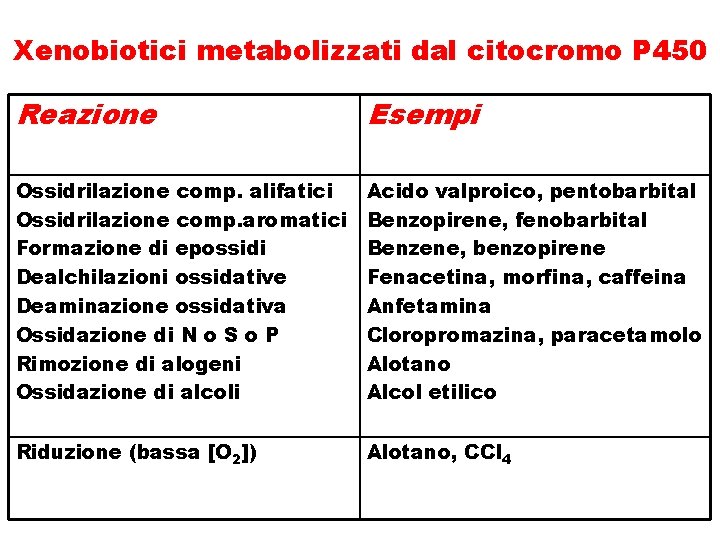
Xenobiotici metabolizzati dal citocromo P 450 Reazione Esempi Ossidrilazione comp. alifatici Ossidrilazione comp. aromatici Formazione di epossidi Dealchilazioni ossidative Deaminazione ossidativa Ossidazione di N o S o P Rimozione di alogeni Ossidazione di alcoli Acido valproico, pentobarbital Benzopirene, fenobarbital Benzene, benzopirene Fenacetina, morfina, caffeina Anfetamina Cloropromazina, paracetamolo Alotano Alcol etilico Riduzione (bassa [O 2]) Alotano, CCl 4
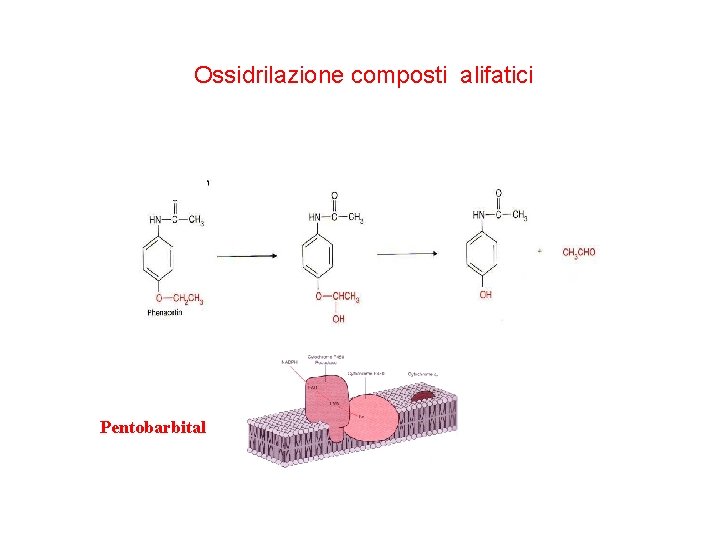
Ossidrilazione composti alifatici Pentobarbital
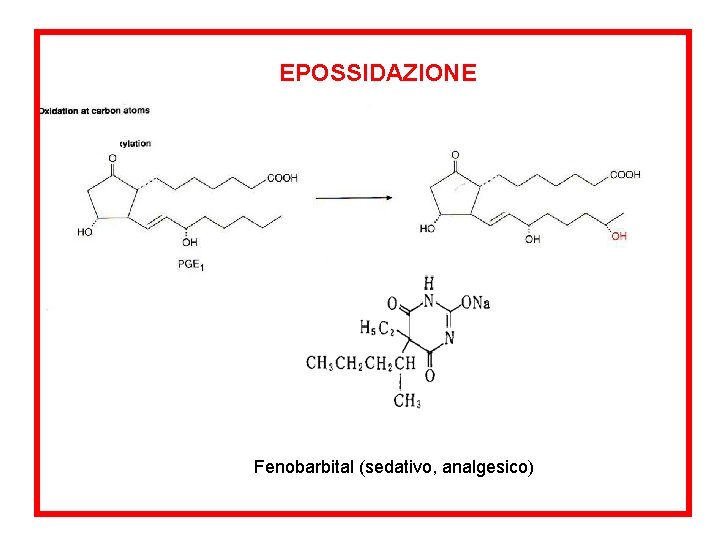
EPOSSIDAZIONE Fenobarbital (sedativo, analgesico)

cancerogeno
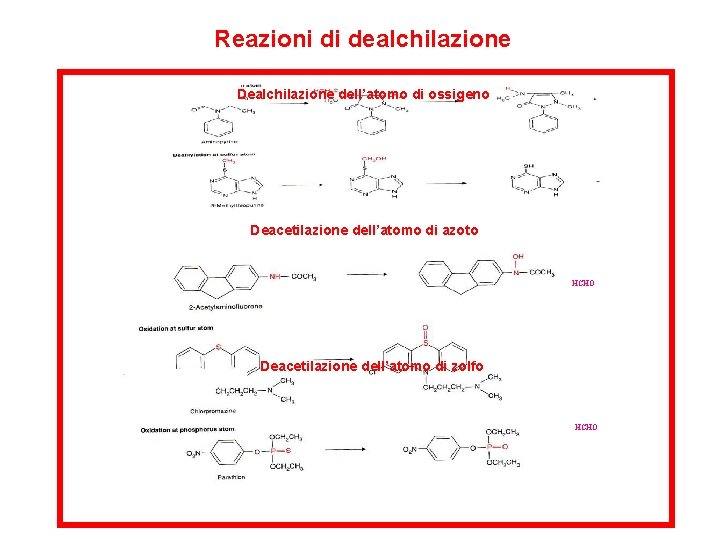
Reazioni di dealchilazione Dealchilazione dell’atomo di ossigeno Deacetilazione dell’atomo di azoto HCHO Deacetilazione dell’atomo di zolfo HCHO
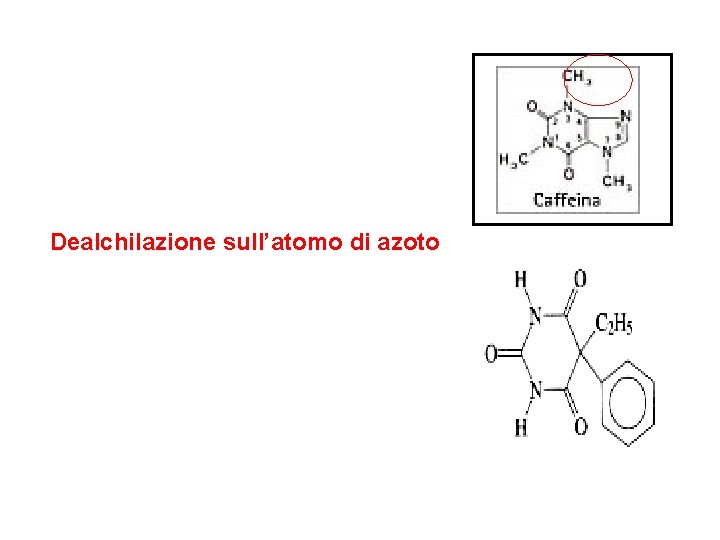
Dealchilazione sull’atomo di azoto
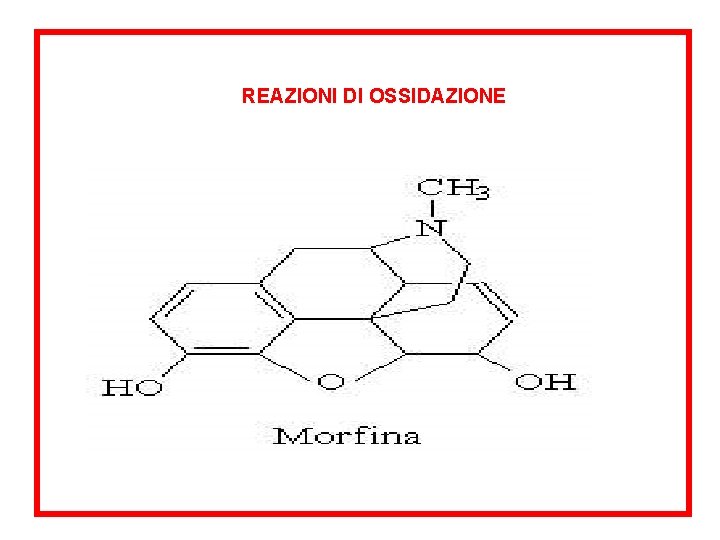
REAZIONI DI OSSIDAZIONE
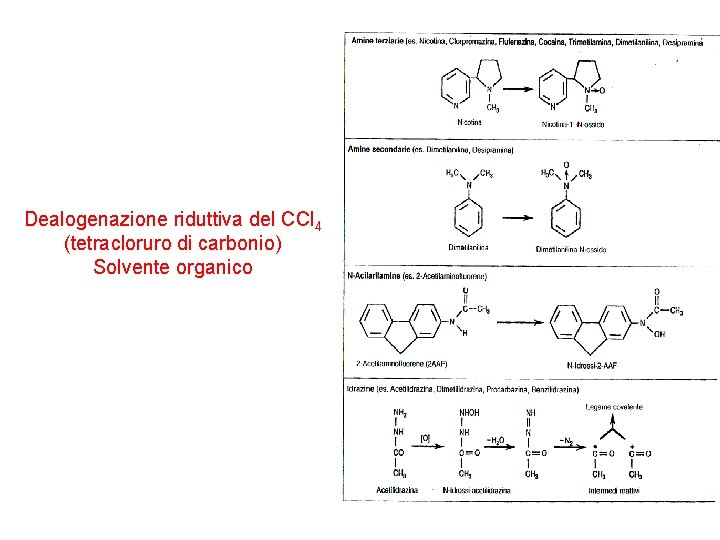
Dealogenazione riduttiva del CCl 4 (tetracloruro di carbonio) Solvente organico
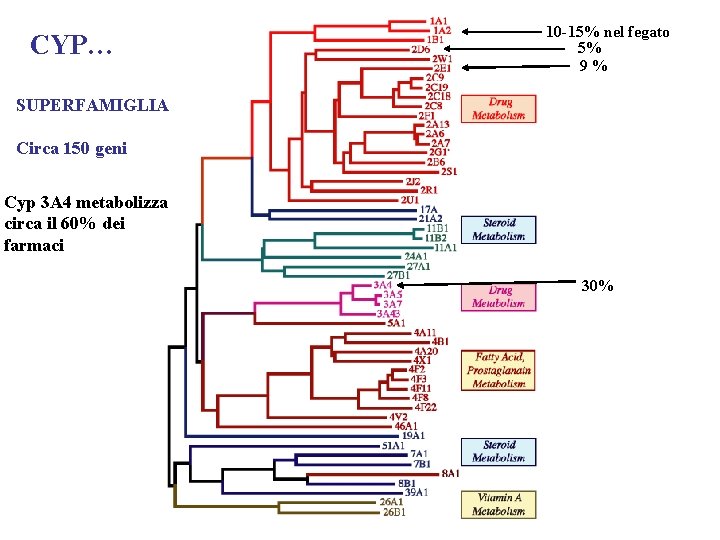
CYP… 10 -15% nel fegato 5% 9% SUPERFAMIGLIA Circa 150 geni Cyp 3 A 4 metabolizza circa il 60% dei farmaci 30%

Farmacogenetica: basi ereditarie delle differenze tra gli individui nell’azione dei farmaci Fenotipi del CYP 2 D 6 “ polimorfismo per la debrisochina” Metabolizzatori Lenti (PM): incapacità di utilizzare la via del CYP 2 D 6 Metabolizzatori Intermedi (IM): capacità fortemente diminuita Metabolizzatori Normali (EM): capacità normale Metabolizzatori Ultrarapidi (UM): capacità eccessiva

Induttori del P 450: appartengono a 5 classi, con diverso meccanismo d’azione • 3 - metilcolantrene, benzopirene, diossina, fumo alimenti cotti a carbone, crocifere • Fenobarbital, DTT • Isoniazide, etanolo • Steroidi, antibiotici • Clofibrato, plastificanti CYP 1 A 1, CYP 1 A 2 CYP 2 B 1, CYP 2 B 2 CYP 2 E 1 CYP 3 A 1, CYP 3 A 2 CYP 4 A 1, CYP 4 A 2, CYP 4 A 3
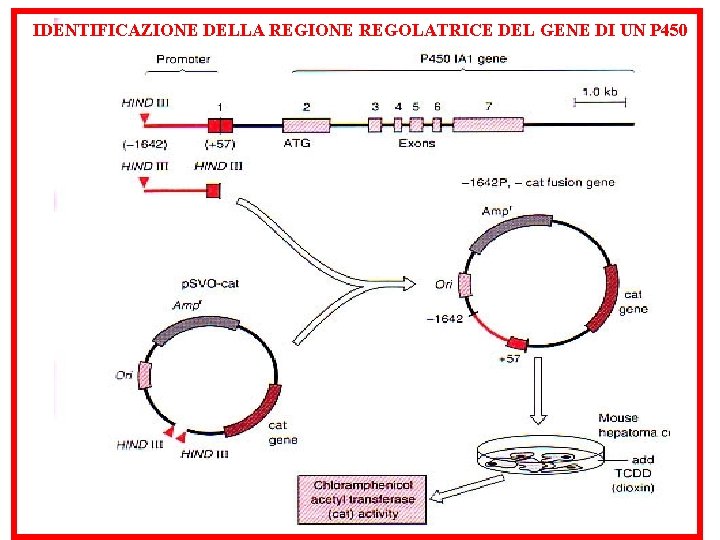
IDENTIFICAZIONE DELLA REGIONE REGOLATRICE DEL GENE DI UN P 450
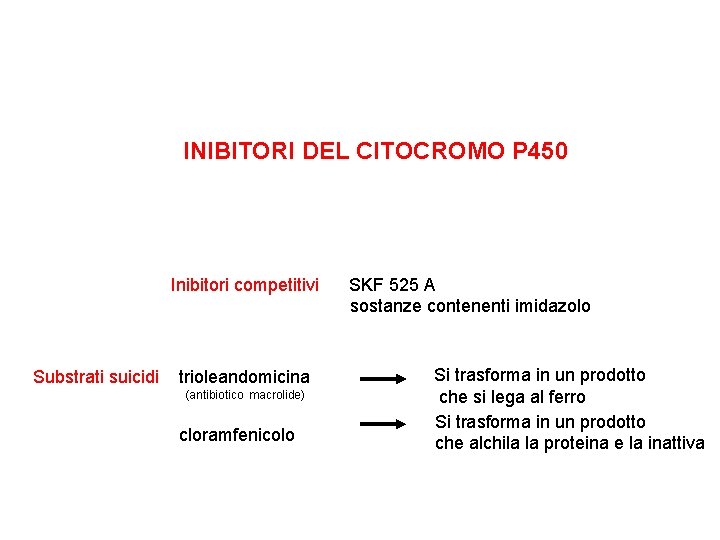
INIBITORI DEL CITOCROMO P 450 Inibitori competitivi Substrati suicidi trioleandomicina (antibiotico macrolide) cloramfenicolo SKF 525 A sostanze contenenti imidazolo Si trasforma in un prodotto che si lega al ferro Si trasforma in un prodotto che alchila la proteina e la inattiva
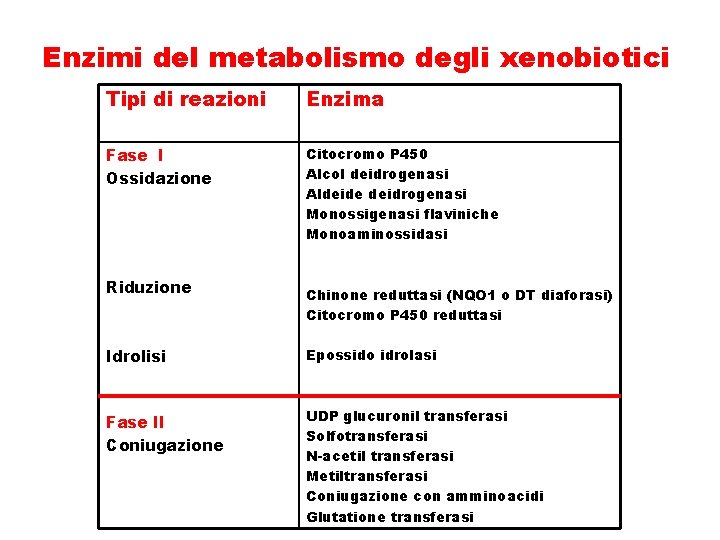
Enzimi del metabolismo degli xenobiotici Tipi di reazioni Enzima Fase I Ossidazione Citocromo P 450 Alcol deidrogenasi Aldeide deidrogenasi Monossigenasi flaviniche Monoaminossidasi Riduzione Chinone reduttasi (NQO 1 o DT diaforasi) Citocromo P 450 reduttasi Idrolisi Epossido idrolasi Fase II Coniugazione UDP glucuronil transferasi Solfotransferasi N-acetil transferasi Metiltransferasi Coniugazione con amminoacidi Glutatione transferasi
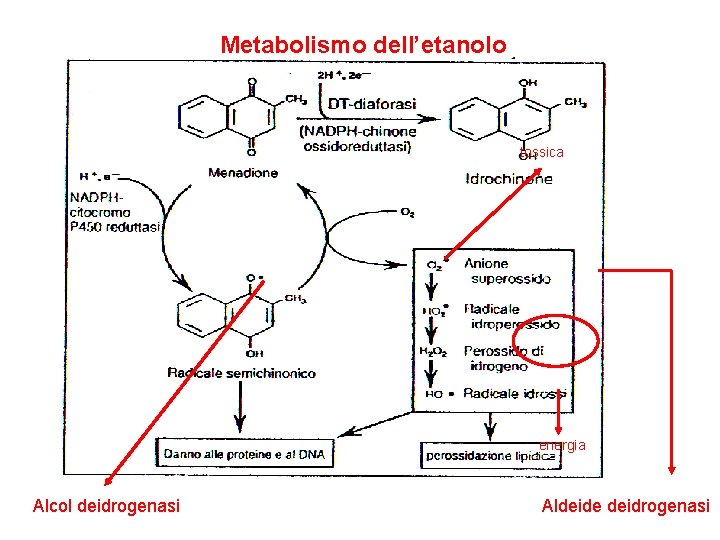
Metabolismo dell’etanolo tossica energia Alcol deidrogenasi Aldeide deidrogenasi
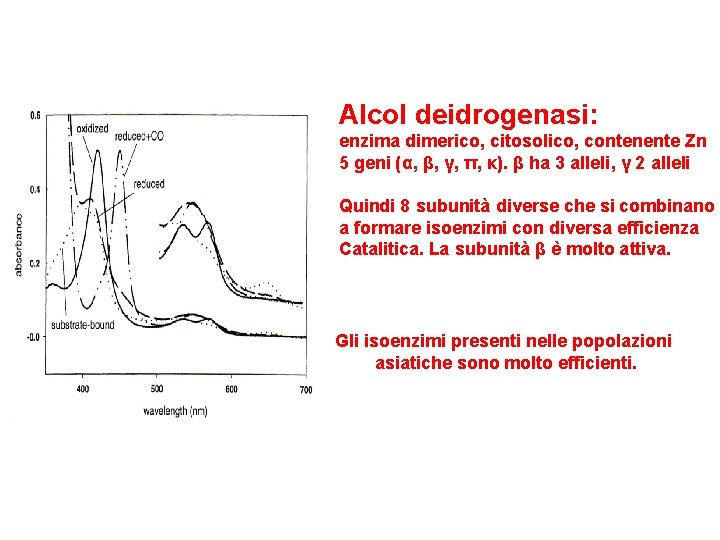
Alcol deidrogenasi: enzima dimerico, citosolico, contenente Zn 5 geni (α, β, γ, π, κ). β ha 3 alleli, γ 2 alleli Quindi 8 subunità diverse che si combinano a formare isoenzimi con diversa efficienza Catalitica. La subunità β è molto attiva. Gli isoenzimi presenti nelle popolazioni asiatiche sono molto efficienti.

Aldeide deidrogenasi (16 geni, famiglia di proteine): Allele di classe 2: basso metabolismo delle aldeide, fattore di rischio per il cancro indotto da alcol Nelle popolazioni orientali: intolleranza all’alcol (vasodilatazione, “flushing syndrome”).
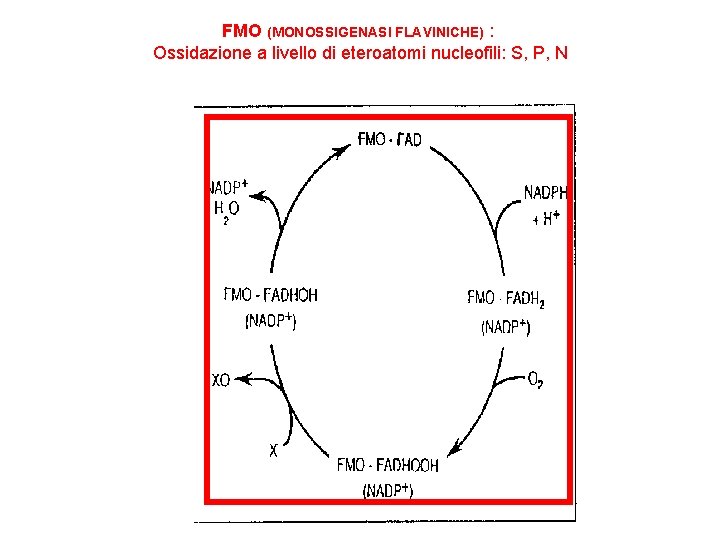
FMO (MONOSSIGENASI FLAVINICHE) : Ossidazione a livello di eteroatomi nucleofili: S, P, N

FMO: MONOSSIGENASI FLAVINICHE DEL RETICOLO ENDOPLASMATICO

Monoamminossidasi (MAO A e B) (flavoproteina mitocondriale) Trasformazione di una ammina in una aldeide (substrati fisiologici: serotonina, adrenalina, noradrenalina) RCH 2 NH 2 + FAD RCH=NH + FADH 2 RCH=NH + H 2 O RCHO + NH 3 FADH 2 + O 2 FAD + H 2 O 2 L’atomo di ossigeno incorporato nel substrato proviene dall’ H 2 O, ed i 2 elettroni sottratti al substrato vengono ceduti all’O 2 formando H 2 O 2
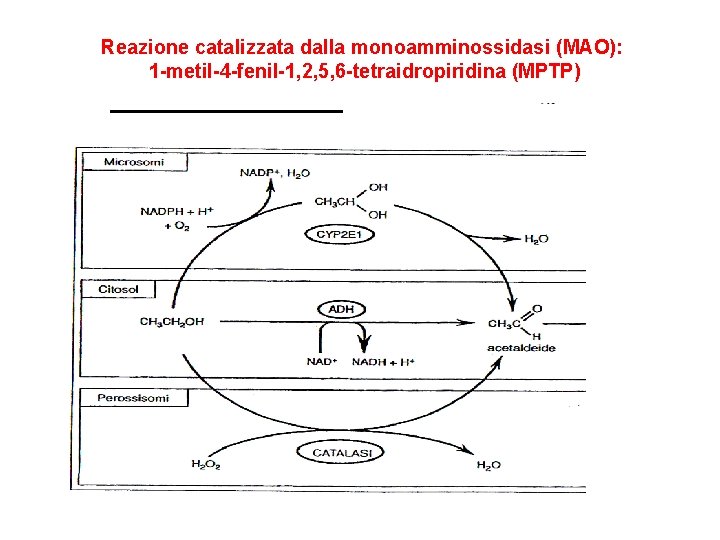
Reazione catalizzata dalla monoamminossidasi (MAO): 1 -metil-4 -fenil-1, 2, 5, 6 -tetraidropiridina (MPTP)

DT-diaforasi o NAD(P)H: chinone ossidoreduttasi 1 (NQO 1) §Enzima citosolico §Omodimero (27 k. Da per subunità) §Flavoproteina (FAD) §Catalizza la riduzione bielettronica di substrati di natura chinonica, in un singolo passaggio • Spesso i suoi livelli sono più alti nelle cellule tumorali (resistenza ai farmaci antitumorali)
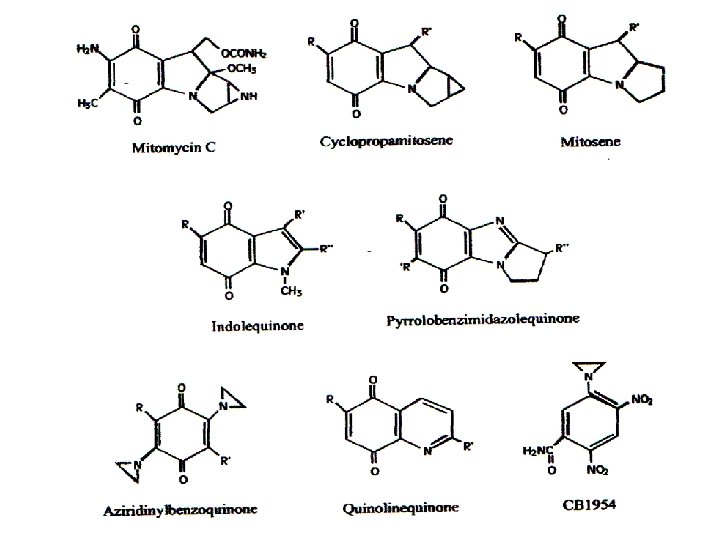

Farmaci antitumorali che vengono attivati dalla NQO 1





Prodotti di degradazione dei lipidi perossidati
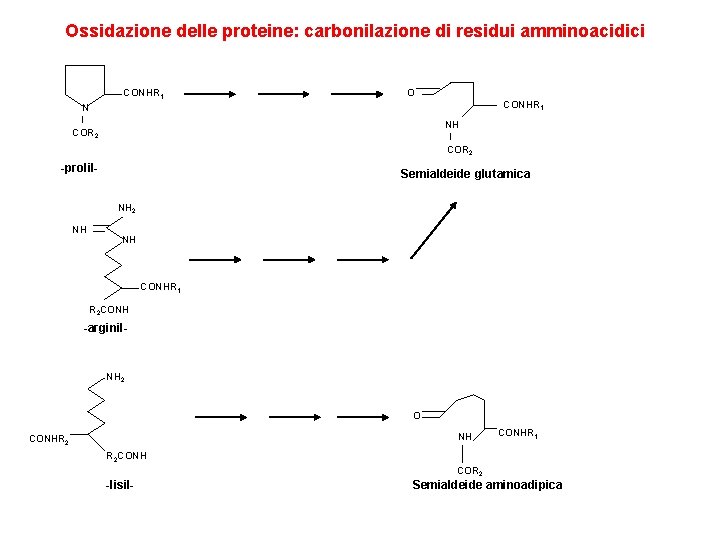
Ossidazione delle proteine: carbonilazione di residui amminoacidici CONHR 1 O CONHR 1 N NH COR 2 -prolil- Semialdeide glutamica NH 2 NH NH CONHR 1 R 2 CONH -arginil- NH 2 O NH CONHR 2 CONHR 1 R 2 CONH COR 2 -lisil- Semialdeide aminoadipica
- Slides: 46