BENZENE E COMPOSTI AROMATICI Il capostipite dei composti

BENZENE E COMPOSTI AROMATICI Il capostipite dei composti aromatici è il benzene: H H H Il benzene è formato da 6 atomi di C, ibridizzati sp 2, di conseguenza ha una struttura planare. Ogni atomo di C completa l’ottetto mediante legame con un atomo di H. Ogni angolo di legame misura 120° H Denominazione IUPAC: cicloesatriene Fu il chimico inglese Kekulè che per primo ha identificato la struttura del benezene nel 1865. Prima di allora qualsiasi composto che avesse un aroma era considerato aromatico. Oggi denominiamo “aromatici” solo quei composti che presentano una particolare configurazione elettronica. 1
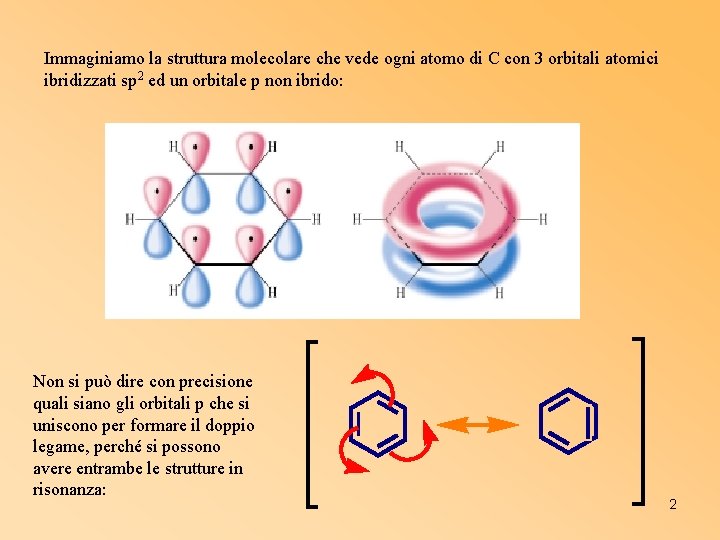
Immaginiamo la struttura molecolare che vede ogni atomo di C con 3 orbitali atomici ibridizzati sp 2 ed un orbitale p non ibrido: Non si può dire con precisione quali siano gli orbitali p che si uniscono per formare il doppio legame, perché si possono avere entrambe le strutture in risonanza: 2
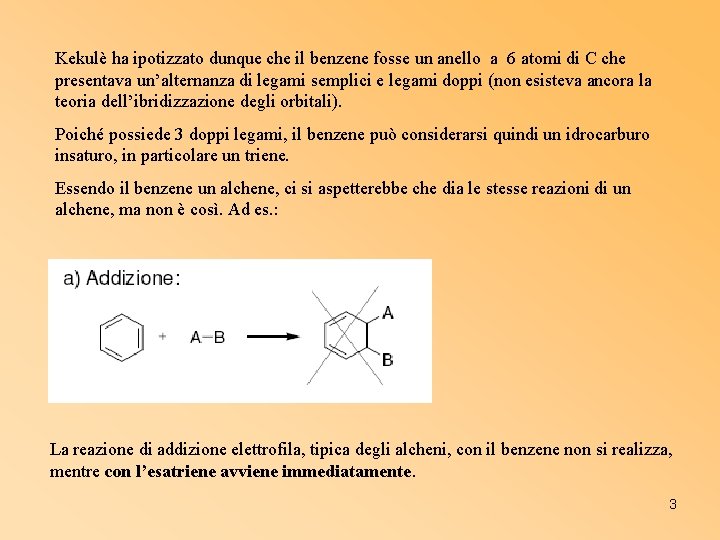
Kekulè ha ipotizzato dunque che il benzene fosse un anello a 6 atomi di C che presentava un’alternanza di legami semplici e legami doppi (non esisteva ancora la teoria dell’ibridizzazione degli orbitali). Poiché possiede 3 doppi legami, il benzene può considerarsi quindi un idrocarburo insaturo, in particolare un triene. Essendo il benzene un alchene, ci si aspetterebbe che dia le stesse reazioni di un alchene, ma non è così. Ad es. : La reazione di addizione elettrofila, tipica degli alcheni, con il benzene non si realizza, mentre con l’esatriene avviene immediatamente. 3
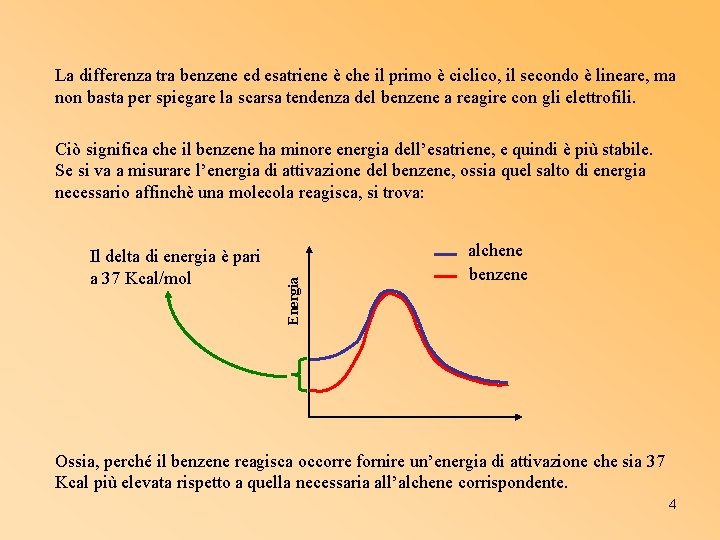
La differenza tra benzene ed esatriene è che il primo è ciclico, il secondo è lineare, ma non basta per spiegare la scarsa tendenza del benzene a reagire con gli elettrofili. Il delta di energia è pari a 37 Kcal/mol Energia Ciò significa che il benzene ha minore energia dell’esatriene, e quindi è più stabile. Se si va a misurare l’energia di attivazione del benzene, ossia quel salto di energia necessario affinchè una molecola reagisca, si trova: alchene benzene Ossia, perché il benzene reagisca occorre fornire un’energia di attivazione che sia 37 Kcal più elevata rispetto a quella necessaria all’alchene corrispondente. 4
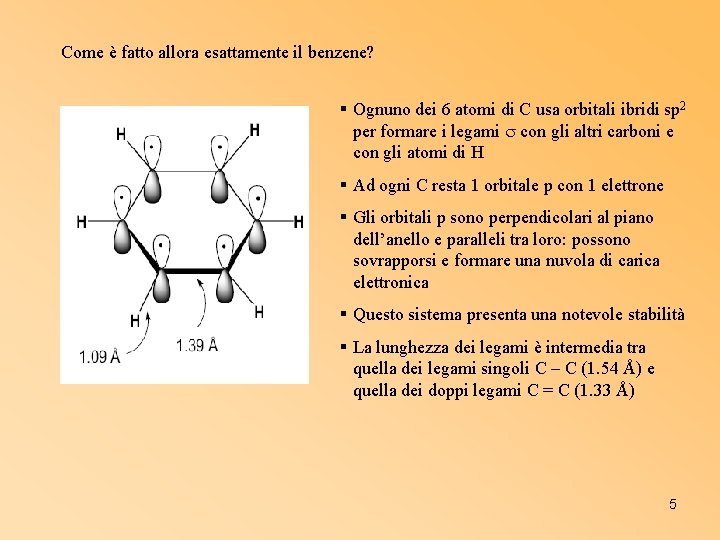
Come è fatto allora esattamente il benzene? § Ognuno dei 6 atomi di C usa orbitali ibridi sp 2 per formare i legami con gli altri carboni e con gli atomi di H § Ad ogni C resta 1 orbitale p con 1 elettrone § Gli orbitali p sono perpendicolari al piano dell’anello e paralleli tra loro: possono sovrapporsi e formare una nuvola di carica elettronica § Questo sistema presenta una notevole stabilità § La lunghezza dei legami è intermedia tra quella dei legami singoli C – C (1. 54 Å) e quella dei doppi legami C = C (1. 33 Å) 5

Il benzene, quindi, è molto meno reattivo rispetto all’esatriene, in quanto i 6 elettroni presenti nella nuvola elettronica sono delocalizzati. L’anello benzenico è dunque un anello “AROMATICO”. Il concetto di “Aromaticità” non è confinato solo al benzene, però perché un composto sia considerato aromatico è importante che sia presente una particolare configurazione elettronica. CRITERI PER L’AROMATICITA’: REGOLA DI HÜCKEL v Il sistema deve essere ciclico v Il sistema deve essere planare v Ogni atomo dell’anello deve far parte di un sistema π esteso v Il sistema π esteso deve contenere un ben preciso n° di elettroni π, e cioè: n° elettroni π = 4 n + 2 (n = numero intero: 0, 1, 2, 3, ecc. ), quindi in base al valore di n avremo, rispettivamente, 2, 6, 10, 14 elettroni, ecc. 8 elettroni p: non è aromatico 1 C non ha l’orbitale p: non è aromatico 6

Consideriamo l’anione del ciclo-pentadiene: ─ 2 1 5 ─ ─ 4 3 ─ ─ Questo anione è molto stabile, perché delocalizza la carica su 5 atomi di C. L’anione del ciclo-pentadiene è aromatico? Soddisfa la regola di Hückel? Sì, perchè la carica negativa consta di due elettroni, quindi 4 elettroni del ciclo + 2 elettroni della carica negativa = 6 elettroni (6 è un n° di elettroni consentito dalla regola di Hückel. Consideriamo adesso il carbocatione del ciclopentadiene. La carica positiva viene delocalizzata sempre su 5 atomi di C, ma il carbocatione del ciclopentadiene non è aromatico perché non possiede 6 elettroni ma 4 (la carica è assenza di elettroni) DELOCALIZZAZIONE NON EQUIVALE AD AROMATICITÀ. 7
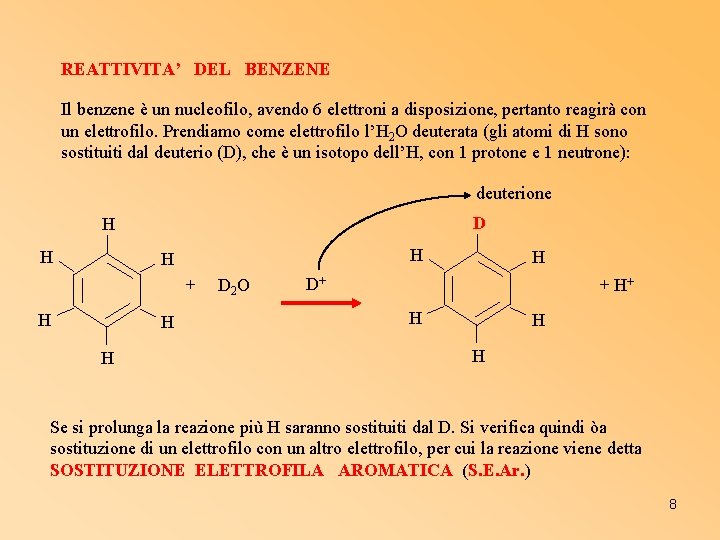
REATTIVITA’ DEL BENZENE Il benzene è un nucleofilo, avendo 6 elettroni a disposizione, pertanto reagirà con un elettrofilo. Prendiamo come elettrofilo l’H 2 O deuterata (gli atomi di H sono sostituiti dal deuterio (D), che è un isotopo dell’H, con 1 protone e 1 neutrone): deuterione D H H + H H H D 2 O H D+ + H+ H H H Se si prolunga la reazione più H saranno sostituiti dal D. Si verifica quindi òa sostituzione di un elettrofilo con un altro elettrofilo, per cui la reazione viene detta SOSTITUZIONE ELETTROFILA AROMATICA (S. E. Ar. ) 8
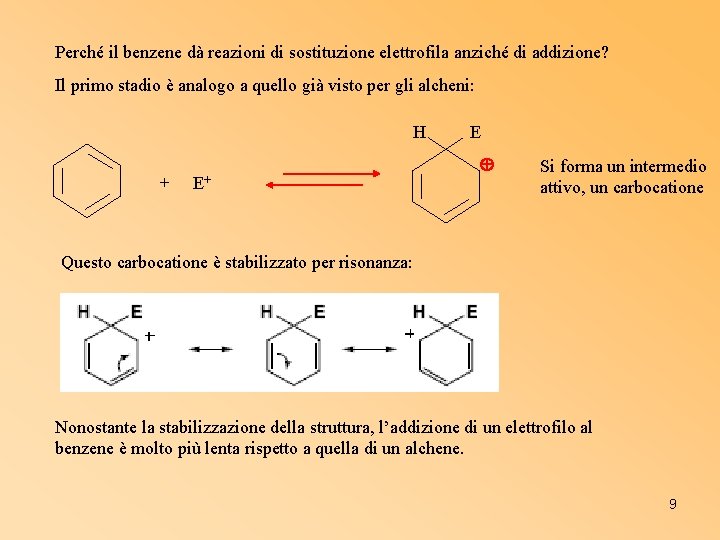
Perché il benzene dà reazioni di sostituzione elettrofila anziché di addizione? Il primo stadio è analogo a quello già visto per gli alcheni: H + E+ E Si forma un intermedio attivo, un carbocatione Questo carbocatione è stabilizzato per risonanza: Nonostante la stabilizzazione della struttura, l’addizione di un elettrofilo al benzene è molto più lenta rispetto a quella di un alchene. 9
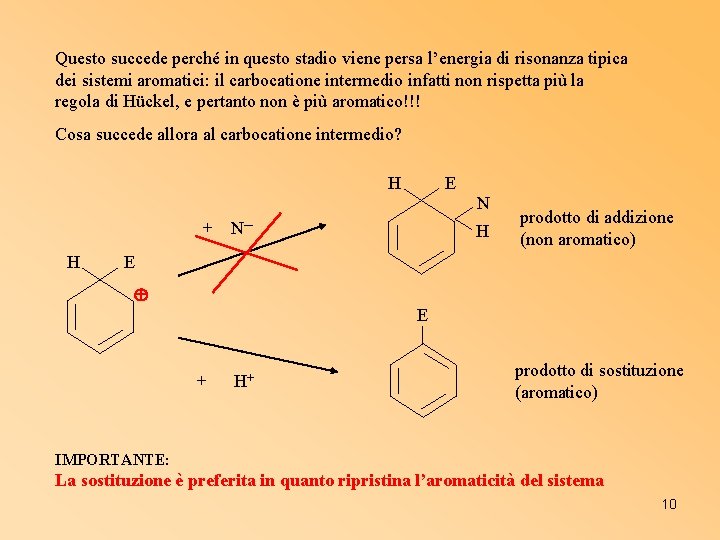
Questo succede perché in questo stadio viene persa l’energia di risonanza tipica dei sistemi aromatici: il carbocatione intermedio infatti non rispetta più la regola di Hückel, e pertanto non è più aromatico!!! Cosa succede allora al carbocatione intermedio? H E N + H N─ H prodotto di addizione (non aromatico) E E + H+ prodotto di sostituzione (aromatico) IMPORTANTE: La sostituzione è preferita in quanto ripristina l’aromaticità del sistema 10
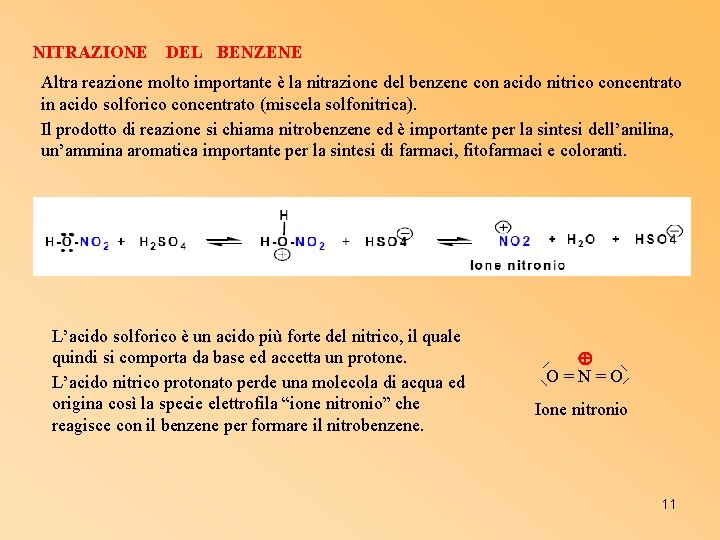
NITRAZIONE DEL BENZENE Altra reazione molto importante è la nitrazione del benzene con acido nitrico concentrato in acido solforico concentrato (miscela solfonitrica). Il prodotto di reazione si chiama nitrobenzene ed è importante per la sintesi dell’anilina, un’ammina aromatica importante per la sintesi di farmaci, fitofarmaci e coloranti. L’acido solforico è un acido più forte del nitrico, il quale quindi si comporta da base ed accetta un protone. L’acido nitrico protonato perde una molecola di acqua ed origina così la specie elettrofila “ione nitronio” che reagisce con il benzene per formare il nitrobenzene. O=N=O Ione nitronio 11
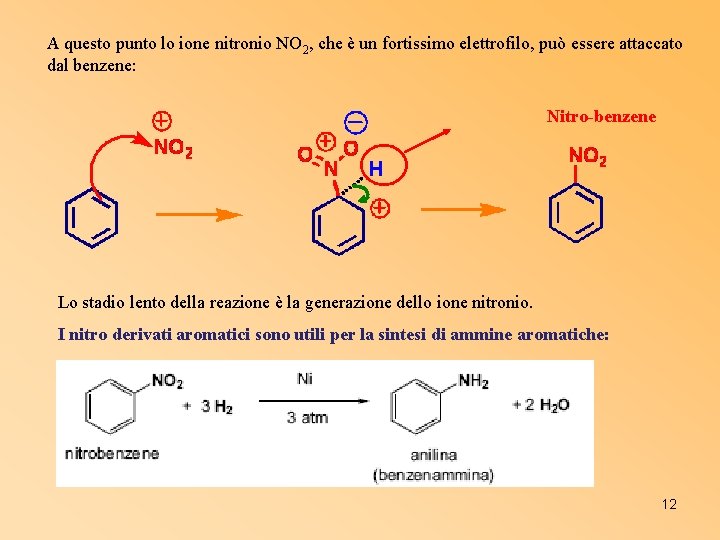
A questo punto lo ione nitronio NO 2, che è un fortissimo elettrofilo, può essere attaccato dal benzene: Nitro-benzene Lo stadio lento della reazione è la generazione dello ione nitronio. I nitro derivati aromatici sono utili per la sintesi di ammine aromatiche: 12
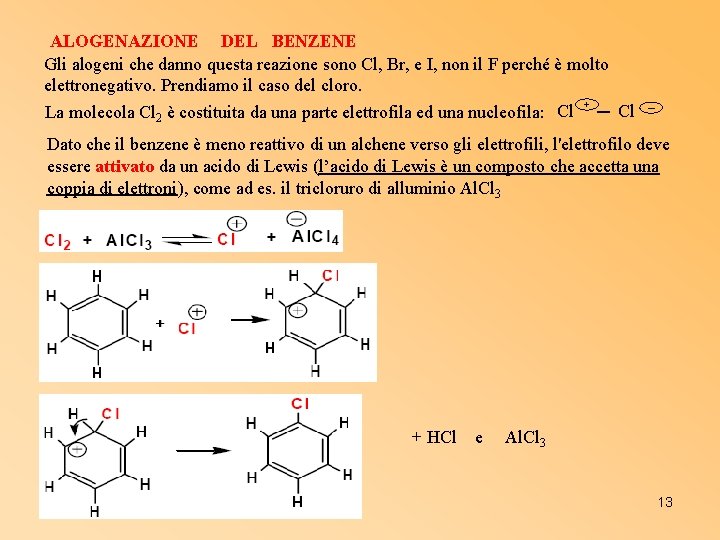
ALOGENAZIONE DEL BENZENE Gli alogeni che danno questa reazione sono Cl, Br, e I, non il F perché è molto elettronegativo. Prendiamo il caso del cloro. + La molecola Cl 2 è costituita da una parte elettrofila ed una nucleofila: Cl ─ Dato che il benzene è meno reattivo di un alchene verso gli elettrofili, l'elettrofilo deve essere attivato da un acido di Lewis (l’acido di Lewis è un composto che accetta una coppia di elettroni), come ad es. il tricloruro di alluminio Al. Cl 3 + HCl e Al. Cl 3 13
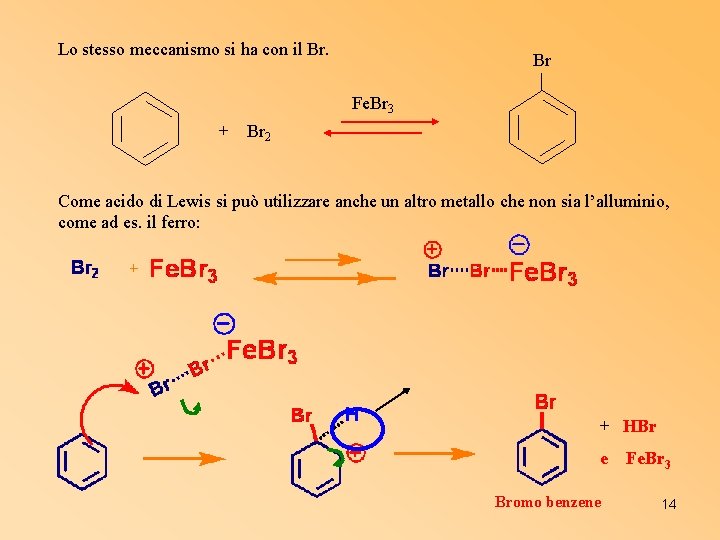
Lo stesso meccanismo si ha con il Br. Br Fe. Br 3 + Br 2 Come acido di Lewis si può utilizzare anche un altro metallo che non sia l’alluminio, come ad es. il ferro: + HBr e Bromo benzene Fe. Br 3 14
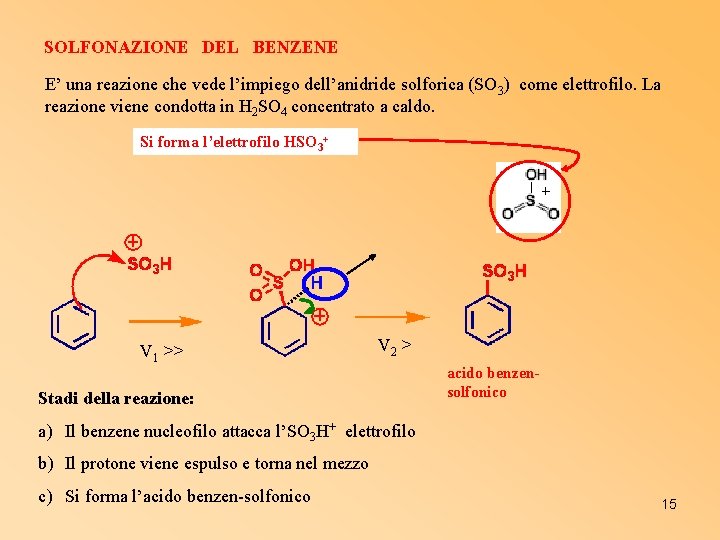
SOLFONAZIONE DEL BENZENE E’ una reazione che vede l’impiego dell’anidride solforica (SO 3) come elettrofilo. La reazione viene condotta in H 2 SO 4 concentrato a caldo. Si forma l’elettrofilo HSO 3+ V 1 >> V 2 > Stadi della reazione: acido benzensolfonico a) Il benzene nucleofilo attacca l’SO 3 H+ elettrofilo b) Il protone viene espulso e torna nel mezzo c) Si forma l’acido benzen-solfonico 15
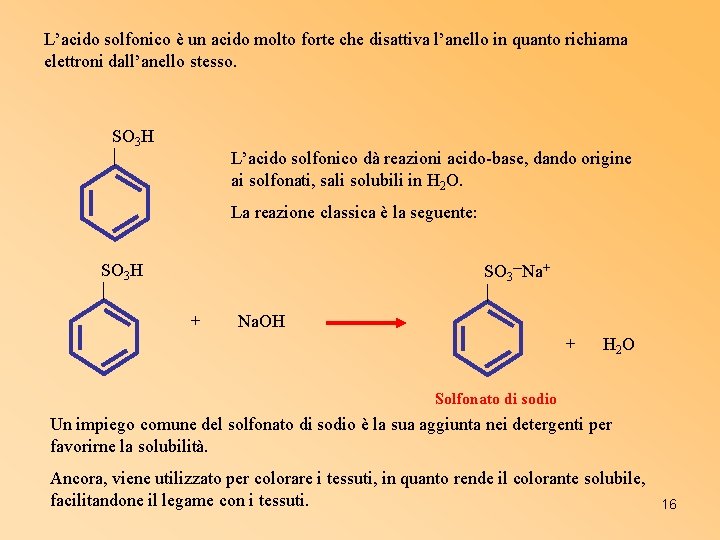
L’acido solfonico è un acido molto forte che disattiva l’anello in quanto richiama elettroni dall’anello stesso. SO 3 H L’acido solfonico dà reazioni acido-base, dando origine ai solfonati, sali solubili in H 2 O. La reazione classica è la seguente: SO 3 H SO 3─Na+ + Na. OH + H 2 O Solfonato di sodio Un impiego comune del solfonato di sodio è la sua aggiunta nei detergenti per favorirne la solubilità. Ancora, viene utilizzato per colorare i tessuti, in quanto rende il colorante solubile, facilitandone il legame con i tessuti. 16
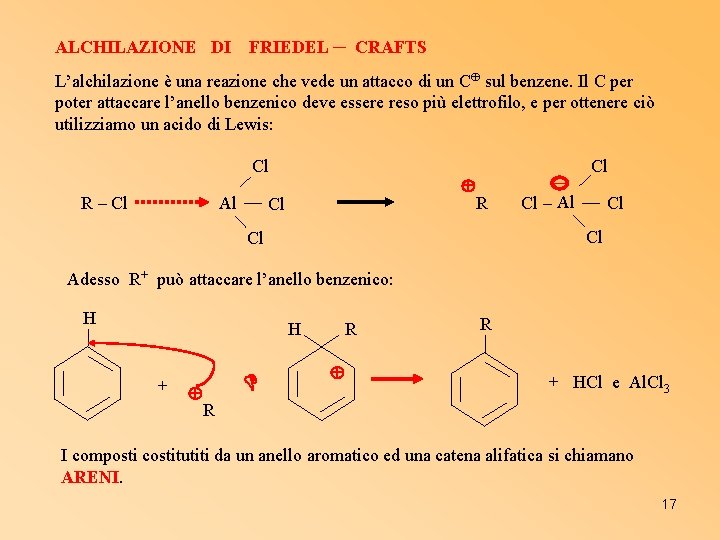
ALCHILAZIONE DI FRIEDEL ─ CRAFTS L’alchilazione è una reazione che vede un attacco di un C sul benzene. Il C per poter attaccare l’anello benzenico deve essere reso più elettrofilo, e per ottenere ciò utilizziamo un acido di Lewis: Cl Al R – Cl Cl ─ R Cl Cl – Al Cl Cl Cl Adesso R+ può attaccare l’anello benzenico: H H + R R + HCl e Al. Cl 3 R I composti costitutiti da un anello aromatico ed una catena alifatica si chiamano ARENI. 17
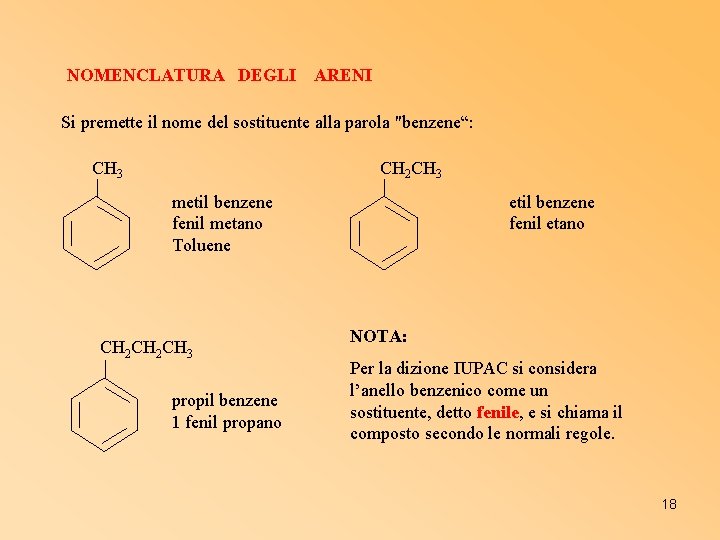
NOMENCLATURA DEGLI ARENI Si premette il nome del sostituente alla parola "benzene“: CH 3 CH 2 CH 3 metil benzene fenil metano Toluene CH 2 CH 3 propil benzene 1 fenil propano etil benzene fenil etano NOTA: Per la dizione IUPAC si considera l’anello benzenico come un sostituente, detto fenile, e si chiama il composto secondo le normali regole. 18
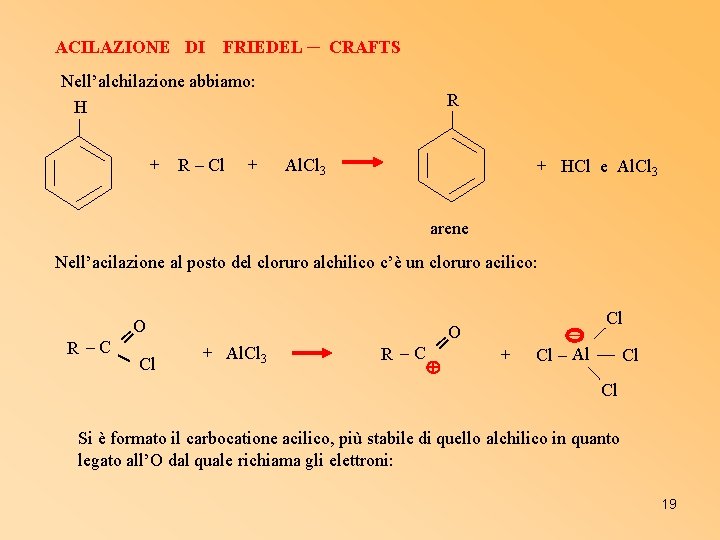
ACILAZIONE DI FRIEDEL ─ CRAFTS Nell’alchilazione abbiamo: H + R – Cl + R Al. Cl 3 + HCl e Al. Cl 3 arene Nell’acilazione al posto del cloruro alchilico c’è un cloruro acilico: O R –C ═ Cl + Al. Cl 3 O ═ R –C ─ + Cl Cl – Al Cl Cl Si è formato il carbocatione acilico, più stabile di quello alchilico in quanto legato all’O dal quale richiama gli elettroni: 19
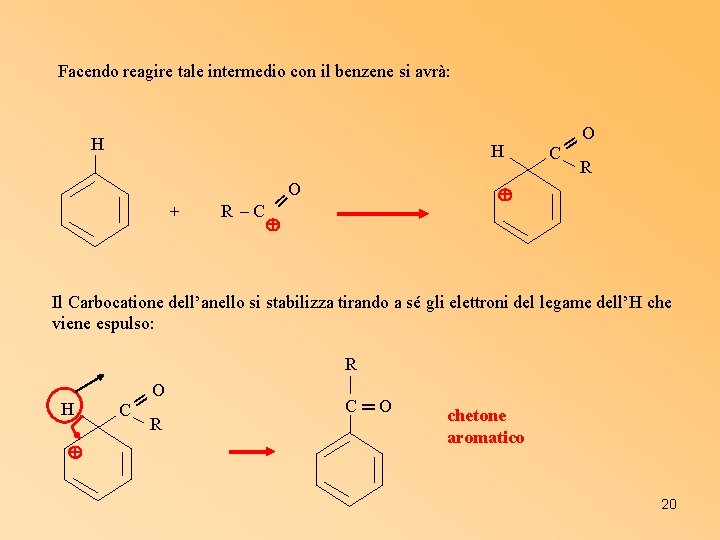
Facendo reagire tale intermedio con il benzene si avrà: H H + O R –C ═ O R Il Carbocatione dell’anello si stabilizza tirando a sé gli elettroni del legame dell’H che viene espulso: R H C ═ O R C═O chetone aromatico 20
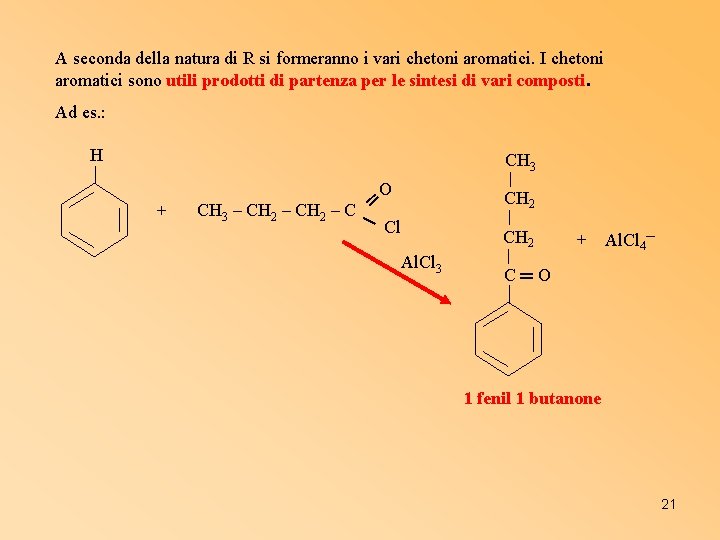
A seconda della natura di R si formeranno i vari chetoni aromatici. I chetoni aromatici sono utili prodotti di partenza per le sintesi di vari composti. Ad es. : H CH 3 + O ═ CH 3 – CH 2 – C Cl CH 2 Al. Cl 3 + Al. Cl 4─ C═O 1 fenil 1 butanone 21
- Slides: 21