I composti organici sono composti chimici formati da









- Slides: 30


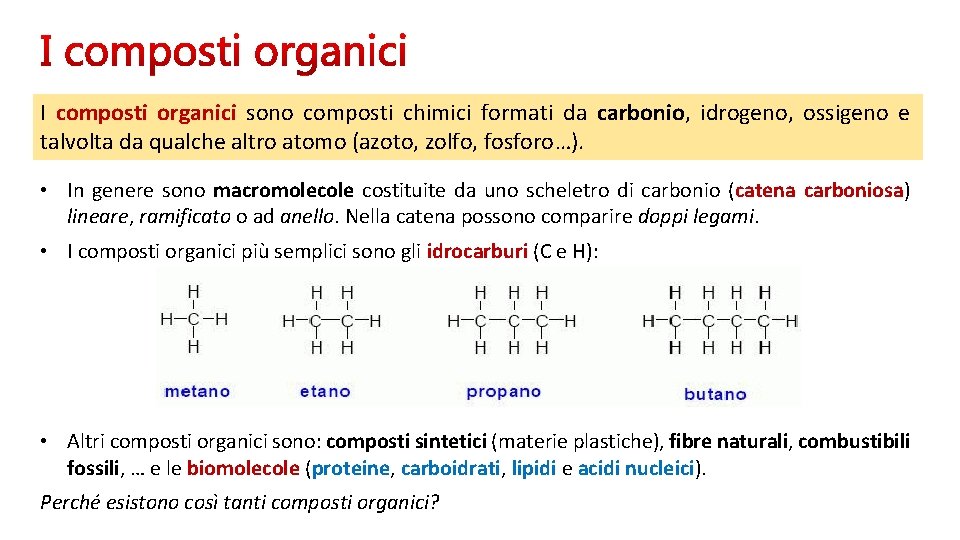
I composti organici sono composti chimici formati da carbonio, idrogeno, ossigeno e talvolta da qualche altro atomo (azoto, zolfo, fosforo…). • In genere sono macromolecole costituite da uno scheletro di carbonio (catena carboniosa) lineare, ramificato o ad anello. Nella catena possono comparire doppi legami. • I composti organici più semplici sono gli idrocarburi (C e H): • Altri composti organici sono: composti sintetici (materie plastiche), fibre naturali, combustibili fossili, … e le biomolecole (proteine, carboidrati, lipidi e acidi nucleici). Perché esistono così tanti composti organici?

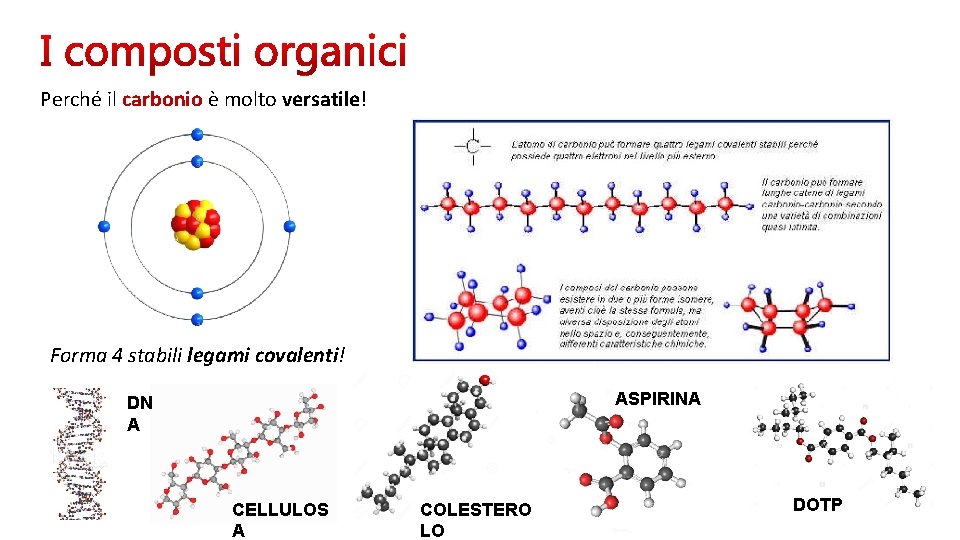
Perché il carbonio è molto versatile! Forma 4 stabili legami covalenti! ASPIRINA DN A CELLULOS A COLESTERO LO DOTP

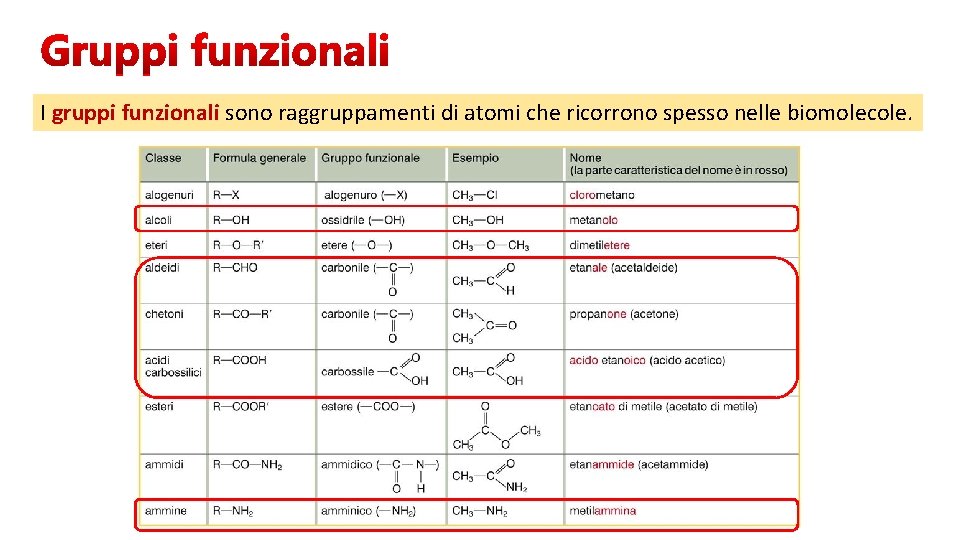
I gruppi funzionali sono raggruppamenti di atomi che ricorrono spesso nelle biomolecole.

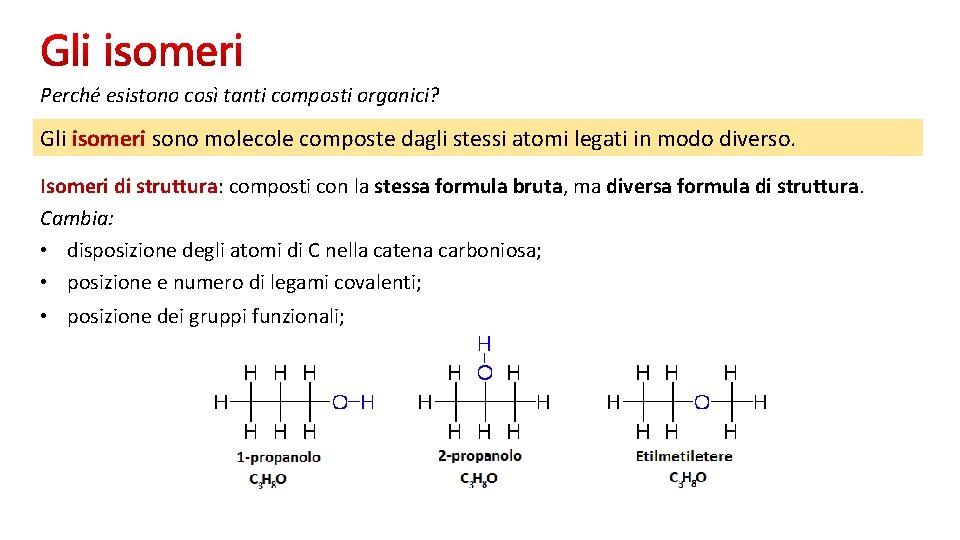
Perché esistono così tanti composti organici? Gli isomeri sono molecole composte dagli stessi atomi legati in modo diverso. Isomeri di struttura: composti con la stessa formula bruta, ma diversa formula di struttura. Cambia: • disposizione degli atomi di C nella catena carboniosa; • posizione e numero di legami covalenti; • posizione dei gruppi funzionali;

Le molecole biologiche… …sono macromolecole: molecole che contengono un numero elevato di atomi …sono spesso polimeri: molecole composte formate dall’assemblaggio di unità di base, monomeri. Possono essere: • • Polisaccaridi: polimeri degli zuccheri formati dall’unione di più monosaccaridi; Proteine: polimeri formati dall’unione di più amminoacidi; Acidi nucleici: polimeri formati dall’unione di più nucleotidi; Lipidi: non costituiscono polimeri. Hanno queste caratteristiche: • Hanno una precisa struttura in relazione con la funzione che svolgono; • Possiedono specifiche proprietà chimico-fisiche determinano fora e funzione.

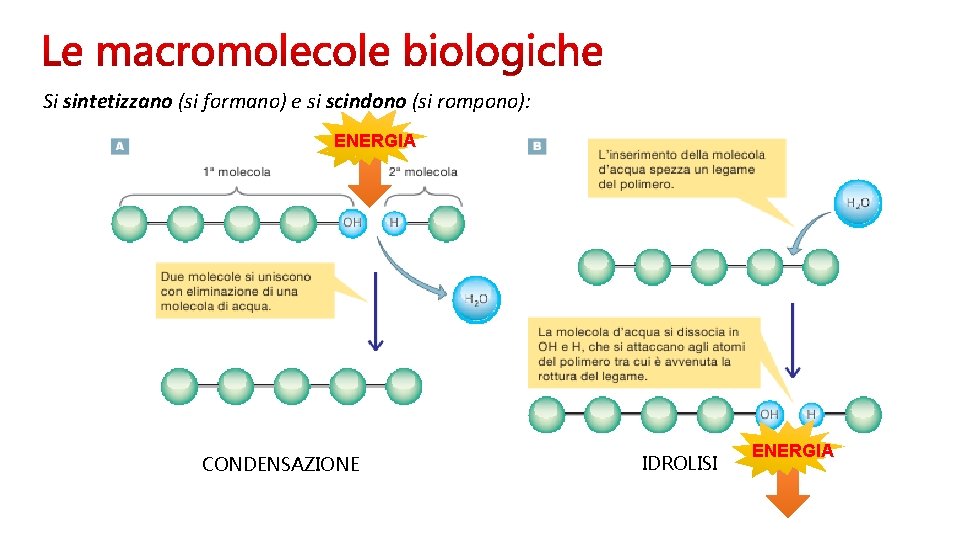
Si sintetizzano (si formano) e si scindono (si rompono): ENERGIA CONDENSAZIONE IDROLISI ENERGIA

Sono formati dai seguenti elementi: CARBONIO (C) + IDROGENO (H) + OSSIGENO (O) Svolgono le seguenti funzioni… • Sono fonte di energia per le cellule; • Costituiscono una riserva di energia a breve termine; • Forniscono scheletri di carbonio che possono essere impiegati per sintetizzare altre molecole; • Sono importanti per il sostegno e il rivestimento cellulare. In base alla struttura possono essere: • • Monosaccaridi: zuccheri semplici formati da 3 -7 atomi di C; Disaccaridi: 2 monosaccaridi uniti per condensazione; Oligosaccaridi: 3 -20 monosaccaridi uniti per condensazione; Polisaccaridi: polimeri complessi formati da 100 -1000 di monosaccaridi uniti per condensazione.

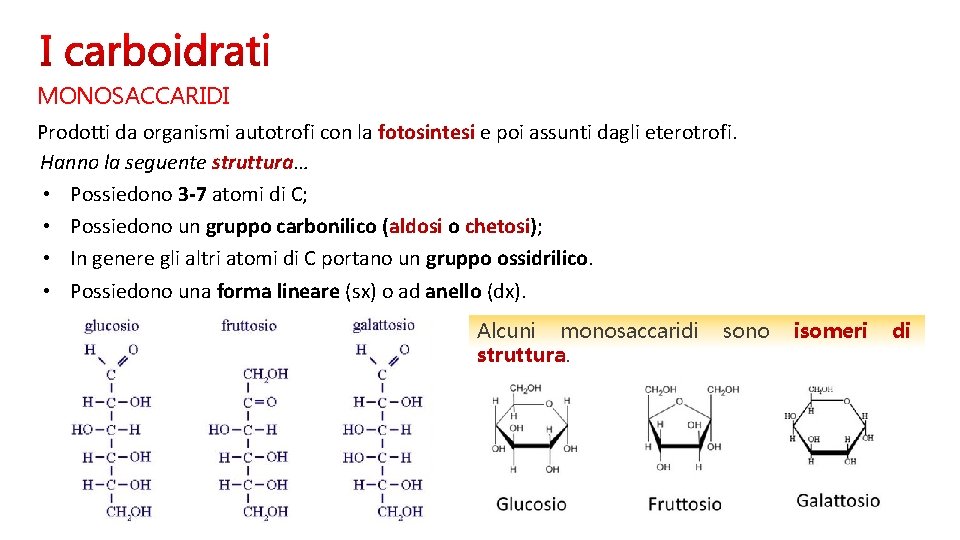
MONOSACCARIDI Prodotti da organismi autotrofi con la fotosintesi e poi assunti dagli eterotrofi. Hanno la seguente struttura… • Possiedono 3 -7 atomi di C; • Possiedono un gruppo carbonilico (aldosi o chetosi); • In genere gli altri atomi di C portano un gruppo ossidrilico. • Possiedono una forma lineare (sx) o ad anello (dx). Alcuni monosaccaridi struttura. sono isomeri di


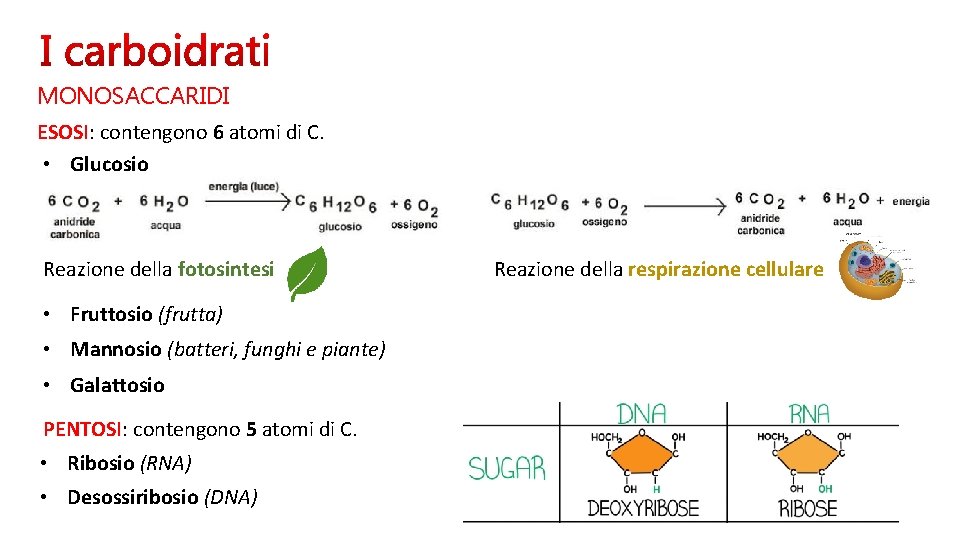
MONOSACCARIDI ESOSI: contengono 6 atomi di C. • Glucosio Reazione della fotosintesi • Fruttosio (frutta) • Mannosio (batteri, funghi e piante) • Galattosio PENTOSI: contengono 5 atomi di C. • Ribosio (RNA) • Desossiribosio (DNA) Reazione della respirazione cellulare

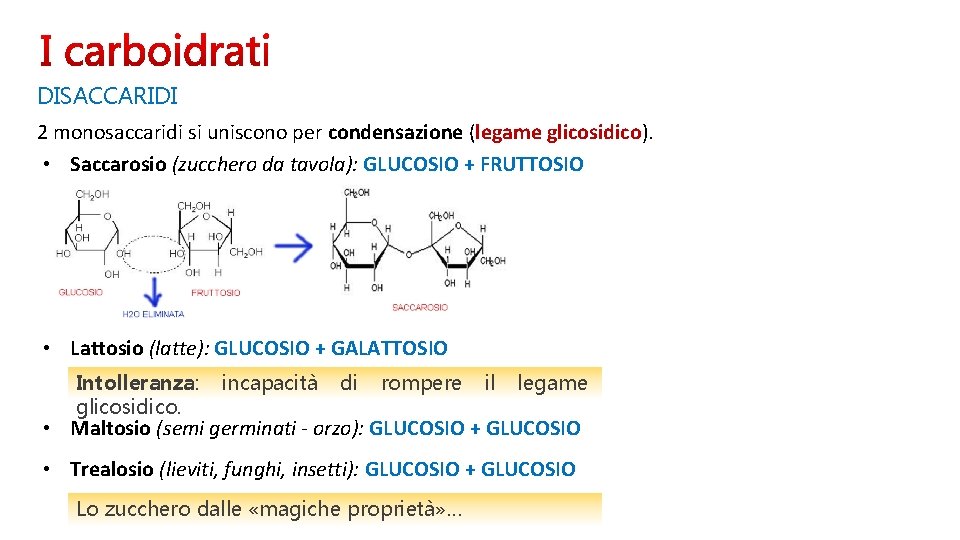
DISACCARIDI 2 monosaccaridi si uniscono per condensazione (legame glicosidico). • Saccarosio (zucchero da tavola): GLUCOSIO + FRUTTOSIO • Lattosio (latte): GLUCOSIO + GALATTOSIO Intolleranza: glicosidico. incapacità di rompere il legame • Maltosio (semi germinati - orzo): GLUCOSIO + GLUCOSIO • Trealosio (lieviti, funghi, insetti): GLUCOSIO + GLUCOSIO Lo zucchero dalle «magiche proprietà» …

POLISACCARIDI Molti monosaccaridi si uniscono per condensazione (legame glicosidico). • Amido (riserva energetica nelle piante – cereali, patate): catene di GLUCOSIO RAMIFICATE • Glicogeno (riserva energetica negli animali – fegato e muscoli): catene di GLUCOSIO RAMIFICATE • Cellulosa (funzione strutturale nelle piante – parete cellulare): catene di GLUCOSIO LINEARI La sostanza organica abbondante sulla Terra. più • Chitina (funzione strutturale – esoscheletro di insetti e parete cellulare dei funghi): catene di ACETILGLUCOSAMMINA LINEARI La seconda sostanza organica più abbondante sulla Terra.

Sono biomolecole apolari e pertanto insolubili in acqua. Sono formati prevalentemente dai seguenti elementi: CARBONIO (C) + IDROGENO (H) Svolgono le seguenti funzioni… • Sono una riserva energetica e isolanti termici negli animali (oli e grassi); • Sono importanti per il rivestimento cellulare (fosfolipidi); • Catturano l’energia luminosa e fungono da antiossidanti (carotenoidi e clorofille); • Hanno un ruolo di regolazione (ormoni e vitamine); • Hanno funzione idrorepellente e impediscono la disidratazione (cere); I lipidi più semplici sono trigliceridi e possono essere: • Grassi (solidi a t ambiente); • Oli (liquidi a t ambiente).

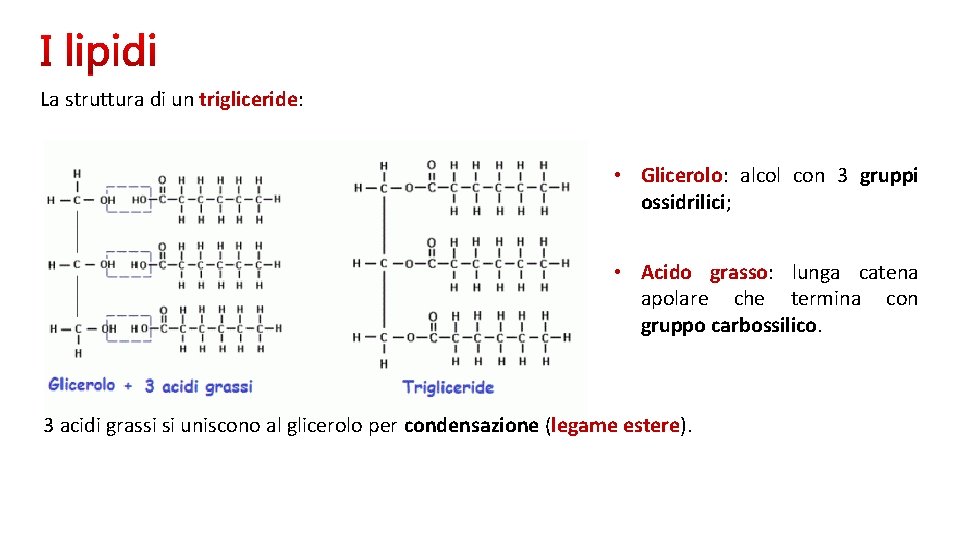
La struttura di un trigliceride: • Glicerolo: alcol con 3 gruppi ossidrilici; • Acido grasso: lunga catena apolare che termina con gruppo carbossilico. 3 acidi grassi si uniscono al glicerolo per condensazione (legame estere).

La struttura di un trigliceride: • Acidi grassi saturi: § Legami semplici; § Catene affiancate; § Solidi a t ambiente; § Grassi animali. • Acidi grassi insaturi: § Legami semplici e doppi; § Catene con curvature; § Liquidi a t ambiente; § Oli vegetali.

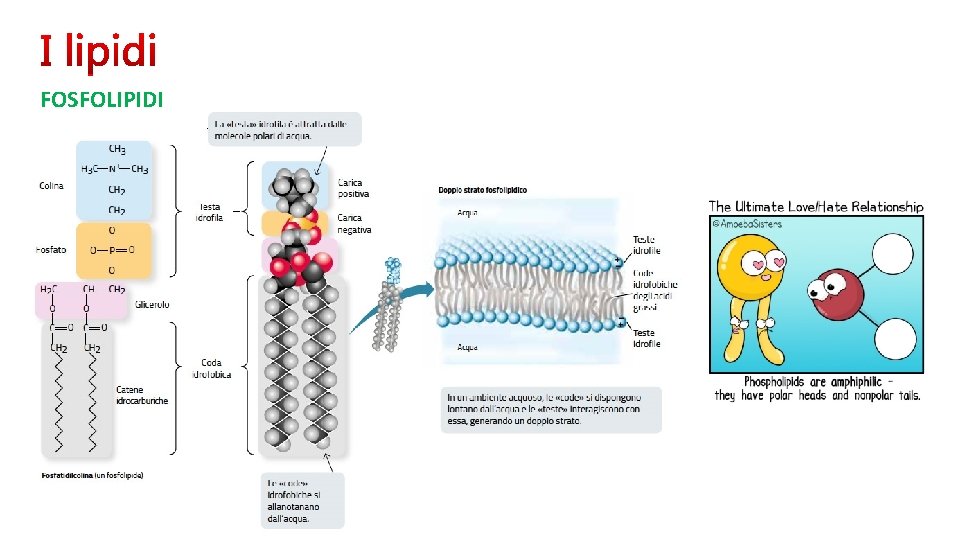
FOSFOLIPIDI

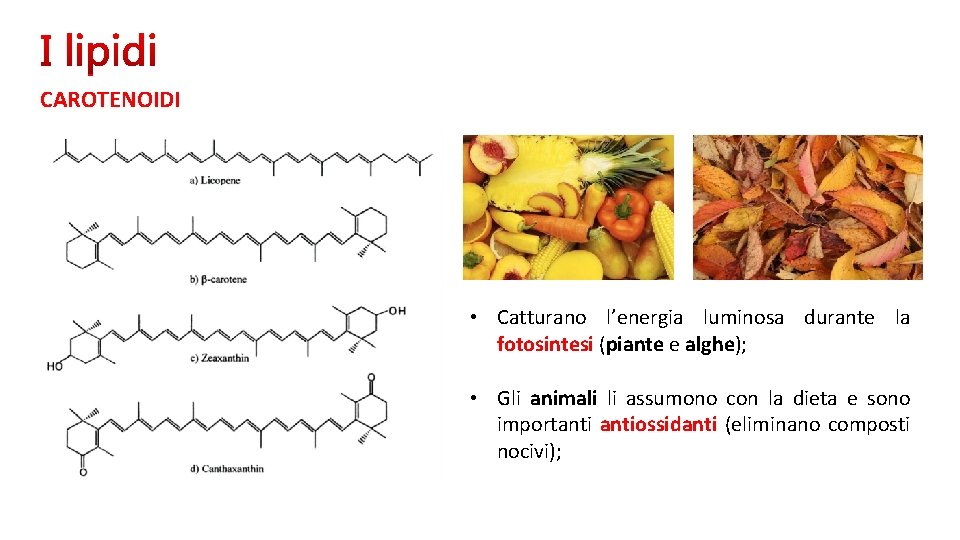
CAROTENOIDI • Catturano l’energia luminosa durante la fotosintesi (piante e alghe); • Gli animali li assumono con la dieta e sono importantiossidanti (eliminano composti nocivi);

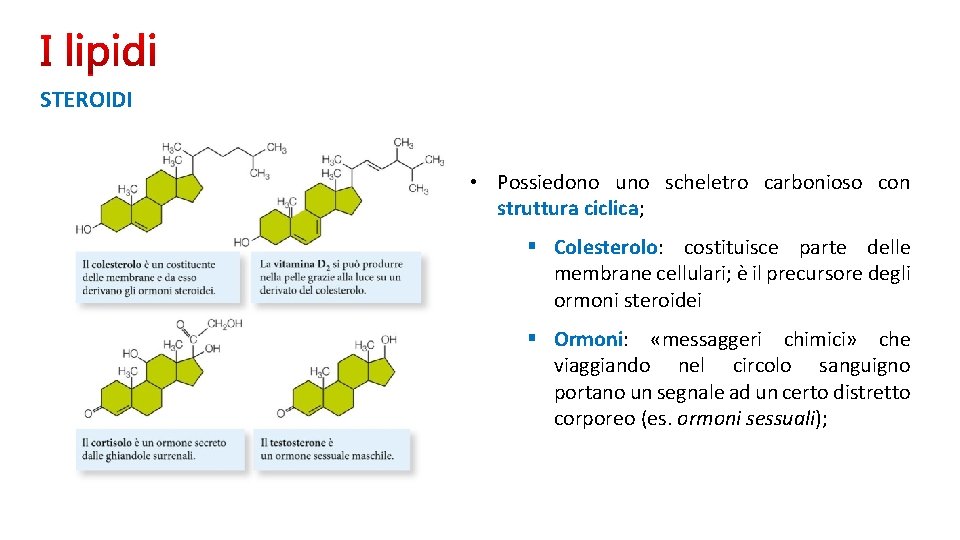
STEROIDI • Possiedono uno scheletro carbonioso con struttura ciclica; § Colesterolo: costituisce parte delle membrane cellulari; è il precursore degli ormoni steroidei § Ormoni: «messaggeri chimici» che viaggiando nel circolo sanguigno portano un segnale ad un certo distretto corporeo (es. ormoni sessuali);

VITAMINE LIPOSOLUBILI • Molecole con funzione regolatrice che il nostro organismo non è in grado di sintetizzare in quantità sufficiente e quindi deve assumere con l’alimentazione;

CERE • Cere vegetali: ricoprono la superficie delle foglie e di alcuni frutti. Riducono la perdita d’acqua per traspirazione della pianta (proteggono da essicamento); forniscono protezione da malattie e parassiti; facilitano l’eluizione dell’acqua ed evitano il ristagno. • Cere animali: secrezioni sebacee che rendono impermeabile una superficie corporea. Utili per la difesa da malattie e patogeni; ispessimento e addensamento del pelo della pelliccia; isolamento termico; idrodinamicità…

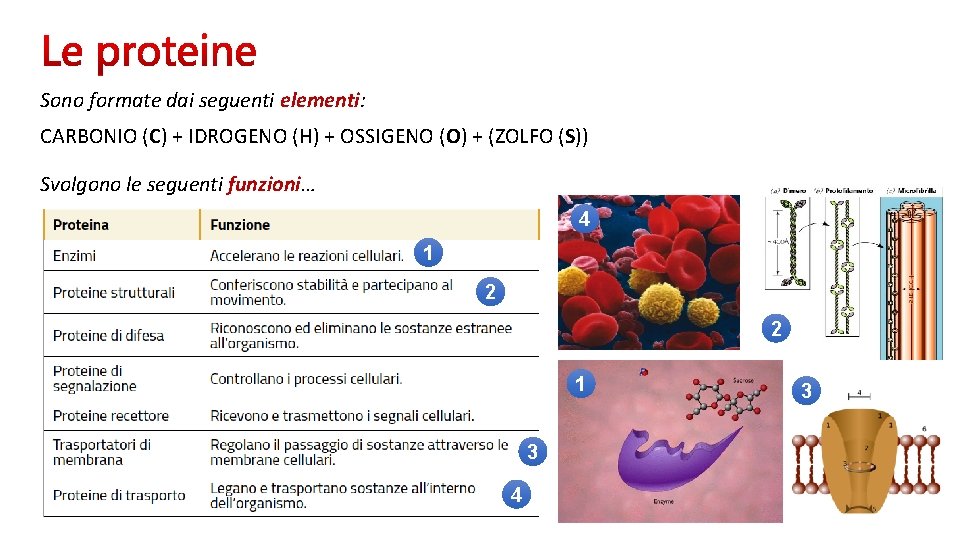
Sono formate dai seguenti elementi: CARBONIO (C) + IDROGENO (H) + OSSIGENO (O) + (ZOLFO (S)) Svolgono le seguenti funzioni… 4 1 2 2 1 3 4 3

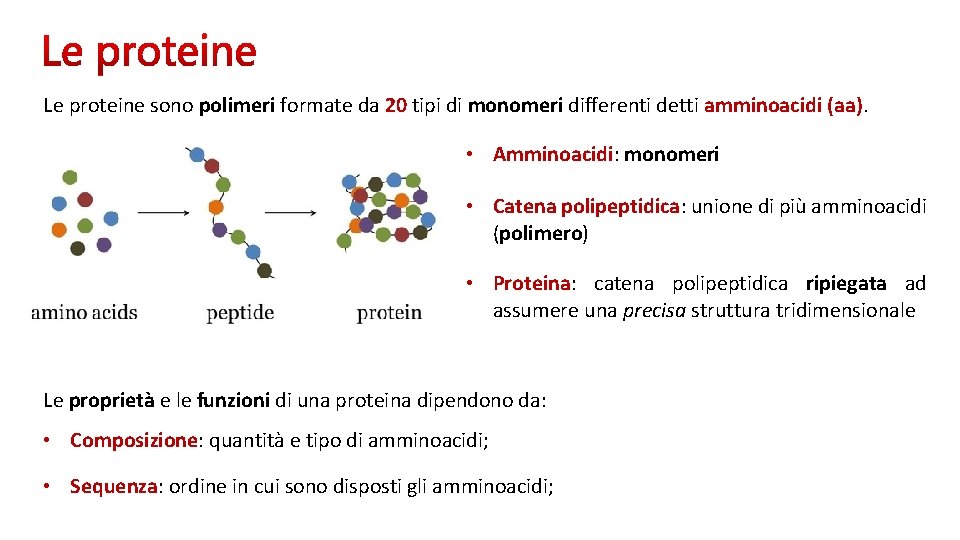
Le proteine sono polimeri formate da 20 tipi di monomeri differenti detti amminoacidi (aa). • Amminoacidi: monomeri • Catena polipeptidica: unione di più amminoacidi (polimero) • Proteina: catena polipeptidica ripiegata ad assumere una precisa struttura tridimensionale Le proprietà e le funzioni di una proteina dipendono da: • Composizione: quantità e tipo di amminoacidi; • Sequenza: ordine in cui sono disposti gli amminoacidi;

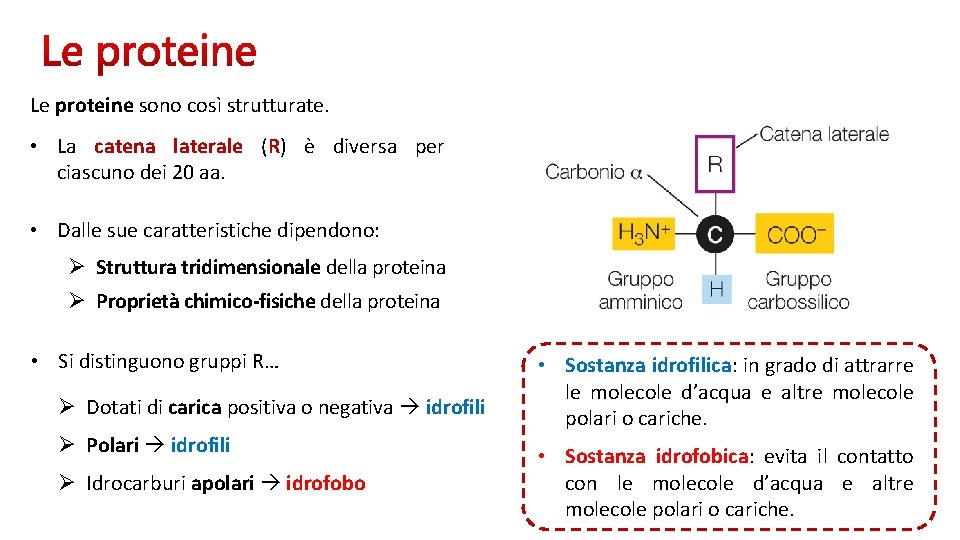
Le proteine sono così strutturate. • La catena laterale (R) è diversa per ciascuno dei 20 aa. • Dalle sue caratteristiche dipendono: Ø Struttura tridimensionale della proteina Ø Proprietà chimico-fisiche della proteina • Si distinguono gruppi R… Ø Dotati di carica positiva o negativa idrofili Ø Polari idrofili Ø Idrocarburi apolari idrofobo • Sostanza idrofilica: in grado di attrarre le molecole d’acqua e altre molecole polari o cariche. • Sostanza idrofobica: evita il contatto con le molecole d’acqua e altre molecole polari o cariche.

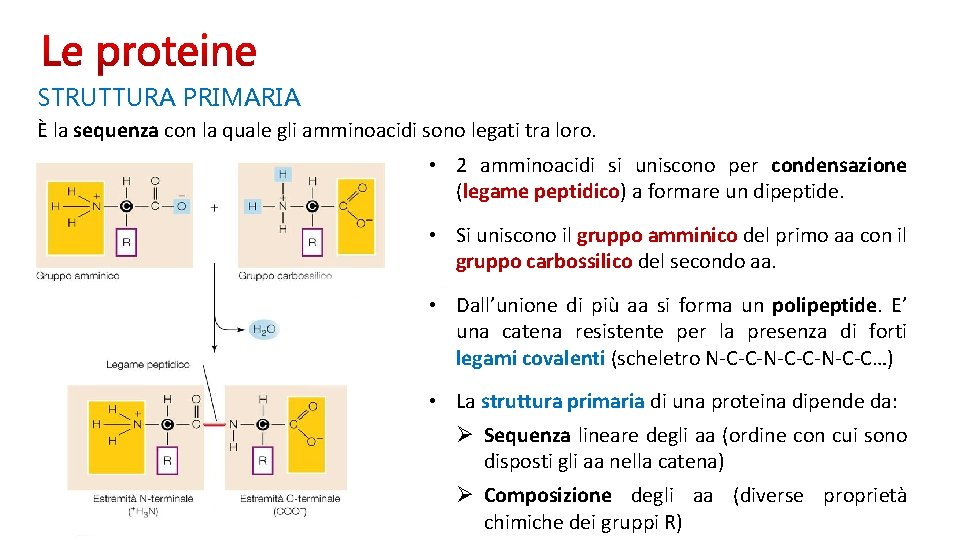
STRUTTURA PRIMARIA È la sequenza con la quale gli amminoacidi sono legati tra loro. • 2 amminoacidi si uniscono per condensazione (legame peptidico) a formare un dipeptide. • Si uniscono il gruppo amminico del primo aa con il gruppo carbossilico del secondo aa. • Dall’unione di più aa si forma un polipeptide. E’ una catena resistente per la presenza di forti legami covalenti (scheletro N-C-C-N-C-C…) • La struttura primaria di una proteina dipende da: Ø Sequenza lineare degli aa (ordine con cui sono disposti gli aa nella catena) Ø Composizione degli aa (diverse proprietà chimiche dei gruppi R)

STRUTTURA SECONDARIA È la regolare ripetizione di ripiegamenti caratteristici che interessano regioni della catena polipetidica. • I ripiegamenti, la disposizione degli atomi nello spazio, dipendono dalla struttura primaria. • La conformazione è stabile per la presenza di legami a idrogeno • Esistono due tipi principali di struttura secondaria: Ø α elica Ø foglietto β pieghettato • Il ripiegamento beta è responsabile dei cambiamenti di direzione delle catene polipeptidiche. Spesso collega le estremità di due segmenti adiacenti aventi strutture ad alfa-elica o a foglietto beta-pieghettato. Sono spesso presenti aa di prolina e glicina.

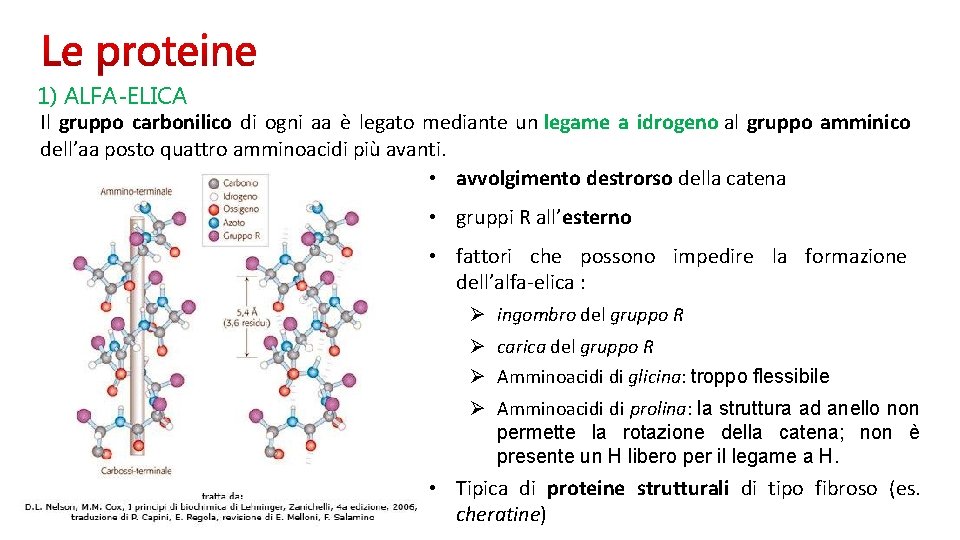
1) ALFA-ELICA Il gruppo carbonilico di ogni aa è legato mediante un legame a idrogeno al gruppo amminico dell’aa posto quattro amminoacidi più avanti. • avvolgimento destrorso della catena • gruppi R all’esterno • fattori che possono impedire la formazione dell’alfa-elica : Ø ingombro del gruppo R Ø carica del gruppo R Ø Amminoacidi di glicina: troppo flessibile Ø Amminoacidi di prolina: la struttura ad anello non permette la rotazione della catena; non è presente un H libero per il legame a H. • Tipica di proteine strutturali di tipo fibroso (es. cheratine)

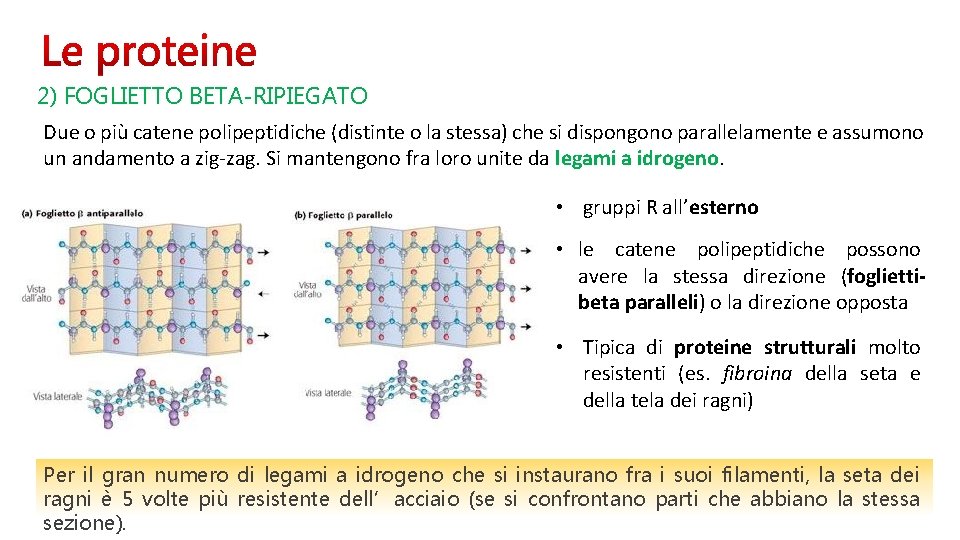
2) FOGLIETTO BETA-RIPIEGATO Due o più catene polipeptidiche (distinte o la stessa) che si dispongono parallelamente e assumono un andamento a zig-zag. Si mantengono fra loro unite da legami a idrogeno. • gruppi R all’esterno • le catene polipeptidiche possono avere la stessa direzione (fogliettibeta paralleli) o la direzione opposta • Tipica di proteine strutturali molto resistenti (es. fibroina della seta e della tela dei ragni) Per il gran numero di legami a idrogeno che si instaurano fra i suoi filamenti, la seta dei ragni è 5 volte più resistente dell’acciaio (se si confrontano parti che abbiano la stessa sezione).

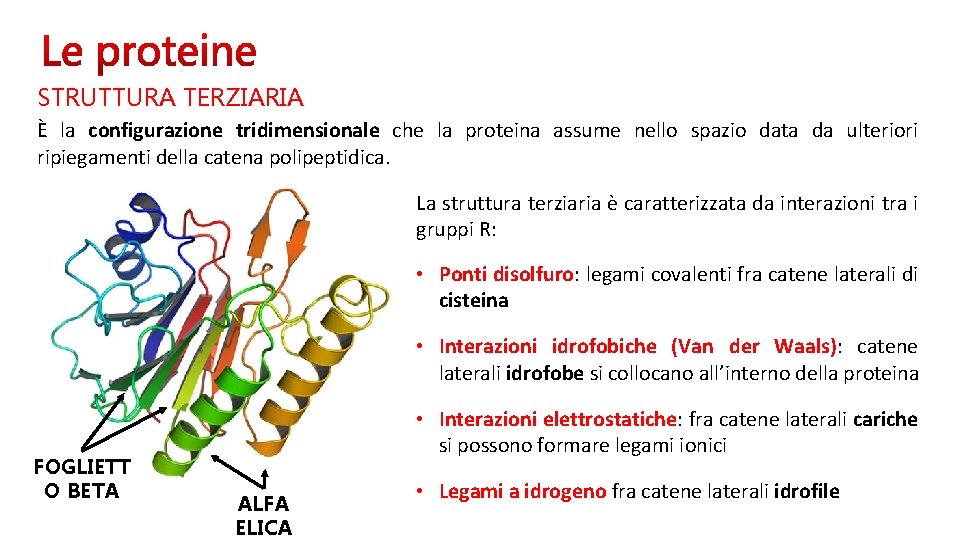
STRUTTURA TERZIARIA È la configurazione tridimensionale che la proteina assume nello spazio data da ulteriori ripiegamenti della catena polipeptidica. La struttura terziaria è caratterizzata da interazioni tra i gruppi R: • Ponti disolfuro: legami covalenti fra catene laterali di cisteina • Interazioni idrofobiche (Van der Waals): catene laterali idrofobe si collocano all’interno della proteina FOGLIETT O BETA • Interazioni elettrostatiche: fra catene laterali cariche si possono formare legami ionici ALFA ELICA • Legami a idrogeno fra catene laterali idrofile

STRUTTURA QUATERNARIA Alcune proteine sono costituite da più catene polipeptidiche dette subunità, che sono uguali o diverse. È il risultato dell’unione delle subunità in complessi tridimensionali. • Le subunità sono unite da: Ø Legami a idrogeno Ø Interazioni idrofobiche Ø Interazioni elettrostatiche • Le subunità possono avere la stessa funzione o funzioni diverse, ma correlate (es. enzimi). Possono funzionare indipendentemente l’una dall’altra, o in maniera cooperativa. Nell’uomo adulto l’emoglobina è costituita da 2 subunità α e 2 subunità β. Tutte portano un gruppo eme.