Tehniki fakultet Mihajlo Pupin u Zrenjaninu Industrijsko inenjerstvo


































- Slides: 34

Tehnički fakultet „Mihajlo Pupin“ u Zrenjaninu Industrijsko inženjerstvo u eksploataciji nafte i gasa Tehnika i tehnologija proizvodnje gasa (4) Predavanja: Doc. dr. sc. Radoslav D. Mićić rmicic@beotel. rs 1

Zakonitosti i jednačine koje određuju karakteristike gasova • U gasovima molekuli su jako udaljene jedni od drugih pa svojstva gasa ne zavise od međumolekulske sile. • Zato se svi gasovi slično ponašaju, osim pri velikom pritisku i temperaturi. • Za razliku od gasova, svojstva tečnost i čvrstih supstanci jako zavisi od međumolekulskih sila. 2

• Gas je homogeni fluid bez oblika i zapremine; gas ispunjava zapremine rezervoara i za razliku od tečnosti nema površine, odnosno međupovršine. • Svaki gas se ponaša kao idealni gas pri niskom pritisku i višoj temperaturi, na pr. pri standardnim uslovima (STP, standardni pritisak i temperatura, psc = 1, 01325 bar, Tsc = 15 °C

Svojstva idealnog gasa su: 1. Zapremina samih molekula gasa beznačajna je u odnosu na zapreminu koju zauzima gas, 2. Nema sila privlačenja ili odbijanja između molekula gasa niti između molekula i zidova rezervoara. 3. Sudari između molekula su elastični i nema gubitka unutrašnje energije molekula pri sudaru. 4

Šta definiše zakon idealnog gasa? • Zakon idealnog gasa definiše zavisnost zapremine gasa od pritiska i temperature i količine materije, a izveden je na osnovu eksperimentalnih radova: • Boylea, Daltona, Guy-Lussaca односно Charlesa и Avogadra.

Boyleov zakon • Za koliko puta povećamo pritisak gasa, toliko puta ćemo smanjiti zapreminu i obrnuto, uz uslov da je temperatura konstantna. 6

• Vrednost konstante-(const) k je izračunata iz merenja zapremine i pritiska stalno iste količine gasa. • Nakon promene u sistemu, najčešće prisilnom promenom u obimu cevi koje sadrži istu količinu gasa, mere se nova zapremina i novi pritisak. • Rezultat izračunatog logaritma novog pritiska i nove zapremine bi trebalo da budu originalna vrednost k konstante (const). • Zapremina V i pritisak p su obrnuto proporcionalni: veća zapremina znači manji pritisak, te manji obim znači veći pritisak.

Zavisnost zapremine gasa od temperature određivali su Dalton (1801), zatim Guy-Lussac (1778 -1850), dok je prva neobjavljena mjerenja obavio Charles (1787).


Avogadrov zakon (Čarlsov) Avogadrov дефинише једнозначни однос запремине гаса и количине материје. За чисте гасове и гасне смеше, A. Avogadrov definiše jednoznačni odnos zapremine gasa i količine materije. Za čiste gasove i gasne smeše, A. Avogadro je ustanovio (1811. ) da pri konstantnom pritisku i temperaturi, ista zapremina svih gasova sadrži isti broj čestica (molekula ili atoma; Avogadrov zakon). Drugim rečima ista količina materije, napr. 1 mol bilo kog gasa pri istim p, T-uslovima zauzima istu zapreminu.


Zakon idealnog gasa • 12


Opšta i Individualna gasna konstanta • 14


Vrednost R Jedinice 82. 06 atm, cc/g – mole, o. K 1. 987 Btu/lb – mole, o. R 10. 73 psia, ft 3/lb – mole, o. R 62. 37 mm. Hg, liters/g – mole, o. K 8. 314 J/kg – mole, o. K 8. 314 k. Pa, m 3/kg-mole,

Smeša idealnih gasova Molarna masa, molarna zapremina, Avogadrov broj Mol je ona količina supstance koja u sebi sadrži toliko čestica koliko ima atoma u 12 g ugljenikovog izotopa C-12, a u tih 12 g ugljenika 12 C ima 6, 023 x 1023 atoma (to jest ako se zaokruži 6 x 1023 atoma) Avogadrov broj je konstanta koja pokazuje "da u 1 mol supstance ima 6 x 1023 čestica" NA = 6 x 1023 1/mol. 17

Molarni (molski) udeo frakcija (yi) • 18

Broj molova • 19

Molarna zapremina • 20

• Ukoliko se koriste ove formule mora se voditi računa da ukoliko je n (mol) količina atoma, onda se sve u formuli odnosi na atome! • Ukoliko je n(mol) količina molekula, onda se sve u formulama odnosi na molekule. • * molekula je količina supstance koja se koristi za supstance izgradjene kao molekuli • (H 2 - 1 molekula vodonika) • * mol atom je količina supstance koja može uvek da se koristi, ali se posmatra broj atoma - indeksi u formuli (H 2 - 2 mol atoma vodonika) 21

Molarna zapremina nije uvek 22, 4 dm 3/mol. Njena vrednost se menja sa promenom pritiska i temperature. Ako je temperatura 0 o. C i pritisak 101, 3 k. Pa onda Vm=22, 4 dm 3/mol, to se dobija iz jednačine idealnog gasnog stanja: p. V=n. RT p-pritisak u k. Pa, V-zapremina u dm 3, n - količina supstance (mol), R = 8, 314 k. Padm 3/(mol. K)-gasna konstanta, T-temperatura u kelvinima (K) Jednačina idealnog gasnog stanja može da se iskoristi ukoliko uslovi nisu normalni a traži se količina supstance ili masa ili zapremina gasa! 22

Tečne supstance: • Voda ima gustinu 1 g/cm 3 (na 4 o. C) ili blizu 1 g/cm 3 na temperaturama od 0 do 100 stepeni Celzijusa. • Zbog toga je 1 g vode isto što i 1 cm 3 (to jest 1 ml). • Za ostale supstance: ukoliko je zadata masa, a traži se zapremina, potreban je podatak o gustini. • Ukoliko se zna gustina tečne supstnce, "može se iz grama dobiti cm 3, i obrnuto". 23

Maseni udeo • 24

Zapreminski udeo • 25

Odnos između zapreminskih i molskih udela Za idealni gas je odnos između zapreminskog udela komponentata(ri) i molskih udela jednaka(yi), ri = yi, što je u skladu sa Avogadro's zakonom. Za sistem idealnih gasova, kao što su naftni gasovi, sastav se može izračunati na osnovu nekog od sledećih podataka: Mase komponenata, zapremine, gustine, napona para itd. 26

Molekulska težina (masa) • 27

Daltonov zakon parcijalnih pritisaka postulira da je ukupni pritisak gasne smeše jednak zbiru pritisaka komponenti smeše. Parcijalni pritisak svake komponente u smeši jednak je pritisku, koji bi vladao u rezervoaru iste zapremine, ispunjenom istom količinom samo te komponente. pi = p yi 28

Amagatov zakon parcijalnih, odnosno aditivnih zapremina, definiše da je ukupna zapremina idealne gasne smeše zbir zapremina, koje bi pojedine komponente zauzimale, same, pri istom pritisku i temperaturi. (Zapremine čistih komponenti su parcijalne zapremine). 29



Relativna gustina •


 Fakultet mihajlo pupin zrenjanin
Fakultet mihajlo pupin zrenjanin Ets mihajlo pupin novi sad
Ets mihajlo pupin novi sad Tfzr predmeti
Tfzr predmeti Fakultet u zrenjaninu
Fakultet u zrenjaninu Mehaničar pula
Mehaničar pula Dobijanje aluminijum hidroksida
Dobijanje aluminijum hidroksida Monoprotonska kiselina
Monoprotonska kiselina Univerzitet u rijeci
Univerzitet u rijeci Tehniki
Tehniki Tehniki
Tehniki Tehniki
Tehniki Plašt kvadra
Plašt kvadra Tehniki
Tehniki Mihajlo strelec
Mihajlo strelec Mihajlo jovanovic
Mihajlo jovanovic Oliver toskovic filozofski fakultet
Oliver toskovic filozofski fakultet Ekonomski fakultet skopje
Ekonomski fakultet skopje En fakultet
En fakultet Fakultet organizacionih nauka smerovi
Fakultet organizacionih nauka smerovi Industrijski dizajn fakultet
Industrijski dizajn fakultet Biohemija poljoprivredni fakultet
Biohemija poljoprivredni fakultet Med fak foca
Med fak foca Sociologija pravni fakultet
Sociologija pravni fakultet Poslovni fakultet singidunum
Poslovni fakultet singidunum Filozofski fakultet beograd
Filozofski fakultet beograd Ekonomski fakultet banja luka
Ekonomski fakultet banja luka Fakultet za rehabilitaciju i edukaciju zagreb
Fakultet za rehabilitaciju i edukaciju zagreb Arhitektonski fakultet osijek
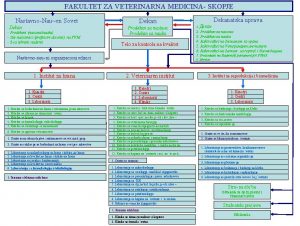
Arhitektonski fakultet osijek Veterinaren fakultet skopje
Veterinaren fakultet skopje Medicinski fakultet zadar
Medicinski fakultet zadar Sociologija ekonomski fakultet
Sociologija ekonomski fakultet Fakultet za hotelijerstvo i turizam
Fakultet za hotelijerstvo i turizam Pravni fakultet sarajevo
Pravni fakultet sarajevo Filozofski fakultet nikšić
Filozofski fakultet nikšić Poslovni fakultet singidunum
Poslovni fakultet singidunum