Propriedades coligativas Professor Abiney Lemos Cardoso EFEITOS COLIGATIVOS

Propriedades coligativas Professor: Abiney Lemos Cardoso

EFEITOS COLIGATIVOS A água pura à pressão de 1 atm possui ponto de fusão de 0 o. C e ponto de ebulição de 100 o. C. No entanto, quando adicionamos um soluto não volátil à água, o soluto modifica as propriedades físicas da água. Agora a água congela abaixo de 0 o. C e ferve acima de 100 o. C. Estas alterações das propriedades físicas da água devido à adição do soluto são denominados de efeitos coligativos. Adição de um soluto não volátil à água

Propriedades Coligativas Propriedades coligativas das soluções são propriedades que se somam pela presença de dois ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão dispersas na solução, não dependendo da natureza do soluto. Isso significa dizer que a quantidade, e não a qualidade (e. g. tamanho, estrutura molecular ou massa), das partículas que estão juntas na solução é que irá influenciar na formação das propriedades (ou efeitos) coligativas. Situações Cotidianas O uso de aditivos, como o etilenoglicol, à água do radiador de carros evita que ela entre em ebulição, no caso de um superaquecimento do motor.

Propriedades Coligativas Situações Cotidianas Nos países em que o inverno é rigoroso, esse mesmo aditivo tem o efeito de evitar o congelamento da água do radiador. Nesses países, joga-se SAL nas estradas e ruas com acúmulo de neve para derretê-la. Em verduras cruas com sal, as células perdem água mais rapidamente, murchando em pouco tempo.

EFEITOS COLIGATIVOS EFEITO COLIGATIVO Diminuição da pressão de vapor Aumento do Ponto de Ebulição Diminuição do Ponto de Congelamento Aumento da Pressão Osmótica PROPRIEDADE COLIGATIVA Tonoscopia Ebulioscopia Crioscopia Osmoscopia Os efeitos coligativos dependem somente do número de partículas do soluto dissolvidas. Quanto maior for o número de partículas do soluto dissolvidas, maiores serão os efeitos coligativos.

Algumas definições importantes Pressão Máxima de Vapor Definição : Vamos imaginar um cilindro munido de um êmbolo totalmente apoiado em um líquido puro contido no seu interior. Se elevarmos o êmbolo, criaremos um espaço vazio, e o líquido começará a vaporizar-se. I) Inicialmente temos evaporação, pois ainda não existem moléculas no estado de vapor; II) A velocidade de evaporação é maior que a velocidade de condensação; III) Após algum tempo, a velocidade de condensação iguala-se à velocidade de evaporação e o sistema atinge um equilíbrio dinâmico: a cada unidade de tempo, o número de moléculas que passam para o estado gasoso é igual ao nº de moléculas que retornam para a fase líquida; Nesta situação, dizemos que foi atingida a pressão máxima de vapor do líquido.
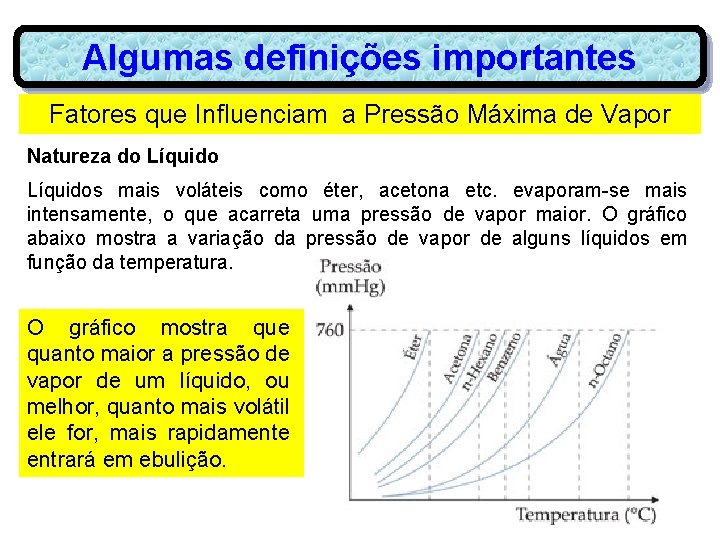
Algumas definições importantes Fatores que Influenciam a Pressão Máxima de Vapor Natureza do Líquidos mais voláteis como éter, acetona etc. evaporam-se mais intensamente, o que acarreta uma pressão de vapor maior. O gráfico abaixo mostra a variação da pressão de vapor de alguns líquidos em função da temperatura. O gráfico mostra que quanto maior a pressão de vapor de um líquido, ou melhor, quanto mais volátil ele for, mais rapidamente entrará em ebulição.
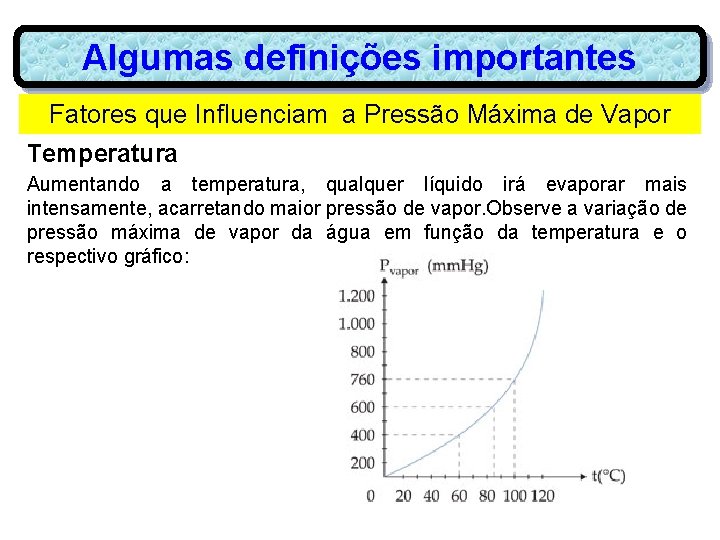
Algumas definições importantes Fatores que Influenciam a Pressão Máxima de Vapor Temperatura Aumentando a temperatura, qualquer líquido irá evaporar mais intensamente, acarretando maior pressão de vapor. Observe a variação de pressão máxima de vapor da água em função da temperatura e o respectivo gráfico:
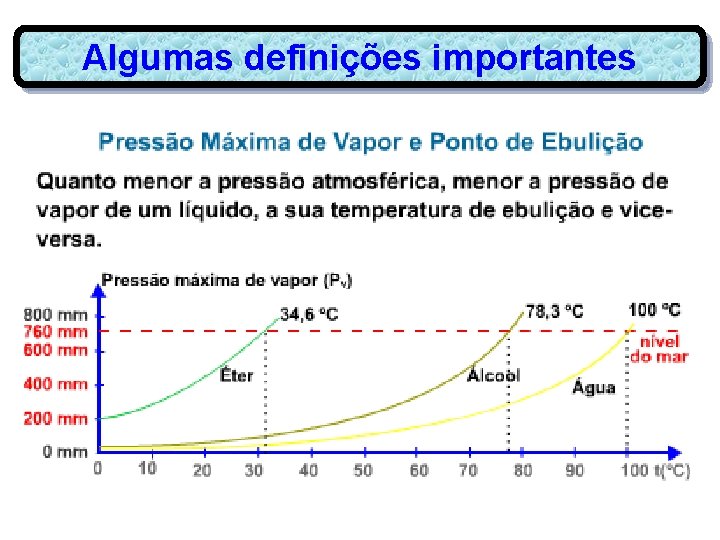
Algumas definições importantes

Algumas definições importantes Observação – A passagem de uma substância da fase líquida para a fase gasosa pode ocorrer de duas formas: Evaporação: Consiste em uma vaporização relativamente lenta, em que as moléculas mais velozes vencem as forças de atração intermoleculares e passam para o estado gasoso. Ebulição : É uma vaporização turbulenta, na qual a passagem da fase líquida para a gasosa pode ocorrer em qualquer ponto da fase líquida, e não apenas na superfície.
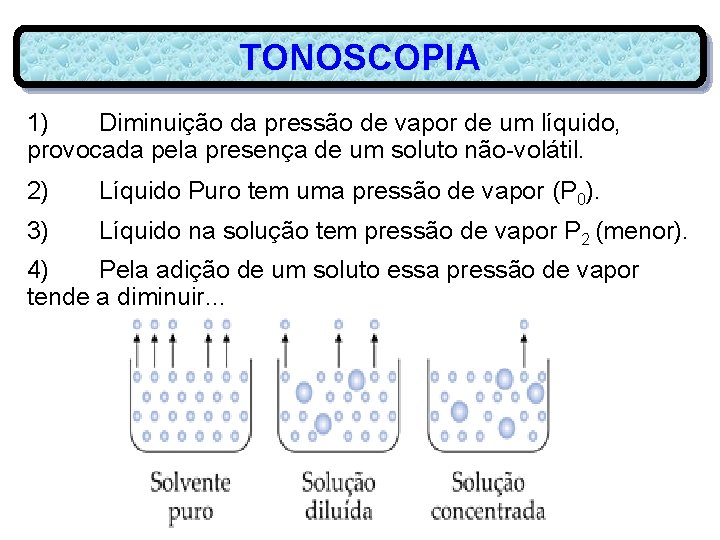
TONOSCOPIA 1) Diminuição da pressão de vapor de um líquido, provocada pela presença de um soluto não-volátil. 2) Líquido Puro tem uma pressão de vapor (P 0). 3) Líquido na solução tem pressão de vapor P 2 (menor). 4) Pela adição de um soluto essa pressão de vapor tende a diminuir. . .

TONOSCOPIA Num sistema fechado: o líquido tende a evaporar e o vapor tende a se condensar até que atinjam um equilíbrio. Quando a Vevaporação = Vcondensação dizemos que a pressão exercida pelos vapores saturantes do líquido atingiram a Pressão Máxima de Vapor.
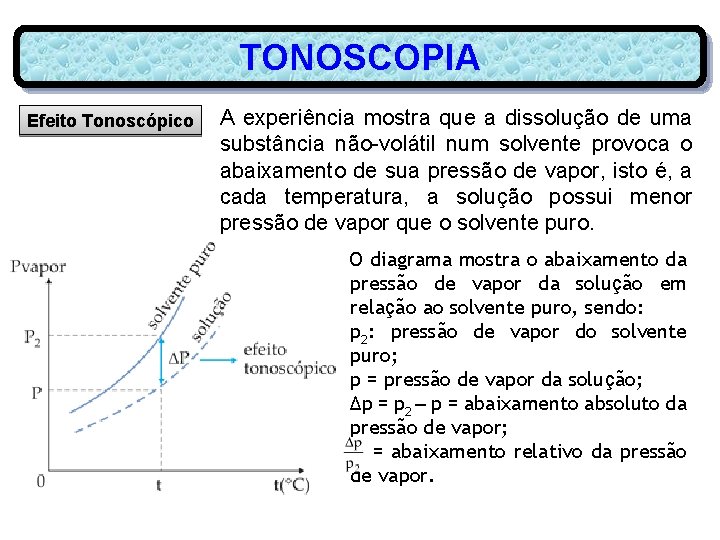
TONOSCOPIA Efeito Tonoscópico A experiência mostra que a dissolução de uma substância não-volátil num solvente provoca o abaixamento de sua pressão de vapor, isto é, a cada temperatura, a solução possui menor pressão de vapor que o solvente puro. O diagrama mostra o abaixamento da pressão de vapor da solução em relação ao solvente puro, sendo: p 2: pressão de vapor do solvente puro; p = pressão de vapor da solução; Δp = p 2 – p = abaixamento absoluto da pressão de vapor; = abaixamento relativo da pressão de vapor.
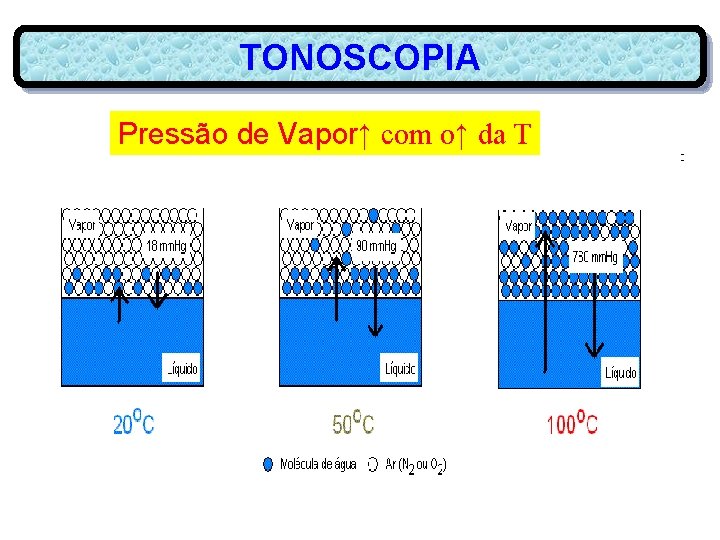
TONOSCOPIA Pressão de Vapor↑ com o↑ da T

EBULIOSCOPIA É o estudo da elevação da temperatura de ebulição de um líquido, por meio da adição de um soluto não volátil. A diminuição da pressão máxima de vapor do solvente, devido à adição de um soluto, leva inevitavelmente ao aumento da temperatura de ebulição. Quanto maior a concentração do soluto, maior a elevação da temperatura de ebulição do solvente e maior a temperatura de ebulição do mesmo. te = Elevação da temperatura de ebulição

EBULIOSCOPIA • Pressão Atmosférica = 760 mm. Hg = 1 atm • Água ferve à 100 ºC • Onde a pressão for menor, a temperatura de ebulição será menor. Ex: [La Paz (Bolívia) 90ºc] • Onde a pressão for maior que 1 atm, a temperatura de ebulição será maior. Ex: [panela de pressão 120 ºC]

EBULIOSCOPIA LEI DE RAOULT Em 1878 o químico francês François-Marie Raoult (1830 -1901) afirma que a elevação do ponto de ebulição de um líquido, provocada pela presença de um soluto não-volátil, é diretamente proporcional à molalidade da solução. R = constante de gases T = temperatura em Kelvin Lv = calor latente de vaporização

CRIOSCOPIA Abaixamento do ponto de congelamento de um líquido, provocado pela presença de um soluto não-volátil Com a adição de soluto, a pressão de vapor diminui, a temperatura de ebulição aumenta e a temperatura de congelamento diminui. Efeito Crioscopico do sal no Ponto de Solidificação da água: à direita água pura com Ponto de Solidificação de 0 o. C e a esquerda água e sal com Ponto de Solidificação de -18 o. C.

CRIOSCOPIA
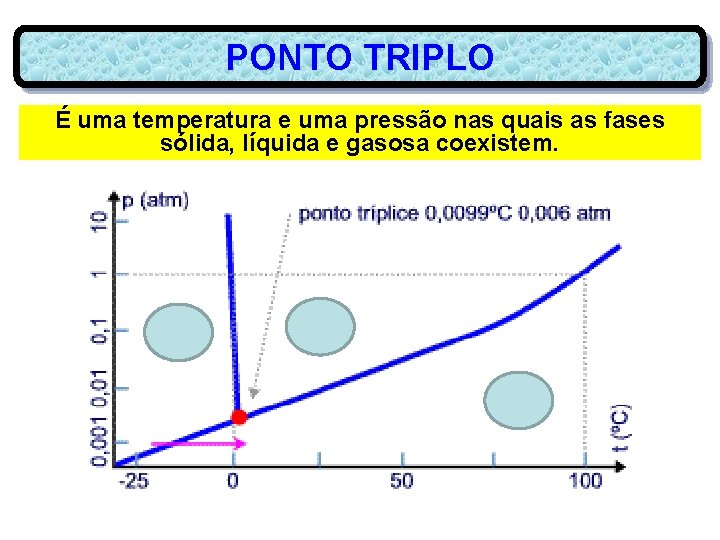
PONTO TRIPLO É uma temperatura e uma pressão nas quais as fases sólida, líquida e gasosa coexistem.

PONTO TRIPLO A Figura ilustra o ponto triplo. Gelo (iceberg) coexistindo com o líquido no qual flutua, e com a fase gasosa (ar e vapor de água).

Gelo-seco nome popular para o dióxido de carbono solidificado ao ser resfriado a uma temperatura inferior a -78ºC. Ao ser aquecido na pressão atmosférica torna-se imediatamente gás de dióxido de carbono, sem passar pelo estado líquido (processo conhecido por sublimação). Se o ar quente sopra sobre o gelo -seco, forma-se uma nuvem branca densa, que permanece ao nível do chão, utilizado no teatro.

OSMOSCOPIA Osmose é a passagem de um solvente para o interior de uma solução feita desse mesmo solvente, através de uma membrana semipermeável (MSP). A osmose também é uma propriedade coligativa da solução, pois depende do número de partículas dissolvidas. Aumento da Pressão Osmótica. Fenômeno da disseminação espontânea entre um líquido em outro e vice-versa. A difusão de um líquido para outro através de membranas semipermeáveis recebe o nome de OSMOSE.
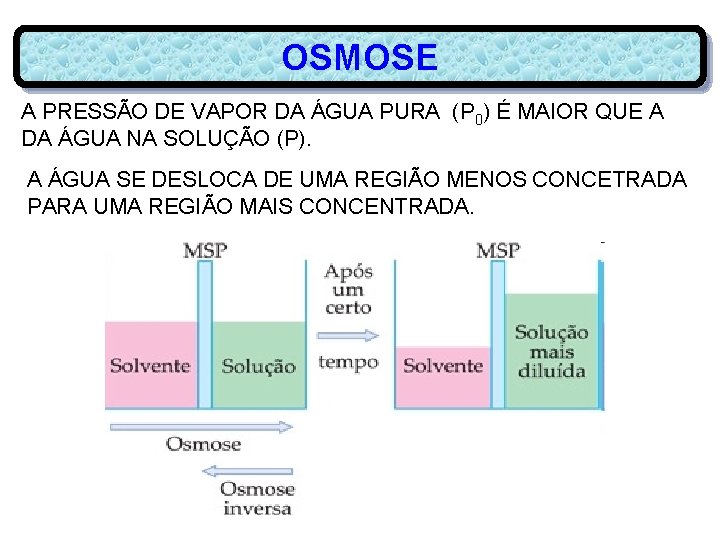
OSMOSE A PRESSÃO DE VAPOR DA ÁGUA PURA (P 0) É MAIOR QUE A DA ÁGUA NA SOLUÇÃO (P). A ÁGUA SE DESLOCA DE UMA REGIÃO MENOS CONCETRADA PARA UMA REGIÃO MAIS CONCENTRADA.

Estabilidade dos colóides Quem congela primeiro: água quente ou água fria? Trata-se do seguinte: colocando-se no congelador dois coposmais iguais cheios de Bom, na verdade a água quente não congela rapidamente queágua, a água fria, é claro. Mas se um vocêaferve água e depois deixa que ela resfrie até a temperatura ambiente (30°C) e outro temperatura ambiente, ela congelará mais(70°C), rapidamente uma outra saído da chaleira qual que congelará quantidade de água que não tenha sido aquecida antes. Estranho? primeiro? Surpreendemente, a água que Não, e vamos ver o porquê. Quando você aquece a água, ela perde parte inicia do ar dissolvido nela, quemais sai emquente forma decongela bolhas, e oprimeiro ar é um mau condutor térmico. Assim, o ar presente na água dificulta as trocas de calor com o meio e dificulta a perda de calor que a água precisa sofrer para que aconteça o congelamento Por essa mesma razão, o gelo formado por água previamente fervida tem densidade maior do que aquele que se obtém com água que não passou por esse processo. Em países muito frios, o que não é o caso do Brasil, os canos de água quente tendem a arrebentar antes do que os de água fria, pois congelam primeiro

Professor Abiney Lemos Cardoso abineylemos@yahoo. com. br FIM Devemos concentrar todos os nossos pensamentos no trabalho que temos entre mãos. Os raios do sol não queimam se não forem focados. Alexander Graham Bell.
- Slides: 26














































