Propriedades peridicas Propriedades peridicas e aperidicas Propriedades peridicas







- Slides: 17

Propriedades periódicas

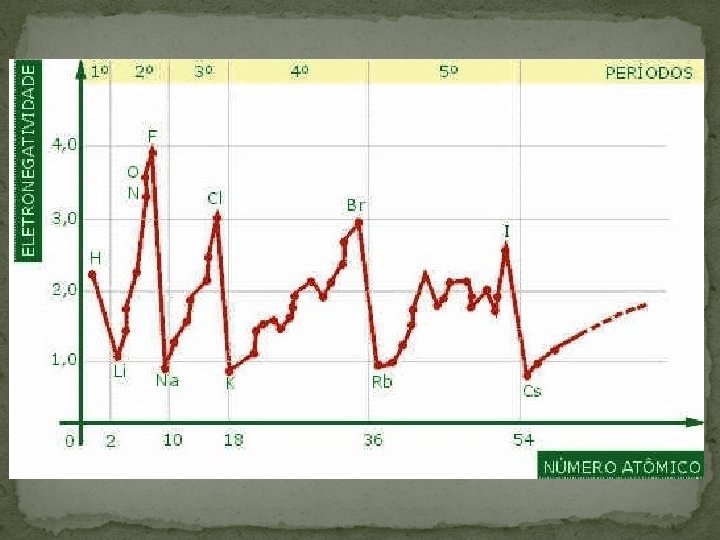
Propriedades periódicas e aperiódicas Propriedades periódicas: ocorrem à medida que o número atômico de um elemento químico aumenta, ou seja, assume valores que crescem e decrescem em cada período da Tabela Periódica. Entre as propriedades periódicas temos: raio atômico, energia de ionização, eletroafinidade, eletronegatividade

Propriedades periódicas e aperiódicas Propriedades aperiódicas: os valores desta propriedade variam à medida que o número atômico aumenta, mas não obedecem a posição na Tabela, ou seja, não se repetem em períodos regulares. Entre as propriedades aperiódicas temos: calor específico, índice de refração, dureza e massa atômica.

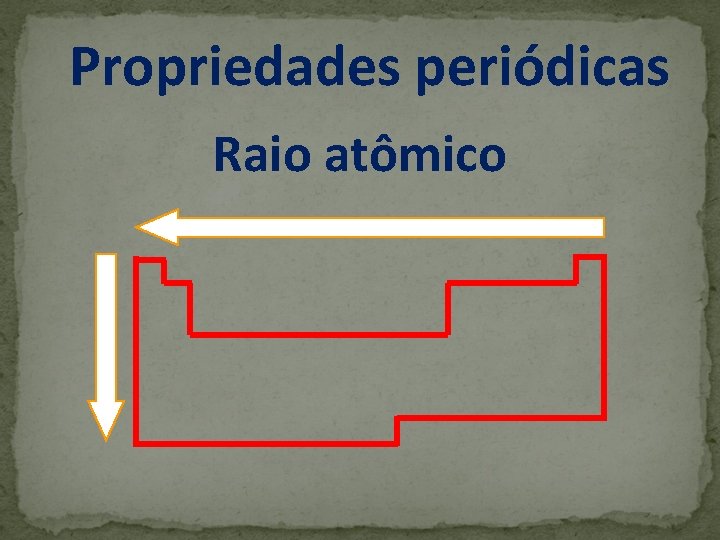
Raio atômico É a distância do núcleo do átomo até o seu elétron mais externo (camada de valência). Como consequência do átomo não ser rígido é impossível calcular o seu raio atômico exato. Deste modo, calcula-se o seu raio atômico médio.

Propriedades periódicas Raio atômico


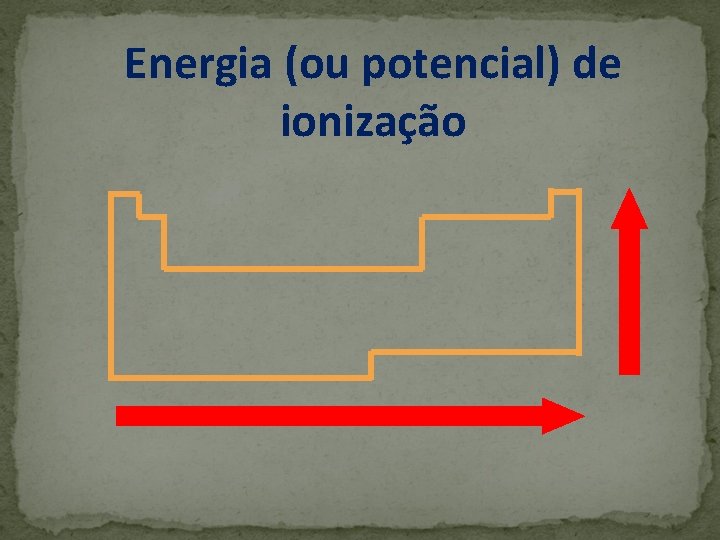
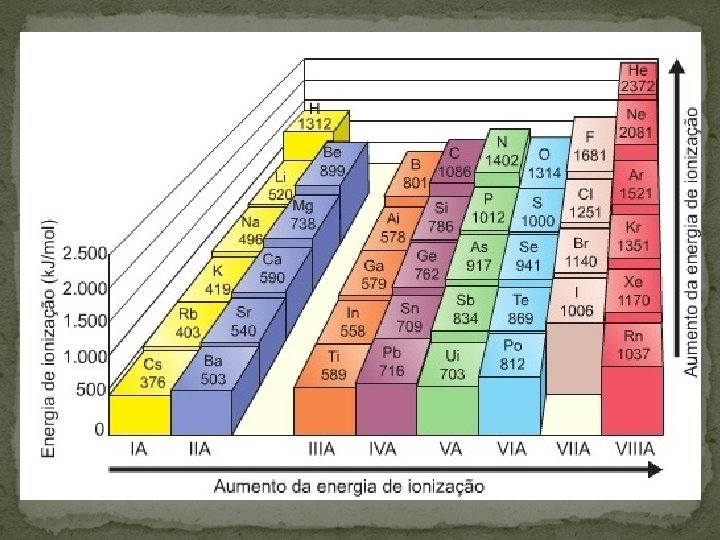
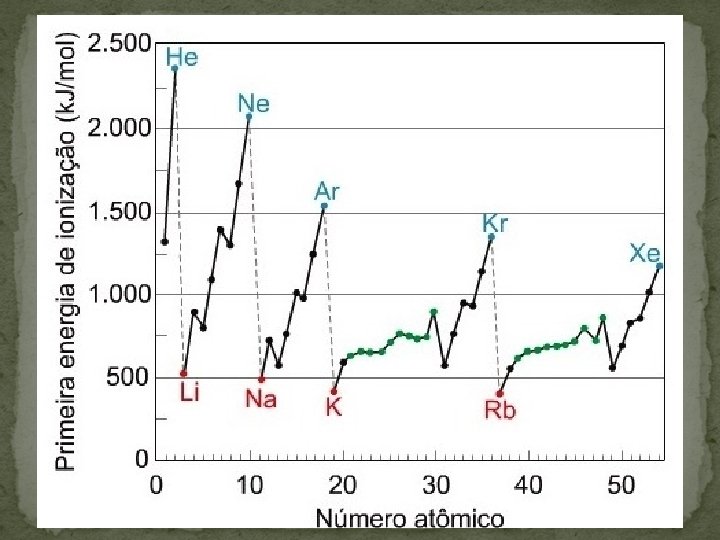
Energia (ou potencial) de ionização É a energia necessária para remover um ou mais elétrons de um átomo isolado no estado gasoso. Em uma família cresce de cima para baixo, a medida em que as camadas eletrônicas aumentam, sendo o elétron menos atraído pelo núcleo. No período, cresce da direita para a esquerda, acompanhando o crescimento do número atômico (Z), o que faz a camada de valência ficar mais próxima do núcleo. X (g) + Energia → X+(g) + e-

Energia (ou potencial) de ionização


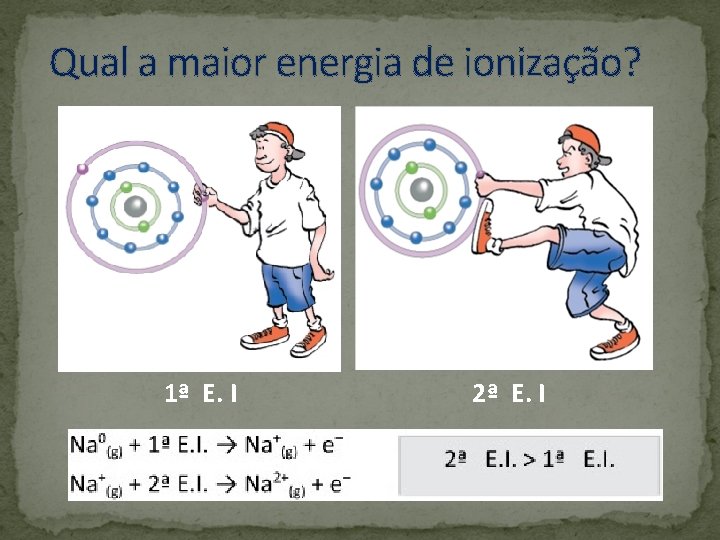
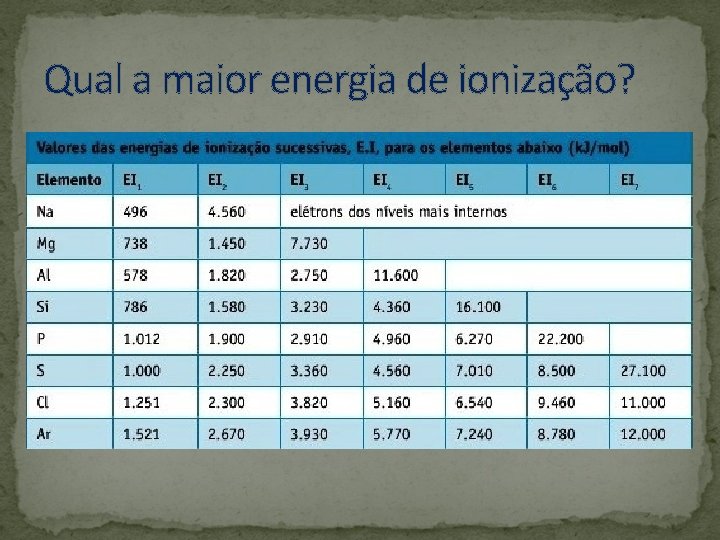
Qual a maior energia de ionização? 1ª E. I 2ª E. I

Qual a maior energia de ionização?


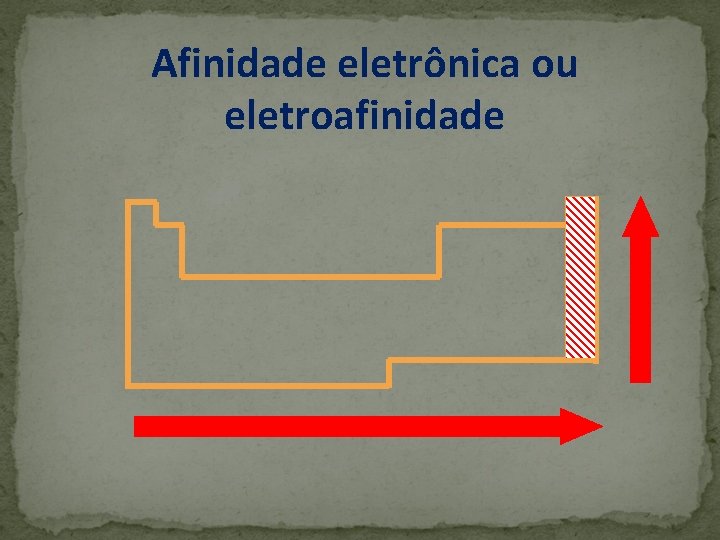
Afinidade eletrônica ou eletroafinidade É a quantidade de energia envolvida quando um átomo isolado, no estado gasoso, recebe um elétron formando um íon negativo. X (g) + e- → X-(g) + Energia

Afinidade eletrônica ou eletroafinidade

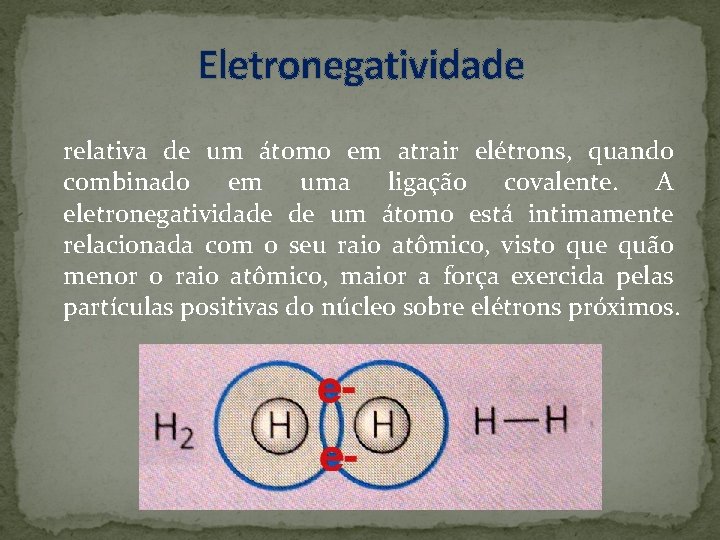
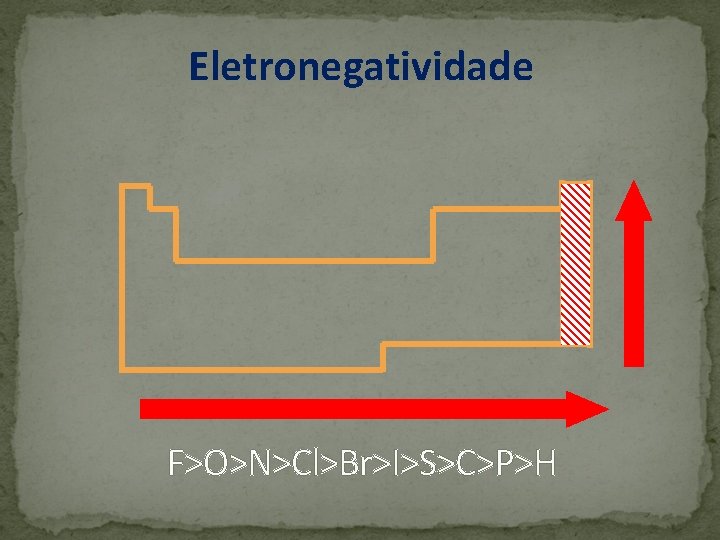
Eletronegatividade relativa de um átomo em atrair elétrons, quando combinado em uma ligação covalente. A eletronegatividade de um átomo está intimamente relacionada com o seu raio atômico, visto que quão menor o raio atômico, maior a força exercida pelas partículas positivas do núcleo sobre elétrons próximos.

Eletronegatividade F>O>N>Cl>Br>I>S>C>P>H
