Mtodos de esterilizacin y desinfeccin Medios de cultivo

























- Slides: 28

Métodos de esterilización y desinfección. Medios de cultivo. Curso: Diagnóstico de enfermedades vegetales 27 de mayo de 2011 Ing. Agr. MSc. Vivienne Gepp

Objetivo • Que el estudiante se familiarice con los procesos de desinfección y esterilización comúnmente utilizados en un Laboratorio de Fitopatología. • Conocer los medios de cultivo más usados.

Definiciones Esterilización = proceso mediante el cual se matan o eliminan todas las formas de vida microbiana. estéril o no estéril. Desinfección = eliminar microorganismos patógenos total o parcialmente niveles de desinfección. Asepsia = exclusión continuada de microorganismos contaminantes.

Métodos de esterilización • FISICOS: – Calor • seco (llama, horno) • húmedo (autoclave) – Radiaciones • MECÁNICOS – Filtración • QUIMICOS – Gaseosos – No gaseosos

Calor seco • Esterilización directa en la llama

Calor seco alcohol 96% + mechero

Calor seco alcohol 96% + mechero

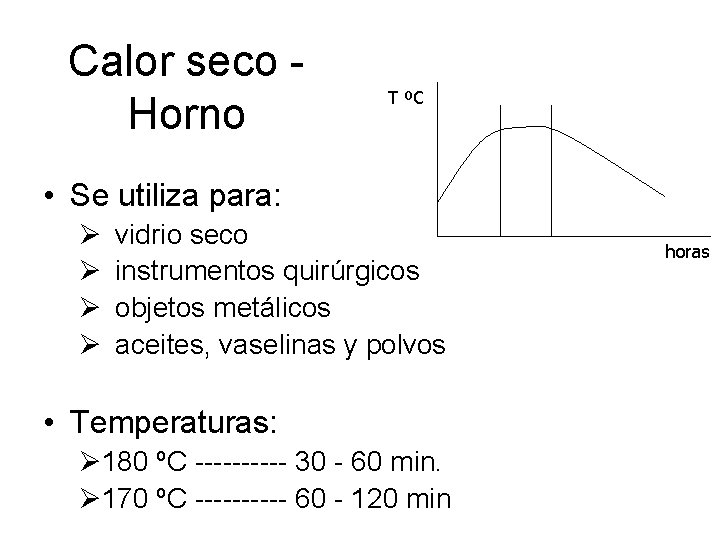
Calor seco Horno

Calor seco Horno T ºC • Se utiliza para: Ø Ø vidrio seco instrumentos quirúrgicos objetos metálicos aceites, vaselinas y polvos • Temperaturas: Ø 180 ºC ----- 30 - 60 min. Ø 170 ºC ----- 60 - 120 min horas

Calor seco • Recipientes de metal o envolver en papel (usar temp. menor en este caso) • Dejar que vuelva a temp. ambiente antes de abrir

Calor húmedo • Con presión: autoclave, olla presión • Para sustancias estables al calor – ¿combinaciones reactivos a temp altas? • Temperatura – presión – tiempo Temp. 100 115 Tiempo 20 h 2, 5 h 51 min. 121 125 130 15 min. 6, 4 min. 2, 4 min.

Autoclave

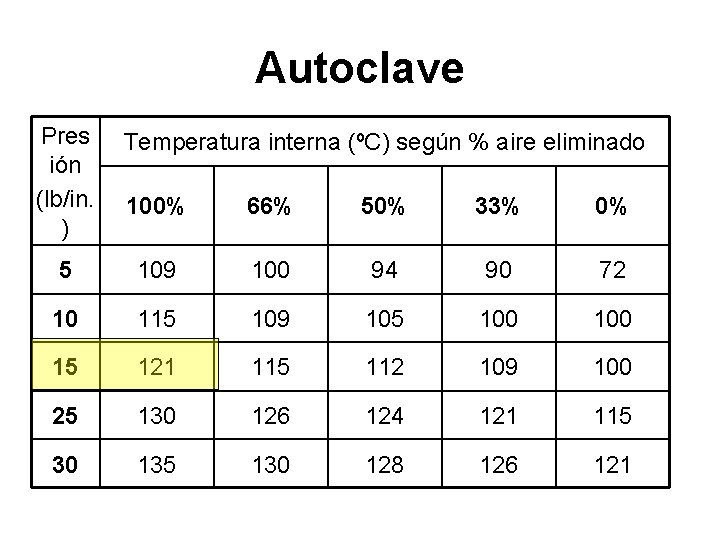
Autoclave Pres ión (lb/in. ) Temperatura interna (ºC) según % aire eliminado 100% 66% 50% 33% 0% 5 109 100 94 90 72 10 115 109 105 100 15 121 115 112 109 100 25 130 126 124 121 115 30 135 130 128 126 121

Calor húmedo - Autoclave • ¿cómo optimizar eficacia? – eliminar aire, – contenidos similares, – no apretados, dejar espacios verticales, • Precauciones: – tapas sueltas, – recipientes con hasta 1/3 de volumen, – vuelta a presión normal lenta.

Controles de esterilización a. Físicos b. Químicos c. Biológicos

Controles de esterilización a. Físicos b. Químicos c. Biológicos

Esterilización química • Ventajas: no requiere altas temperaturas ni aparatos costosos • Desventajas: mayor tiempo, sustancias inflamables y muy tóxicos y alto costo • Ejemplos: óxido de etileno, formaldehído

Esterilización por filtrado • • • Elimina microorganismos >virus Ventaja: no modifica composición Para: cantidades pequeñas Para: vitaminas, hormonas, antibióticos, etc. Requiere bomba de vacío Ejemplo membranas de ésteres de celulosa: 1 uso, “poros” de 0, 22 µm

CAMPANAS DE FLUJO LAMINAR

Radiaciones UV

Desinfección superficial

Desinfección superficial Técnicas comunes en Fitopatología: • Lavado previo en agua corriente – detergente? cepillo? • Agua corriente 2 o más horas • Alcohol 70% • Hipoclorito de sodio: – 1% Cloro activo, 2 %, 0, 35% etc. – minutos – enjuague posterior

Desinfección superficial Selección de técnica(s) según: • tejido: grosor, consistencia • hongo a aislar: ej. Oomycetes, Rhizoctonia • dónde pensamos que está el patógeno

Medios de cultivo • Componentes básicos • ¿Sólido o líquido? • Ajuste de p. H • Inhibidores de “contaminantes”: – bacterias – hongos no deseados

Clasificación de medios de cultivo • Sintéticos – más complicados para elaborar, muchos componentes • Naturales – raíces y frutos aportan lo necesario para hongos, ¿bacterias necesitan más? • Semi-sintéticos

¿Qué aportan los medios? • Soporte - Agentes solidificantes: – gelatina: fusión a 37ºC, solidifica 25 -30ºC, se descompone a 121ºC – agar: fusión a 80 -100ºC, solidifica a 35 -50ºC • Carbono orgánico – Azúcares inducen crecimiento micelio, pueden inhibir esporulación temporal- o permanentemente. • • Vitaminas y otros factores de crecimiento Inhibidores Sustancias que permiten diferenciar spp. o biotipos Indicadores

Medios comunes: • Agar papa dextrosa • Agar agua • Nutriente agar dextrosa • Agar harina de maíz • Extracto de levadura dextrosa con carbonato de calcio (Yeast Dextrose Ca. C 03) • Agar V 8 • B de King • Agar malta

Dispensado de medios • Temperatura: 45 -50ºC – mayor: condensa H 2 O – menor: solidificación prematura • Placas de Petri: aprox. 20 ml c/u • Tubos de ensayo: vertical o pico de flauta