AGENTES ANTIMICROBIANOS LIMPIEZA DESINFECCIN ESTERILIZACIN DEL MATERIAL DE

AGENTES ANTIMICROBIANOS. LIMPIEZA, DESINFECCIÓN, ESTERILIZACIÓN DEL MATERIAL DE VIDRIO E INSTRUMENTOS

• TÉCNICAS DE DESCONTAMINACIÓN – MÉTODOS FÍSICOS – MÉTODOS QUÍMICOS • OTROS AGENTES MICROBIOSTÁTICOS • TRABAJO EN AMBIENTE ESTÉRIL • APLICACIÓN DE DICHAS TÉCNICAS: – MATERIAL DE VIDRIO – EQUIPOS Y MUESTRAS
LABORATORIO TRABAJO EN AUSENCIA DE MICROORGANISMOS DESCONTAMINACIÓN • Limpieza previa a la esterilización. • Esterilización del material que estará en contacto con los microorganismos. • Desinfección periódica: reduce nº microorganismos ambientales e índices de descontaminación

IMPORTANTE: la expansión de microorganismos dará lugar a errores. MATERIAL UTILIZADO: a. - Desechable incineración b. - Reutilizable descontaminación

Conceptos 1. DESCONTAMINACIÓN: eliminación de los microorganismos patógenos que se encuentran en el material utilizado para el estudio de una muestra antes de su manejo. 2. DESINFECCIÓN: destrucción de todas las formas de vida patógenas, en proporciones causantes de enfermedades. 3. ESTERILIZACIÓN: destrucción de todas las formas de vida microbiana y de las formas de resistencia. 4. ANTISEPSIA: eliminación de microorganismos de la piel y otros tejidos vivos.

PRINCIPIOS BÁSICOS DE DESCONTAMINACIÓN 1º- Destrucción del germen por esterilización o desinfección. 2º- Limpieza DESINFECCIÓN: para superficies inertes para materiales ANTISESIA: para mucosas, piel, mano Desinfectantes Antisépticos ESTERILIZACIÓN: para reutilización del material

MÉTODOS DE DESCONTAMINACIÓN • Métodos físicos: modifican la actividad fisiológica de los microorganismos, influyendo en su desarrollo. (esterilizantes y microbiostáticos) • Métodos químicos: se utilizan sustancias químicas que actúan sobre los microorganismos. (desinfectantes y microbiostáticos)

MÉTODOS FÍSICOS Térmicos Calor directo flameado incineración Calor seco Calor húmedo Horno Pasteur o estufa Poupinel Ebullición Tindalización Métodos que utilizan vapor de agua Autoclave Vapor fluente Pasteurización Uperización No térmicos Filtración Radiaciones No ionizantes: luz solar, rayos UV, . . Ionizantes: rayos X, rayos, . . � Sedimentación

FLAMEADO: agujas, espátulas, asas tubos de ensayo… INCINERACIÓN: hornos crematorios. Guantes, jeringas, catéteres….

FLAMEAR

FLAMEAR UN ASA DE SIEMBRA
FLAMEAR LA BOCA DEL TUBO DE ENSAYO

HORNOS DE CALOR SECO • Material que se oxida en el autoclave : vidrio, porcelana. • Nunca líquidos, telas, medios de cultivo. • Carboniza la materia orgánica • Tª elevada (160 -180ºC), de 1 a 2 h y media • Esterilizan: desnaturalización de proteinas Horno Pasteur: fuente de calor, gas Horno Poupinel: fuente de calor eléctrica

CALOR HÚMEDO • EBULLICIÓN: no esteriliza. • TINDALIZACIÓN: esterilizaciones discontinuas. • AUTOCLAVE: vapor saturado a presión. Esteriliza • VAPOR FLUENTE • UPERIZACIÓN • PASTEURIZACIÓN

Ebullición: • No esteriliza • No mata las esporas • Tª 100ºC BAÑO MARIA


1 at - 120º - 20´ 2 at – 134º - 10´ 3 at – 144º - 4´ El vapor penetra por osmosis a través de la membrana, coagulando el protoplasma

• Vapor fluente: autoclave, 30´ a 100ºC. Llave de purga abierta. • Pasteurización: 30´ a 62, 8ºC. No esteriliza. Mata sólo a algunos micro. • Uperización: 1 a 20´´ a 150ºC. Esteriliza. • Tindalización: tres días a Tª entre 55º y 95º

FACTORES QUE INFLUYEN EN LA MUERTE DE LOS MICROORGANISMOS POR EL CALOR • • Nº de microorganismos. Naturaleza de los microorganismos Temperatura Tiempo de actuación: - Tiempo de penetración - Tiempo de calefacción - Tiempo de seguridad - Tiempo de enfriamiento • Método empleado: tiempo de muerte térmica. El calor húmedo es más eficaz.
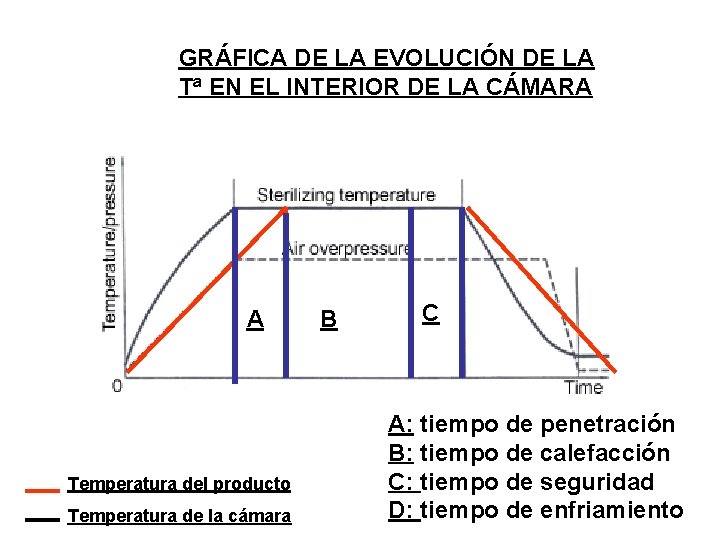
GRÁFICA DE LA EVOLUCIÓN DE LA Tª EN EL INTERIOR DE LA CÁMARA A Temperatura del producto Temperatura de la cámara B C A: tiempo de penetración B: tiempo de calefacción C: tiempo de seguridad D: tiempo de enfriamiento
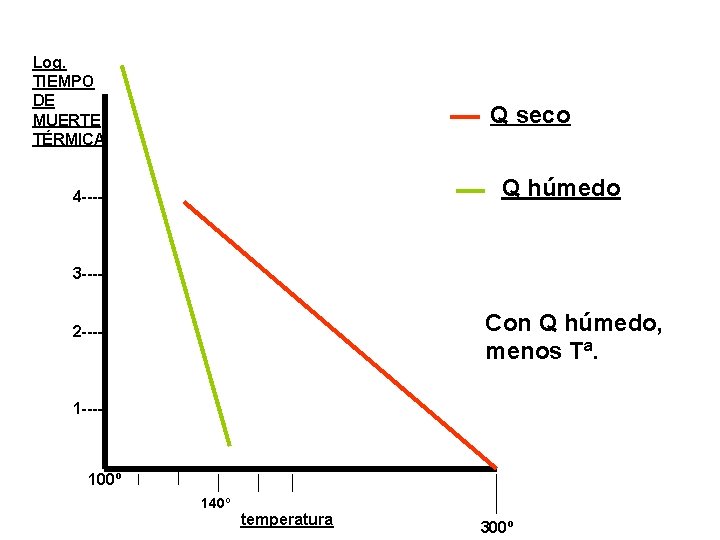
Log. TIEMPO DE MUERTE TÉRMICA Q seco Q húmedo 4 ---- 3 ---- Con Q húmedo, menos Tª. 2 ---- 100º 140º temperatura 300º

MÉTODOS NO TÉRMICOS • FILTRACIÓN: para líquidos y gases. No destruyen, sólo separan. • RADIACIONES: - Rayos UV: actúan sobre la Timina. - Rayos X ionizan el protoplasma - Rayos gamma • SEDIMENTACIÓN: en plantas potabilizadoras de agua.

Filtros: • de VERKELFELD: tierra de diatomeas • de CHAMBERLAND: porcelana porosa • de FLUJO LAMINAR: campanas • de SEITZ: discos de amianto • de MEMBRANA: de esteres de celulosa • ULTRAFILTROS: membrana coloidal
RAMPA DE FILTRACIÓN


FILTROS DE MEMBRANA

INDICADORES DE ESTERILIZACIÓN FÍSICA • MÉTODOS TÉRMICOS: Del proceso de esterilización: 1. - Químicos: Tiras reactivas. Tubos de Brown Otros: anhídrido succínico , acetanilina. 2. - Biológicos: tubos con esporas. Bacillus stearothermophillus. Del producto esterilizado: cultivar muestras. • DE FILTRACIÓN
TIRAS REACTIVAS

MÉTODOS QUÍMICOS • Se utilizan para la desinfección. • Se basan en la acción de ciertas sustancias químicas sobre los microbios. • A. - Germicidas B. - Bactericidas C. - Viricidas D. - Fungicidas E. - Amebicidas.

Los desinfectantes: caracteísticas. • • • Poder germicida No tóxicos Alto poder de penetración Económicos Inertes al material a tratar Estables y homogéneos en su composición

Los desinfectantes: actuación • • Oxidación de la célula Hidrólisis Coagulación de proteinas Alteración de la permeabilidad de la membrana • Inactivación de los enzimas • Lisis de las células En su acción influye la concentración y el modo de aplicación.

DESINFECTANTES Y ANTISÉPTICOS • DESINFECTANTES • ANTISÉPTICOS • Clorofenoles • Compuestos clorados • Ácido fénico • Detergentes catiónicos • Alcoholes • Mercurio cromo • Derivados yodados

ESTERILIZANTES • Óxido de etileno: gas. Mezclado con CO 2, a 40ºC, 5 h. Instalaciones • Glutaraldehído activado: líquido. Diluido, durante 3 horas. Material quirúrgico • Vapores de formol: desde 17º hasta 50ºC, de 48 a 2 h

OTROS AGENTES MICROBIOSTÁTICOS • Presión osmótica • Frío • Ondas sonoras • Humedad • p. H

TRABAJO EN AMBIENTE ESTÉRIL • Mechero • Cámara de flujo laminar • Esterilizantes: a. - óxido de etileno: con CO 2. A 40º, 6 h b. -Glutaraldehido: diluido. 12 h. c. - Vapores de formol: 17º 48 h, 50º 2 h

APLICACIÓN DE LOS MÉTODOS DE DESCONTAMINACIÓN 1. PREPARACIÓN DEL MATERIAL PARA LA ESTERILIZACIÓN 2. TRATAMIENTO DEL MATERIAL UNA VEZ USADO 3. MANIPULACIÓN DEL MATERIAL Y LAS MUESTRAS DE MICROBIOLOGÍA

PREPARACIÓN DEL MATERIAL PARA SU ESTERILIZACIÓN • • • Limpiar el material Envolver (así se mantendrá estéril) Papel de aluminio , poroso no inflamable (hornos) poroso para vapor para óxido de etileno. Cajas metálicas Elección de método de esterilización.

¿Cómo se prepara el material? • Pipetas: algodón en boquilla. Horno. Envueltas. • Placas de petri de vidrio: envolver, separando la tapa de la base y marcarlas. • Tubos: tapar las bocas (algodón, tapones) • Material irregular: envolver. • Material de cirugía: en cajas metálicas.

Autoclave • Tapa • Válvula de seguridad • Llave de purga: tres posiciones: - vapor: para vapor fluente - cerrada: uso normal - desagüe: para vaciado • • Selector de presión Manómetro Temporizador Tubo de purga de desagüe

AUTOCLAVE • Funcionamiento: comprobaciones • Material: vidrio, metal no oxidable, porcelana, goma, tela, medios de cultivo. • Ventajas: barato, no tóxico, útil para gran cantidad de materiales. • Desventajas: no seca, deteriora el material, menos poder de penetración. • Duración: tres meses

HORNOS DE CALOR SECO • 160º a 180º • Material: vidrio, porcelana, metal. Seco Nunca para líquidos ni material inflamable. • Ventajas: barato, fácil manejo, mayor poder de penetración. • Desventajas: estropea el material, lento • Duración de la esterilización: tres meses.

TRATAMIENTO DEL MATERIAL USADO • 1. 2. 3. Todo material que haya estado en contacto con los microorganismos debe esterilizarse en el autoclave. Después se sigue su tratamiento habitual: Vidrio: quitar tapones y otros ajustes. Lavar, aclarar, agua destilada, secar. Si han tenido vaselina o parafinar lavar aparte. Pipetas: recipientes con desinfectantes. Muy útiles en ocasiones las desechables. Material desechable: tras el autoclave, basura.

MANIPULACIÓN DE MUESTRAS Y MATERIAL 1. Material estéril 2. Manipulación en cabina o alrededor del mechero (10 -15 cm de radio) 3. Todo el material cerca 4. Rapidez al trabajar

MATERIAL • Asas: flamear • Pipetas: siempre de seguridad o automáticas. Flamear si son de vidrio. Nunca en posición horizontal. • Recipientes de vidrio (tapados): abrir, flamear, coger muestra, flamear, cerrar. • Placas: manipular semiabiertas y cerca de la llama. Si hay que abrirla totalmente, la tapa en la mesa, boca abajo.

• Muestras líquidas: asas o pipetas estériles. Recordar como se toma la muestra del tubo. • Muestras sólidas: con asa. Coger del extremo de la colonia. Precaución al abrir el tubo o la placa.
- Slides: 45