Longitud y energa de enlace ENLACES QUIMICOS Los













- Slides: 24

Longitud y energía de enlace

ENLACES QUIMICOS Los enlaces interatómicos se clasifican en: Enlaces iónicos Enlaces covalentes Enlaces metálicos

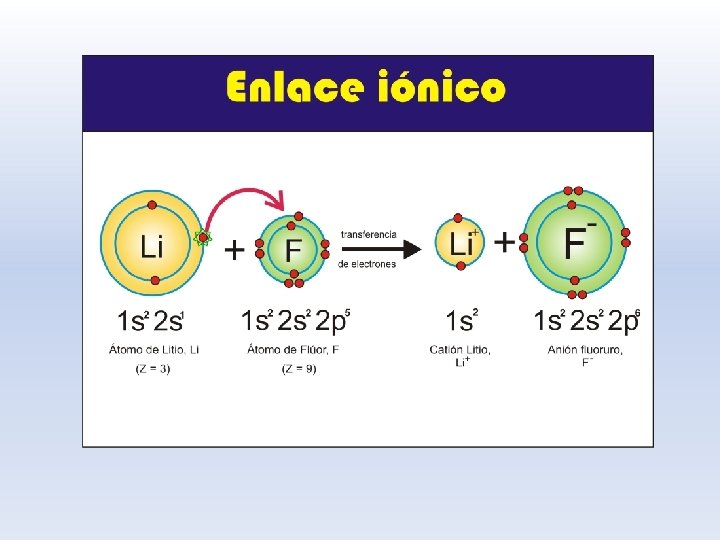
ENLACE IÓNICO: Transferencia de electrones Li F El litio le regala al flúor su electrón de valencia


¿Qué elementos forman compuestos iónicos? METAL Y UN NO METAL Recordemos: Son metales cuando electrones de valencia <4 Son no metales cuando electrones de valencia > 4 Si EN entre 2 átomos es mayor a 2 unidades

ENLACE COVALENTE: Comparte los electrones En el HCl, el hidrógeno y el cloro comparten un par de electrones

Enlace covalente : Se comparten electrones de valencia y no existe transferencia de éstos. Unión entre un No Metal y un No Metal

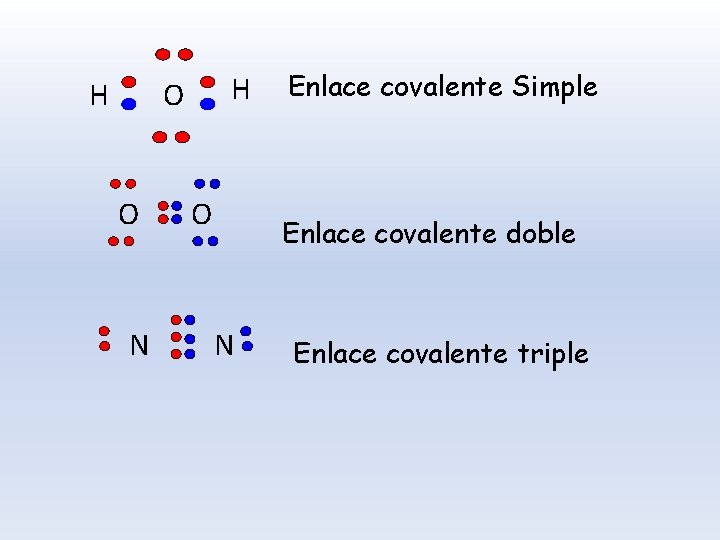
Dependiendo del número de pares de electrones que se comparten entre dos átomos, el enlace covalente puede ser simple (H 2), doble (O 2) o triple (N 2)

H H O O N O Enlace covalente Simple Enlace covalente doble N Enlace covalente triple

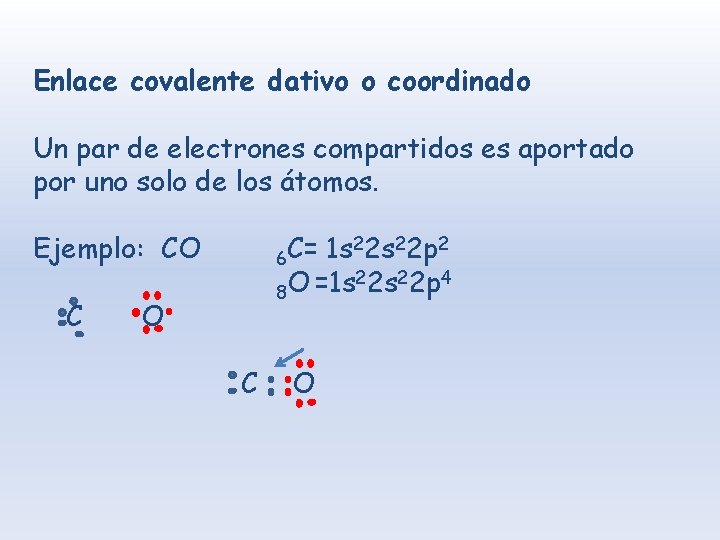
Enlace covalente dativo o coordinado Un par de electrones compartidos es aportado por uno solo de los átomos. Ejemplo: CO C 22 s 22 p 2 C= 1 s 6 22 s 22 p 4 O =1 s 8 O C O

CLASIFICACION DEL ENLACE COVALENTE Enlaces covalentes polares Enlaces covalentes apolares

Enlace covalente apolar: Se produce entre 2 átomos que presentan igual electronegatividad o levemente diferente. Los electrones compartidos son atraídos por los núcleos de similar intensidad, los è se distribuyen de manera simétrica entre los núcleos de los átomos y no generan polos o cargas parciales Ej: H 2, CH 4, CO 2

Enlace covalente polar Se produce entre átomos que tienen distinta electronegatividad. Los è no son atraídos por la misma fuerza por cada núcleo, lo cual origina cargas parciales positivas y negativas en los extremos del enlace

Enlace metálico: Es la fuerza de atracción que se establece entre un gran número de iones positivos que se mantienen unidos por una nube de electrones

Propiedades de los metales a)Tienden a oxidarse, porque ceden electrones, convirtiéndose en iones positivos b)Buenos conductores de calor y electricidad, por el movimiento de los electrones externos. c) Son dúctiles y maleables, ya que los iones de la red se desplazan sin que haya repulsión de las cargas de igual signo. d) Presentan brillo metálico debido a que la luz recibida es reflejada por los electrones libres e)Son densos, duros y alto puntos de fusión y ebullición, debido a su modelo de empaquetamiento.

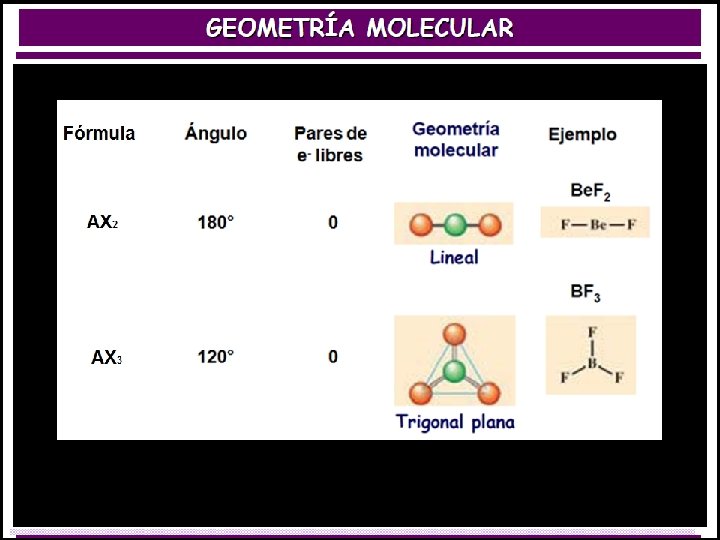
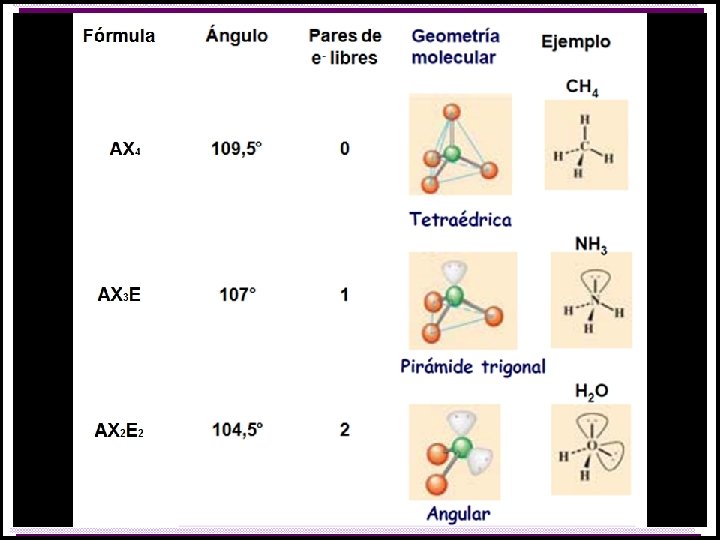
Geometría molecular Ordenamiento tridimensional de los átomos o iones en una molécula o red cristalina.



Enlaces intermoleculares: uniones entre moléculas Son las fuerzas de atracción entre moléculas. Los enlaces entre moléculas son más débiles que los enlaces interatómicos.

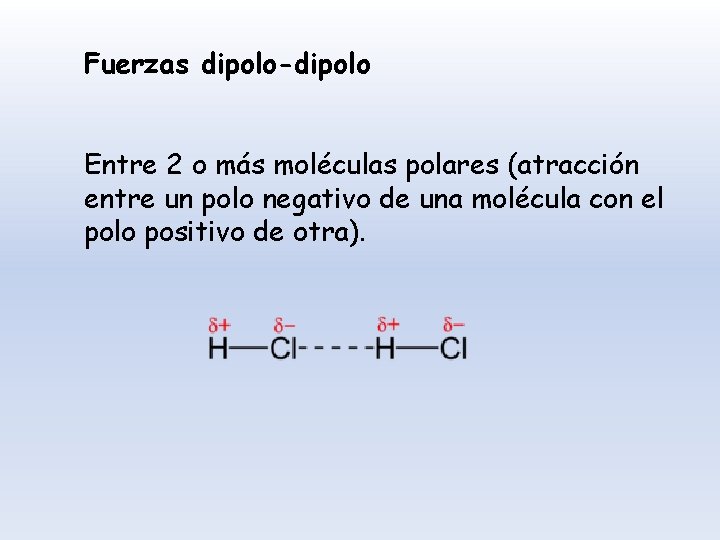
Fuerzas dipolo-dipolo Entre 2 o más moléculas polares (atracción entre un polo negativo de una molécula con el polo positivo de otra).

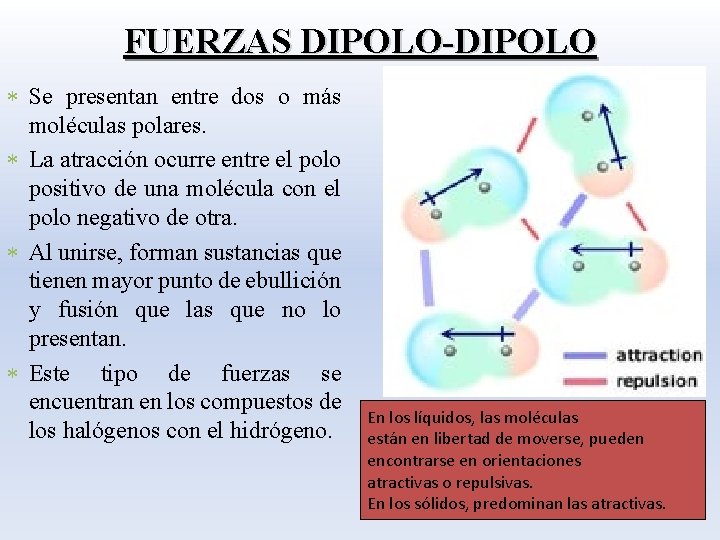
FUERZAS DIPOLO-DIPOLO * Se presentan entre dos o más moléculas polares. * La atracción ocurre entre el polo positivo de una molécula con el polo negativo de otra. * Al unirse, forman sustancias que tienen mayor punto de ebullición y fusión que las que no lo presentan. * Este tipo de fuerzas se encuentran en los compuestos de los halógenos con el hidrógeno. En los líquidos, las moléculas están en libertad de moverse, pueden encontrarse en orientaciones atractivas o repulsivas. En los sólidos, predominan las atractivas.

FUERZAS IÓN-DIPOLO * Se presenta entre los iones de una sustancia que interactúan con los polos de las moléculas covalentes polares. * Así, el polo negativo de una molécula atrae el ión positivo y el polo positivo interactúa con el ión negativo; es decir, las partes de cada molécula se unen por fuerzas de atracción de cargas opuestas.

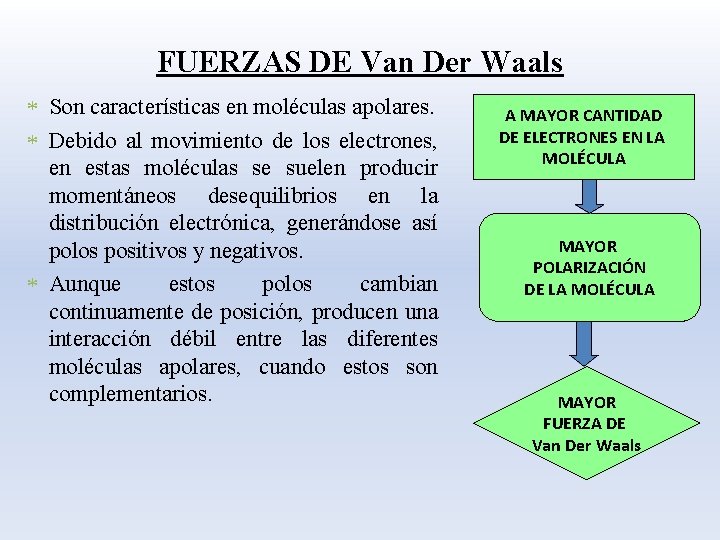
FUERZAS DE Van Der Waals * Son características en moléculas apolares. * Debido al movimiento de los electrones, en estas moléculas se suelen producir momentáneos desequilibrios en la distribución electrónica, generándose así polos positivos y negativos. * Aunque estos polos cambian continuamente de posición, producen una interacción débil entre las diferentes moléculas apolares, cuando estos son complementarios. A MAYOR CANTIDAD DE ELECTRONES EN LA MOLÉCULA MAYOR POLARIZACIÓN DE LA MOLÉCULA MAYOR FUERZA DE Van Der Waals

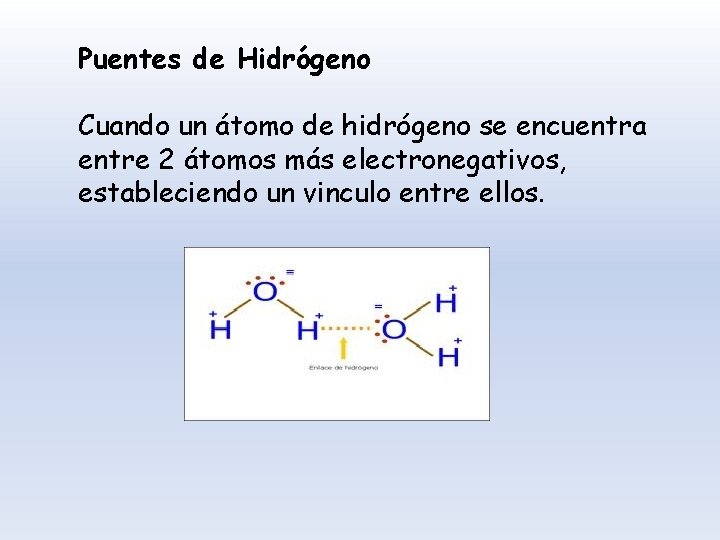
Puentes de Hidrógeno Cuando un átomo de hidrógeno se encuentra entre 2 átomos más electronegativos, estableciendo un vinculo entre ellos.