FORMULACIN INORGNICA COMPUESTOS TERNARIOS COMPUESTOS INORGNICOS COMPUESTOS BINARIOS

FORMULACIÓN INORGÁNICA COMPUESTOS TERNARIOS
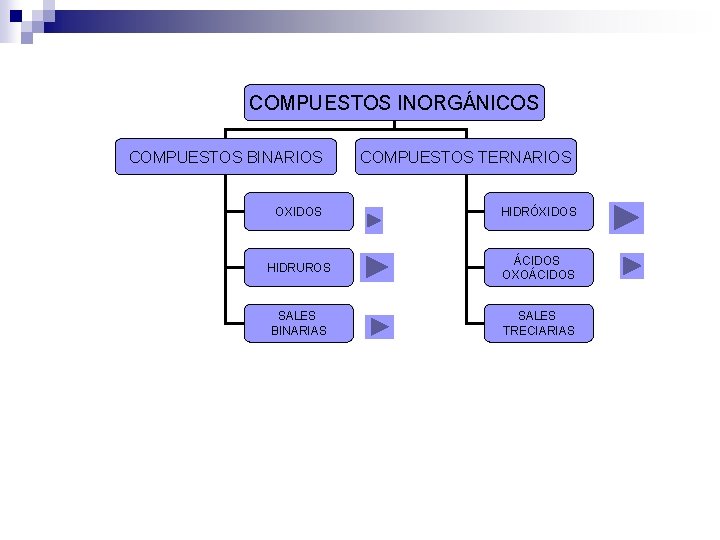
COMPUESTOS INORGÁNICOS COMPUESTOS BINARIOS COMPUESTOS TERNARIOS OXIDOS HIDRÓXIDOS HIDRUROS ÁCIDOS OXOÁCIDOS SALES BINARIAS SALES TRECIARIAS
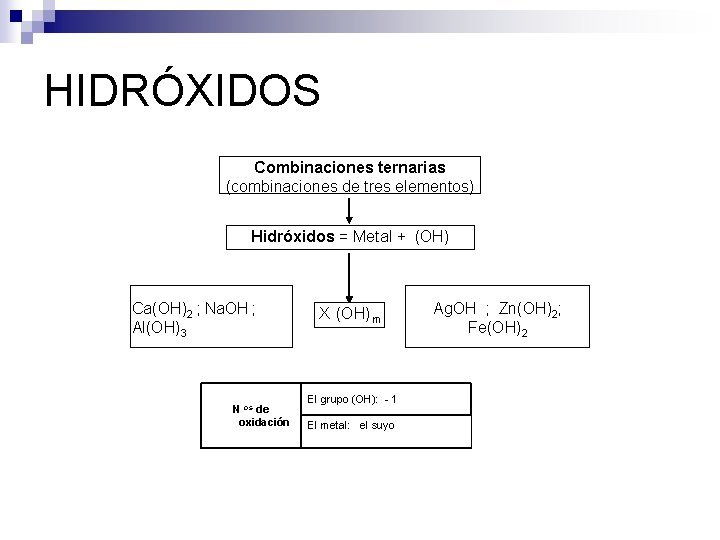
HIDRÓXIDOS Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal + (OH) Ca(OH)2 ; Na. OH ; Al(OH)3 N os de oxidación X (OH) m El grupo (OH): - 1 El metal: el suyo Ag. OH ; Zn(OH)2; Fe(OH)2
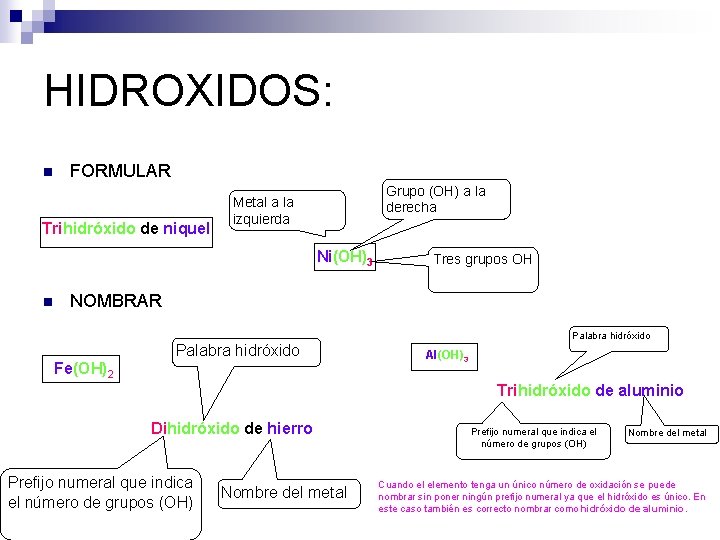
HIDROXIDOS: n FORMULAR Trihidróxido de niquel Grupo (OH) a la derecha Metal a la izquierda Ni(OH)3 n Tres grupos OH NOMBRAR Palabra hidróxido Fe(OH)2 Al(OH)3 Trihidróxido de aluminio Dihidróxido de hierro Prefijo numeral que indica el número de grupos (OH) Nombre del metal Cuando el elemento tenga un único número de oxidación se puede nombrar sin poner ningún prefijo numeral ya que el hidróxido es único. En este caso también es correcto nombrar como hidróxido de aluminio.

ACIDOS OXOACIDOS ¿Qué son? Se llaman oxácidos u oxoácidos, y obedecen a una fórmula general: OXOÁCIDOS = Hidrógeno - No metal - Oxígeno Ha. Xb. Oc en la que X es normalmente un no metal, pero a veces también puede ser un metal de transición que se encuentra en un número de oxidación elevado, como Cr+6, Mn+6 o Mn+7.
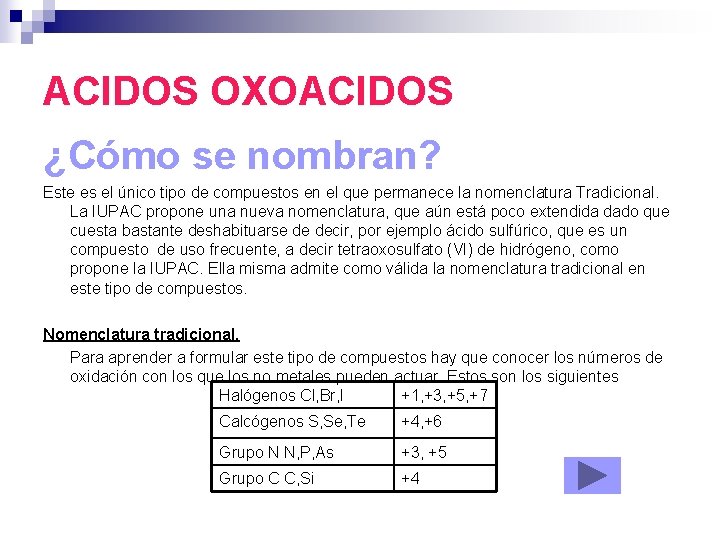
ACIDOS OXOACIDOS ¿Cómo se nombran? Este es el único tipo de compuestos en el que permanece la nomenclatura Tradicional. La IUPAC propone una nueva nomenclatura, que aún está poco extendida dado que cuesta bastante deshabituarse de decir, por ejemplo ácido sulfúrico, que es un compuesto de uso frecuente, a decir tetraoxosulfato (VI) de hidrógeno, como propone la IUPAC. Ella misma admite como válida la nomenclatura tradicional en este tipo de compuestos. Nomenclatura tradicional. Para aprender a formular este tipo de compuestos hay que conocer los números de oxidación con los que los no metales pueden actuar. Estos son los siguientes Halógenos Cl, Br, I +1, +3, +5, +7 Calcógenos S, Se, Te +4, +6 Grupo N N, P, As +3, +5 Grupo C C, Si +4

ACIDOS OXOACIDOS Nomenclatura tradicional NOMBRAR +n -2 Si nos dan la fórmula del ácido tenemos que deducir el número de oxidación del +1 elemento central X (+n). Una vez deducido añadiremos los prefijos según la tabla de -1*a+2*b (+1)*a+b*(+n)+c*(-2)=0 despejamos n n= abajo. Ha X b O c Nº Oxidación Cl, Br, I (+1, +3, +5, +7) Mas bajo Hipo____-oso Bajo b S, Se, Te (+4, +6) N, P, As (+3, +5) ________-oso Alto ________-ico Más alto Per_____-ico C, Si (+4) ____-ico
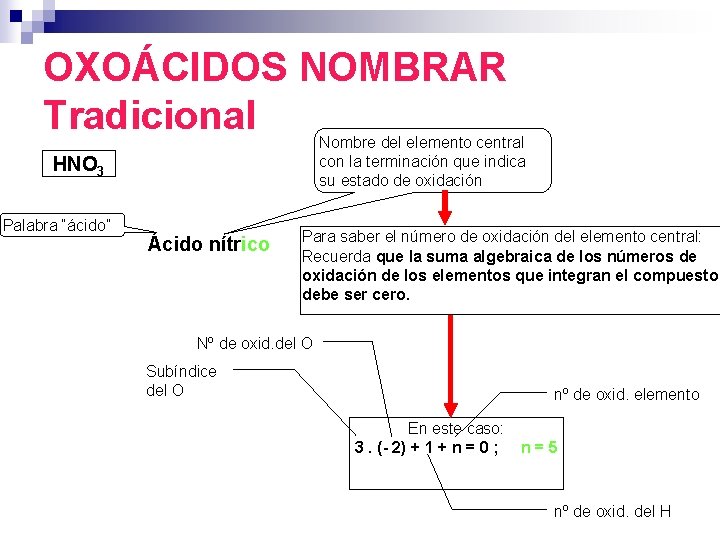
OXOÁCIDOS NOMBRAR Tradicional Nombre del elemento central con la terminación que indica su estado de oxidación HNO 3 Palabra “ácido” Ácido nítrico Para saber el número de oxidación del elemento central: Recuerda que la suma algebraica de los números de oxidación de los elementos que integran el compuesto debe ser cero. Nº de oxid. del O Subíndice del O nº de oxid. elemento En este caso: 3. (- 2) + 1 + n = 0 ; n=5 nº de oxid. del H
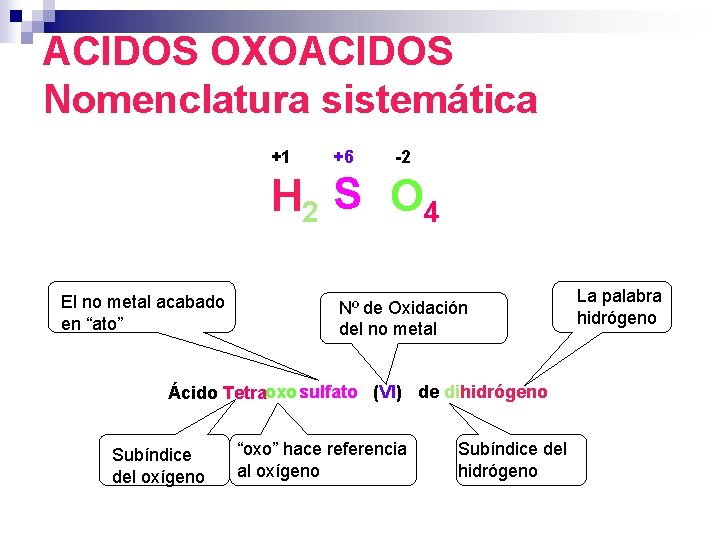
ACIDOS OXOACIDOS Nomenclatura sistemática +1 +6 -2 H 2 S O 4 El no metal acabado en “ato” Nº de Oxidación del no metal Ácido Tetraoxo sulfato (VI) de dihidrógeno Subíndice del oxígeno “oxo” hace referencia al oxígeno Subíndice del hidrógeno La palabra hidrógeno
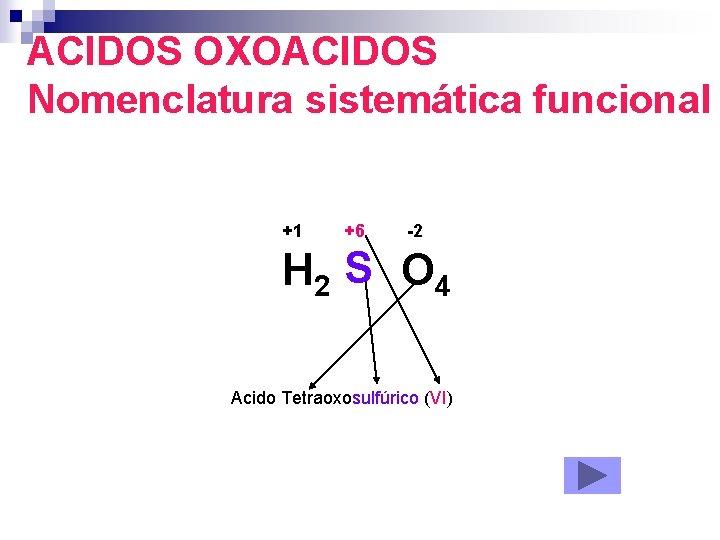
ACIDOS OXOACIDOS Nomenclatura sistemática funcional +1 +6 -2 H 2 S O 4 Acido Tetraoxosulfúrico (VI)

ACIDOS OXOACIDOS Formulación tradicional A partir de los prefijos y sufijos deducimos el número de oxidación del elemento central. El hidrógeno tiene número de oxidación +1 y el oxígeno -2. Buscamos luego unos coeficientes que hagan que la carga aportada por los oxígenos sea igual y de signo contrario a la aportada por los hidrógenos y el elemento central. Ácido perclórico +1 +7 -2 H Cl O 4
- Slides: 11