IMMUNOSUPPRESSION ET SES COMPLICATIONS 09 2006 Pr Lionel





























- Slides: 33

IMMUNOSUPPRESSION ET SES COMPLICATIONS 09 -2006 Pr. Lionel Rostaing

n Cellules impliquées dans les défenses : l Polynucléaires neutrophiles : phagocytent les bactéries, les parasites l Monocytes : produisent des médiateurs de l ’inflammation l Macrophages : cellules tissulaires; détruisent des parasites, les virus, certaines bactéries; présentent l ’antigène au lymphocytes T l Lymphocytes B : produisent des anticorps l Lymphocytes T CD 4 : reconnaissent l ’antigène étranger; sécrètent de l ’IL 2 qui va activer les lymphocytes l Lymphocytes T CD 8 : sont des cellules tueuses des cellules infectées ou des cellules étrangères.

Traitement immunosuppresseur n Deux situations : Ü Organe greffé : Ü il faut un traitement immunosuppresseur puissant bloquant la présentation de l’antigène, les lymphocytes T (réponse allogénique cellulaire contribuant au rejet aigu) et les lymphocytes B (réponse allogénique humorale contribuant au rejet chronique) Ü Maladie auto-immune : Ü il faut un traitement immunosuppresseur puissant bloquant essentiellement les lymphocytes B car ces maladies sont médiées par des auto-anticorps

Conséquences : n Greffe d’organe : Ü Il faut bloquer toutes les étapes de la réponse immune allant de la reconnaissance de l’antigène à l’activation lymphocytaire T et B. Cela implique d’utiliser une COMBINAISON d’immunosuppresseurs n Maladies auto-immunes : Ü Il faut bloquer uniquement la réponse immunitaire médiée par les lymphocytes B : UN SEUL médicament suffit souvent

Traitement immunosuppresseur en greffe d’organes 1. Mise en place d ’un organe HLA différent : il n’y a pas de tolérance 1. réaction de rejet aigu : présentation des antigènes du greffon par les macrophages du donneur (présentation directe) ou du receveur (présentation indirecte) au système immunitaire (lymphocytes T) du receveur 1. activation des lymphocytes T 2. production d ’interleukine 2 3. génération de lymphocytes T cytotoxiques ( « destructeurs » ) 4. génération de lymphocytes B dirigés spécifiquement contre les Ag HLA du donneur


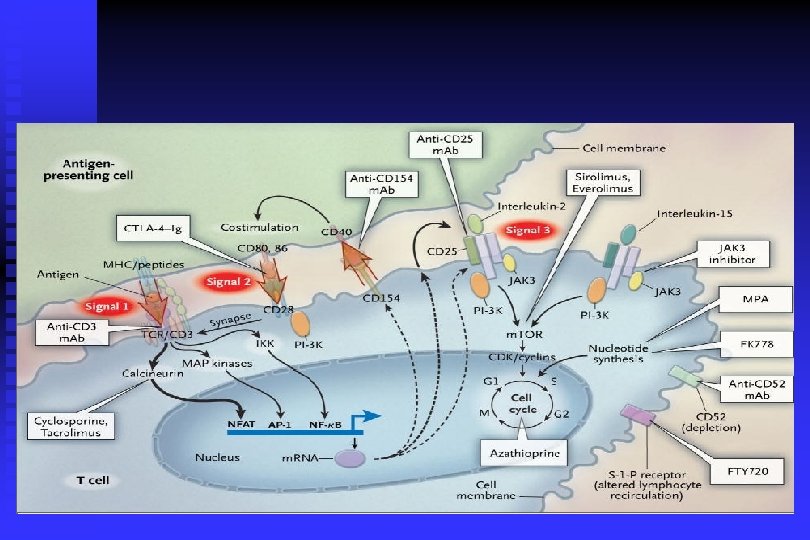
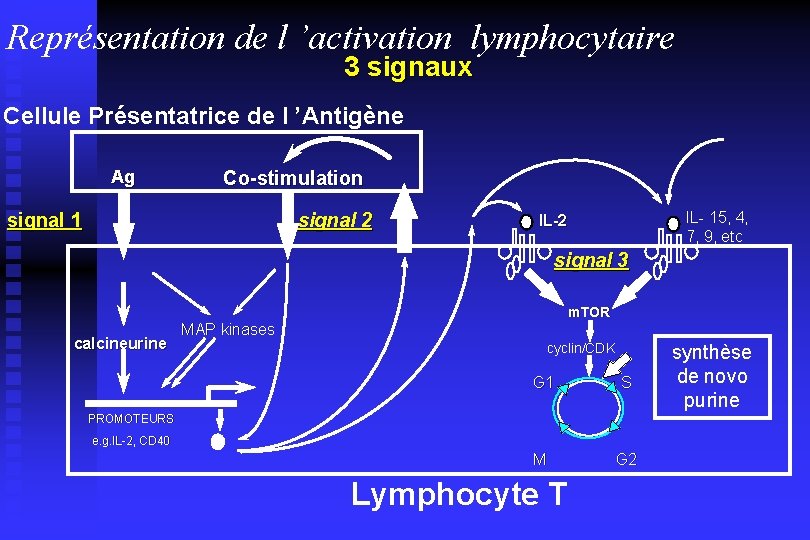
Représentation de l ’activation lymphocytaire 3 signaux Cellule Présentatrice de l ’Antigène Ag Co-stimulation signal 2 signal 1 IL- 15, 4, 7, 9, etc IL-2 signal 3 calcineurine m. TOR MAP kinases cyclin/CDK G 1 S M G 2 PROMOTEURS e. g. IL-2, CD 40 Lymphocyte T synthèse de novo purine

Les immunosuppresseurs Corticoïdes : Solumédrol®, Cortancyl®, Solupred® Azathioprine : Imurel® (Glaxo-Welcome) Ciclosporine : Sandimmun®/Néoral® (Novartis) Tacrolimus/FK 506 : Prograf® (Astellas) Mycophenolate Mofetil : Cell. Cept® (Roche); Myfortic® (Novartis) Sirolimus/Rapamycine : Rapamune® (Wyeth-Ayerst) Evérolimus : Certican® (Novartis) Sérums anti-lymphocytaires et Anticorps Polyclonaux : ATG/ALG; Thymoglobulins® (Genzyme, Frésénius) Monoclonaux : Murin : OKT 3, Orthoclone® (Janssen-Cilag), anti-CD 2 Chimérique : Basiliximab, Simulect® (Novartis), anti-RIL 2 Humanisé : Daclizumab, Zénapax® (Roche), anti-RIL 2 Dirigé contre le 2° signal (B 7/CD 28): Bélatacept (BMS)

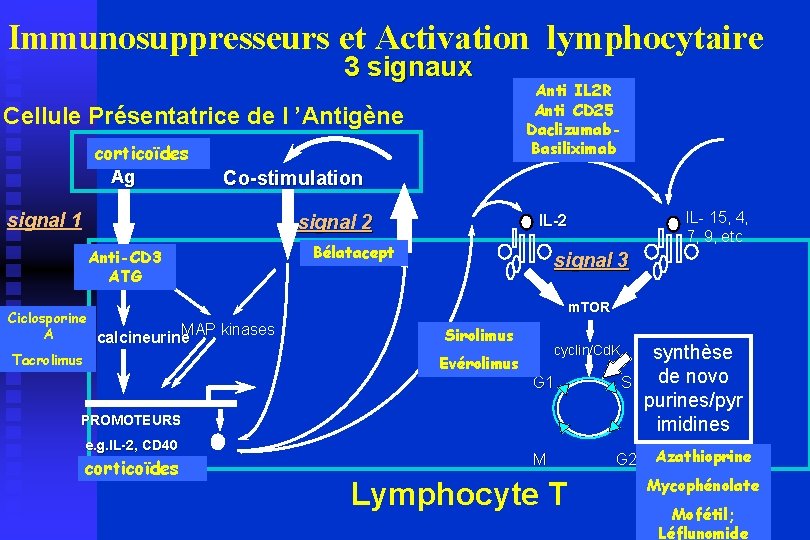
Immunosuppresseurs et Activation lymphocytaire 3 signaux Cellule Présentatrice de l ’Antigène corticoïdes Ag Co-stimulation signal 1 signal 2 Anti-CD 3 ATG Ciclosporine MAP kinases A calcineurine Tacrolimus Anti IL 2 R Anti CD 25 Daclizumab. Basiliximab IL- 15, 4, 7, 9, etc IL-2 Bélatacept signal 3 m. TOR Sirolimus Evérolimus cyclin/Cd. K G 1 S M G 2 PROMOTEURS e. g. IL-2, CD 40 corticoïdes Lymphocyte T synthèse de novo purines/pyr imidines Azathioprine Mycophénolate Mofétil; Léflunomide

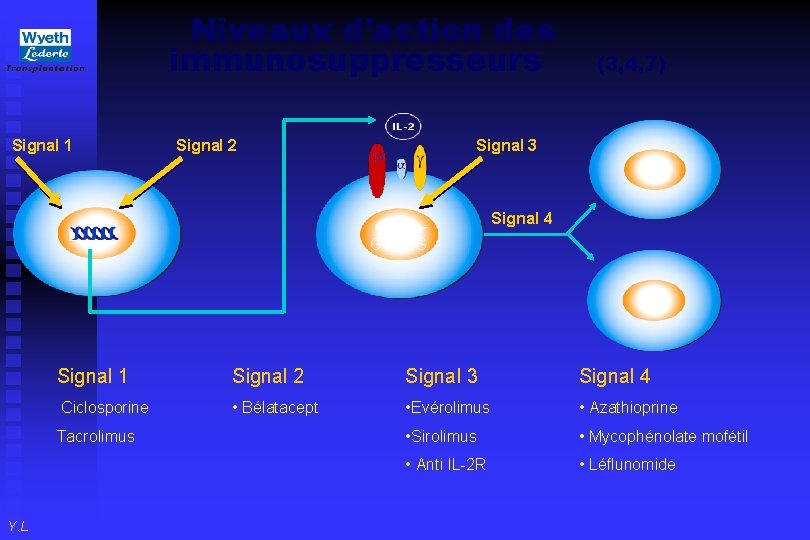
Niveaux d’action des immunosuppresseurs Signal 1 Signal 2 (3, 4, 7) Signal 3 Signal 4 G 1 Signal 2 Signal 3 Signal 4 Ciclosporine • Bélatacept • Evérolimus • Azathioprine • Sirolimus • Mycophénolate mofétil • Anti IL-2 R • Léflunomide Tacrolimus Y. L S

n Immunosuppression u Indispensable F maximale de J 0 à J 90 puis lentement dégressive « vitesse de croisière à 1 an » u Très diversifiée Présentation de l ’antigène * corticoïdes * sérum antilymphocytaire Activation du Ly T CD 4+ IL 2 *anti-calcineurines *Ac Anti-RIL 2 (Ciclosporine A =Néoral® Tacrolimus = Prograf®) * blocage 2° signal (Bélatacept) X X Recrutement des Ly T CD 8+ et de Ly B * Antimétabolites (Azathioprine = Imurel ®, Mycophénolate mofétil = Cellcept ® / Myfortic ®) *Antiprolifératifs (Sirolimus = Rapamune ®) les corticoïdes une anti-calcineurine un anti-prolifératif ou un anti-métabolite ± traitement d ’induction en post-greffe immédiat

n Avec les immunosuppresseurs actuels : u peu de rejets aigus (< 20 %) u forte immunosuppression initiale (3 à 6 premiers mois) puis décroissance u utiliser peu (pas) de corticoïdes u prévenir la néphrotoxicité des anti-calcineurines (Néoral® , Prograf®)

Traitement d’nduction : n En post-opératoire précoce n administration d’anticorps dirigés contre les lymphocytes T permettant de détruire transitoirement les lymphocytes T (sérum anti-) ou de leurrer les lymphocytes T (anticorps dirigés contre le récepteur de l’interleukine 2) : Ü Pas de réponse immune dans jours qui suivent Ü Permet aux autres médicaments anti-rejet d’être efficaces ( « steady state » )

Ciclosporine A / Néoral® n 22 ans d ’utilisation comme immunosuppresseur Sandimmun® u Néoral® Sandimmun® à 2 prises par jour u Bloque la production d’IL 2 par les lymphocytes T activés (réversible) à moins de rejets aigus u n Surveillance du traitement par ciclosporine A u u u clinique = créatininémie (néphrotoxique) C 2 = taux mesuré 2 heures ± 10 mn après prise (500 à 1000 ng/ml) Aire sous la courbe abrégée (AUC) à patients de novo : éviter le rejet aigu patients en maintenance : prévenir la néphrotoxicité chronique / le rejet chronique à Allongement de la 1/2 vie des greffons rénaux (16 ans) à

n Indication de la Ciclosporine A n Prévention du rejet de greffe d ’organe n Maladies auto-immunes : ª Aplasie médullaire primitive ª Syndrome néphrotique cortico-résistant ª Uvéite ª Autres : l psoriasis l polyarthrite rhumatoïde

Tacrolimus: Prograf® n 15 ans d ’utilisation comme immunosuppresseur n Bloque de façon réversible la production d’IL 2 par les lymphocytes T activés n 2 prises par jour n Surveillance du traitement par le taux résiduel (5 à 15 ng/ml) n Est néphrotoxique n Effet diabétogène : n u dépend des doses utilisées u majoré par l ’administration de corticoïdes Allongement de la 1/2 vie des greffons rénaux (18 ans)

n Indications du Prograf® n Prévention du rejet aigu de greffe d ’organes n Traitement de certains rejets aigus (greffe hépatique) n Maladies auto-immunes ª Psoriasis (forme générale et topique) ª Autres ?

Effets secondaires

n Corticoïdes n n Anti-inflammatoires Bloquent le système immunitaire ª monocytes ª lymphocytes T à très fortes doses prévention du rejet aigu (< 1 mg/kg/j) traitement du rejet aigu (10 mg/kg/j) n Effets secondaires n n Faciès cushingoïde Ostéopénie ª densitométie osseuse annuelle ª traitement substitutif n n n Ostéonécrose (tête fémorale) Cholestérol et triglycérides Intolérance aux glucides Cataracte HTA (rétention hydrosodée) Fragilité cutanée

Cellcept® / Myfortic® n Prodrogues de l ’acide mycophénolique (MPA) u u u Mycophénolate mofétil : Cellcept® : absorption gastrique Mycophénolate sodique : Myfortic®: absorption intestinale meilleure exposition au MPA Bloquent la synthèse des bases puriques (lymphocytes T, lymphocytes B) : diminution de la réponse T et baisse de la production d’anticorps 2 prises par jour Effets secondaires F F u leucopénie thrombopénie anémie troubles digestifs : diarrhée, nausées, atrophie villositaire syndrome de malabsorption Dosage F F taux résiduel, non informatif aire sous la courbe (AUC)

Sirolimus (Rapamune®) / Evélorimus (Certican®) n Inhibiteurs de la protéine m. Tor dans le lymphocyte T inhibition de la prolifération cellulaire n Action sur la cellule endothéliale/myocytes à inhibition de la prolifération vasculaire n Propriétés anti-tumorales u chez l ’animal u chez l ’homme ? n Effets synergiques quand utilisés avec la ciclosporine A ; effets additifs quand utilisés avec le Cellcept® ou le Prograf® n Une prise par jour n Taux résiduel : 7 à 15 ng/ml

n Effets secondaires (dose-dépendants) u leucopénie u thrombopénie u anémie microcytaire u dyslipidémie F cholestérol (LDL) F triglycérides u LDH u rénaux F F tubulopathie (hypokaliémie, hypophosphorémie) toxicité glomérulaire et tubulo-interstitielle quand donnés au long cours avec le Néoral®

Parmi les médicaments efficaces sur le lymphocyte B u Corticoïdes Cellcept® / Myfortic® Rituximab (Mabthéra ®) (anticorps monoclonal anti-CD 20) u Cyclophosphamide = Endoxan® u u F Agent cytostatique S’intercale au niveau de l’ADN : toxicité à long terme (leucémies) 1 prise par jour F Surveillance F F • clinique – leucopénie / thrombopénie – anémie – Troubles vésicaux • biologique : pas de dosage

Quelques complications des traitements immunosuppresseurs n Infectieuses n Néoplasiques

COMPLICATIONS INFECTIEUSES n n Infections opportunistes ++ Infection parasitaire : pneumocystis jiroveci u n prévenues par la prise pendant les 6 premiers mois de greffe de Bacrtim ® Infections virales : u La plus fréquente est l’infection à cytomégalovirus (CMV) : risque important u (primoinfection, réactivation, réinfection) pendant les 6 premiers mois Clinique * fièvre, leucopénie * cytolyse hépatique * créatininémie avec protéinurie de novo u u Diagnostic : virémie Traitement Curatif: Ganciclovir IV 2 à 3 semaines Préventif: valganciclivir oral pendant 3 à 6 mois

COMPLICATIONS CANCEREUSES u Incidence augmente ( X 5 à 1000 en fonction du type de cancer) F u durée d ’exposition aux immunosuppresseurs (1/2 vie du greffon de 8 -10 ans à 1618 ans) Cancers cutanés F F F spino/basocellulaires avec durée de greffe varie en fonction • des types de peau • des régions du globe Ü risque de dissémination Ø dépistage annuel Ø si présent chirurgie Ø si récidive envisager modification immunosuppression ( arrêt anti-calcineurine, arrêt anti-métabolite, switch pour le sirolimus) • mélanomes : rares, mais beaucoup plus graves

n Lymphomes u Précoces : induits par le virus Epstein Barr (EBV) u Tardifs F localisés (greffon, ou autre organe) F disséminés F polymorphes ou monomorphes (polyclonal ou monoclonal) F phénotype B (> 90 % des cas), souvent CD 20+ F pronostic transformé depuis l ’utilisation d ’anticorps monoclonal anti CD 20 (Mabthéra®) : > 50 % de guérison Ø Traitement : Ø Mabthéra® : si échec, chimiothérapie Ø baisse immunosuppression : arrêt anti-calcineurine, switch sirolimus

n Autres cancers u Col utérin (papilloma virus) F dépistage annuel u Sarcome de Kaposi (dû à l’herpès virus HHV 8) F les populations à risque : pourtour méditerranéen ; Afrique noire ; Asie du Sud Est) u Sein F mammographie tous les 2 ans u Poumons F radiographie pulmonaire annuelle

n Rénales : u Insuffisance rénale iatrogène (quelque soit l’organe) reliée à la prise d’anti-calcineurines (Néoral ® / Prograf ®) u Dysfonction chronique du greffon rénal de créatininémie F protéinurie de-novo F u Prévention facteurs de risque (HTA associée, tabac, dyslipidémie, …) F optimiser immunosuppression/C 2 pour le Néoral ® /nouveaux immunosuppresseurs F

n Cardio-vasculaires : u Première cause de mortalité chez le transplanté rénal u Facteurs de risque • période pré- transplantation • produit phosphocalcique élevé • hyperhomocystéinémie • dyslipidémie • HVG • HTA • tabagisme F période post-transplantation • • tabagisme dyslipidémie insulino-résistance HTA ØDépistage ØPrise en charge des facteurs de risque ØMinimiser les corticoïdes

n Métaboliques : u Dyslipidémie : F F F corticoïdes Sirolimus/Evérolimus anticalcineurines (Néoral® > Prograf®) 1. LDL (cible < 1 g/l) 2. triglycérides 1. • • • u prise en chargediététique statines fibrates Médiator® Insulino-résistance/diabète : corticoïdes F anticalcineurines (Prograf® > Néoral®) 1. surveiller Hb glyquée 2. prise en charge : • diététique • antidiabétiques oraux : Amarel®; Glucor® F

n Osseuses : u Précoces : F ostéonécrose aseptique de la tête fémorale • corticothérapie à fortes doses (rejet aigu) • hypertriglycéridémie… F algodystrophie reliée à la prise d ’anticalcineurines (SAPIC) • lésions touchant les genoux, les chevilles, le massif tarsien • facteurs associés : – hyperparathyroïdie préexistante ou persistante – long passé d ’hémodialyse u Tardives : F ostéopénie/ostéoporose • corticothérapie • anticalcineurines (Néoral®) Ø Ménopause Ø ostéodensitométrie annuelle Ø prise au long cours d ’un traitement vitamino-calcique (Ca++, Vita D 3) associé à un biphosphonate Ø efficace à terme

n Evaluer les risques du patient n n n 1ère greffe sujet agé (> 60 ans) race blanche pas d ’Ac anti-HLA donneur vivant Antécédents de vs vs vs greffe itérative enfant race noire Ac anti-HLA donneur cadavérique ª maladie virale (hépatites B ou C) ª cancer n Choix d ’une immunosuppression plus ou moins lourde ª phase initiale (< 3 mois) ª phase ultérieure (> 6 mois) : prévenir le rejet aigu : prévenir le rejet chronique