HPV vaccinatie QA INTERACTIEVE CURSUS COLPOSCOPIE EN LAGE










![Anti-HPV response (GMT Levels with 95% CI [log 10 scale]) Demonstration of Immune Memory Anti-HPV response (GMT Levels with 95% CI [log 10 scale]) Demonstration of Immune Memory](https://slidetodoc.com/presentation_image/7d9f81defbe6b762321ebd061736525c/image-21.jpg)

















- Slides: 41

HPV vaccinatie: Q&A INTERACTIEVE CURSUS COLPOSCOPIE EN LAGE GENITALE TRACTUS PATHOLOGIE

dankbetuiging • Vragen o. a. afkomstig van de lentevergadering van de VVOG, maart 2007: – – – Philippe De Sutter Patrick Dhont Marc de Ridder Patricia Claeys Willy Poppe UZ Brussel SP-MSD GSK UZ Gent, Volksgezondheid UZ Leuven

1. HPV vaccins : 1. Zijn in Vlaanderen overbodig vermits cervixkanker geen belangrijk probleem is 2. Bieden weinig meerwaarde vermits we in Vlaanderen toch een goed screeningsbeleid hebben 3. Zijn enkel nuttig indien ze gelinkt worden aan regelmatige screening 4. Worden pas nuttig wanneer er voldoende types in verwerkt worden zodat screening overbodig wordt

Nut van HPV vaccins voor Vlaanderen • Huidige vaccins bieden zeker meerwaarde! • Op dit ogenblik: slechts 60% van vrouwen regelmatig gescreend • Echter: indien niet gelinkt aan regelmatige screening gaat voordeel verloren!!!

2. Het eerste meetbare effect van de vaccinatie in de populatie is : 1. Vermindering van het aantal patiënten met genitale wratten 2. Vermindering van het aantal abnormale uitstrijkjes met een LSIL celbeeld 3. Vermindering van het aantal abnormale uitstrijkjes met een ASCUS celbeeld 4. Vermindering van het aantal patiënten met JORRP

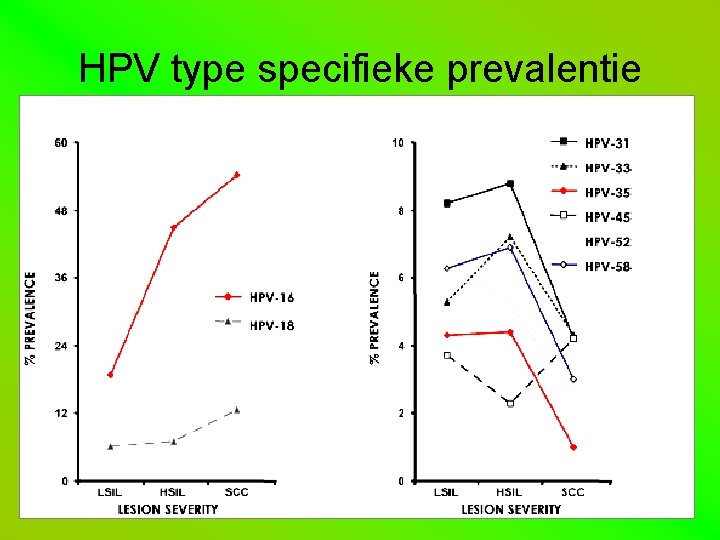
HPV type specifieke prevalentie

Target van het vaccin = reductie van cervicale afwijkingen op alle levels ICC PREVENTIE: 67 -76% HSIL PREVENTIE: 52 -60% LSIL PREVENTIE: 14 -25% ASC-US PREVENTIE: ~20%

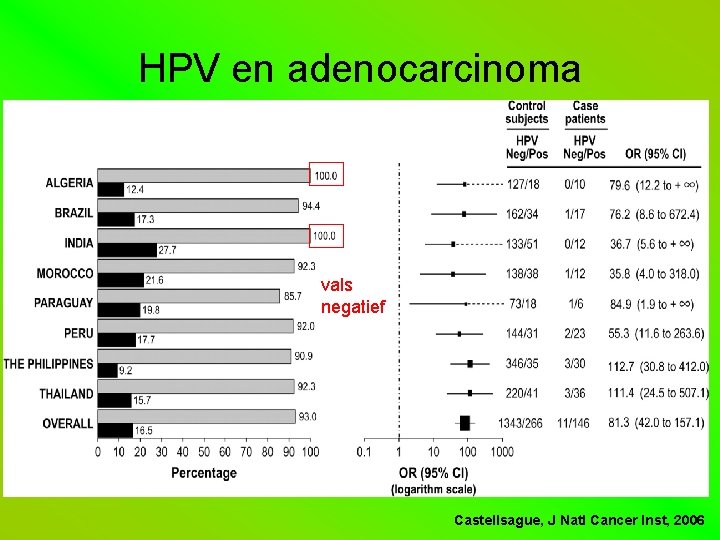
HPV en adenocarcinoma vals negatief Castellsague, J Natl Cancer Inst, 2006

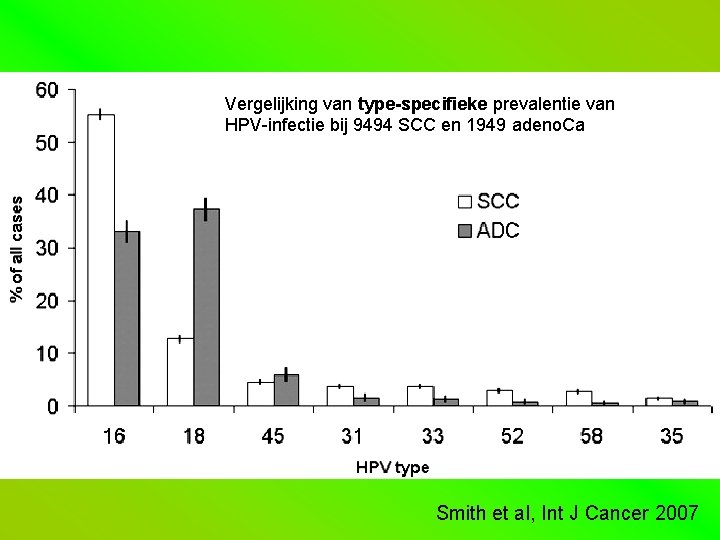
Vergelijking van type-specifieke prevalentie van HPV-infectie bij 9494 SCC en 1949 adeno. Ca Smith et al, Int J Cancer 2007

3. Een bivalent HPV 16/18 vaccin werd bestudeerd in een RCT voor de preventie van pre-cancereuse letsels bij sero (-) en HPV DNA (-) vrouwen van 15 -25 j. 1. 100 % efficiëntie tegen persisterende infecties gedurende 12 maanden 2. Een klinische kruisbescherming tegen HPV 45 en 31 die respectievelijk de 3 e en 4 e meest voorkomende oncogene HPV types zijn 3. Dat de antilichaam titer na vaccinatie, 14 à 17 maal hoger is dan de natuurlijke infectie en dit 4, 5 jaar na vaccinatie 4. Alle antwoorden zijn correct

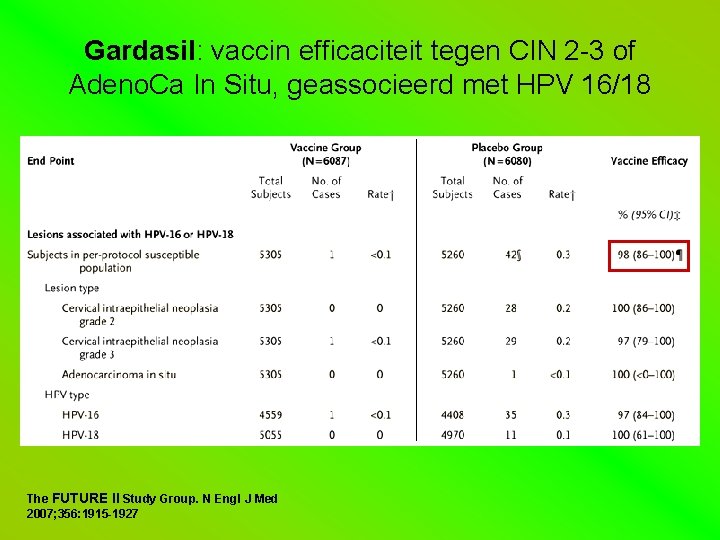
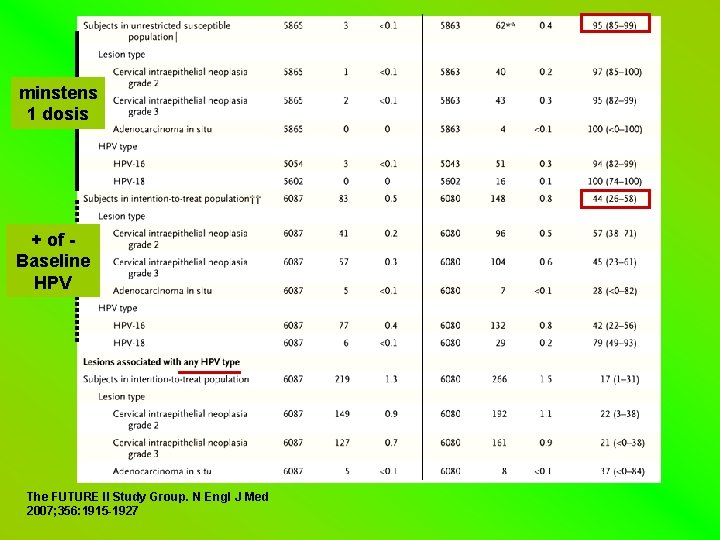
Gardasil: vaccin efficaciteit tegen CIN 2 -3 of Adeno. Ca In Situ, geassocieerd met HPV 16/18 The FUTURE II Study Group. N Engl J Med 2007; 356: 1915 -1927

minstens 1 dosis + of Baseline HPV The FUTURE II Study Group. N Engl J Med 2007; 356: 1915 -1927

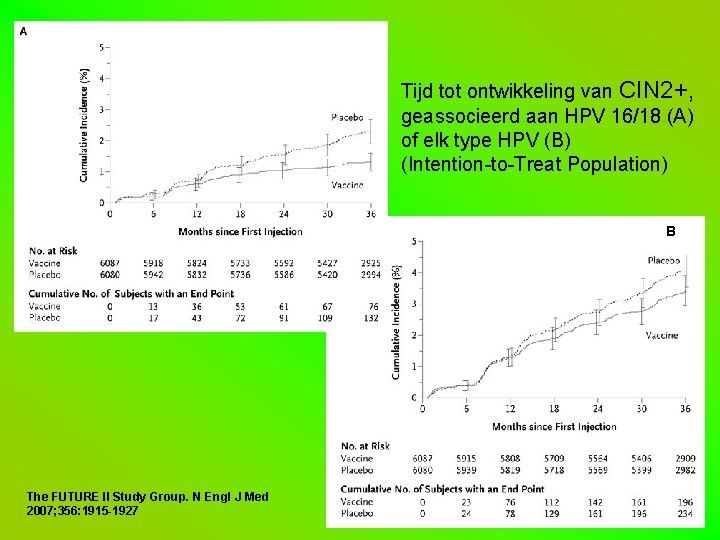
Tijd tot ontwikkeling van CIN 2+, geassocieerd aan HPV 16/18 (A) of elk type HPV (B) (Intention-to-Treat Population) B The FUTURE II Study Group. N Engl J Med 2007; 356: 1915 -1927

4. Huidige vaccin(s) tegen HPV type 16/18 beschermen enkel tegen deze HR-HPV types. 1. Ja 2. Nee 3. Weet niet

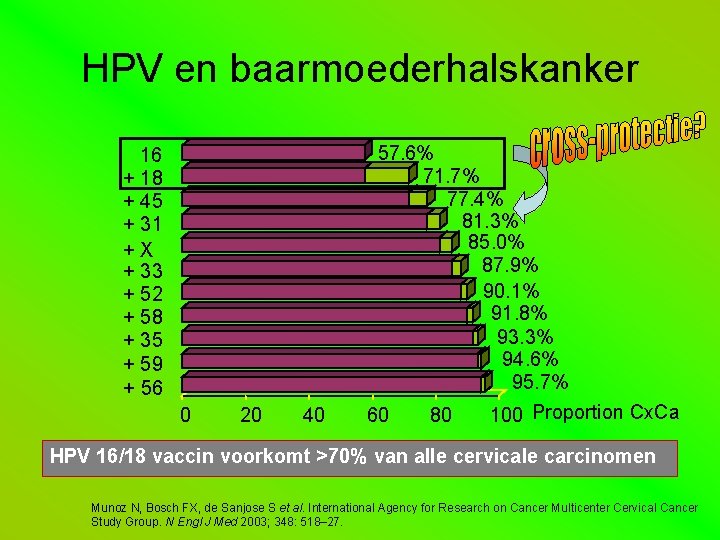
HPV en baarmoederhalskanker 16 + 18 + 45 + 31 +X + 33 + 52 + 58 + 35 + 59 + 56 0 20 40 57. 6% 71. 7% 77. 4% 81. 3% 85. 0% 87. 9% 90. 1% 91. 8% 93. 3% 94. 6% 95. 7% 60 80 100 Proportion Cx. Ca HPV 16/18 vaccin voorkomt >70% van alle cervicale carcinomen Munoz N, Bosch FX, de Sanjose S et al. International Agency for Research on Cancer Multicenter Cervical Cancer Study Group. N Engl J Med 2003; 348: 518– 27.


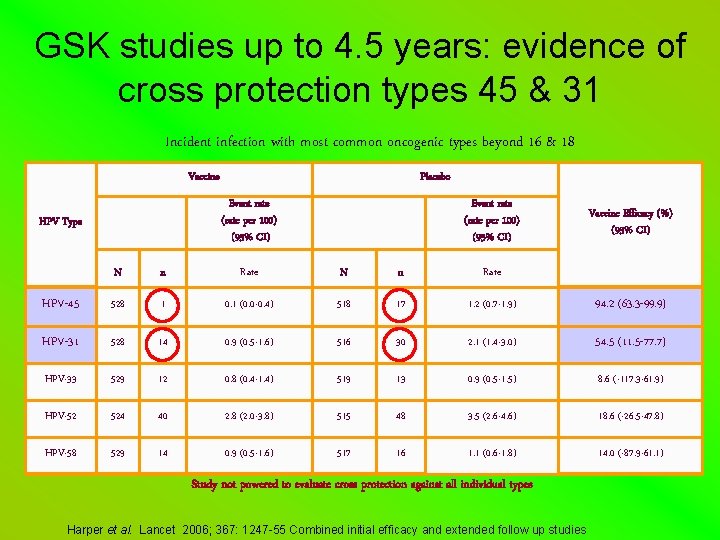
GSK studies up to 4. 5 years: evidence of cross protection types 45 & 31 Incident infection with most common oncogenic types beyond 16 & 18 Vaccine Placebo Event rate (rate per 100) (95% CI) HPV Type Event rate (rate per 100) (95% CI) Vaccine Efficacy (%) (95% CI) N n Rate HPV-45 528 1 0. 1 (0. 0 -0. 4) 518 17 1. 2 (0. 7 -1. 9) 94. 2 (63. 3 -99. 9) HPV-31 528 14 0. 9 (0. 5 -1. 6) 516 30 2. 1 (1. 4 -3. 0) 54. 5 (11. 5 -77. 7) HPV-33 529 12 0. 8 (0. 4 -1. 4) 519 13 0. 9 (0. 5 -1. 5) 8. 6 (-117. 3 -61. 9) HPV-52 524 40 2. 8 (2. 0 -3. 8) 515 48 3. 5 (2. 6 -4. 6) 18. 6 (-26. 5 -47. 8) HPV-58 529 14 0. 9 (0. 5 -1. 6) 517 16 1. 1 (0. 6 -1. 8) 14. 0 (-87. 9 -61. 1) Study not powered to evaluate cross protection against all individual types Harper et al. Lancet 2006; 367: 1247 -55 Combined initial efficacy and extended follow up studies

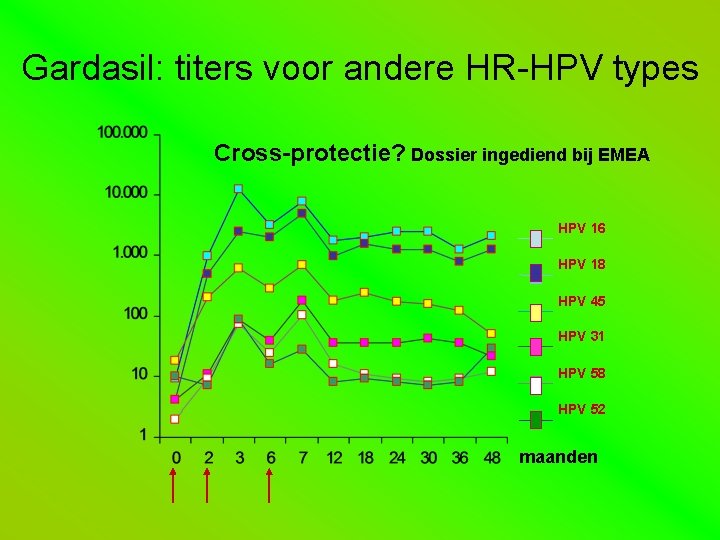
Gardasil: titers voor andere HR-HPV types Cross-protectie? Dossier ingediend bij EMEA HPV 16 HPV 18 HPV 45 HPV 31 HPV 58 HPV 52 maanden

5. Hoe lang werkt het vaccin? 1. 2. 3. 4. 5. 5 jaar 10 jaar 15 jaar 20 jaar Men weet het nog niet

Bescherming met HPV vaccinatie (Gardasil) op lange termijn • Studiegegevens tot 5 jaar na vaccinatie tonen behoud van bescherming van 100 % op CIN 2 -3 (Villa et al Br J Cancer 2006) • HPV antistoffen titers vertonen een plateaufase na 2 jaar (Villa et al Vaccine 2006) • Aanwijzingen voor anamnestische respons: Groep vrouwen nieuwe toediening 5 jaar na basisvaccinatie met 3 doses (cfr infra) • Modeling antistoffen anti HPV-16 geven indicatie voor “near life-long persistance of detectable anti-HPV 16” (Fraser C – ICID 2006)
![AntiHPV response GMT Levels with 95 CI log 10 scale Demonstration of Immune Memory Anti-HPV response (GMT Levels with 95% CI [log 10 scale]) Demonstration of Immune Memory](https://slidetodoc.com/presentation_image/7d9f81defbe6b762321ebd061736525c/image-21.jpg)
Anti-HPV response (GMT Levels with 95% CI [log 10 scale]) Demonstration of Immune Memory with an Antigen Challenge at Month 601 10, 000 Immune memory demonstrated after immune challenge HPV 16 1000 Quadrivalent HPV Vaccine n=78 100 10 Placebo (Sero (–) and PCR (–)) n=70 ↴ 0 2 3 6 7 12 18 24 30 36 Months Vaccination on day 0, at two and six months Immune challenge at 60 months • Similar results seen with HPV 18, 6, and 11 *In subjects naïve to the relevant HPV type from day 1 through month 60 1. Data on file, MSD. 54 60 61 60+1 week

6. Effect van Gardasil toegediend na infectie met HPV type(s) van het vaccin? Vaccinatie van een vrouw met een actieve infectie met één van de HPV types aanwezig in het vaccin – zonder klinisch letsel thv cervix- geeft een reductie van CIN 2 -3 met ongeveer …. • • • 0% 25 % 75 % 100 % Weet niet

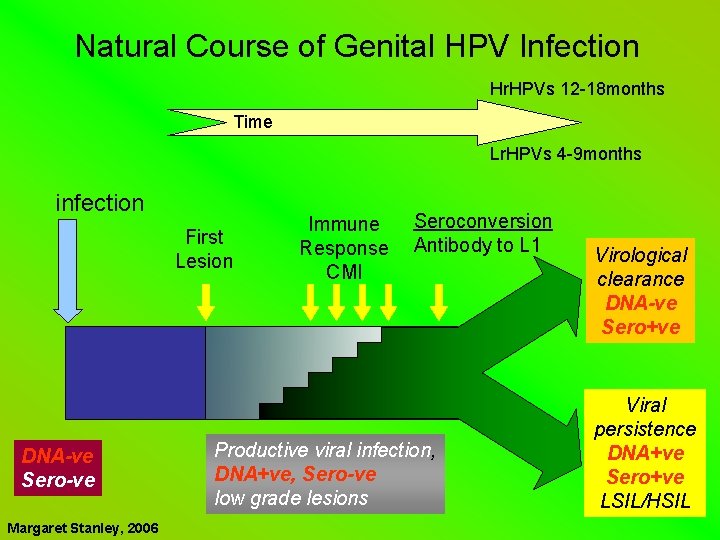
Natural Course of Genital HPV Infection Hr. HPVs 12 -18 months Time Lr. HPVs 4 -9 months infection First Lesion DNA-ve Sero-ve Margaret Stanley, 2006 Immune Response CMI Seroconversion Antibody to L 1 Productive viral infection, DNA+ve, Sero-ve low grade lesions Virological clearance DNA-ve Sero+ve Viral persistence DNA+ve Sero+ve LSIL/HSIL

Effect van Gardasil op de incidentie van cervicale neoplasie bij vrouwen recent blootgesteld aan HPV Serologie Negatief HPV Serologie Positief PCR Negatief HPV-naïef Vroeger blootgesteld, infectie geklaard PCR Positief Recente/huidige Infectie Persistente HPV infectie, gefaalde immuunrespons

Effect of quadrivalent HPV L 1 VLP vaccine on incidence of cervical neoplasia in women recently or previously exposed to HPV PCR +/(= DNA +/-) At day 1 Serology* +/At day 1 Quid? Efficacy cervix Reference - + - - + + No sign of HPV infection Not infected or past infection without antibodies detected 100% Bijsluiter Gardasil *test not commercially available – serology only analysed in study Typespecifieke immunoassays, “competitive Luminex-based immunoassay” (c. LIA) met typespecifieke standaarden werden gebruikt om de immunogeniciteit voor elk type van het vaccin te beoordelen. Deze test meet antilichamen tegen neutraliserende epitopen voor elk HPV-type. New – recent HPV infection No antibodies detected (yet) Past HPV infection Current or Persistant HPV Infection with production of antibodies but unsatisfactory immune respons Trend of 28% reduction of CIN 2 -3 (NS) Higher antibody titers compared to naïve population ** No efficacy Olsson et al. (Eurogin 2006) Villa et al Vaccine 2006 Olsson et al. (Eurogin 2006) ** At month 2 (postdose 1), among women with vaccine-types antibodies at baseline, vaccine-induced anti-HPV responses were ~ 12 - to 26 -fold higher than those observed In baseline-naïve women, suggesting an anamnestic response.

7. Op middellange termijn zal als gevolg van de HPV vaccinatie : • Het screeningsbeleid niet veranderen • Het risico op cervixkanker verminderen en zullen vrouwen dus minder vaak gescreend moeten worden • Het risico op cervixkanker op jonge leeftijd verminderen en zullen vrouwen dus later gescreend moeten worden • HPV testing gebruikt worden als screeningstest in plaats van cytologie

Invloed vaccinatie op screeningsbeleid • Op korte termijn: geen • Op middellange termijn: minder letsels, cytologie wordt minder gevoelig • HPV testen zullen hoogstwaarschijnlijk meer en meer gebruikt worden als primaire screeningstest (echter nog geen richtlijnen ter zake) • Mogelijks ook invloed op leeftijd en frequentie van screenen, maar follow-up data hiervoor nodig

8. Moet je een HPV test uitvoeren voor vaccinatie? 1. Ja, omdat HPV positieven niet meer moeten gevaccineerd worden 2. Ja, omdat HPV testing exact bepaalt wie nog HPV ‘naief’ is 3. Ja, omdat HPV negatieven die gevaccineerd worden, niet meer moeten gescreend worden 4. Nee, omdat het de kostprijs van de vaccinatie verhoogt 5. Nee, omdat een HPV test niet aangeeft wie reeds in het verleden met een HPV type in contact geweest is, een serologische test wel. 6. Nee, omdat het vaccin toch beschermt tegen de andere HPV types waarmee men nog niet in contact geweest is.

HPV-bepaling & Vaccinatie • Doel HPV-test in het kader van vaccinatie tegen HPV – meisjes/vrouwen identificeren die nog niet in contact geweest zijn met HPV types aanwezig in het vaccin • Verloop Natuurlijke HPV-infectie – Virus slechts tijdelijk aanwezig/aantoonbaar – HPV infectie aantoonbaar maar frequent voor ander types dan deze van het vaccin (Lancet 2005) – Seksueel debuut staat niet onmiddellijk gelijk aan verwerven van HPV infectie, laat staan van HPV infectie met de vaccintypes (doch risico stijgt met leeftijd, aantal partners…) – HPV-DNA test identificeert enkel actieve infectie, geen eerder contact – HPV-DNA type-specifiek test is niet kosteloos – Serologische HPV-test is weinig betrouwbaar en niet commercieel beschikbaar; voorlopig enkel gebruikt in studieverband

9. Wanneer de derde dosis toedienen wanneer patiënte zwanger wordt • • Na het eerste trimester Na de zwangerschap Na de borstvoeding Nooit

10. Het heeft bewezen nut om ook mannen te vaccineren • Ja • Nee • Weet het niet

HPV vaccinatie bij mannen? • Geen bewijs van effectiviteit • Niet kosten-effectief

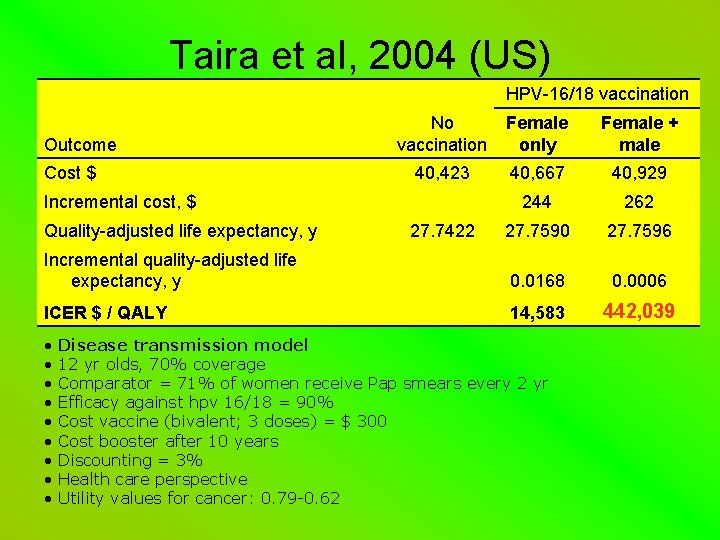
Taira et al, 2004 (US) HPV-16/18 vaccination No vaccination Female only Female + male 40, 423 40, 667 40, 929 244 262 27. 7590 27. 7596 Incremental quality-adjusted life expectancy, y 0. 0168 0. 0006 ICER $ / QALY 14, 583 442, 039 Outcome Cost $ Incremental cost, $ Quality-adjusted life expectancy, y 27. 7422 • Disease transmission model • 12 yr olds, 70% coverage • Comparator = 71% of women receive Pap smears every 2 yr • Efficacy against hpv 16/18 = 90% • Cost vaccine (bivalent; 3 doses) = $ 300 • Cost booster after 10 years • Discounting = 3% • Health care perspective • Utility values for cancer: 0. 79 -0. 62

11. De introductie van HPV vaccinatie zal : • Geen invloed hebben op de vraag van mijn patiënten naar uitstrijkjes • Er toe leiden dat meer vrouwen spontaan vragen naar een uitstrijkje • Er toe leiden dat minder vrouwen spontaan vragen naar een uitstrijkje • Er toe leiden dat vooral jonge vrouwen sneller naar uitstrijkjes vragen

• Meer informatie kan leiden tot verhoogde vraag naar screening MAAR • Gevaar dat gevaccineerde personen zich “beschermd” voelen en zich niet meer laten screenen

Het vaccin: practisch • 0, 5 m. L, intramusculair (SC en intradermaal nooit getest) • schema: 0 -2 -6 maanden – 2 e toediening minstens 1 maand na de 1 e – 3 e minstens 3 maanden na de 2 e – Alle 3 binnen het jaar

neveneffecten • Geen SAE • Meer bij adolescents dan bij jonge vrouwen (13 vs 7%) • Injectieplaats: – – Pijn Zwelling Erytheem Pruritus 84% 25% 3% (vs. 75%) (vs. 16%) (vs. 18%) (vs. 3%) • Koorts 10% (vs. 9%) • Hoofdpijn, gastro-enteritis, appendicitis, PID (0, 02 -0, 03%) • 0, 1% kon geen vaccin meer krijgen wegens neveneffecten



