Hoofdstuk 5 Paragraaf 3 Rekenen aan reacties Voorkennis









































- Slides: 57

Hoofdstuk 5 Paragraaf 3 Rekenen aan reacties

Voorkennis Molaire massa: De massa van 1 mol. . . . (Tabel 98 of 99) Molair volume van een gas: . . Het volume van 1 mol gas 3 mol⁻ 1 Bij 273 K en p=p 0: Vm = 22, 4. 10⁻. . . . =. . . 22, 4 dm 3 mol⁻ 1 Bij 298 K en p=p 0: Vm = 24, 5. 10⁻. . . . = 24, 5 dm 3 mol⁻ 1. . . Molariteit (van een oplossing): . . . . Het aantal (m)mol opgeloste stof in 1 (m)L

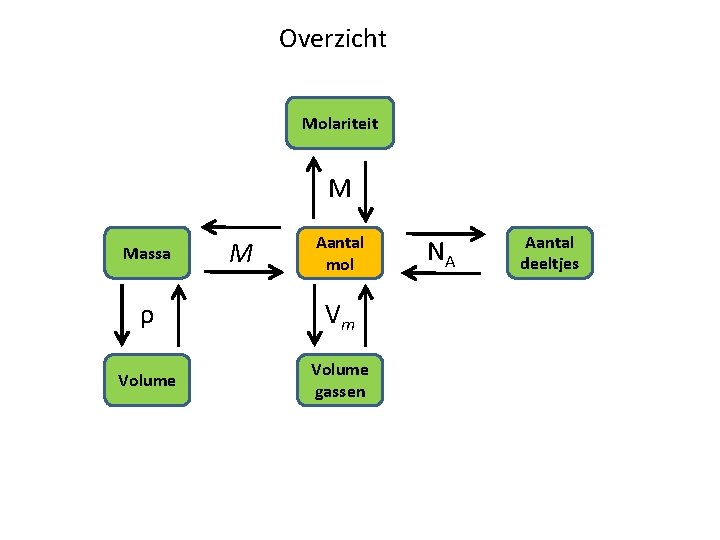
Overzicht Gebruikte symbolen: g mol⁻ 1 M : Molaire. . . . . massa. . . Vm : . . . . Molair volume (gas) 3 mol⁻ 1 dm. . . M: Molariteit (oplossing). . . . mol L⁻ 1 of mmol m. L⁻ 1. . . . ρ: Dichtheid. . . kg m⁻ 3 / (k)g dm⁻ 3 / g cm⁻ 3. . . . .

Overzicht Molariteit M Massa M Aantal mol ρ Vm Volume gassen NA Aantal deeltjes

De vergelijking van de reactie van waterstof met zuurstof is: 2 H 2 O(l) 2 H 2(g) + O 2(g) Microniveau: 2 moleculen H 2 reageren met. . . . . 1 molecuul O 2 waarbij 2. . . moleculen H 2 O ontstaan Macroniveau: 2 mol H 2 moleculen reageren met 1. . . . mol O 2 moleculen mol H 2 O moleculen ontstaan waarbij 2. . . .

De vergelijking van de reactie van waterstof met zuurstof is: 2 H 2 O(l) 2 H 2(g) + O 2(g) Hoeveel mol H 2 moleculen zijn nodig om met 4, 0 mol O 2 moleculen te reageren? Uit de reactievergelijking blijkt: 2 mol H 2 moleculen 1 mol O 2 moleculen reageren met. . Dus: 4 mol O 2 moleculen reageren met. . . 8 mol H 2 moleculen

Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Wanneer er over een stof iets gevraagd wordt en er over een andere stof iets gegeven is, gebruik je het 7. . . . . stappenplan

Het 7 stappenplan Stap 1: Stap 2: Stap 3: Stap 4: Stap 5: Stel de (kloppende) reactievergelijking op. Van welke stof is de hoeveelheid gegeven en van welke stof is de hoeveelheid gevraagd? Wat is de molverhouding tussen de gegeven stof en de gevraagde stof? Reken de gegeven hoeveelheid stof om in mol. Bereken uit het aantal mol van de gegeven stof (stap 4) en de molverhouding (stap 3) het aantal mol van de gevraagde stof.

Het 7 stappenplan Stap 6: Reken het aantal mol van de gevraagde stof (stap 5) om in de gevraagde eenheid. Stap 7: Rond je eindantwoord af op de juiste significantie.

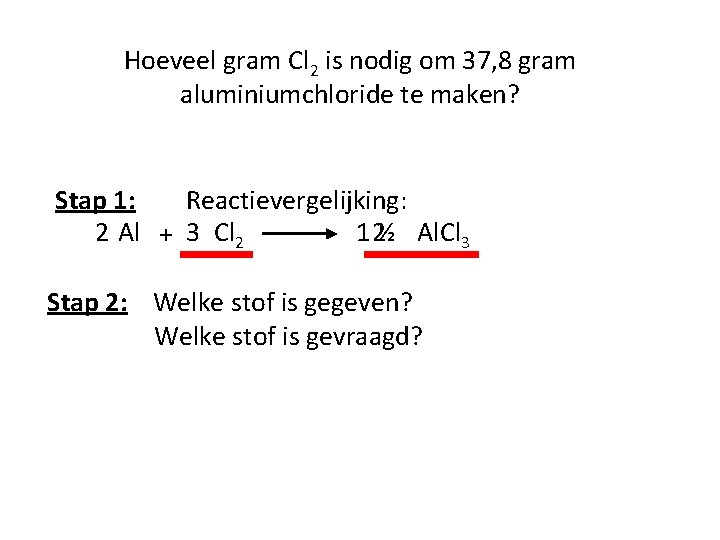
Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 1: Reactievergelijking: 2 Al + 3 Cl 2 1 2½ Al. Cl 3 Stap 2: Welke stof is gegeven? Welke stof is gevraagd?

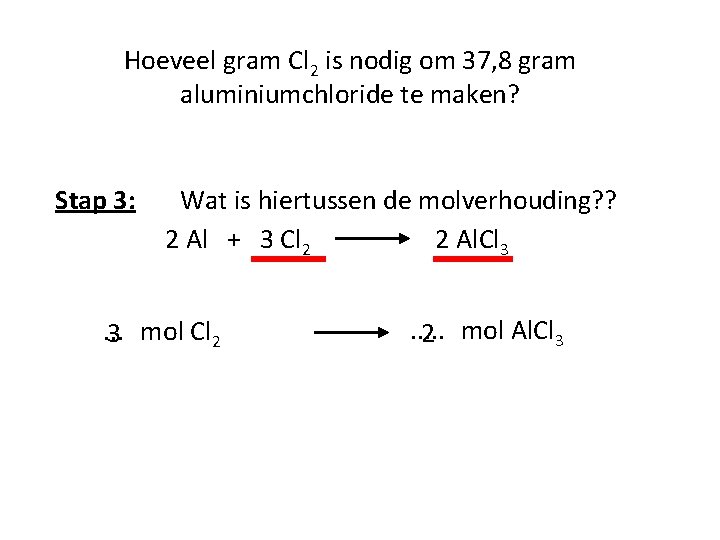
Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 3: Wat is hiertussen de molverhouding? ? 2 Al + 3 Cl 2 2 Al. Cl 3 . . . 3 mol Cl 2 . . . 2 mol Al. Cl 3

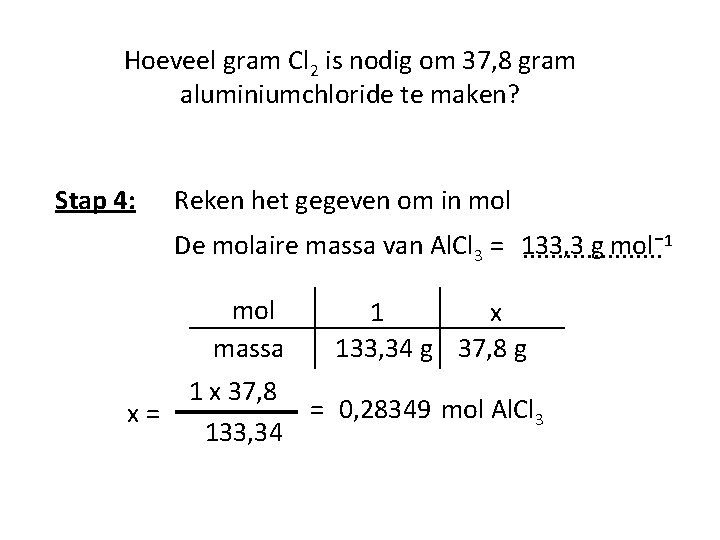
Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 4: Reken het gegeven om in mol g mol⁻ 1 De molaire massa van Al. Cl 3 = 133, 3. . . . . mol massa x= 1 x 133, 34 g 37, 8 g 1 x 37, 8 = 0, 28349 mol Al. Cl 3 133, 34

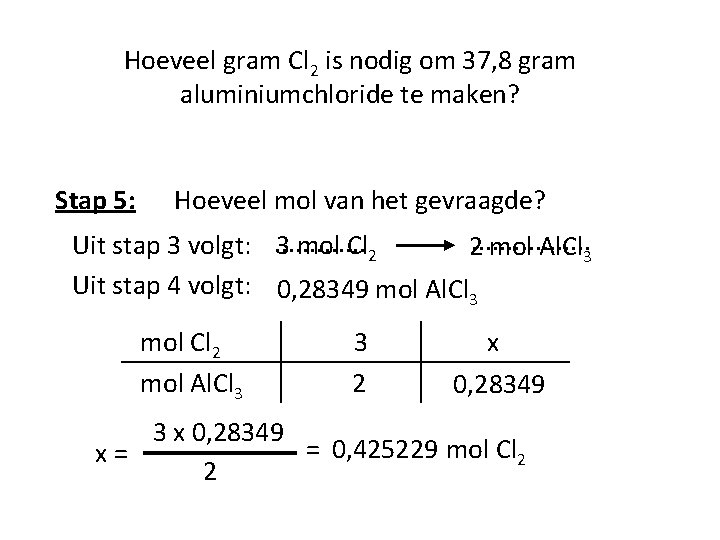
Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 5: Hoeveel mol van het gevraagde? Uit stap 3 volgt: . . . 3 mol Cl 2 2. . . . mol Al. Cl 3 Uit stap 4 volgt: 0, 28349 mol Al. Cl 3 mol Cl 2 mol Al. Cl 3 3 2 x 0, 28349 3 x 0, 28349 = 0, 425229 mol Cl 2 x= 2

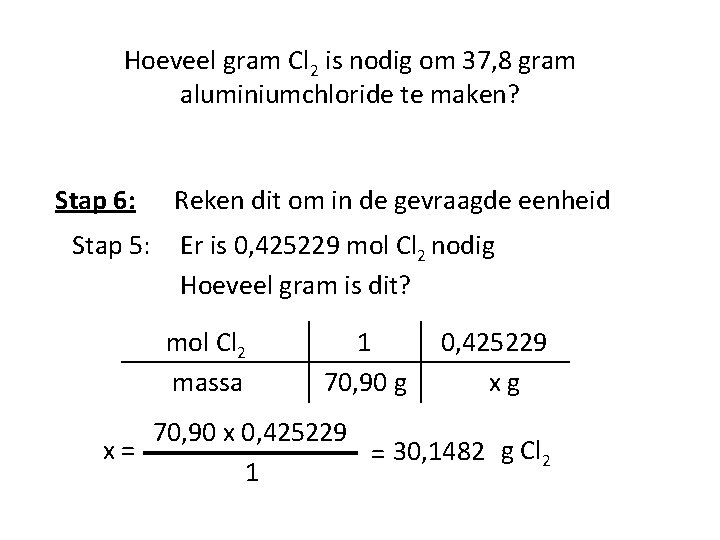
Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er is 0, 425229 mol Cl 2 nodig Hoeveel gram is dit? mol Cl 2 massa 1 70, 90 g 0, 425229 xg 70, 90 x 0, 425229 x= = 30, 1482 g Cl 2 1

Hoeveel gram Cl 2 is nodig om 37, 8 gram aluminiumchloride te maken? Stap 7: Let op de significantie !!! Stap 6: Er is 30, 1482 g Cl 2 nodig Het gegeven is in. . . 3 significante cijfers Om 37, 8 g Al. Cl 3 te maken is. . . . 30, 1 g Cl 2 nodig

En nu zelf

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Antwoord: 4. 9 g Fe

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 1: Reactievergelijking: 2 Fe 2 O 3 2 Fe + 13½ O 2 4 Stap 2: Welke stof is gegeven? Welke stof is gevraagd?

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 3: Wat is hiertussen de molverhouding? ? 4 Fe + 3 O 2 2 Fe 2 O 3. 4. . mol Fe + . . . 3 mol O 2

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 4: Reken het gegeven om in mol 2, 1 g O 2 = ? mol massa x= 1 x 2, 1 32, 00 g x 2, 1 g = 0, 065625 mol O 2

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 5: Hoeveel mol van het gevraagde? Stap 3: 4 mol Fe + 3 mol O 2 Stap 4: ? mol Fe + 0, 065625 mol O 2 mol Fe mol O 2 4 3 4 x 0, 065625 = 0, 0875 x= 3 x 0, 065625 mol Fe

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er is 0, 0875 mol Fe nodig Hoeveel gram is dit? mol Fe massa 55, 85 x 0, 0875 x= 1 1 55, 85 g 0, 0875 xg = 4, 886875 g Fe

Met hoeveel gram ijzer kan 2, 1 gram zuurstof tot ijzer(III)oxide reageren? Stap 7: Let op de significantie !!! Stap 6: Er is 4, 886875 g Fe nodig Het gegeven is in. . . 2 significante cijfers 2, 1 g O 2 kan met. . . . 4, 9 g Fe reageren

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Antwoord: 4, 61 g P

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 1: Reactievergelijking: 5 O 2 2 P 2 O 5 4 P + Stap 2: Welke stof is gegeven? Welke stof is gevraagd?

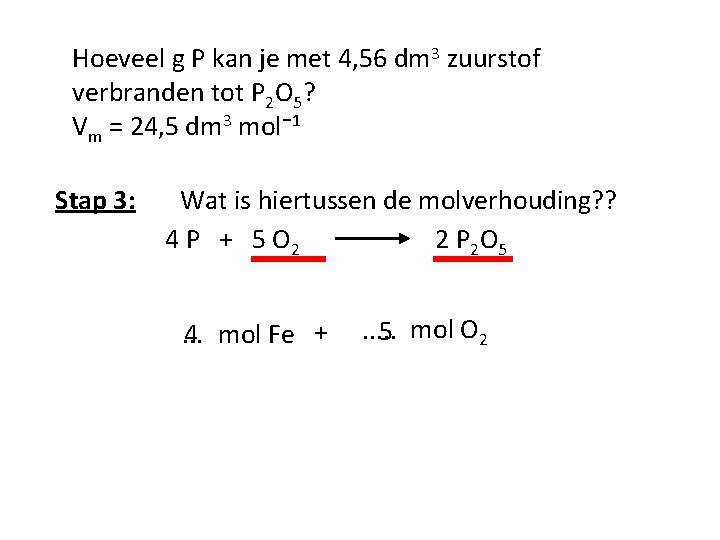
Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 3: Wat is hiertussen de molverhouding? ? 4 P + 5 O 2 2 P 2 O 5. 4. . mol Fe + . . . 5 mol O 2

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 4: Reken het gegeven om in mol 4, 56 dm 3 O 2 = ? mol dm 3 x= 1 x 4, 56 24, 5 1 24, 5 x 4, 56 = 0, 18622 mol O 2

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 5: Hoeveel mol van het gevraagde? Stap 3: 4 mol P + 5 mol O 2 Stap 4: ? mol P + 0, 18622 mol O 2 mol P mol O 2 4 5 x 0, 18622 4 x 0, 18622 = 0, 148898 mol P x= 5

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er is 0, 148898 mol P nodig Hoeveel gram is dit? mol P massa 1 30, 97 g 0, 148898 xg 30, 97 x 0, 148898 x= = 4, 61137 g P 1

Hoeveel g P kan je met 4, 56 dm 3 zuurstof verbranden tot P 2 O 5? Vm = 24, 5 dm 3 mol⁻ 1 Stap 7: Let op de significantie !!! Stap 6: Er is 4, 61137 g P nodig Het gegeven is in. . . 3 significante cijfers 4, 61 g P reageren 4, 56 dm 3 O 2 kan met. . . .

En nog drie moeilijkere !

1. Een auto verbrandt voor 15 km 1, 0 kg benzine (C 8 H 18). Hoeveel kg CO 2 stoot deze auto dan uit? 2. Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 3. Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Antwoorden: 1: 3, 08 kg 3. 1, 6 g 2. 8, 18 dm 3

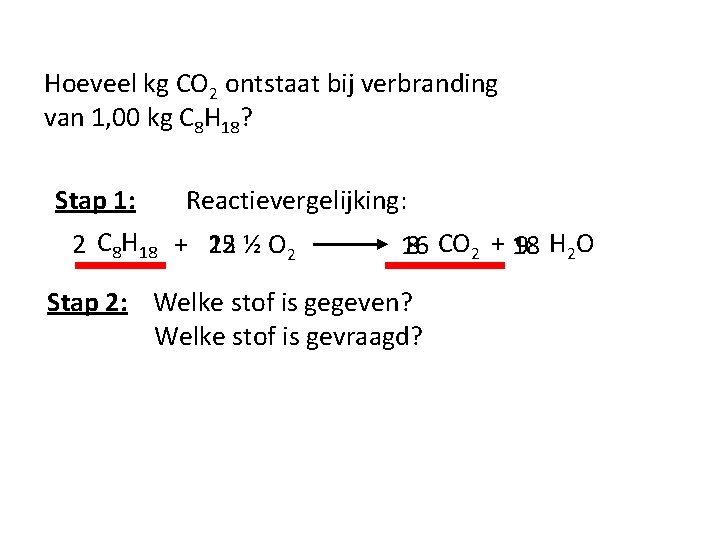
Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 1: Reactievergelijking: 2 C 8 H 18 + 25 12 ½ O 2 8 CO 2 + 18 9 H 2 O 16 Stap 2: Welke stof is gegeven? Welke stof is gevraagd?

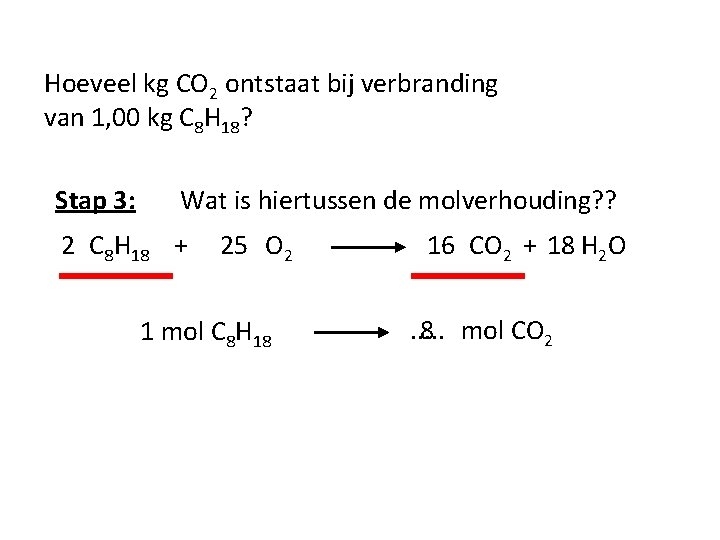
Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 3: Wat is hiertussen de molverhouding? ? 2 C 8 H 18 + 25 O 2 1 mol C 8 H 18 16 CO 2 + 18 H 2 O. . . 8 mol CO 2

Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 4: Reken het gegeven om in mol 1000 g C 8 H 18 = ? mol massa x= 1 114, 2 g x 1000 g 1 x 1000 = 8, 75657 mol C 8 H 18 114, 2

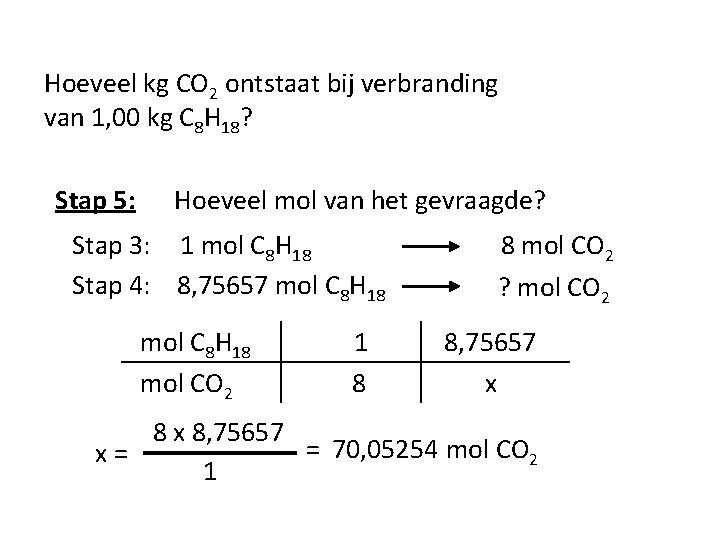
Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 5: Hoeveel mol van het gevraagde? Stap 3: 1 mol C 8 H 18 Stap 4: 8, 75657 mol C 8 H 18 mol CO 2 1 8 8 mol CO 2 ? mol CO 2 8, 75657 x 8, 75657 = 70, 05254 mol CO 2 x= 1

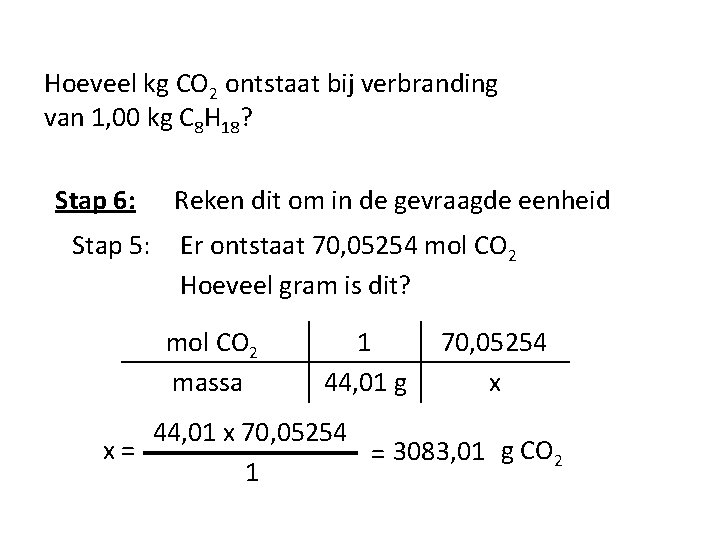
Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er ontstaat 70, 05254 mol CO 2 Hoeveel gram is dit? mol CO 2 massa 1 44, 01 g 70, 05254 x 44, 01 x 70, 05254 x= = 3083, 01 g CO 2 1

Hoeveel kg CO 2 ontstaat bij verbranding van 1, 00 kg C 8 H 18? Stap 7: Stap 6: Let op de significantie !!! 3083, 01 g CO 2 = 3, 08301. . . kg CO 2 Het gegeven is in. . . 3 significante cijfers Bij de verbranding van 1, 00 kg benzine ontstaat: 3, 08 kg CO 2

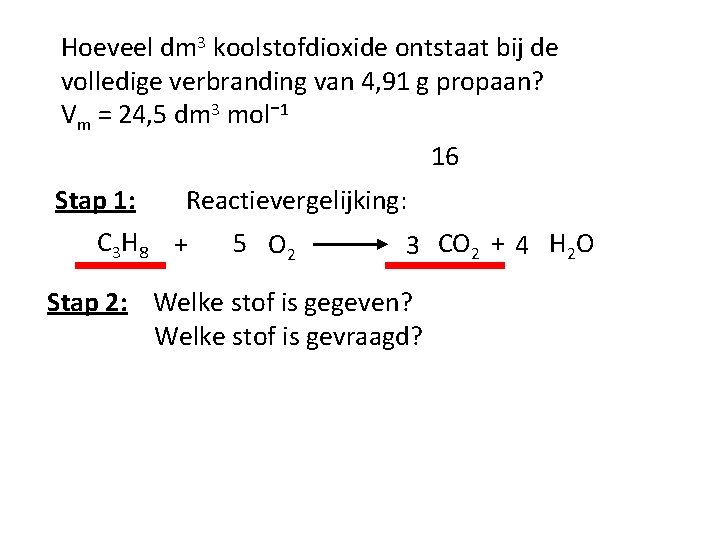
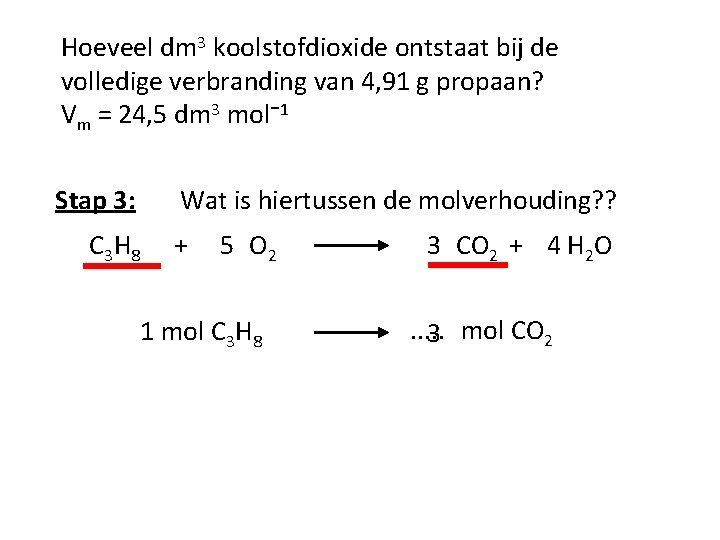
Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 16 Stap 1: Reactievergelijking: C 3 H 8 + 5 O 2 3 CO 2 + 4 H 2 O Stap 2: Welke stof is gegeven? Welke stof is gevraagd?

Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 Stap 3: C 3 H 8 Wat is hiertussen de molverhouding? ? + 5 O 2 1 mol C 3 H 8 3 CO 2 + 4 H 2 O. . . 3 mol CO 2

Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 Stap 4: Reken het gegeven om in mol 4, 91 g C 3 H 8 = ? mol massa x= 1 44, 094 g x 4, 91 g 1 x 4, 91 = 0, 111353 mol C 3 H 8 44, 094

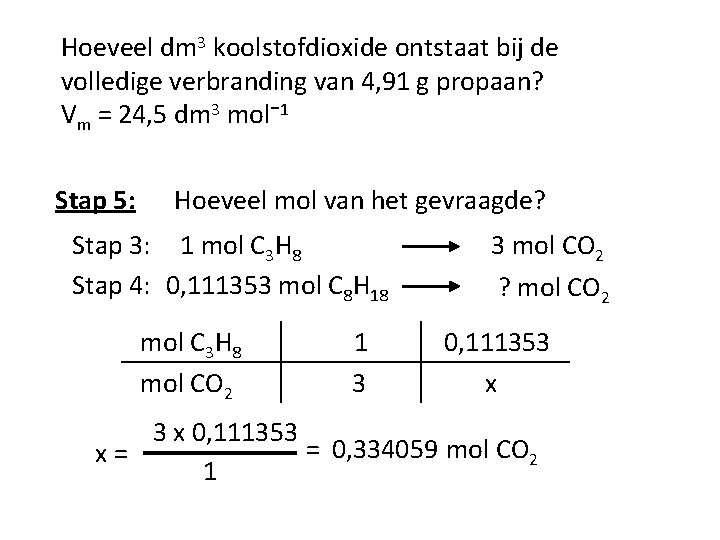
Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 Stap 5: Hoeveel mol van het gevraagde? Stap 3: 1 mol C 3 H 8 Stap 4: 0, 111353 mol C 8 H 18 mol C 3 H 8 mol CO 2 1 3 3 mol CO 2 ? mol CO 2 0, 111353 x 0, 111353 = 0, 334059 mol CO 2 x= 1

Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er ontstaat 0, 334059 mol CO 2 Hoeveel dm 3 is dit? mol CO 2 1 volume 24, 5 dm 3 24, 5 x 0, 334059 x= 1 0, 334059 x dm 3 = 8, 18445 dm 3 CO 2

Hoeveel dm 3 koolstofdioxide ontstaat bij de volledige verbranding van 4, 91 g propaan? Vm = 24, 5 dm 3 mol⁻ 1 Stap 7: Stap 6: Er ontstaat 8, 18445 dm 3 CO 2 Het gegeven is in. . . 3 significante cijfers Bij de verbranding van 4, 91 g propaan ontstaat: 8, 18 g CO 2

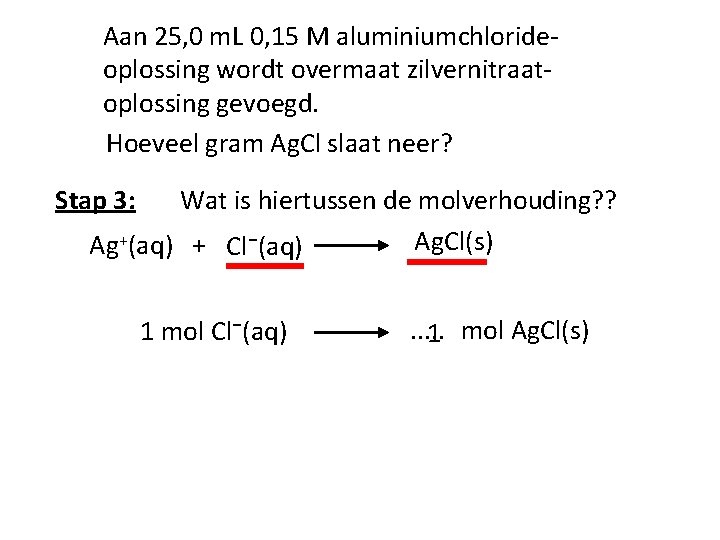
Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 1: Reactievergelijking: Ag+(aq) + Cl⁻(aq) Stap 2: Welke stof is gegeven? Welke stof is gevraagd? Ag. Cl(s)

Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 3: Wat is hiertussen de molverhouding? ? Ag. Cl(s) Ag+(aq) + Cl⁻(aq) 1 mol Cl⁻(aq) . . . 1 mol Ag. Cl(s)

Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 4: Reken het gegeven om in mol 25, 0 m. L 0, 15 M bevat = ? mol Al. Cl 3? mmol 0, 15 mmol 1 m. L volume 25, 0 x 0, 15 x= 1 x mmol 25, 0 m. L = 3, 75 mmol Al. Cl 3

Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 4: Reken het gegeven om in mol 3, 75 mmol Al. Cl 3 bevat = ? mol Cl⁻ ? mmol Al. Cl 3 mmol Cl⁻ 3 x 3, 75 x= 1 1 mmol 3, 75 mmol 3 mmol x mmol = 11, 25 mmol Cl⁻

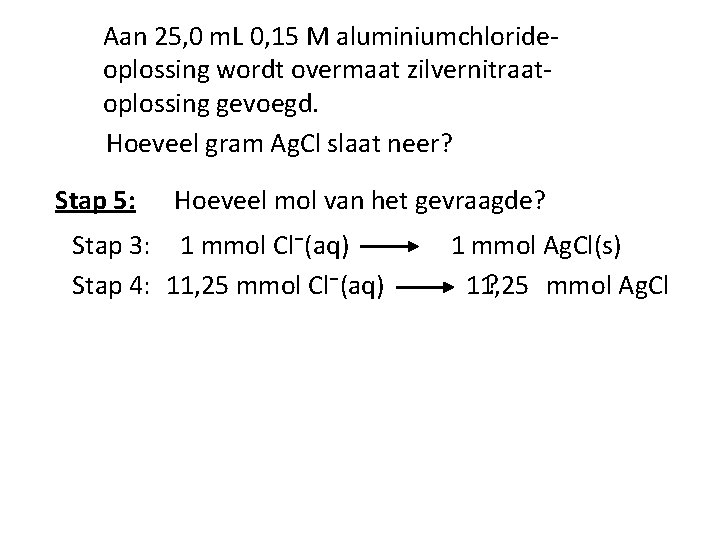
Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 5: Hoeveel mol van het gevraagde? Stap 3: 1 mmol Cl⁻(aq) Stap 4: 11, 25 mmol Cl⁻(aq) 1 mmol Ag. Cl(s) ? mmol Ag. Cl 11, 25

Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 6: Stap 5: Reken dit om in de gevraagde eenheid Er ontstaat 11, 25 mmol Ag. Cl(s) Hoeveel g is dit? mol Ag. Cl 1 massa 143, 32 g 11, 25 x 143, 32 x= 1 11, 25 mmol x mg = 1612, 35 mg Ag. Cl(s)

Aan 25, 0 m. L 0, 15 M aluminiumchlorideoplossing wordt overmaat zilvernitraatoplossing gevoegd. Hoeveel gram Ag. Cl slaat neer? Stap 7: Stap 6: Er ontstaat 1612, 35 mg = 1, 61235 g Ag. Cl(s) Het gegeven is in. . . 2 significante cijfers Er onontstaat: 1, 6 g Ag. Cl(s)

Nu nog wat moeilijker: Wanneer je een Ca. Cl 2 opl. bij een Na 3 PO 4 opl. voegt, treedt de volgende (neerslag)reactie op: 3 Ca 2+(aq) + 2 PO 43⁻(aq) Ca 3(PO 4)2(s) Je wilt 5, 3 g Ca 3(PO 4)2(s) maken. Je hebt een 2, 1 M Ca. Cl 2 opl. Hoeveel m. L van deze opl. heb je nodig? Antwoord: 24 m. L

Hoeveel m. L Ca. Cl 2 opl. (2, 1 M) is nodig om 5, 3 g Ca 3(PO 4)2 te maken? Stap 1: Stel de reactievergelijking op. Ca 3(PO 4) 2(s) 3 Ca 2+(aq) + 2 PO 43⁻(aq) Stap 2: Welke stof is gegeven? Welke stof wordt gevraagd? Stap 3: Wat is de molverhouding? 3 mol Ca 2+ 1 mol Ca 3(PO 4)2

Hoeveel m. L Ca. Cl 2 opl. (2, 1 M) is nodig om 5, 3 g Ca 3(PO 4)2 te maken? Stap 4: Reken het gegeven om in mol massa x= x 1 310, 18 g 1 x 5, 3 310, 18 5, 3 g = 0, 017087 mol Ca 3(CO 3)4

Hoeveel m. L Ca. Cl 2 opl. (2, 1 M) is nodig om 5, 3 g Ca 3(PO 4)2 te maken? Stap 5: Hoeveel mol van het gevraagde? Stap 3: 3 mol Ca 2+ 1 mol Ca 3(CO 3)2 Stap 4: 0, 051261 mol Ca 2+ 0, 017087 mol Ca 3(PO 4)2

Hoeveel m. L Ca. Cl 2 opl. (2, 1 M) is nodig om 5, 3 g Ca 3(PO 4)2 te maken? Stap 6: Reken dit om in de gevraagde eenheid Stap 5: We hebben 0, 051261 mol Ca 2+ nodig De molariteit van de Ca 2+ is 2, 1 M mol Ca 2+ Volume 2, 1 1 L 0. 051261 x. L 1 x 0, 051261 = 0, 02441 L = 24, 41 m. L x= 2, 1

Hoeveel m. L Ca. Cl 2 opl. (2, 1 M) is nodig om 5, 3 g Ca 3(PO 4)2 te maken? Stap 7: Let op de significantie!!! Stap 6: We hebben 24, 41 m. L Ca 2+ opl. nodig Het gegeven is in: 2 significante cijfers Om 5, 3 g Ca. CO 3 te maken is nodig: 24 m. L Ca 2+ opl. (2, 1 M)