HLA systm MHC glykoproteiny J Ochotn MHC glykoproteiny




































- Slides: 58

HLA systém (MHC glykoproteiny) J. Ochotná

MHC glykoproteiny I. třídy (major histocompatibility complex) § Funkcí MHC gp. I je prezentace peptidových fragmentů, které jsou produkovány buňkou (včetně virových, pokud jsou přítomny), na buněčném povrchu tak, aby byly rozpoznávány T lymfocyty (cytotoxickými CD 8)

MHC glykoproteiny I. třídy (major histocompatibility complex) § Přítomny na všech jaderných buňkách organismu § 3 izotypy klasických lidských MHC gp. ( HLA - A, -B, -C ) § 3 izotypy neklasických MHC gp. ( HLA – E, -F, -G; molekuly CD 1)

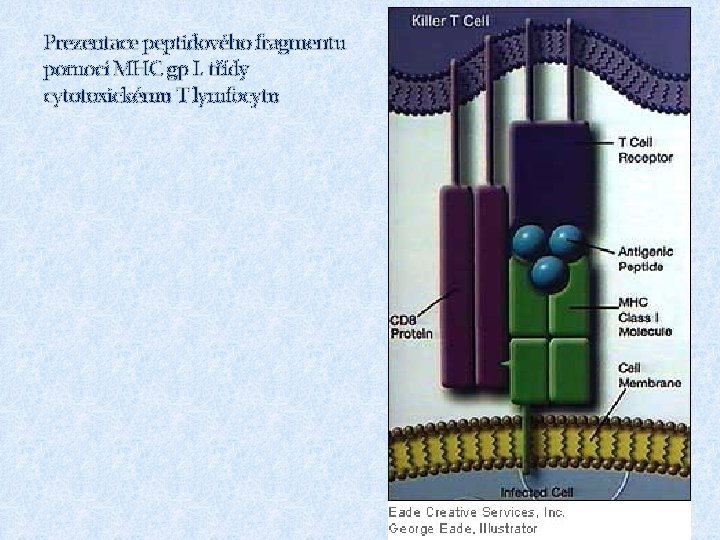
Prezentace peptidového fragmentu pomocí MHC gp I. třídy cytotoxickému T lymfocytu

Struktura MHC gp I § MHC gp. I. třídy se skládají z transmembránového řetězce a a asociovaného b 2 mikroglobulinu § Řetězec a má 3 domény, 2 N-terminální (a 1, a 2 – vazebné místo pro peptidy) a 1 C-terminální doménu (a 3 – zakotvena v cytoplazmatické membráně) § Vazba peptidu je nezbytná pro stabilní konformaci MHC gp a tím zajišťuje jeho dlouhodobou prezentaci na buněčném povrchu

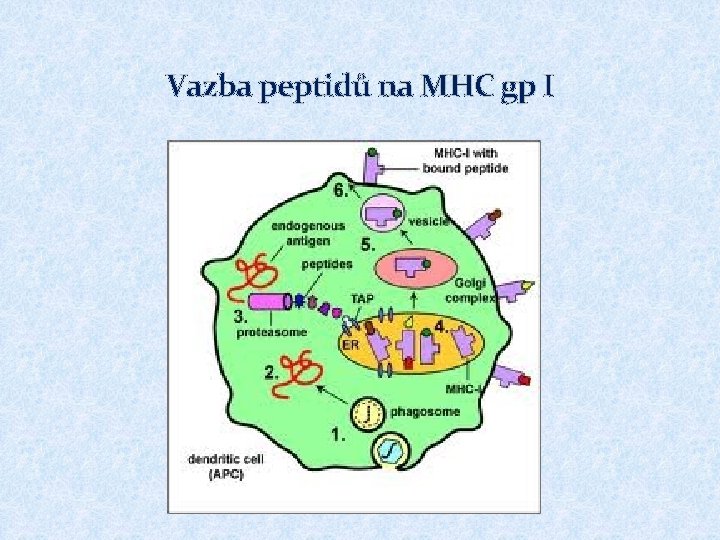
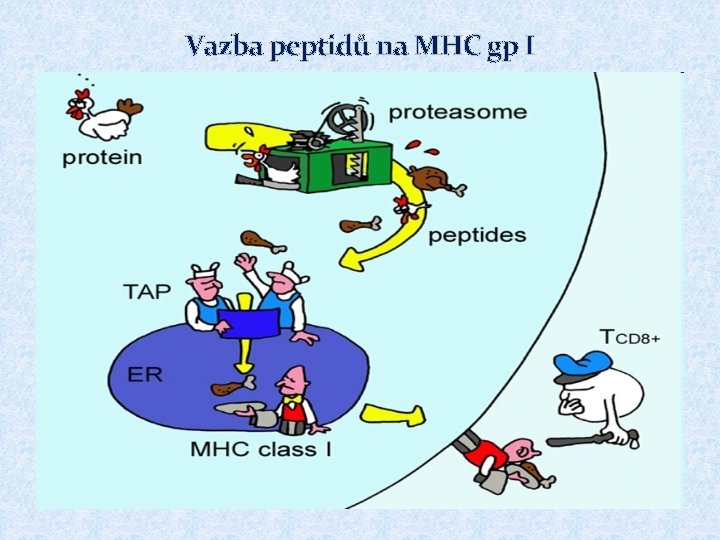
Vazba peptidů na MHC gp I � MHC gp I váží peptidy o délce 8 až 10 AK � Určitá molekula MHC gp váže peptidy sdílející společné strukturní rysy - vazebný motiv (rozhodující jsou AK poblíž konců peptidu) � K vazbě endogenních peptidů dochází v endoplazmatickém retikulu během biosyntézy MHC gp. � Po vytvoření řetězce a a b 2 mikrotubulinu dochází v ER k poskládání do správné konformace a k vzájemné asociaci a k asociaci vhodného peptidu, tento komplex je dále zpracován v Golgiho aparátu a pak je prezentován na buněčném povrchu � Navázané peptidy pocházejí z proteinů degradovaných proteazómem, který štěpí cytoplasmatické proteiny určené k likvidaci (označené ubiquitinem), peptidové fragmenty jsou transportovány do ER pomocí specifických membránových pump

Vazba peptidů na MHC gp I

Vazba peptidů na MHC gp I

Neklasické MHC gp. I �HLA – E, -F, -G; molekuly CD 1 �Strukturně podobné klasickým MHC gp �Jsou méně polymorfní �Vyskytují se jen na některých buňkách �Specializují se na vazbu zvláštních ligandů

Neklasické MHC gp. I � HLA-E a HLA-G - vyskytují se na buňkách trofoblastu � Komplexy HLA-E a HLA-G s peptidy jsou rozpoznávány inhibičními receptory NK buněk a přispívají k toleranci plodu v děloze

MHC glykoproteiny II. třídy � Funkcí MHC gp II je prezentace peptidových fragmentů z proteinů pohlcených buňkou tak, aby byly rozpoznatelné T lymfocyty (pomocnými CD 4) � Vyskytují se na APC ( dendritické buňky, monocyty, makrofágy, B lymfocyty) � 3 izotypy MHC gp II ( DR, DQ, DP )

Struktura MHC gp II § MHC gp. II se skládají ze 2 nekovalentně asociovaných transmembránových podjednotek a a b § Vazebné místo pro peptid je tvořeno N-terminálními doménami a 1 a b 1 § Vazba peptidu je nezbytná pro stabilní konformaci MHC gp a tím zajišťuje jeho dlouhodobou prezentaci na buněčném povrchu

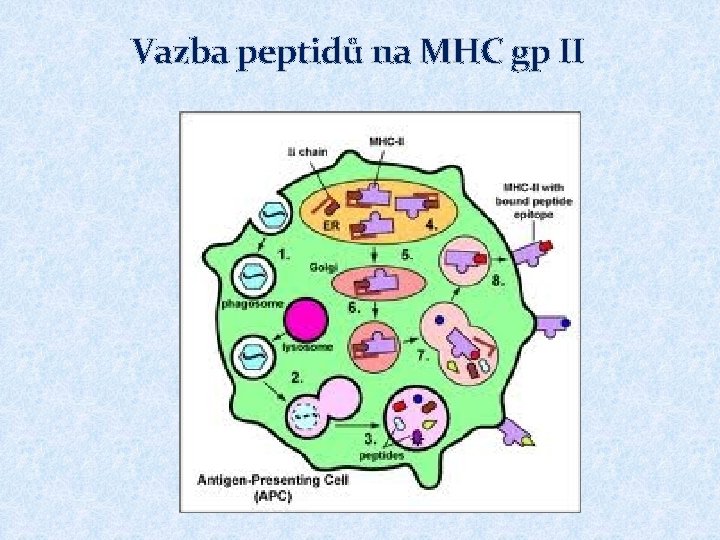
Vazba peptidů na MHC gp II � MHC gp II váží peptidy o délce 15 až 35 AK (ale i delší - vazebné místo pro peptid je na obou koncích otevřené) � Určitá molekula MHC gp váže peptidy sdílející společné strukturní rysy - vazebný motiv � Po vytvoření řetězce a a b v ER dochází k poskládání do správné konformace a k vzájemné asociaci a k připojení dalšího transmembránového řetězce, tzv. invariantního řetězce, který blokuje vazebné místo pro peptid, tento komplex je dále zpracován v Golgiho aparátu; sekreční váčky oddělené od GA fúzují s endozómy, poté se rozštěpí invariantní řetězce a do vazebného místa MHC gp se naváží peptidové fragmenty endocytovaných proteinů a poté je komplex prezentován na buněčném povrchu

Vazba peptidů na MHC gp II

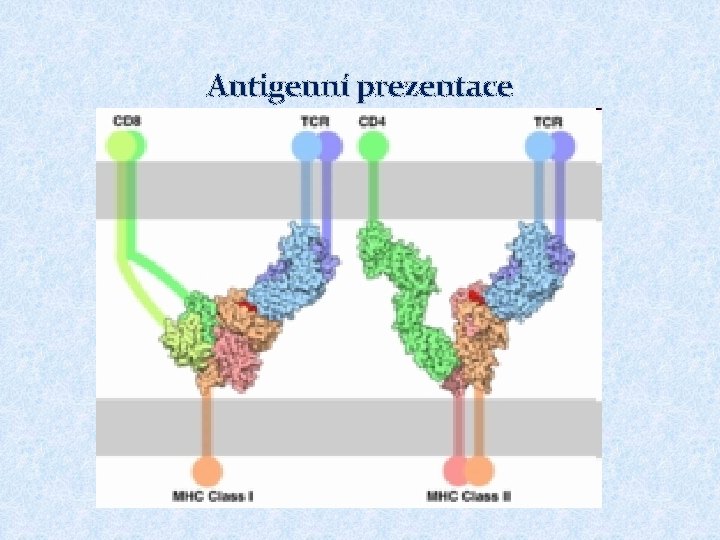
Antigenní prezentace

Antigenní prezentace

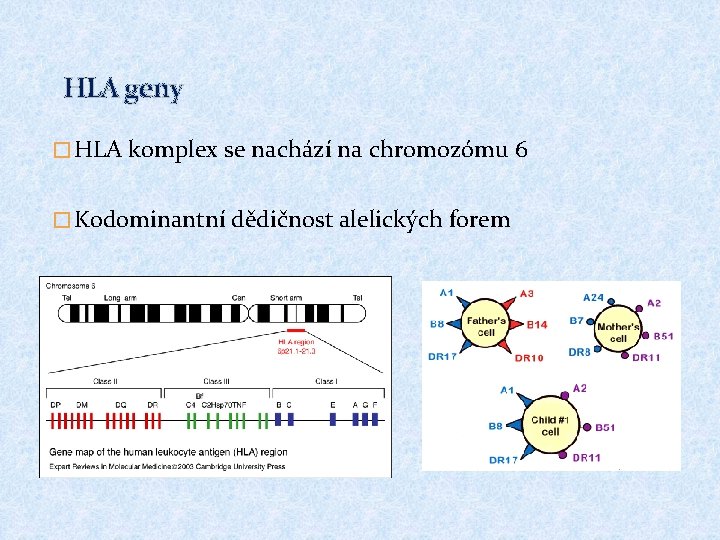
HLA geny � HLA komplex se nachází na chromozómu 6 � Kodominantní dědičnost alelických forem

Polymorfismus MHC glykoproteinů � U MHC gp je vysoký polymorfismus, tzn. existují až stovky různých alelických forem jednotlivých izotypů (kromě neklasických MHC gp. I) � Polymorfismus má ochranný význam na úrovni jedince i na úrovni populace � Polymorfismus MHC gp způsobuje komplikace při transplantacích

HLA typizace = určení HLA antigenů na povrchu lymfocytů Provádí se při předtransplantačním vyšetření a při určení paternity 1) Sérologická typizace � mikrolymfocytotoxický test � allospecifická séra ( získaná od vícenásobných rodiček do 6 týdnů po porodu, získaná vakcinací dobrovolníků, nebo komerčně připravené sety typizačních sér (monoklonální protilátky)) � princip - inkubace lymfocytů s typizačními séry za přítomnosti králičího komplementu, poté je přidáno vitální barvivo, které obarví mrtvé buňky - buňky nesoucí určité HLA jsou usmrceny cytotoxickými Ab proti tomuto Ag, procento mrtvých buněk je mírou toxicity séra (síly a titru antileukocytárních protilátek) � za pozitivní reakci se považuje více než 10% mrtvých bb. � (sérologickou typizaci lze provádět i pomocí průtokové cytometrie)

2) Molekulárně genetické metody � Pro typizaci se používají hypervariabilní úseky ve II. exonu genů kódujících HLA II. třídy, pro určení HLA I. třídy se používá polymorfismus v II. a III. exonu kódujících genů 2 a) PCR-SSP � = polymerázová řetězová reakce se sekvenčními specifickými primery � extrahovaná DNA slouží jako substrát v sadě PCR reakcí � každá PCR reakce obsahuje primerový pár specifický pro určitou alelu (resp. skupinu alel) � pozitivní a negativní reakce se hodnotí elektroforézou � každá kombinace alel má svůj specifický elektroforetický obraz

2 b) PCR-SSO � = PCR reakce se sekvenčně specifickými oligonukleotidy � namnoží se hypervariabilní úseky genů kódujících HLA � hybridizace s enzymaticky nebo radioaktivně značenými DNA sondami specifickými pro jednotlivé alely 2 c) PCR- SBT � = sequencing based typing; sekvenování � nejpřesnější metodika HLA typizace � získáme přesnou sekvenci nukleotidů, kterou porovnáme s databází známých sekvencí HLA alel

T lymfocyty

T lymfocyty § T lymfocyty patří mezi buněčnou složku antigenně specifických mechanismů, při vývoji opouštějí kostní dřeň a migrují do thymu, kde dozrávají § Existuje několik různých subpopulací T lymfocytů § Podílejí se na regulaci imunitních dějů, při likvidaci virem infikovaných buněk či nádorových buněk § Rozpoznávají antigen zpracovaný a prezentovaný APC; prostřednictvím TCR rozpoznávají komplex MHC gp-antigenní peptid § T lymfocyty jsou po aktivaci stimulovány k pomnožení a diferenciaci v efektorové buňky, část se diferencuje v paměťové buňky

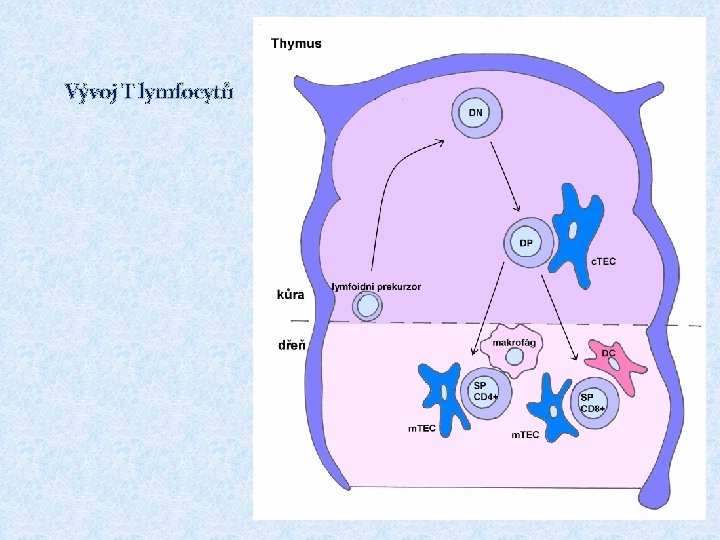
Vývoj T lymfocytů § T lymfocyty vznikají v kostní dřeni a pak migrují do thymu, kde dozrávají (ab. T lymfocyty), konečná diferenciace probíhá až po aktivaci antigenem zpracovaným a prezentovaným APC § gd. T lymfocyty se mohou vyvíjet i mimo thymus (jde o menšinovou populaci) Pluripotentní hematopoetická kmenová buňka Pro-thymocyt – dostává se z kostní dřeně do thymu, kde se začínají přeskupovat geny pro TCRb, exprimuje na svém povrchu tzv. pre-TCR (složený z b řetězce, pre-TCRa a CD 3 komplexu), po té se začínají přeskupovat geny pro TCRa Kortikální thymocyt – exprimuje na svém povrchu TCR (složený z řetězců ab a CD 3) a koreceptory CD 4 a CD 8; v této fázi dochází k selekci autoreaktivních buněk a buněk s nefunkčním TCR Medulární thymocyt (zralá T buňka) – zachovávají si expresi CD 4 či CD 8, usidlují se v sekundárních lymfoidních o rgánech

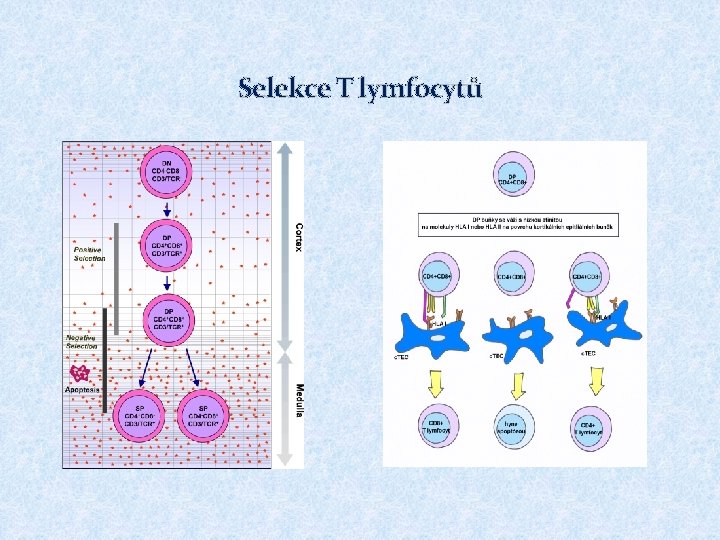
Selekce T lymfocytů § Negativní selekce – eliminace autoreaktivních buněk Pokud thymocyt váže svým TCR dostatečně silně komplex MHCgp s normálními peptidy (z autoantigenů) se kterými se setká na povrchu thymových buněk dostane signály vedoucí k apoptotické smrti buňky PAE buňky (peripherial antigen expressing cells) § Pozitivní selekce – eliminace buněk s nefunkčním TCR Pozitivně selektovány jsou thymocyty, které s nízkou afinitou rozeznávají MHC gp, ty si pak zachovávají expresi CD 4 či CD 8 (váže-li příslušný TCR MHC gp I či II) – tyto zralé T bb. (medulární thymocyty) opouštějí thymus a usidlují se v sekundárních lymfoidních orgánech § Selekce se účastní thymové epiteliální buňky a DC § 98% pro-thymocytů v thymu během svého vývoje zahyne

Vývoj T lymfocytů

Selekce T lymfocytů

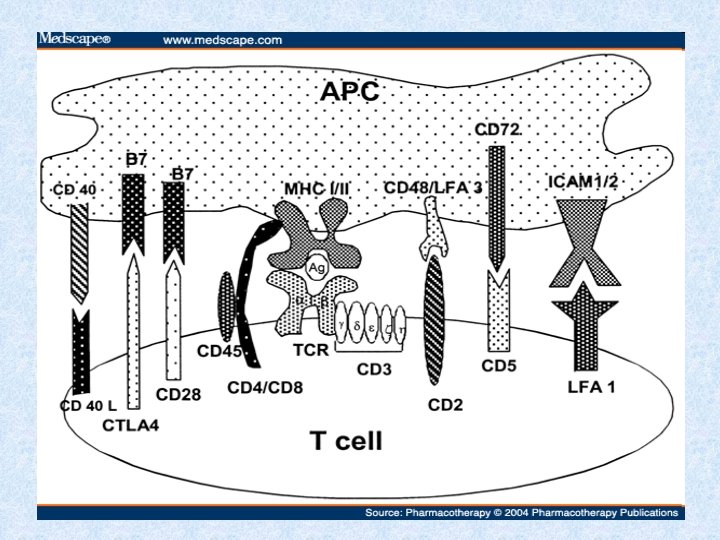
Povrchové znaky T lymfocytů § TCR – rozpoznává Ag peptid v komplexu s MHC gp § CD 3 – součást TCR, účast při přenosu signálu § CD 4 nebo CD 8 – koreceptory, napomáhají k vazbě na MHC gp § CD 28 – kostimulační receptor; váže CD 80, CD 86 § CTLA-4 (CD 152) – inhibiční receptor; váže CD 80, CD 86


Subpopulace T lymfocytů § ab-T lymfocyty – mají TCRab, většinový typ (95 - 98%), k vývoji potřebují thymus, rozeznávají antigeny v komplexu MHC gp-peptid § gd-T lymfocyty – (2 - 5%) mohou se vyvíjet i mimo thymus, některé jsou schopny rozpoznat nativní Ag, uplatňují se při obraně kůže a sliznic § Intraepiteliální T lymfocyty § NK-T lymfocyty – rozeznávají komplexy CD 1 molekul s lipidy

ab-T lymfocyty Exprimující koreceptor CD 4 (koreceptor pro MHC gp II) Jde o prekurzory pomocných T buněk (TH), ty lze rozdělit podle produkce cytokinů na : TH 0 – produkují směs cytokinů jako TH 1 a TH 2 TH 1 – IL-2, IFNg (pomoc makrofágům) TH 2 – IL-4, IL-5, IL-6, IL-10 (pomoc B lymfocytům) TH 3 – TGFb Treg – regulační T lymfocyty, potlačují aktivitu ostatních T lymfocytů, hlavně autoreaktivních klonů T lymfocytů; produkují IL-10 a TGFb

ab-T lymfocyty Exprimující koreceptor CD 8 (koreceptor pro MHC gp I) Jde o prekurzory cytotoxických T buněk (TC) TC – rozpoznávají buňky napadené viry či jinými intracelulárními parazity a některé nádorové buňky

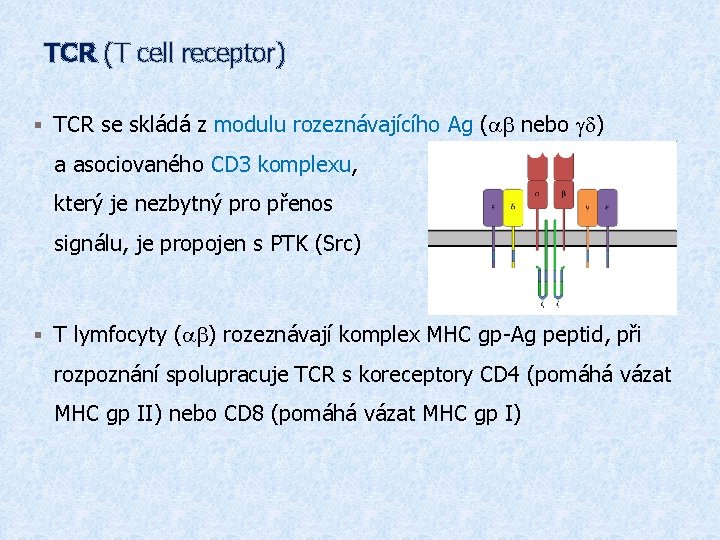
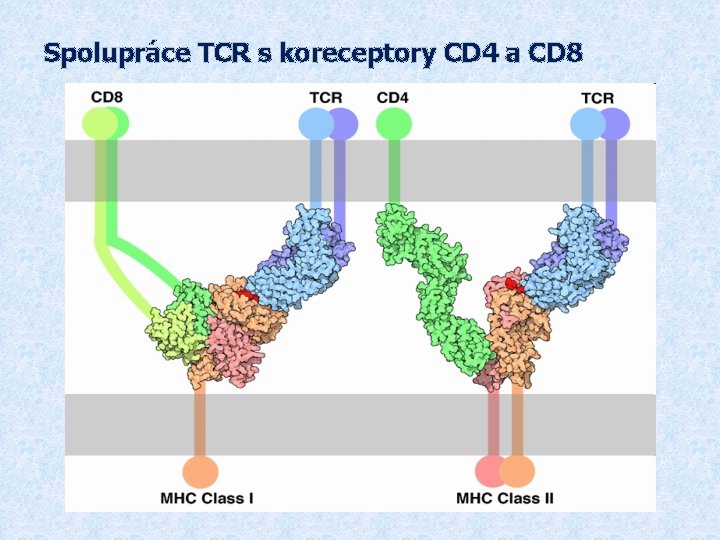
TCR (T cell receptor) § TCR se skládá z modulu rozeznávajícího Ag (ab nebo gd) a asociovaného CD 3 komplexu, který je nezbytný pro přenos signálu, je propojen s PTK (Src) § T lymfocyty (ab) rozeznávají komplex MHC gp-Ag peptid, při rozpoznání spolupracuje TCR s koreceptory CD 4 (pomáhá vázat MHC gp II) nebo CD 8 (pomáhá vázat MHC gp I)

Spolupráce TCR s koreceptory CD 4 a CD 8

Vznik TCR § Obdoba s tvorbou BCR § Řetězce b a d - odpovídají genovému komplexu Ig. H imunoglobulinů - V, D, J, C segmenty § Řetězce a a g - odpovídají genům pro L řetězce imunoglobulinů - V, J, C segmenty § Přeskupování genů probíhá podobně jako u BCR a provádějí je shodné rekombinázy § u genů pro TCR nedochází k somatickým mutacím a afinitní maturaci

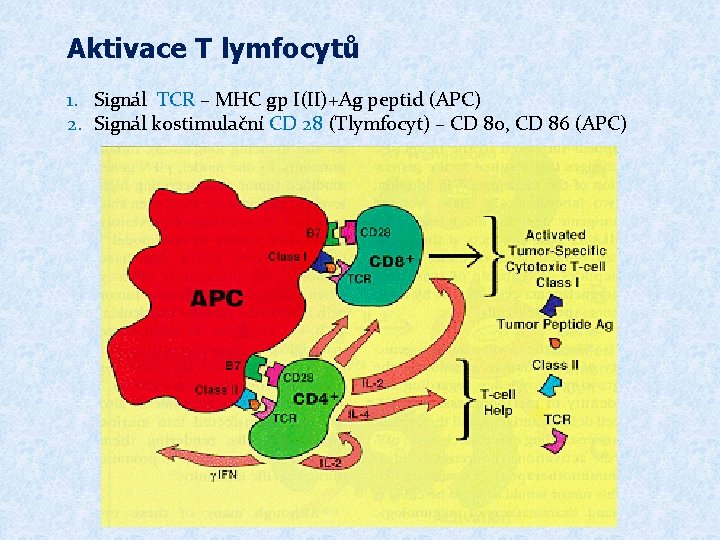
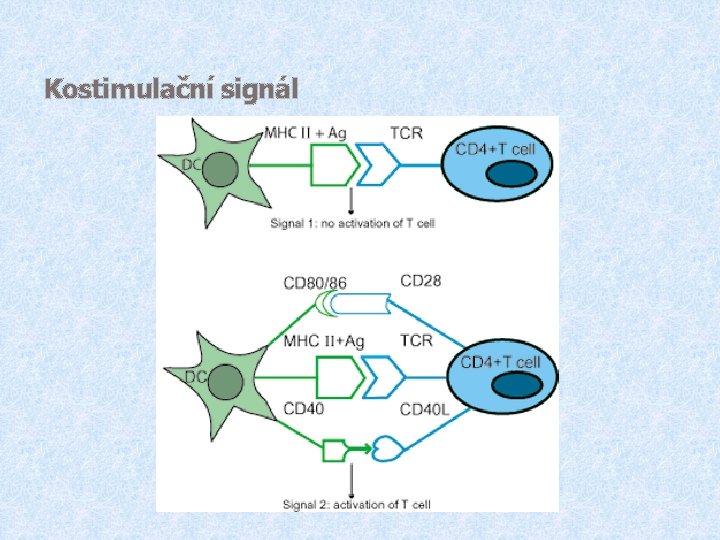
Aktivace T lymfocytů 1. Signál TCR – MHC gp I(II)+Ag peptid (APC) 2. Signál kostimulační CD 28 (Tlymfocyt) – CD 80, CD 86 (APC)

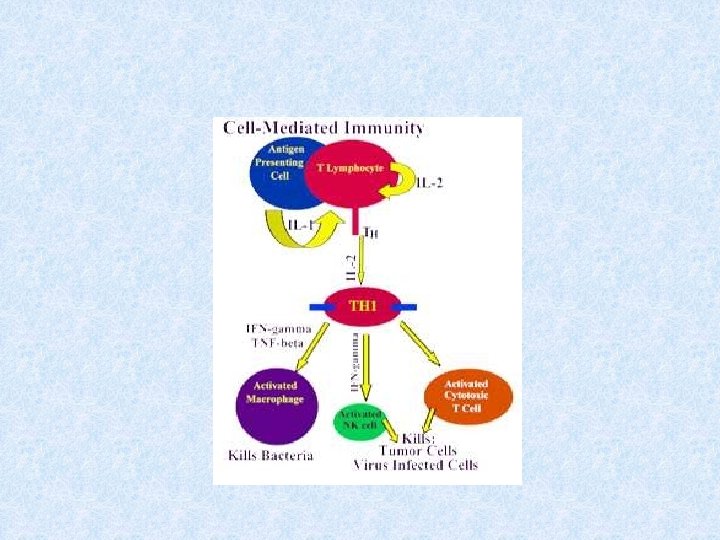
TH 1 imunitní odpověď

TH 1 imunitní odpověď – zánětlivá reakce § Základní funkcí TH 1 buněk je spolupráce s makrofágy a jejich přeměna v aktivované, které jsou schopny produkovat NO, pomocí kterého likvidují své intracelulární parazity § Pro přeměnu makrofágů v aktivované jsou nezbytné cytokiny (IFNg) produkované TH 1 buňkami § Aktivované makrofágy secernují některé cytokiny ( IL-1, TNF…), které napomáhají ke stimulaci T buněk a stimulují lokální zánět, který napomáhá potlačení infekce § Vzájemné působení TH 1 buněk a makrofágů je základním mechanismem imunopatologické reakce opožděného typu (DTH- delayed type hypersensitivity)

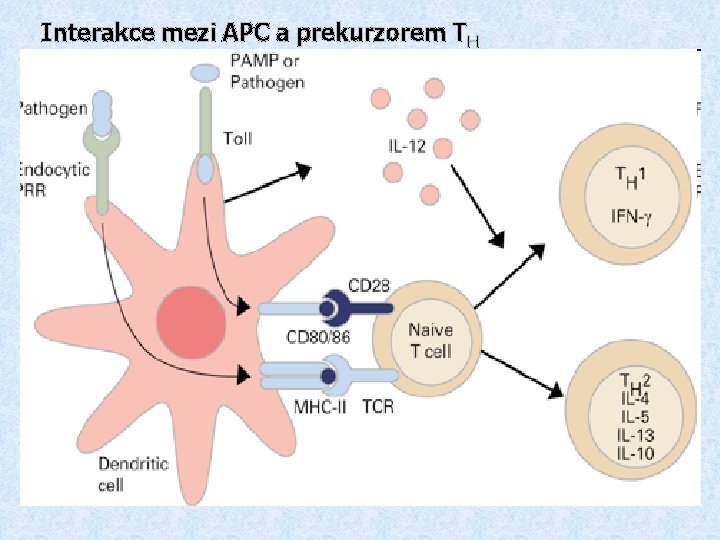
§ Infikovaný makrofág produkuje fragmenty proteinů pocházející z intracelulárního parazita, některé jsou prezentovány na jeho povrchu pomocí MHC gp II § Makrofágy a dendritické buňky stimulované některými mikroorganismy produkují IL-12 § Prekurzor TH , který rozpozná infikovaný makrofág a obdrží signály přes TCR, CD 28 a receptor pro IL-12 a další adhezivní a signalizační molekuly proliferuje a diferencuje se na efektorové TH 1 buňky, které produkují IFNg a IL-2. § IFNg podporuje přeměnu makrofágů v aktivované IL-2 je autokrinní růstový faktor TH 1 lymfocytů.

Interakce mezi APC a prekurzorem TH

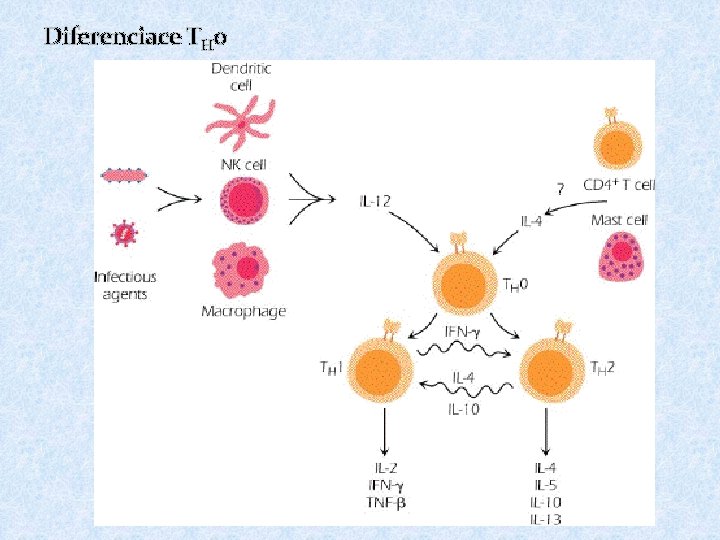
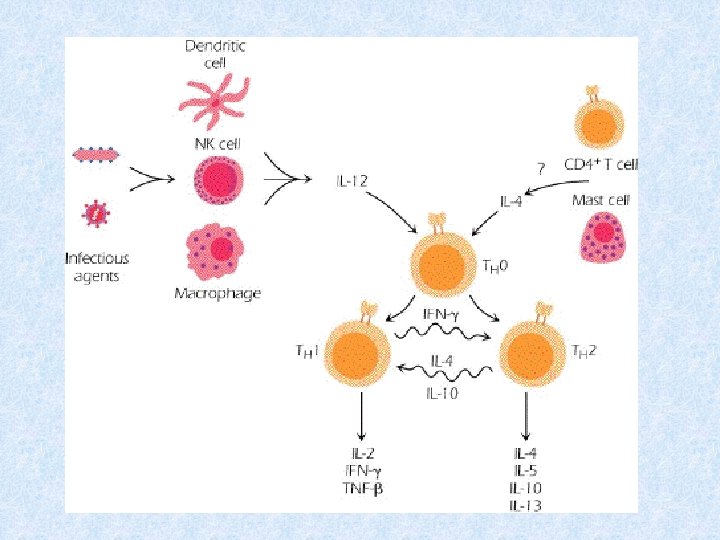
Diferenciace TH 0

Kostimulační signál


TH 2 imunitní odpověď

TH 2 imunitní odpověď – pomoc B lymfocytům § Základní funkcí TH 2 buněk je spolupráce s B lymfocyty (které byly stimulovány Ag) prostřednictvím cytokinů (IL-4, IL-5, IL-6) a přímého mezibuněčného kontaktu § Pro stimulaci B lymfocytů je většinou potřeba spolupráce mezi APC → TH 2 buňkou → B lymfocytem § V případě tzv. minimálního modelu, pokud se z B lymfocytu stane dobrá APC (CD 80, CD 86), stačí spolupráce mezi TH 2 buňkou → B lymfocytem

§ Prekurzor TH , který rozpozná infikovaný makrofág a dostane signály přes TCR, CD 28, receptor pro IL-4 a receptor pro IL-2 a další adhezivní a signalizační molekuly proliferuje a diferencuje se na efektorové TH 2, které poskytují B lymfocytům pomocné signály pomocí sekretovaných cytokinů IL-4, IL-5, IL-6 a prostřednictvím adhezivních molekul CD 40 L, které se váží se na kostimulační receptor B lymfocytů CD 40 § Interakce mezi CD 40 (B lymfocyt) a CD 40 L (TH 2 buňka) je nezbytná pro zahájení somatických mutací, izotypového přesmyku a vznik paměťových buněk § IL-4, IL-5, IL-6 : stimulace B lymfocytů


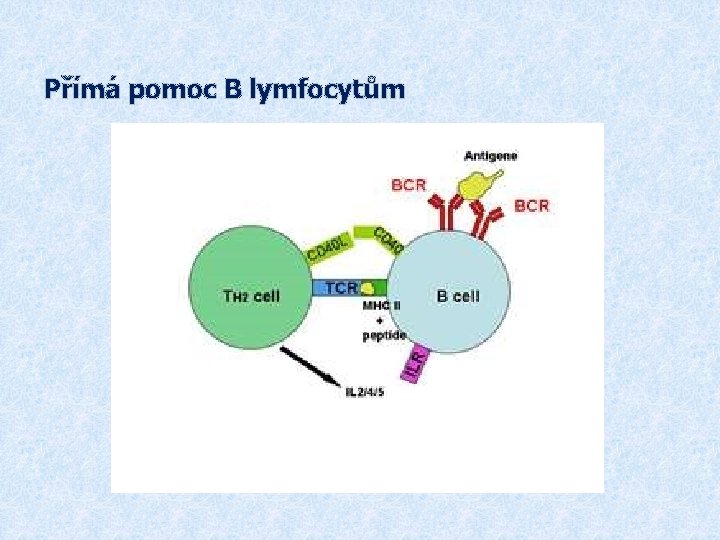
Pomoc B lymfocytům Specifická přímá pomoc B lymfocytům: § TH 2 lymfocyt poskytuje pomoc B lymfocytům, které byly stimulovány stejným Ag, který vyvolal vznik TH 2 § Ke stimulaci sekrece cytokinů TH 2 buňce stačí signál přes TCR (signál přes kostimulační receptor CD 28 již není nutný) § Jeden klon TH 2 buněk může poskytovat specifickou pomoc B lymfocytům různých specifit (musí prezentovat příslušné Ag peptidy pomocí MHC gp II, které rozpoznáváTCR)

Přímá pomoc B lymfocytům

Pomoc B lymfocytům Nepřímá pomoc B lymfocytům („bystander help“): § TH 2 lymfocyt poskytuje pomoc B lymfocytům, které byly stimulovány jiným Ag, než který vyvolal vznik TH 2 § Kontakt mezi TH 2 buňkou → B lymfocytem prostřednictvím adhezivních molekul, sekrece cytokinů, vazba CD 40 -CD 40 L § Nebezpečí aktivace autoreaktivních B lymfocytů

Vzájemná regulace aktivit TH 1 versus TH 2 § Zda se prekurzorové TH lymfocyty budou vyvíjet v TH 1 či TH 2 rozhodne poměr cytokinů IL-12 a IL-4 § § IL-12 je produkován makrofágy a dendritickými buňkami stimulovanými některými mikroorganismy § IL-4 je produkován bazofily a mastocyty § Cytokiny produkované TH 1 (hlavně IFNg) inhibují vývoj TH 2 a stimulují vývoj TH 1 (IL-2 stimuluje i TH 2) § Cytokiny produkované TH 2 (IL-4, IL-10) inhibují vývoj TH 1 a stimulují vývoj TH 2 § Vývoj TH 3 je stimulován specifickým cytokinovým prostředím IL-4, IL- 10, TGFb; TH 3 produkují TGFb, spolupracují s B lymfocyty v MALT


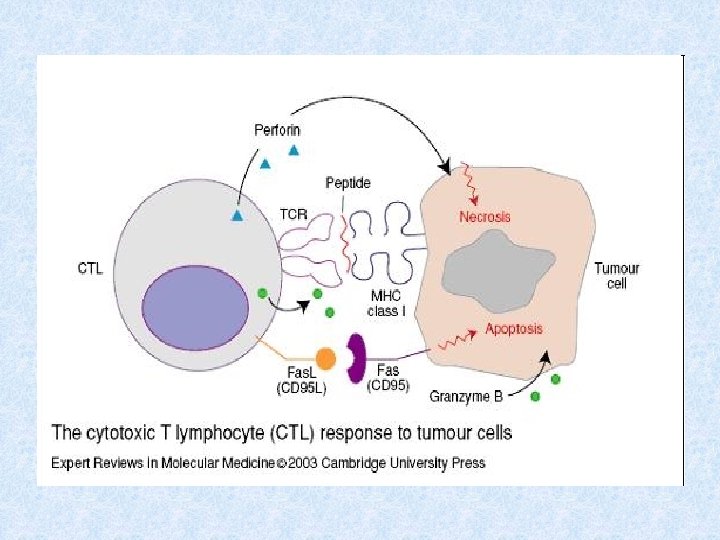
Imunitní reakce založená na TC

Aktivace cytotoxických T lymfocytů § TC rozpoznávají buňky infikované viry či jinými intracelulárními parazity a některé nádorové buňky § Prekurzor TC , který rozpozná komplex MHC gp I- antigenní peptid na povrchu APC přes TCR a dostane signály přes CD 28 proliferuje a diferencuje se na klon zralých efektorových cytotoxických buněk (CTL); toto probíhá za pomoci TH 1 lymfocytů produkujících IL-2 § Efektorové TC jsou rozneseny krevním oběhem do tkání, k aktivaci cytotoxických mechanismů stačí signál přes TCR (signál přes kostimulační receptor CD 28 již není nutný)

§ Profesionální APC jsou dendritické buňky nebo makrofágy, které jsou infikovány virem, nebo pohltili antigeny z odumřelé virem infikované, nádorové nebo stresované buňky § Aby APC mohla aktivovat prekurzor TC , musí být sama stimulována kontaktem s TH buňkami přes CD 40, poté začne dendritická buňka exprimovat CD 80, CD 86 a sekretovat cytokiny (IL-1, IL-12) = přeměna klidové APC v aktivovanou

Efektorové mechanismy TC § Cytotoxická granula obsahující perforin a granzymy (perforin vytváří póry v cytoplazmatické membráně napadené buňky, v některých případech může dojít k osmotické lýze napadené buňky, vytvořenými póry se do buňky dostávají granzymy, které aktivují caspázy, což vede k apoptóze napadené buňky § Fas-ligand (Fas. L) – který se váže na apoptotický receptor Fas (CD 95) přítomný na povrchu mnoha různých bb. (i na povrchu TC) § TNFb


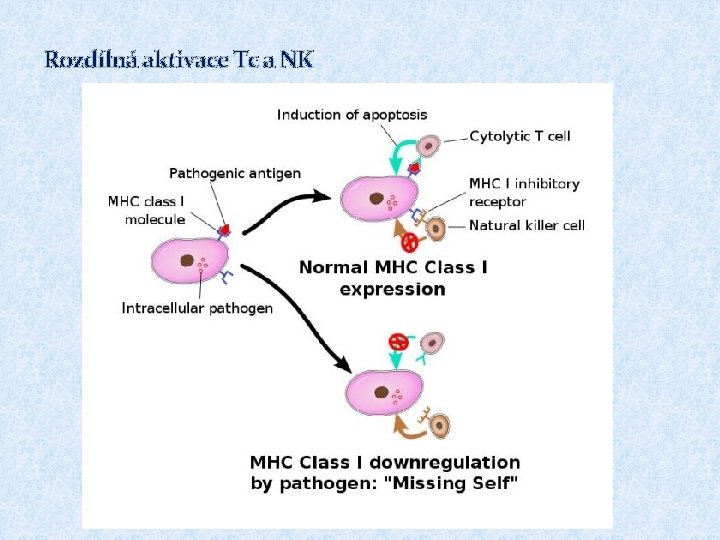
Rozdílná aktivace Tc a NK