HIDROCARBUROS SATURADOS ALCANOS Y CICLOALCANOS SEMANA 16 LICDA

HIDROCARBUROS SATURADOS ALCANOS Y CICLOALCANOS SEMANA 16 LICDA. CORINA MARROQUIN 2021

ORIGEN DE LOS HIDROCARBUROS

Desastre ecológico 30 abril 2010

UTILIDAD HIDROCARBUROS
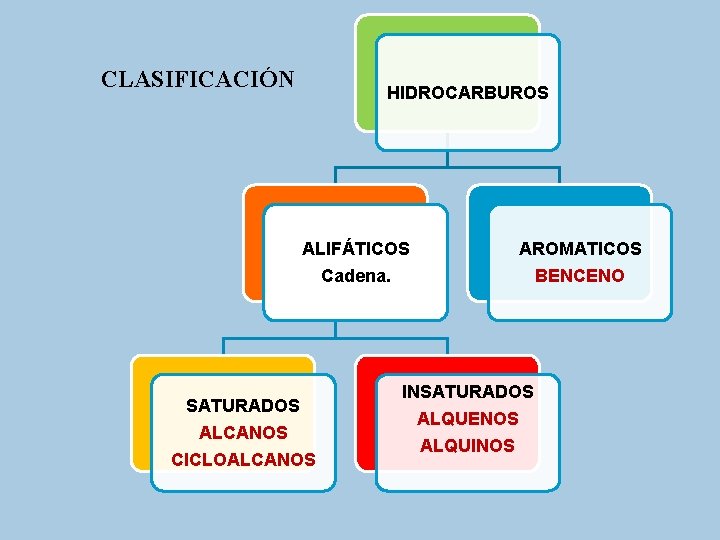
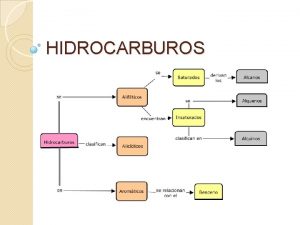
CLASIFICACIÓN HIDROCARBUROS ALIFÁTICOS AROMATICOS Cadena. BENCENO SATURADOS ALCANOS CICLOALCANOS INSATURADOS ALQUENOS ALQUINOS

Los hidrocarburos según el tipo de enlace: SATURADOS E INSATURADOS. Los hidrocarburos pueden ser: lineales , ramificados y cíclicos. Según la naturaleza del enlace se conocen como: a. Alcanos: o hidrocarburos saturados: compuestos formados únicamente por carbono e hidrógeno unidos por enlaces covalentes sencillos entre los carbonos. b. Alquenos: hidrocarburos insaturados que tienen un enlace covalente doble entre dos átomos de carbonos. c. Alquinos: hidrocarburos insaturados que tienen un enlace covalente triple entre dos átomos de carbono.
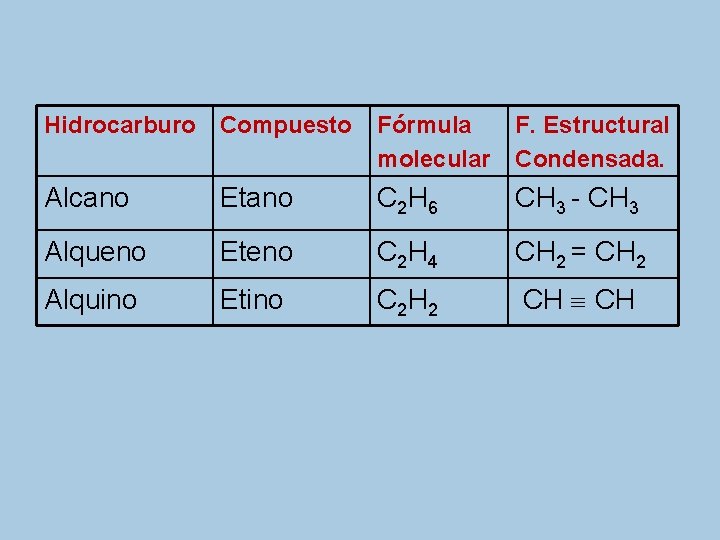
Hidrocarburo Compuesto Fórmula molecular F. Estructural Condensada. Alcano Etano C 2 H 6 CH 3 - CH 3 Alqueno Eteno C 2 H 4 CH 2 = CH 2 Alquino Etino C 2 H 2 CH


ALCANOS o PARAFINAS. Son hidrocarburos saturados que sólo tiene enlaces covalentes sencillos. (Enlaces sigma). Pueden ser: lineales , ramificados y cíclicos. Los hidrocarburos saturados se consideran frecuentemente como los compuestos básicos de la química orgánica, ya que los demás compuestos orgánicos que se conocen pueden considerarse como derivados de ellos. Parafinas significa de poca afinidad.

ALCANOS (sufijo ano) Los alcanos son una serie homóloga, su fórmula general es: Cn. H 2 n+2 n = no. De átomos de carbono. Existen alcanos de cualquier longitud y su nomenclatura debe seguir un patrón.
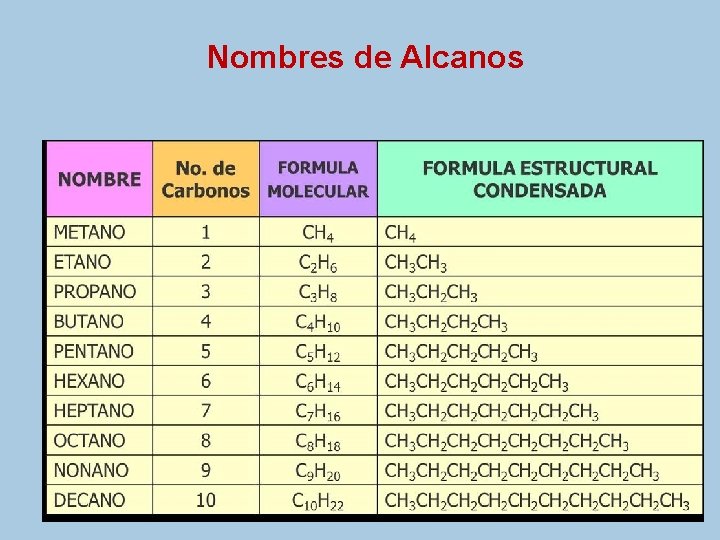
Nombres de Alcanos

Unión Internacional de Química Pura y Aplicada (UIQPA) 1892 IUPAC (International Union of Pure and Apllied Chemistry) La nomenclatura es común y sistemática, algunos nombres existen antes de que la química orgánica fuera una ciencia organizada.

REGLAS PARA NOMBRAR ALCANOS CON SUSTITUYENTES. IUPAC 1. Encuentre la cadena de carbono más larga y nómbrela de acuerdo al no. De C, con el prefijo griego correspondiente seguido del sufijo ano. 2. Dé nombre a las cadena más cortas. (grupos alquilo).

Grupo alquilo. Ramificación formada sólo por carbono e hidrógeno que nada más posea enlaces sencillos. Grupo que se deriva eliminando un hidrógeno de un alcano. Se representa por el símbolo R
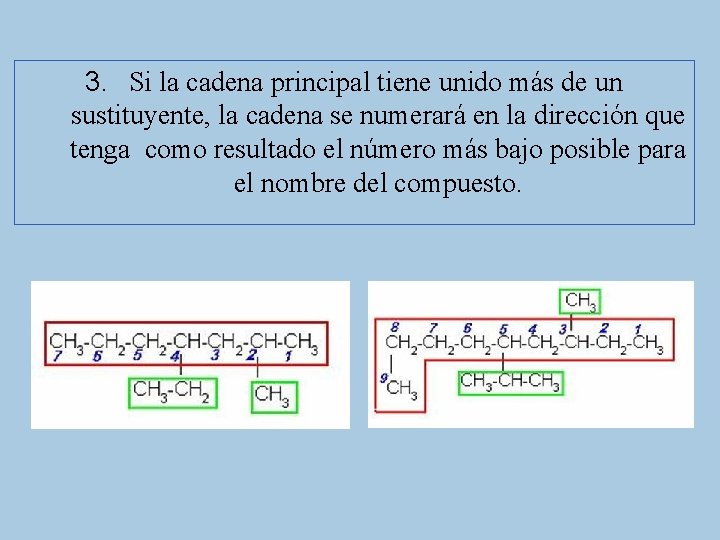
3. Si la cadena principal tiene unido más de un sustituyente, la cadena se numerará en la dirección que tenga como resultado el número más bajo posible para el nombre del compuesto.

4. Los grupos unidos a la cadena principal se denominan radicales o sustituyentes* A cada sustituyente se le da un nombre y se le asigna un número. El número indica el átomo de carbono de la cadena principal con el cual está enlazado. n 5. Cuando el mismo sustituyente se repite más de una vez, se indica el número de cada carbono de la cadena principal. Además se indica el número de veces que ocurre el sustituyente, di-, tri-, tetra-, penta-, hexa-, etc.

6. Cuando hay dos o más sustituyentes idénticos, se numera la cadena principal a partir del extremo que permita dar el número más bajo al sustituyente que se encuentra primero.

7. Si hay dos o más sustituyentes distintos, se mencionan en orden alfabético y se numera la cadena desde el extremo que permite dar el número más bajo al sustituyente que se encuentre primero. Ej. etilo antes de metilo.

8. Los prefijos di-, tri-, tetra-, no se incluyen al alfabetizar. Se alfabetizan primero los nombres de los sustituyentes y después se insertan estos prefijos de multiplicación.

9. Los prefijos con guión como sec- y ter- no se consideran al alfabetizar. El prefijo iso no lleva guión y sí se cuenta para alfabetizar. Entre no. y no. Se pone coma y entre no. y letra guión.
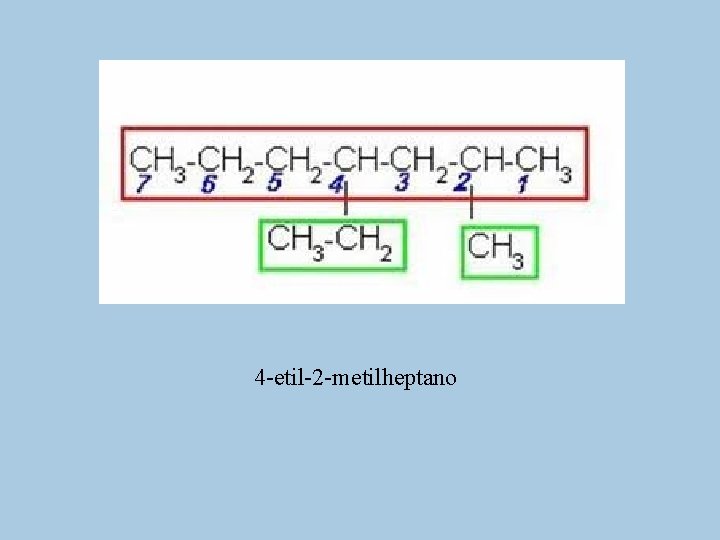
4 -etil-2 -metilheptano

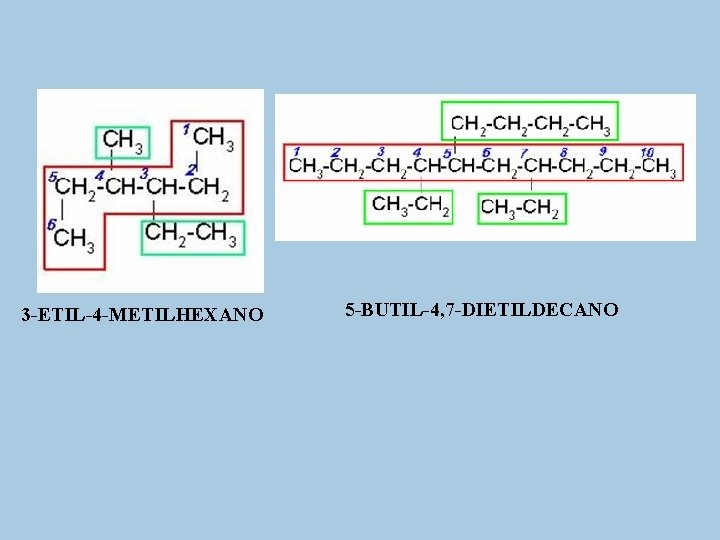
3 -ETIL-4 -METILHEXANO 5 -BUTIL-4, 7 -DIETILDECANO
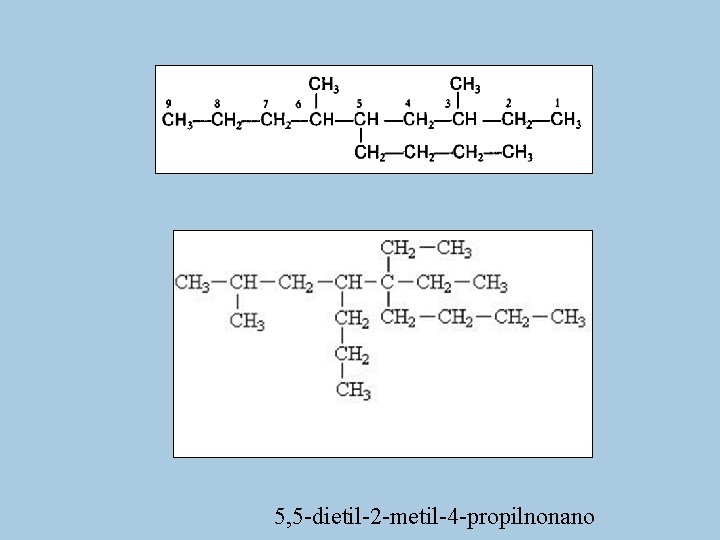
5, 5 -dietil-2 -metil-4 -propilnonano
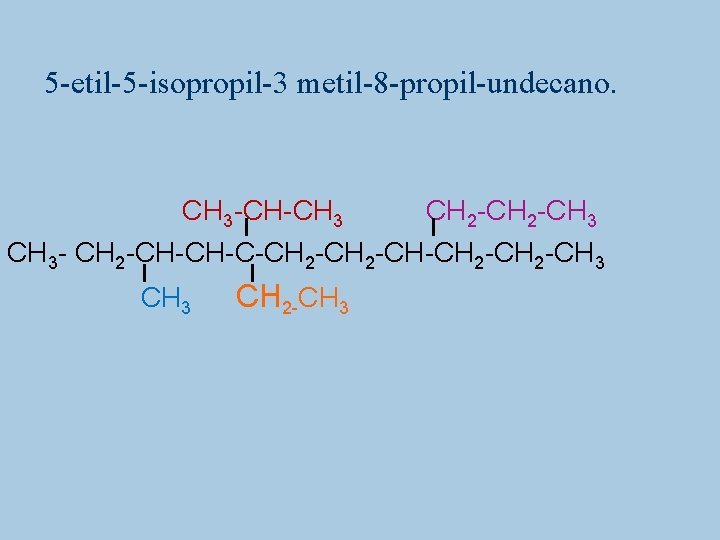
5 -etil-5 -isopropil-3 metil-8 -propil-undecano. CH 3 -CH-CH 3 CH 2 -CH 3 - CH 2 -CH-CH-C-CH 2 -CH 3 CH 2 -CH 3
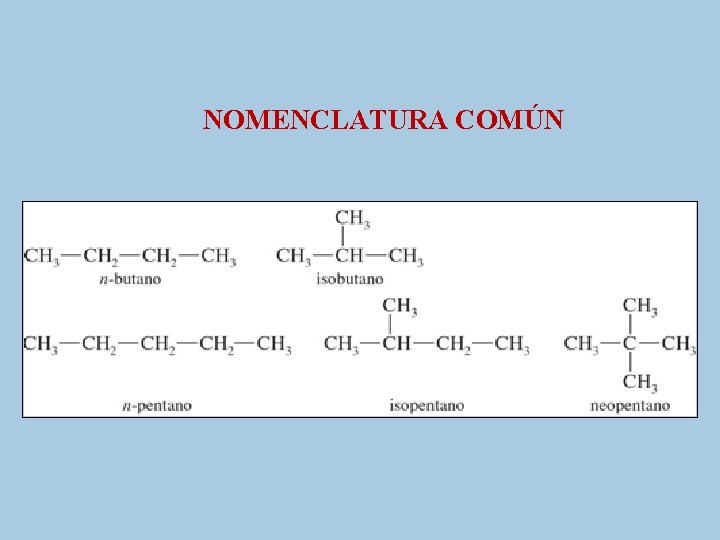
NOMENCLATURA COMÚN
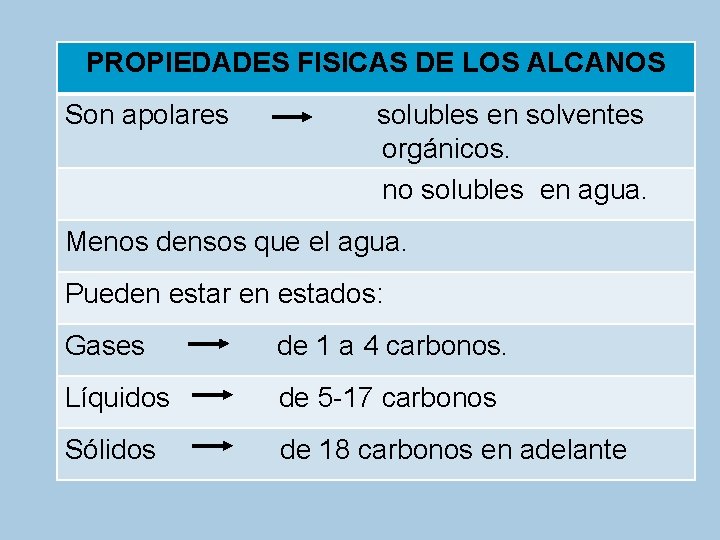
PROPIEDADES FISICAS DE LOS ALCANOS Son apolares solubles en solventes orgánicos. no solubles en agua. Menos densos que el agua. Pueden estar en estados: Gases de 1 a 4 carbonos. Líquidos de 5 -17 carbonos Sólidos de 18 carbonos en adelante

Punto de ebullición: Los alcanos normales muestran un aumento constante en el punto de ebullición al aumentar el peso molecular. Si el alcano es ramificado disminuye notablemente el punto de ebullición y además cuanto más numerosas sean las ramificaciones, menor es su valor.
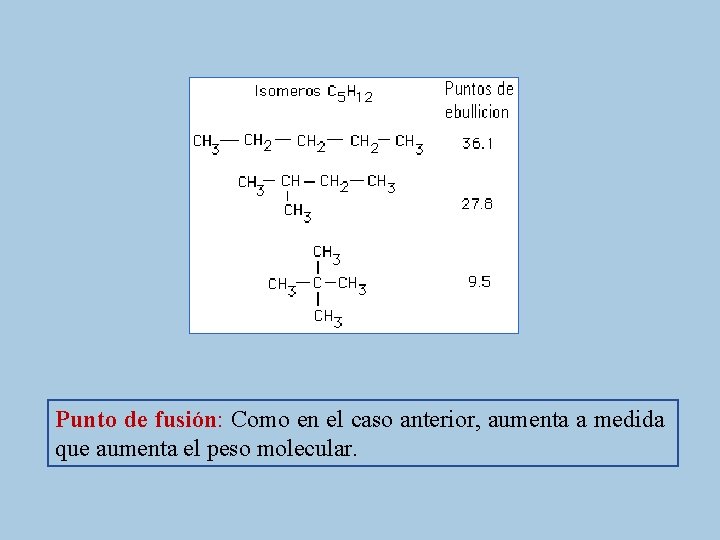
Punto de fusión: Como en el caso anterior, aumenta a medida que aumenta el peso molecular.

CICLOALCANOS Los cicloalcanos son alcanos que contienen un anillo de tres o más átomos de carbono Su fórmula molecular es : Cn. H 2 n Ciclopropano, Ciclobutano, Ciclopentano y Ciclohexano.
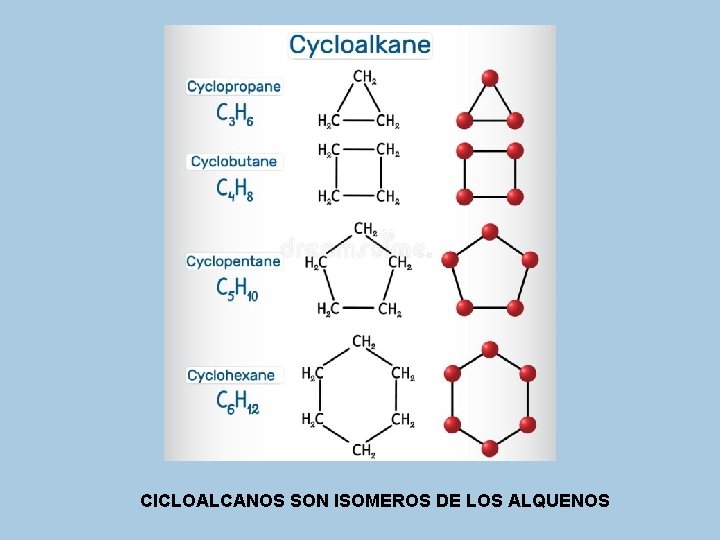
CICLOALCANOS SON ISOMEROS DE LOS ALQUENOS

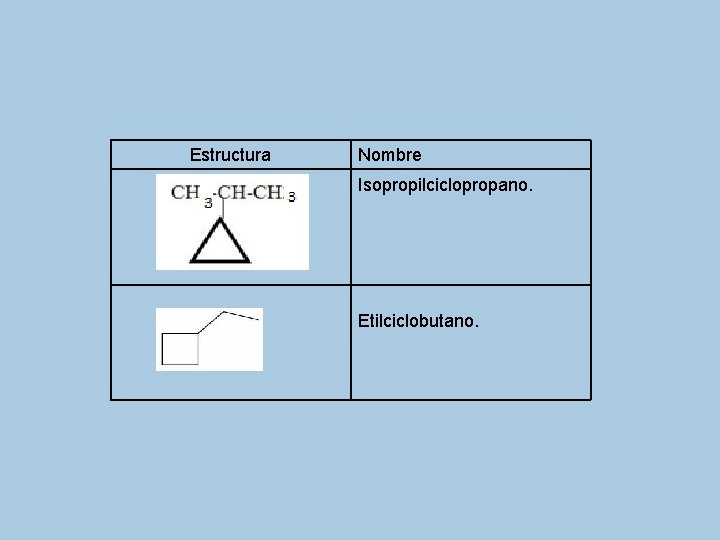
Estructura Nombre Isopropilciclopropano. Etilciclobutano.
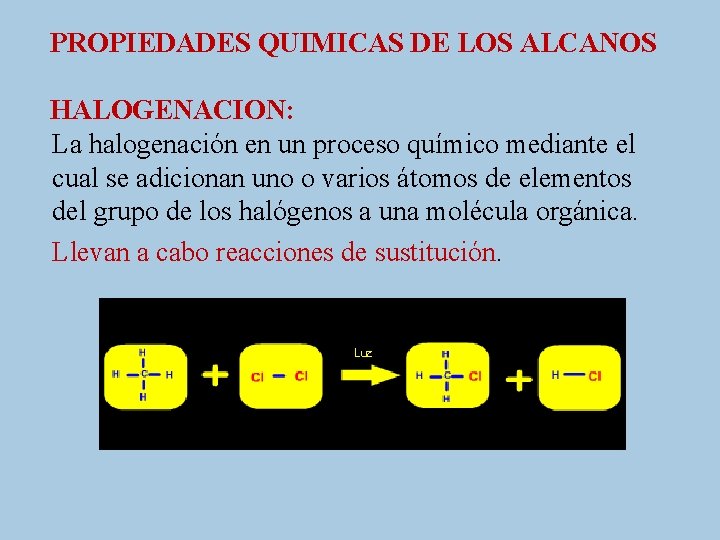
PROPIEDADES QUIMICAS DE LOS ALCANOS HALOGENACION: La halogenación en un proceso químico mediante el cual se adicionan uno o varios átomos de elementos del grupo de los halógenos a una molécula orgánica. Llevan a cabo reacciones de sustitución.

COMBUSTIÓN Es una reacción química que se producen entre el oxígeno y un material oxidable, va acompañada de desprendimiento de energía y habitualmente se manifiesta con llama. Esta foto de Autor desconocido está bajo licencia CC BY-SA



QATAR
- Slides: 38