COMPUESTOS TERNARIOS HIDROXIDOS Los hidrxidos son compuestos inicos








- Slides: 11

COMPUESTOS TERNARIOS

HIDROXIDOS � Los hidróxidos son compuestos iónicos donde los cationes provienen de un metal y los aniones son los iones hidróxido (OH-). � Responden a la fórmula general Me (OH)n y se nombran de la siguiente manera

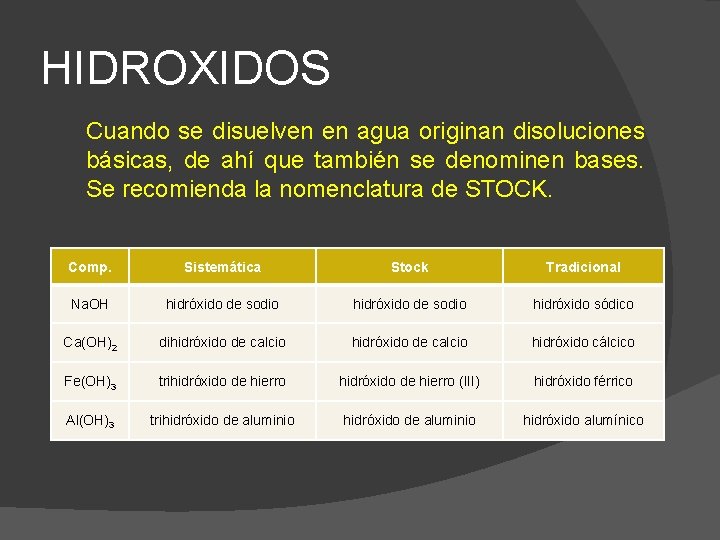
HIDROXIDOS Cuando se disuelven en agua originan disoluciones básicas, de ahí que también se denominen bases. Se recomienda la nomenclatura de STOCK. Comp. Sistemática Stock Tradicional Na. OH hidróxido de sodio hidróxido sódico Ca(OH)2 dihidróxido de calcio hidróxido cálcico Fe(OH)3 trihidróxido de hierro (III) hidróxido férrico Al(OH)3 trihidróxido de aluminio hidróxido alumínico

OXOÁCIDOS � Son los ácidos que tienen oxígeno. Se denominan ácidos porque en solución acuosa se ionizan perdiendo sus hidrógenos como protones y quedando un anión oxigenado con tantas cargas negativas como hidrógenos se disociaron. � Responden en general a la fórmula Ha No. Me Ob, en la que el no-metal se encuentra en el centro y salvo excepciones tiene atomicidad uno.

OXOÁCIDOS Se forman con los óxidos ácidos (anhidridos) + agua a) Acidos oxoácidos de los halógenos, anfígenos y nitrógeno: se forman con una molécula de anhídrido y una de agua • Oxoácidos del grupo de los halógenos: Cl, Br, I (+1, +3, +5, +7) Sistemática Tradicional oxoclorato (I) de hidrógeno ácido hipocloroso • Cl 2 O 3 + H 2 O HCl. O 2 dioxoclorato (III) de hidrógeno ácido cloroso • Cl 2 O 5 + H 2 O HCl. O 3 trioxoclorato (V) de hidrógeno ácido clórico tetraoxoclorato (VII) de hidrógeno ácido perclórico • Cl 2 O + H 2 O HCl. O • Cl 2 O 7 + H 2 O HCl. O 4

OXOÁCIDOS • Oxoácidos del grupo de los anfígenos: S, Se, Te (+2, +4, +6) • SO + H 2 O H 2 SO 2 • SO 2 + H 2 O H 2 SO 3 • SO 3 + H 2 O H 2 SO 4 Sistemática Tradicional dioxosulfato (II) de hidrógeno ácido hiposulfuroso trioxosulfato (IV) de hidrógeno ácido sulfuroso tetraoxosulfato (VI) de hidrógeno ácido sulfúrico • Oxoácidos del grupo de los nitrogenoideos: N (+1, +3, +5), P (+1, +3, +5), As, Sb (+3, +5) Sistemática Tradicional oxonitrato (I) de hidrógeno ácido hiponitroso • N 2 O 3 + H 2 O HNO 2 dioxonitrato (III) de hidrógeno ácido nitroso • N 2 O 5 + H 2 O HNO 3 trioxonitrato (V) de hidrógeno ácido nítrico • N 2 O + H 2 O HNO

OXOÁCIDOS • Oxoácidos del grupo de los nitrogenoideos: N (+1, +3, +5), P (+1, +3, +5), As, Sb (+3, +5) El P, As y Sb pueden formar más de un oxoácido con el mismo n. o. • • anhídrido + H 2 O oxoácido META + H 2 O • 2 oxoácido ORTO - H 2 O • P 2 O 5 + H 2 O HPO 3 • HPO 3 + H 2 O H 3 PO 4 • 2 H 3 PO 4 + H 2 O H 4 P 2 O 7 META oxoácido ORTO oxoácido DI o PIRO Sistemática Tradicional trioxofosfato (V) de hidrógeno ácido metafosfórico tetraoxofosfato (V) de hidrógeno ácido ortofosfórico heptaoxodifosfato (V) de hidrógeno ácido difosfórico

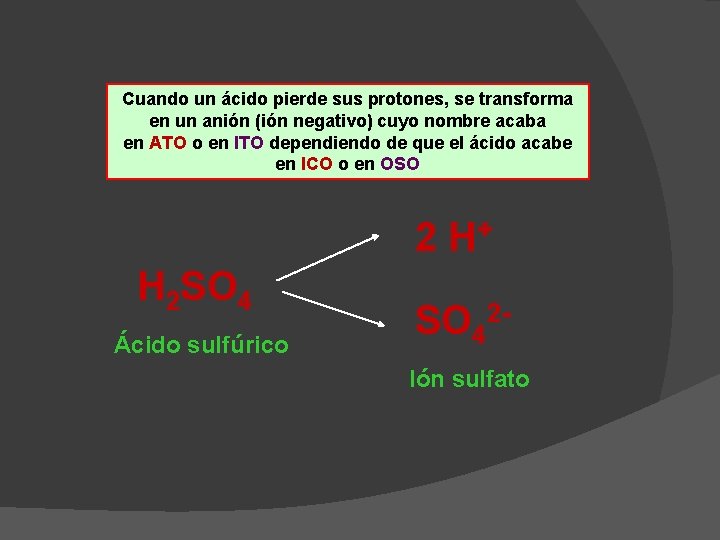
Cuando un ácido pierde sus protones, se transforma en un anión (ión negativo) cuyo nombre acaba en ATO o en ITO dependiendo de que el ácido acabe en ICO o en OSO 2 H+ H 2 SO 4 Ácido sulfúrico SO 42 Ión sulfato

ACIDOS OXOÁCIDOS Y SUS IONES

OXOSALES Son compuestos derivados de un oxoácido, en el que se sustituyen el (los) hidrógeno(s) por un metal(es). Están formados por un metal, no metal y oxígeno. Se obtien por neutralización total de un oxoácido y un hidróxido: • oxoácido + hidróxido oxosal + agua • HNO 3 + Na. OH Na. NO 3 + H 2 O

NOMENCLATURA Tradicional: se nombran sustituyendo, del nombre del no metal, los sufijos –oso e –ico por –ito y –ato, respectivamente Stock: igual que en la tradicional, pero se indica la valencia el metal, si es necesario. Sistemática: se nombran igual que los ácidos; sólo se cambian la palabra hidrógeno por el nombre del metal con la valencia del mismo Se recomienda la Tradicional y la de Stock. Comp. Sistemática Stock Tradicional Na. NO 3 trioxonitrato (V) de sodio nitrato sódico Cd. SO 3 trioxosulfato (IV) de cadmio sulfato de cadmio Cu 3(PO 4)2 tetraoxofosfato (V) de cobre (II) fosfato cúprico Sn(NO 2)4 dioxonitrato (III) de estaño (IV) nitrito estánnico