Los hidrocarburos son compuestos constituidos solamente por tomos

Los hidrocarburos: son compuestos constituidos solamente por átomos de carbono e hidrógeno.
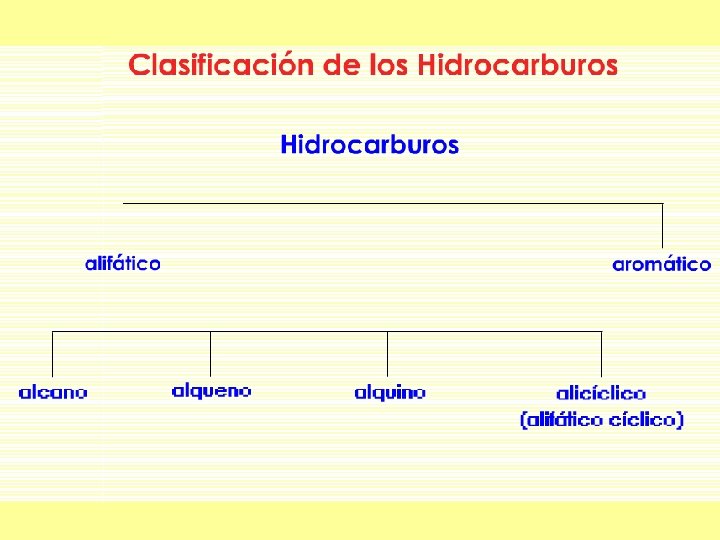

Clases de hidrocarburos según el tipo de enlace: Clasificación: • Alcanos o hidrocarburos saturados: compuestos formados únicamente por carbono e hidrógeno unidos por enlaces covalentes sencillos entre los carbonos.

• Alquenos: hidrocarburos insaturados que tienen un enlace covalente doble entre dos átomos de carbonos. • Alquinos: hidrocarburos insaturados que tienen un enlace covalente triple entre dos átomos de carbono.


Clases de hidrocarburos según la forma de la cadena Hidrocarburos de cadena abierta o acíclicos 1. Lineales o normales: Son cadenas con átomos de carbono unidos cada uno a un máximo de dos carbonos. 2. Ramificados: Cada átomo de carbono se puede unir a 3 o 4 átomos de carbono.

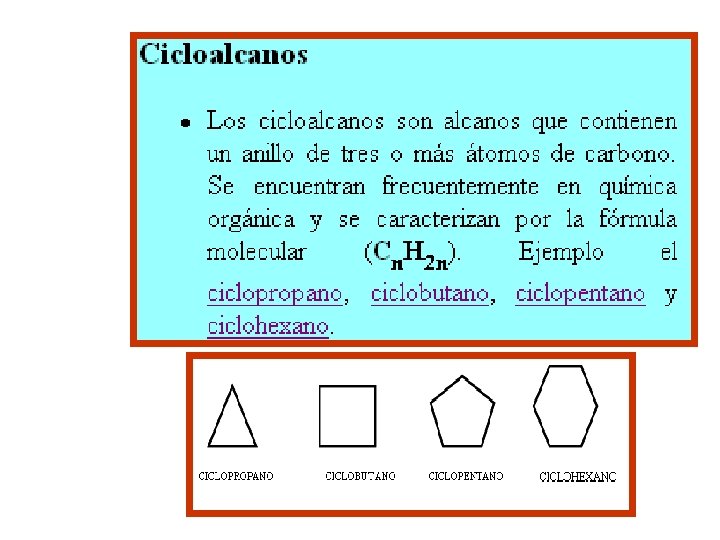
Hidrocarburos de cadena cerrada o cíclicos Están formados por cadenas de átomos que se cierran formando uno o varios anillos o ciclos con tres o más carbonos. Pueden ser: a. Alicíclicos b. Aromáticos

Hidrocarburos saturados: Estos compuestos también se conocen como hidrocarburos parafínicos o alcanos. El nombre parafina viene del latín parum affinis, poca actividad, por su naturaleza no reactiva. Los hidrocarburos saturados se consideran los compuestos básicos de la química orgánica




1. El nombre general de un hidrocarburo saturado de cadena abierta es ALCANO. 2. Para los hidrocarburos de cadena ramificada, la cadena de átomos de carbono más larga se considera como alcano principal.


3. Los grupos unidos a la cadena principal se denominan sustituyentes. A cada sustituyente se le da un nombre y se le asigna un número. Ej: Metilo: -CH 3 Etilo: -CH 2 CH 3 propilo : -CH 2 CH 3 Grupo alquilo: Grupo que se deriva eliminando un hidrógeno de un alcano. Se representa por el símbolo R

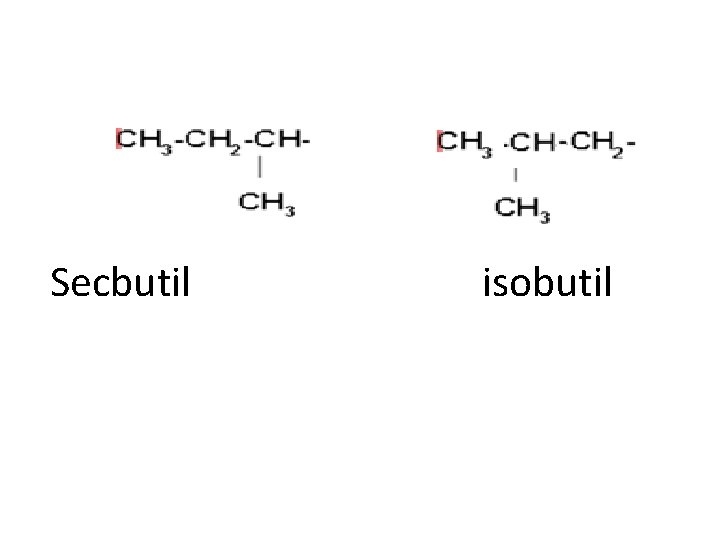
Secbutil isobutil

4. Cuando hay un sustituyente se enumera la cadena principal desde el extremo que permita dar el número más bajo a dicho sustituyente. 5. Cuando el mismo sustituyente se repite, se indica el número: di-, tri-, tetra-, penta-, hexa-, etc. Ojo: Estos prefijos No se incluyen al alfabetizar

6. Si hay dos o más sustituyentes distintos, se mencionan en orden alfabético y se numera la cadena desde el extremo que permite dar el número más bajo al sustituyente que se encuentre primero.
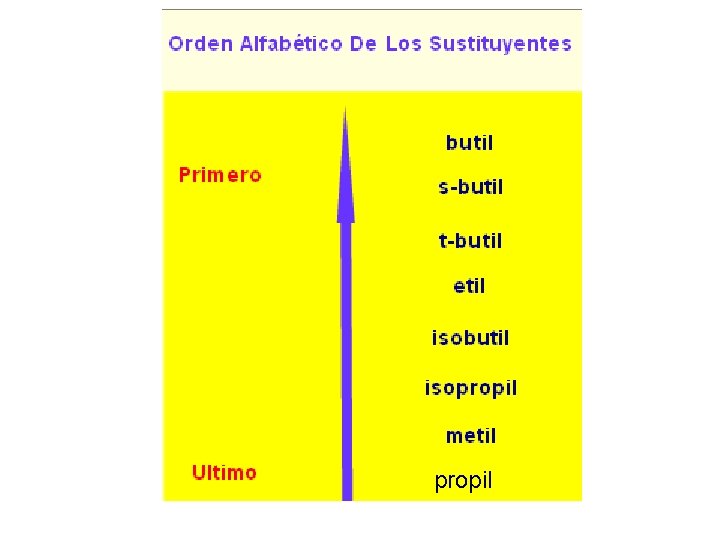
propil
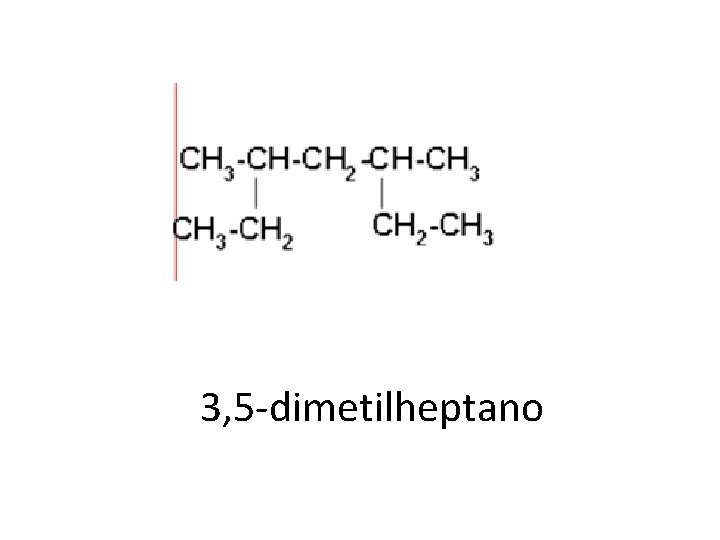
3, 5 -dimetilheptano
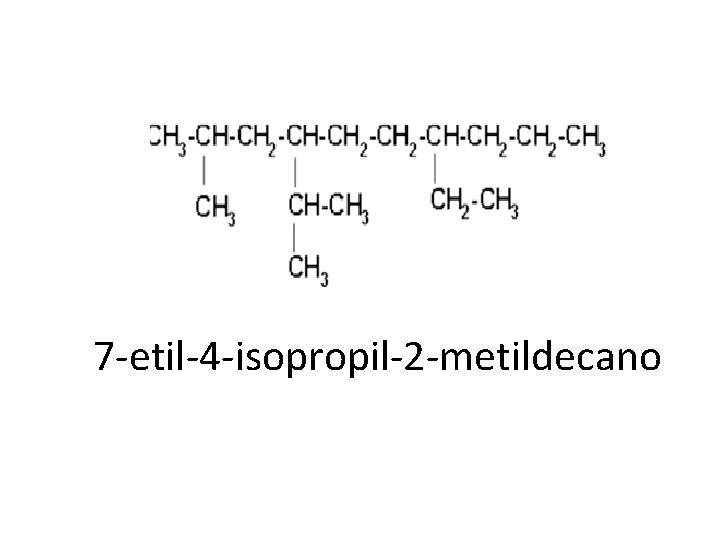
7 -etil-4 -isopropil-2 -metildecano
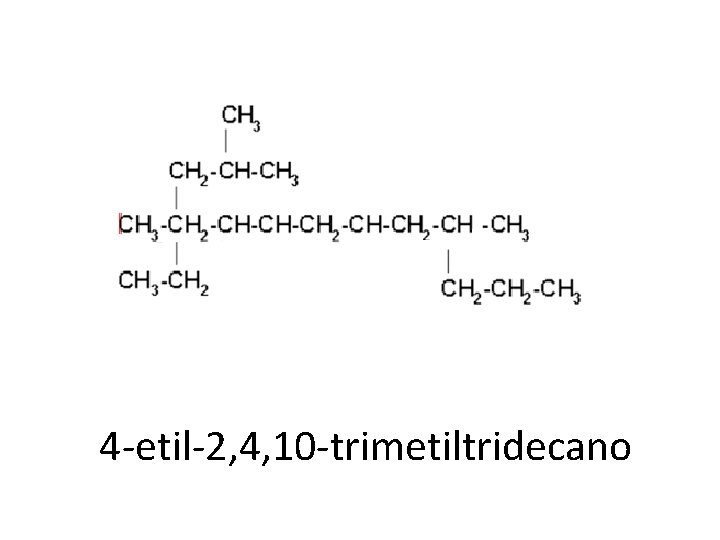
4 -etil-2, 4, 10 -trimetiltridecano


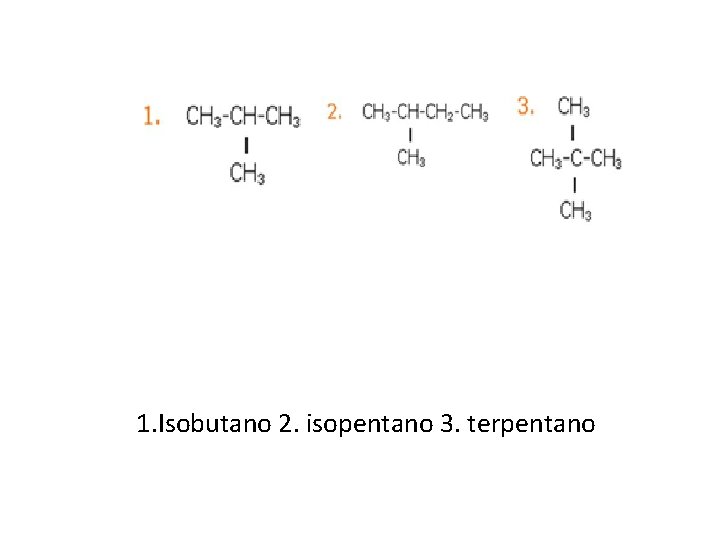
1. Isobutano 2. isopentano 3. terpentano
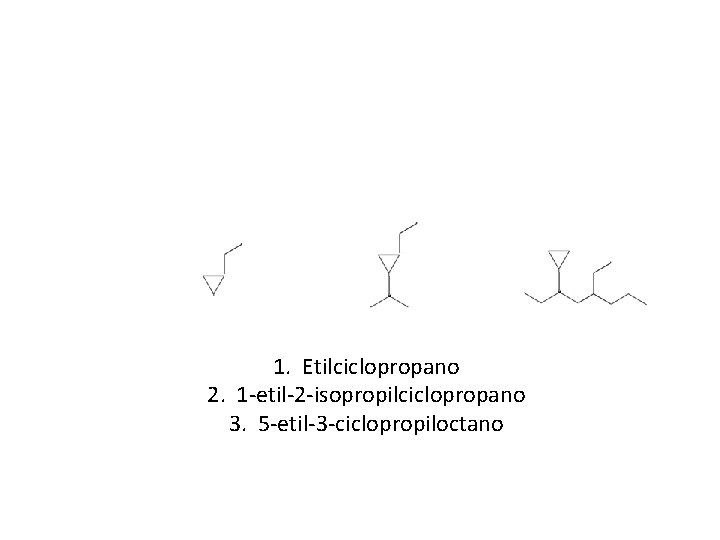
1. Etilciclopropano 2. 1 -etil-2 -isopropilciclopropano 3. 5 -etil-3 -ciclopropiloctano

PROPIEDADES FISICAS DE ALCANOS: • Son apolares, no solubles en agua pero si en solventes orgánicos. • Son menos densos que el agua (flotan). • Pueden estar en estado gaseoso (C 1 -C 4), líquidos (C 5 -C 16) y sólidos (C 17 o más).

Punto de ebullición: aumento en el punto de ebullición al aumentar el peso molecular. Si es ramificado disminuye el punto de ebullición y además cuanto más numerosas sean las ramificaciones, menor es el punto de ebullición.

Punto de fusión: Como en el caso anterior, aumenta a medida que crece el peso molecular.

• Son los menos reactivos de los compuestos orgánicos, No reaccionan con: ácidos fuertes, bases fuertes y casi todos los agentes oxidantes y reductores.

Son poco reactivos experimentan reacciones de: y Sustitución: sale un H y entra otro àtomo o grupo de átomos.



Combustión: Es la Oxidación acompañada de liberación de energía y los productos dependen de la cantidad de energía. Puede ser dependiendo de la cantidad de oxígeno: completa CO 2 + agua + energía (alcanos o hidrocarburos saturados) Incompleta CO + agua + energía C + agua + energía

- Slides: 36