SEMANA 16 HIDROCARBUROS SATURADOS Alcanos y Cicloalcanos Captulo

SEMANA 16 HIDROCARBUROS SATURADOS (Alcanos y Cicloalcanos) Capítulo 11 Licda. Bárbara Toledo Petróleo: mezcla de alcanos y cicloalcanos

Hidrocarburos Se consideran frecuentemente como los compuestos básicos de la química orgánica, ya que ellos le dan origen a muchos de los otros compuestos que se conocen. Los hidrocarburos, como su nombre lo indica, son compuestos constituidos solamente por átomos de carbono e hidrógeno.
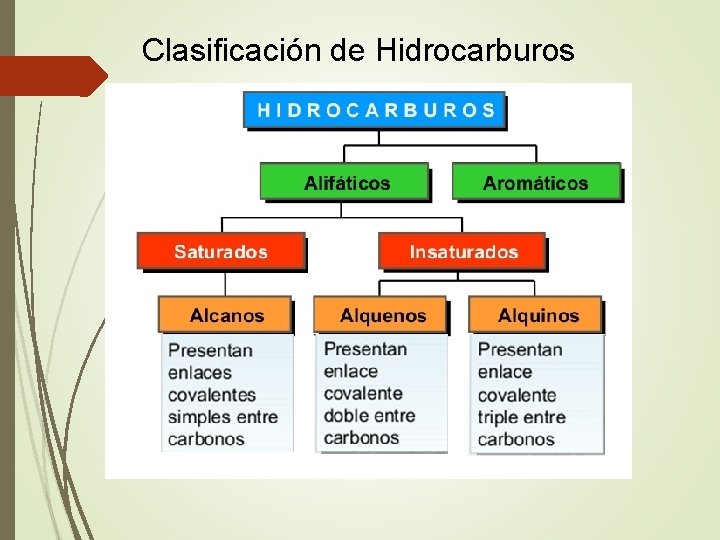
Clasificación de Hidrocarburos
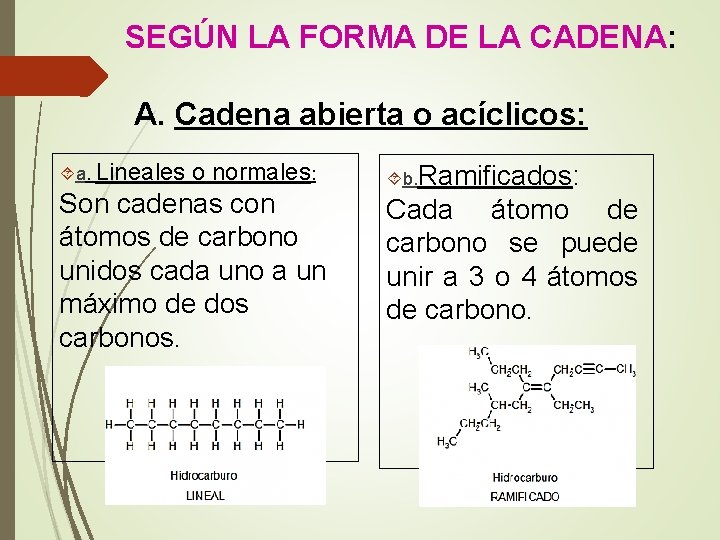
SEGÚN LA FORMA DE LA CADENA: A. Cadena abierta o acíclicos: a. Lineales o normales: Son cadenas con átomos de carbono unidos cada uno a un máximo de dos carbonos. b. Ramificados: Cada átomo de carbono se puede unir a 3 o 4 átomos de carbono.
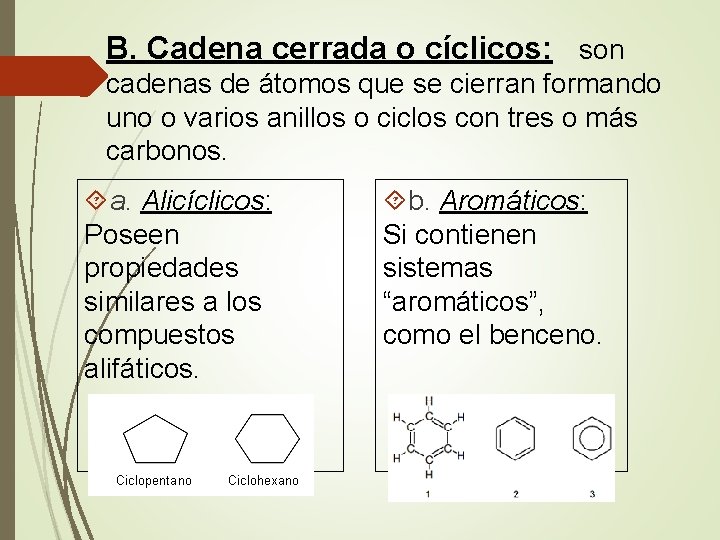
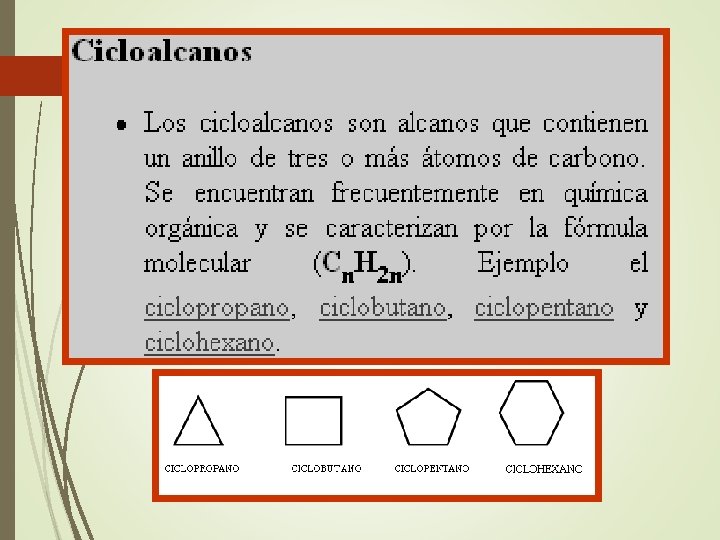
B. Cadena cerrada o cíclicos: son cadenas de átomos que se cierran formando uno o varios anillos o ciclos con tres o más carbonos. a. Alicíclicos: Poseen propiedades similares a los compuestos alifáticos. b. Aromáticos: Si contienen sistemas “aromáticos”, como el benceno.

ALCANOS Son compuestos relativamente inertes comparados con otros; su reactividad depende de la elección del reactivo. La fórmula general de los alcanos es (Cn. H 2 n+2) donde n es el número de átomos de carbonos. Ejemplo: n= 3 entonces C 3 H 2*3+2 = C 3 H 8

Propiedades Físicas • Son apolares • No son solubles en agua pero si en solventes orgánicos. • Son menos densos que el agua (flotan). • Pueden estar en estado • gaseoso (C 1 -C 4), • líquidos (C 5 -C 17) • sólidos (C 18 o más). • Son incoloros, inodoros, insípidos • Presentan isómeros y serie homóloga
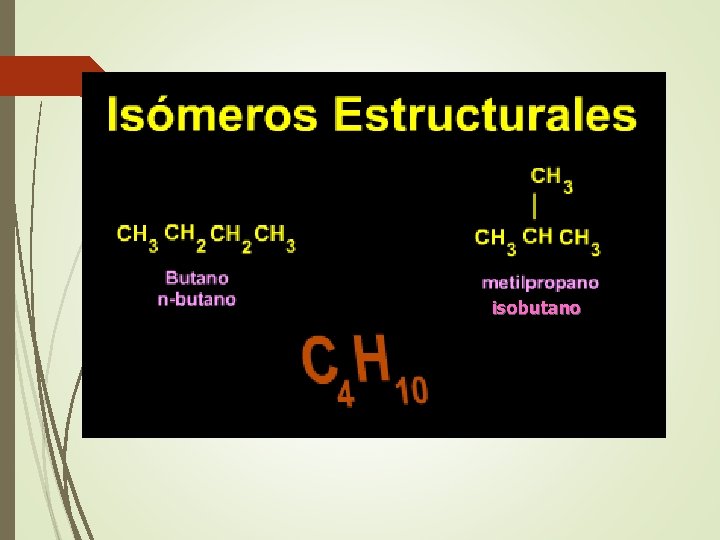
isobutano

Serie Homóloga Conjunto de compuestos que comparten el mismo grupo funcional por lo que poseen propiedades físicas y químicas semejantes. Todos los compuestos de la serie contienen los mismos elementos y pueden representarse mediante una misma fórmula general. La fórmula molecular de cada homólogo difiere de la que precede y de la que le sucede por el incremento de un grupo metileno "-CH 2 -". Existe una variación gradual en las propiedades físicas con el incremento de la masa molecular.

Punto de ebullición: Los alcanos normales (lineales) muestran un aumento constante en el punto de ebullición al aumentar el peso molecular. Si el alcano es ramificado disminuye notablemente el punto de ebullición y además cuanto más numerosas sean las ramificaciones, menor es su valor.

Punto de fusión: Como en el caso anterior, aumenta a medida que crece el peso molecular. Este aumento no es tan regular, debido a que los alcanos con número par de átomos de carbono se compactan en el estado cristalino haciendo que las fuerzas de atracción entre las cadenas individuales sean mayores, y por consiguiente, los puntos de fusión lo sean también.
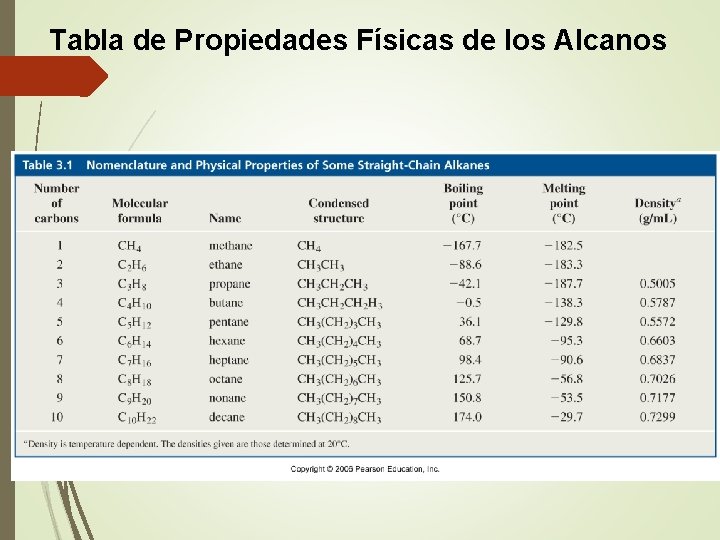
Tabla de Propiedades Físicas de los Alcanos

NOMENCLATURA

NOMENCLATURA SISTEMÁTICA IUPAC International Union of Pure and Applied Chemistry. UIQPA Unión Internacional de Química Pura y Aplicada. Bases del sistema: “cada compuesto diferente debe tener un nombre diferente”.

Nomenclatura 1. Todos llevan la terminación, ano. 2. El nombre base, es el número total de átomos de carbono en la cadena. 3. Los de cadena recta utilizan el prefijo, n –
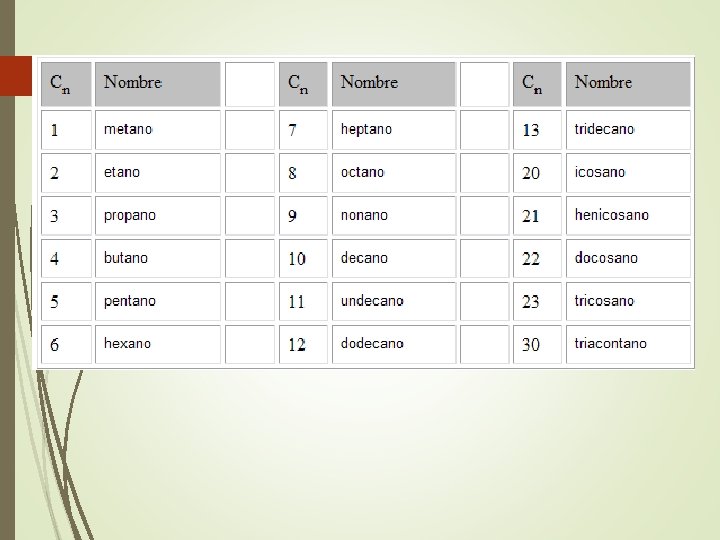
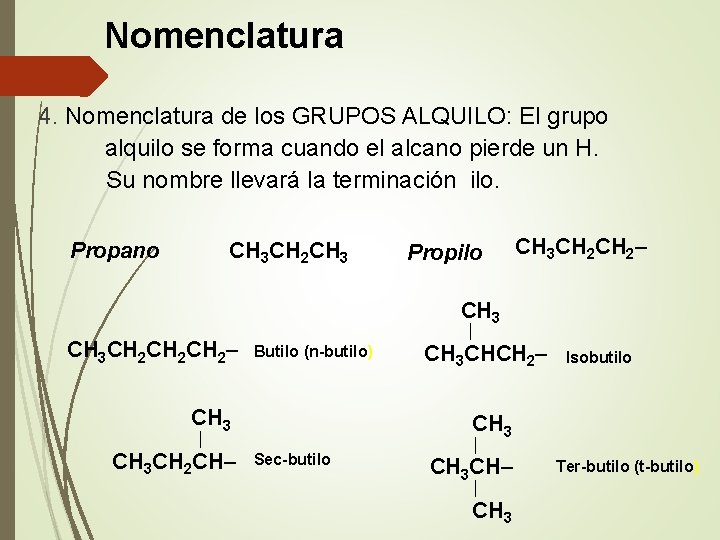
Nomenclatura 4. Nomenclatura de los GRUPOS ALQUILO: El grupo alquilo se forma cuando el alcano pierde un H. Su nombre llevará la terminación ilo. CH 3 CH 2 CH 3 Propano Propilo CH 3 CH 2– CH 3 CH 2 CH 2– │ Butilo (n-butilo) CH 3 Isobutilo CH 3 │ CH 3 CH 2 CH– CH 3 CHCH 2– Sec-butilo │ CH 3 CH– │ CH 3 Ter-butilo (t-butilo)
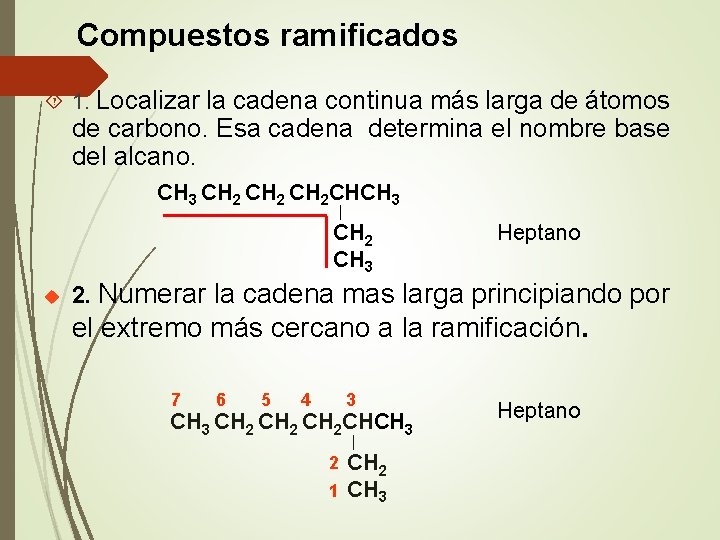
Compuestos ramificados 1. Localizar la cadena continua más larga de átomos de carbono. Esa cadena determina el nombre base del alcano. CH 3 CH 2 CHCH 3 │ CH 2 CH 3 u Heptano 2. Numerar la cadena mas larga principiando por el extremo más cercano a la ramificación. 7 6 5 4 3 CH 2 CHCH 3 │ CH 2 1 CH 3 2 Heptano
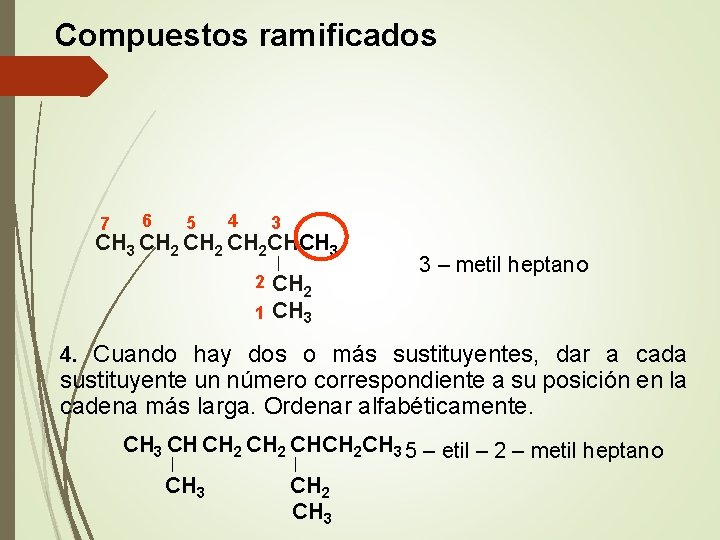
Compuestos ramificados 7 6 5 4 3 CH 2 CHCH 3 │ CH 2 1 CH 3 2 3 – metil heptano 4. Cuando hay dos o más sustituyentes, dar a cada sustituyente un número correspondiente a su posición en la cadena más larga. Ordenar alfabéticamente. CH 3 CH CH 2 CHCH 2 CH 3 5 – etil – 2 – metil heptano │ CH 3 │ CH 2 CH 3
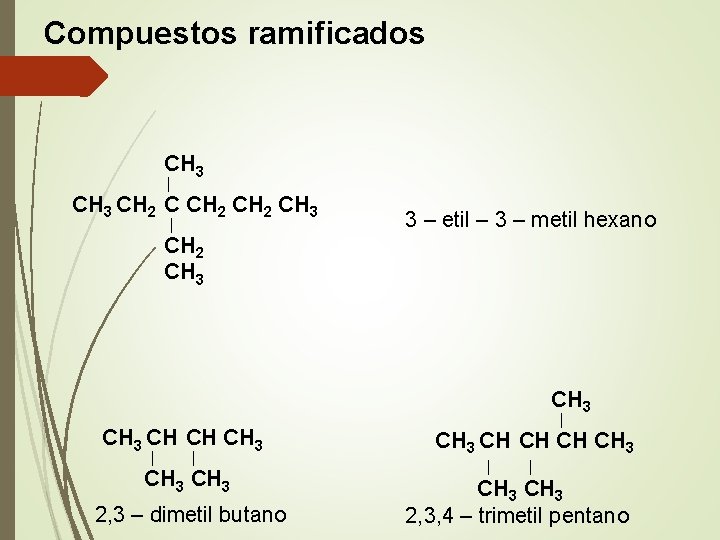
Compuestos ramificados CH 3 │ CH 3 CH 2 CH 3 │ 3 – etil – 3 – metil hexano CH 2 CH 3 CH CH CH 3 │ │ CH 3 2, 3 – dimetil butano │ CH 3 CH CH 3 │ │ CH 3 2, 3, 4 – trimetil pentano
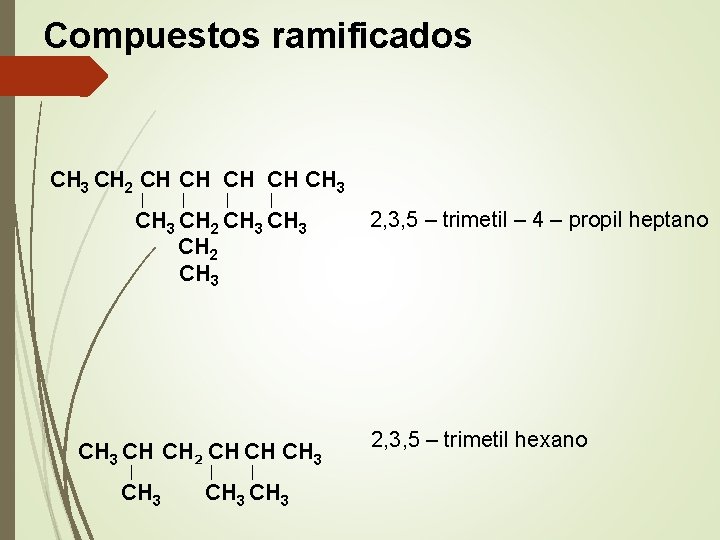
Compuestos ramificados CH 3 CH 2 CH CH CH 3 │ │ CH 3 CH 2 CH 3 CH CH 2 CH CH CH 3 │ │ CH 3 2, 3, 5 – trimetil – 4 – propil heptano 2, 3, 5 – trimetil hexano

Nomenclatura Común La nomenclatura común usa prefijos: n- “normal” se coloca a una cadena sin ramificaciones isogrupo metilo unido a un segundo carbono neo-se utiliza para compuestos de cinco siete a átomos de carbono, con un carbono cuaternario
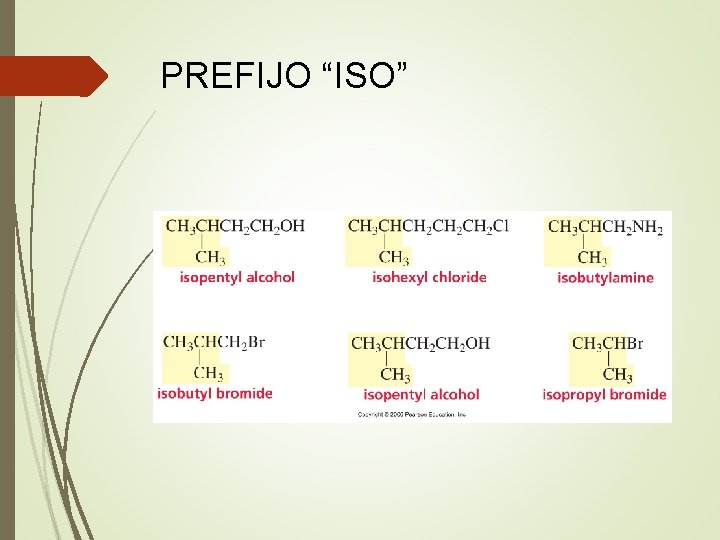
PREFIJO “ISO”
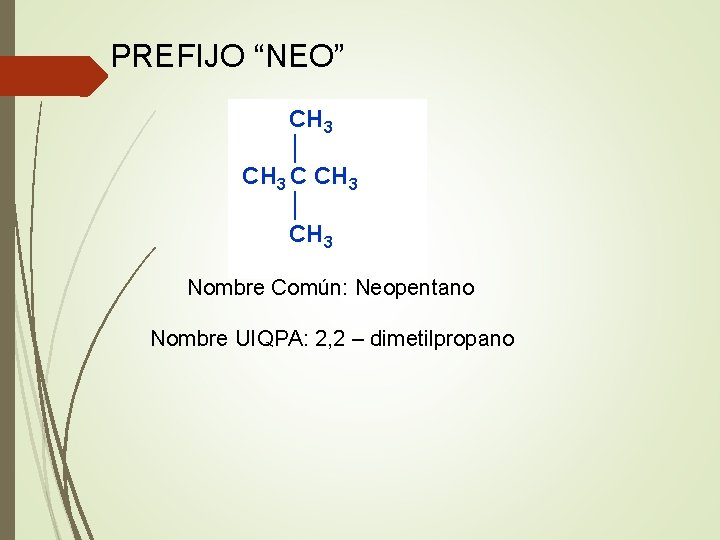
PREFIJO “NEO” CH 3 │ CH 3 C CH 3 │ CH 3 Nombre Común: Neopentano Nombre UIQPA: 2, 2 – dimetilpropano

Propiedades Químicas Son poco reactivos reacciones de: y experimentan Sustitución (sale un H y entra otro átomo o grupo de átomos) Ej: Halogenaciòn CH 3 CH 2 Cl
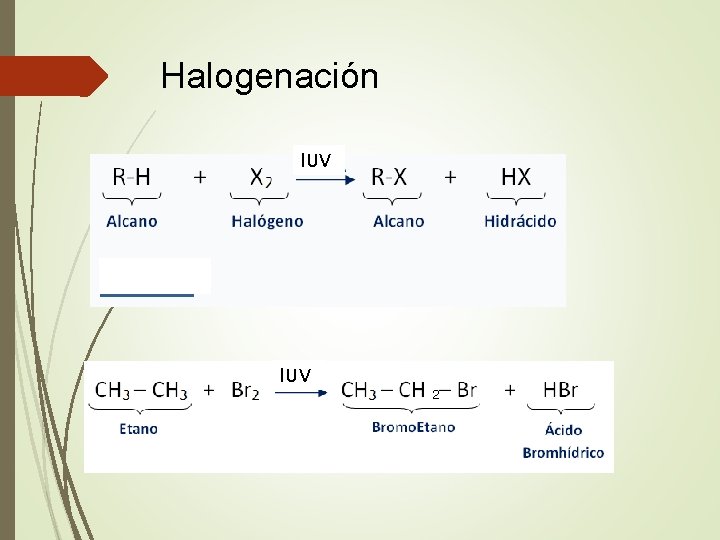
Halogenación l. UV 2

Combustión. Es la Oxidación acompañada de liberación de energía y los productos dependen de la cantidad de oxígeno presente. Puede ser Ø Incompleta: Insuficiente cantidad de O 2, los productos pueden ser CO o C, H 2 O y energía. Ø Completa: Suficiente cantidad de O 2, los productos son CO 2, H 2 O y energía.
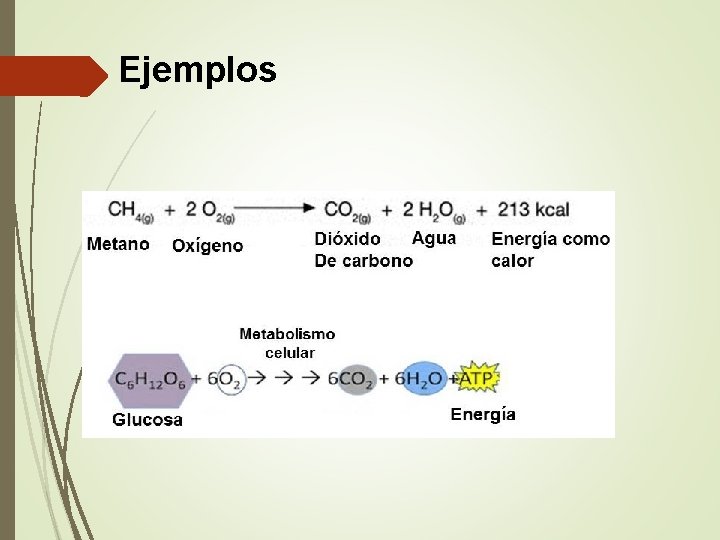
Ejemplos


- Slides: 31