Ecole Nationale Suprieure de Biotechnologie ENSB AliMendjeliConstantine Origine

Ecole Nationale Supérieure de Biotechnologie (ENSB) Ali-Mendjeli-Constantine Origine des éléments Dr. Ammar Azioune ENSB, 13/09/2015

Objectifs 1. Connaitre les premières particules et leur provenance. 2. Connaitre la provenance des premiers éléments. 3. Connaitre la formation des éléments lourds. 4. Connaitre la composition de l’écorce terrestre

Introduction · La Chimie est la seule discipline scientifique qui étudie tous les éléments. · Ceci nous incite à commencer nos cours de cette discipline par connaitre la provenance des éléments et leurs présence sur notre planète. · Remonter à l’aube des temps · Utiliser les connaissances de la terre · Le télescope permettant l’observation des phénomènes très éloignés (ondes émises lors de ces évènements)

1. Les premières particules · Selon la théorie cosmologique, l’Univers s’est développé à partir d’une explosion, connue sous le nom de « Big-Bang » · À t i: La masse-énergie se trouve sous forme de radiation dont: Le volume est infiniment petit et la température est extrêmement élevée ( 1032 K). Masse-énergie r=10µm · Détente adiabatique I. À ti = 1 ere µs suivant le Big-Bang, la température du système baisse mais reste suffisamment élevée pour que l’énergie transformée engendre une masse équivalente de matière & antimatière selon les réactions suivantes:

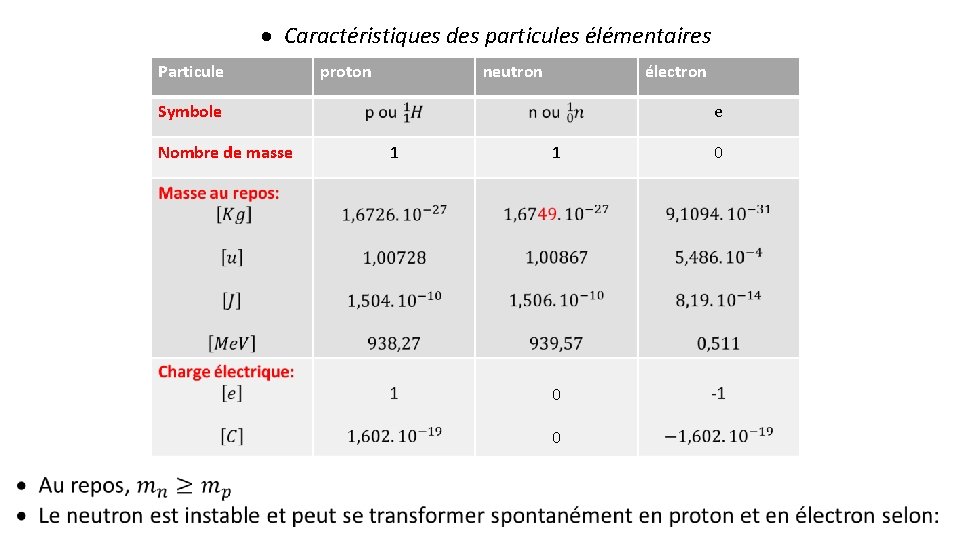
· Caractéristiques des particules élémentaires Particule proton neutron électron Symbole Nombre de masse e 1 1 0 0 0

· Lorsque la température baisse dès les 1 eres seconde suivant le big-bang, l’énergie se transforme en masse. · Lors de cette réaction, un léger surplus de protons et de neutrons est laissé dans un nuage d’électrons et d’anti-électrons, permet l’existence jusqu’à un refroidissement plus avancé de l’Univers.

· Dans ces conditions, protons et neutrons s’interconvertissent l’un dans l’autre par les réactions suivantes: Le système atteint un équilibre dynamique · Dans ces conditions de température, les électrons et positons s’annihilent par la réaction (1. 2) inversée: · L’équilibre proton-neutron est gelé à 25% de neutrons & 75% de protons

· Slide 11 proton neutron deuton · Le deuton (le premier noyau composé) est nait à partir des deux particules présentes
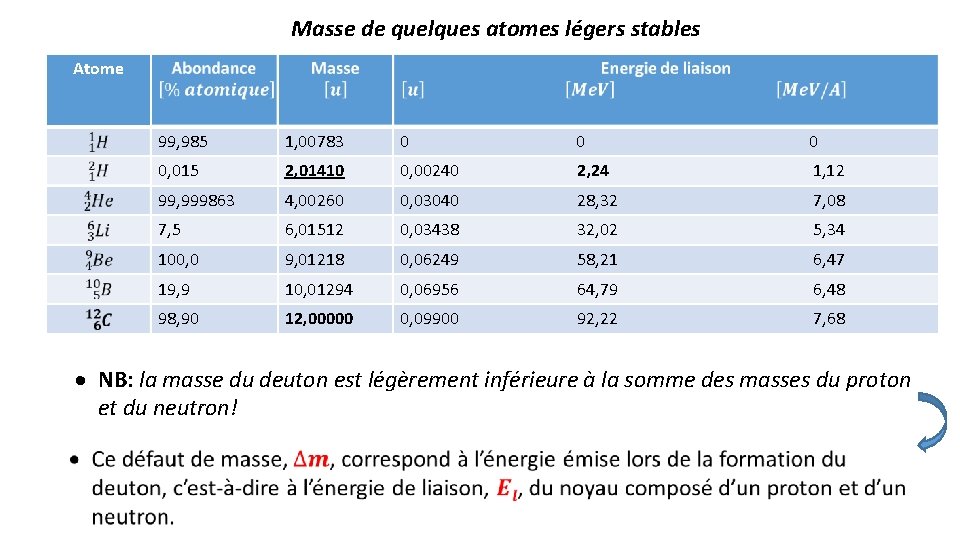
Masse de quelques atomes légers stables Atome 99, 985 1, 00783 0 0, 015 2, 01410 0, 00240 2, 24 1, 12 99, 999863 4, 00260 0, 03040 28, 32 7, 08 7, 5 6, 01512 0, 03438 32, 02 5, 34 100, 0 9, 01218 0, 06249 58, 21 6, 47 19, 9 10, 01294 0, 06956 64, 79 6, 48 98, 90 12, 00000 0, 09900 92, 22 7, 68 · NB: la masse du deuton est légèrement inférieure à la somme des masses du proton et du neutron!

· Slide 9


· Cette réaction libère une énorme quantité d’énergie, transformée sous forme d’énergie cinétique aux deux particules (deuton & positon) émis. · Les deutons formés par les réactions (1. 8) et (1. 9) sont très réactifs à ces températures, l’énergie de liaison du deuton n’étant pas beaucoup plus élevée que l’énergie thermique de « la boule de feu » . Ils peuvent donc réagir avec les noyaux et particules présents pour former d’autres noyaux.

triton hélion · Le stock des neutrons et de protons se régénère par les réactions suivantes: · L’hélion-3, le noyau de l’isotope de l’Hélium (He), peut réagir à son tour pour former l’hélion-4 selon:

L’hélion-4, noyau extrêmement stable comme le montre l’énergie de liaison. ou

· Même si la conversion de l’énergie en masse était cessée, la densité de l’Univers est encore suffisante pour provoquer des couplages masse-rayonnement importants. · Donc, l’énergie de ces couplages (interactions) alimente l’énergie cinétique de la détente: la densité et la température de l’Univers continuent à diminuer. Qqs millions d’années plus tard

2. Formation des premiers éléments · Les molécules neutres peuvent être formées par combinaisons d’électrons libres avec les noyaux d’hydrogène et d’hélium chargés positivement: · L’Univers estimé à 72% de masse d’hydrogène et de 28% de masse d’hélium.

· L’hydrogène atomique peut réagir pour former la molécule d’hydrogène

· Ceci induit une certaine anisotropie de l’expansion des nuages d’hydrogène et d’hélium de l’Univers. · Cette anisotropie provoque des instabilités qui se développent et se propagent. Donc: · Des régions de plus grande densité apparaissent qui conduisent à la formation des galaxies. · Dans ces systèmes, les forces d’attractions des particules neutres (molécule d’H 2 et atomes d’He) provoquent l’effondrement (concentration de matière) local de l’Univers conduisant à la formation d’étoiles. · Dans les étoiles, la source d’énergie provient des réactions nucléaires et de l’énergie gravitationnelle qui augmente pendant le processus de l’effondrement.

· Ces effondrements locaux induisent une augmentation de la densité par rapprochement des particules et les réactions nucléaires reprennent, dont la plus importante implique une autre forme de la fusion de l’hydrogène: · Le cœur de l’étoile s’enrichit donc d’hélium jusqu’à former un noyau d’hélium pur. · À la surface de l’étoile, le processus de fusion de l’hydrogène se poursuit.

3. Formation des éléments lourds · Le phénomène d’effondrement conduit à l’augmentation de la température locale jusqu’à rendre possible la fusion de l’hélium, induisant une nouvelle nucléosynthèse:

· Dans ce cas, le système est stable pour produire le carbone-12 et les éléments plus lourds à savoir, 16 O, 20 Ne, …, 40 Ca, par addition successive de noyaux d’hélium:
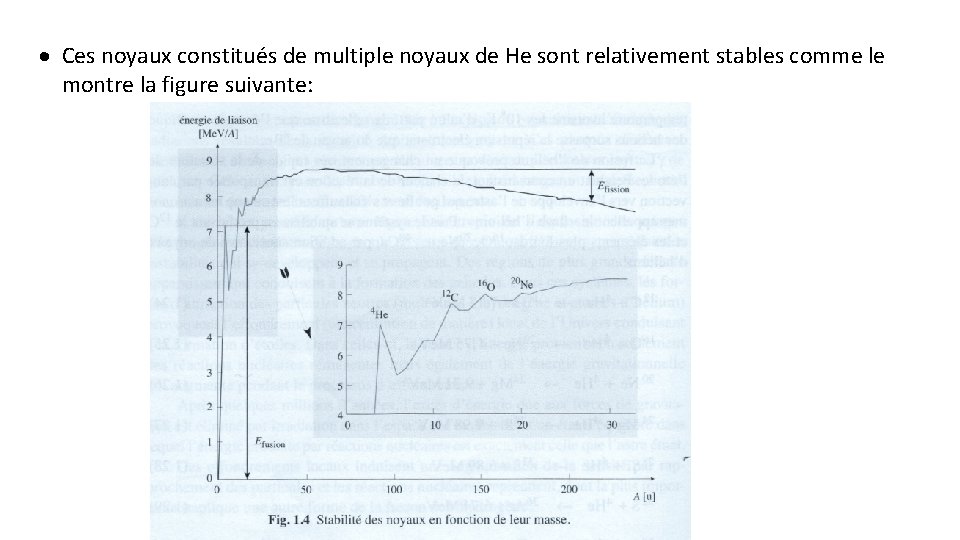
· Ces noyaux constitués de multiple noyaux de He sont relativement stables comme le montre la figure suivante:
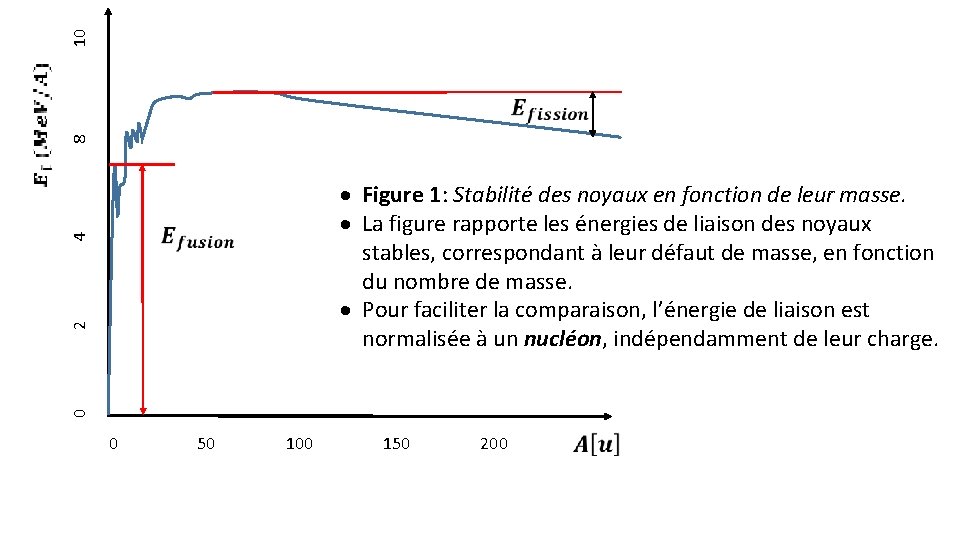
10 8 0 2 4 · Figure 1: Stabilité des noyaux en fonction de leur masse. · La figure rapporte les énergies de liaison des noyaux stables, correspondant à leur défaut de masse, en fonction du nombre de masse. · Pour faciliter la comparaison, l’énergie de liaison est normalisée à un nucléon, indépendamment de leur charge. 0 50 100 150 200


· En parallèle à ces réactions de fusion de l’hélium, le mécanisme de fusion de l’hydrogène se poursuit: · Ces réactions de fusion avec l’hydrogène conduisent à la formation d’une nouvelle série par des réactions de fusion avec l’hélium.

· L’oxygène-18 peut, à son tour, fusionner avec l’hélium en libérant des neutrons: ou ou

· Les éléments, formés par fusion avec l’hélium, participent à une nouvelle série de réactions nucléaires par « capture neutronique » , suivi d’une émission d’électrons:

· Toutes ces réactions fournissent de l’énergie thermique et lorsque la température atteint 109 K, d’autres procédés de nucléosynthèse deviennent possibles, par exemple: ou · Ces éléments accélèrent encore la naissance de nouveaux éléments

· Dans l’intense flux des neutrons, un noyau subit de multiples captures neutroniques avant d’une émission d’un électron puisse avoir lieu, les périodes noyaux intermédiaires étant très courtes par rapport à la vitesse de capture des neutrons. · Ce phénomène conduit à une augmentation du numéro atomique. Il participe à la formation du bismuth (Z = 83), Thorium (Z= 90) et l’Uranium (Z = 92). Z 90 92 Symbole Th U Terre 6. 0 2. 0 Univers 4. 10 -4 2. 10 -4 · L’abondance de Th et de l’U sur la terre suggère que la matière terrestre a passé par plusieurs cycles de formation d’étoiles, évolutions thermiques et effondrements avant d’atteindre la composition actuelle.

4. Composition de l’écorce terrestre · Lorsque la température est suffisamment basse, les électrons « se stabilisent » autour des noyaux pour former les éléments. · Actuellement, on connait 111 éléments dont 82 sont représentés par 275 isotopes stables ou la période est très longue qui rend les mesures de leur abondance naturelle (% atomique) possible. · La présence de ces isotopes explique en partie le niveau de radioactivité de notre environnement.
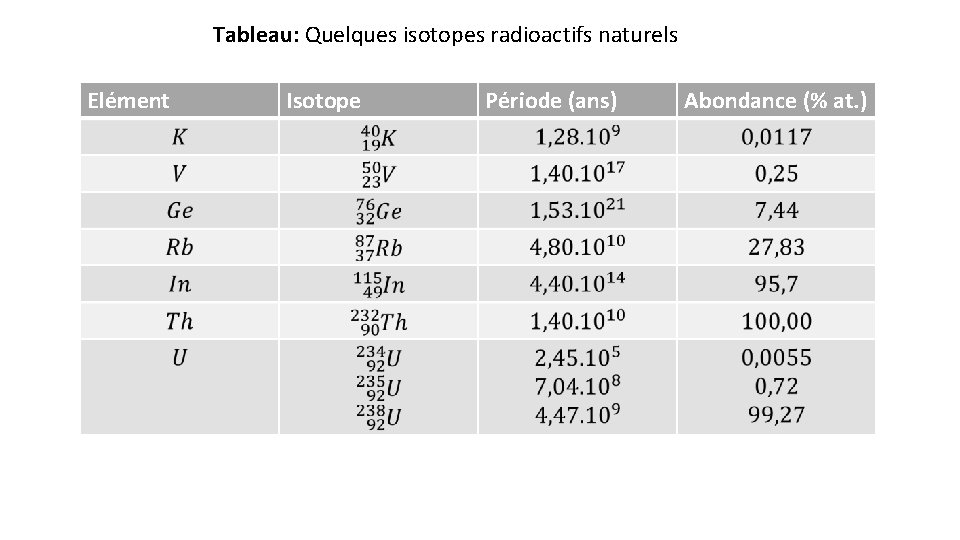
Tableau: Quelques isotopes radioactifs naturels Elément Isotope Période (ans) Abondance (% at. )
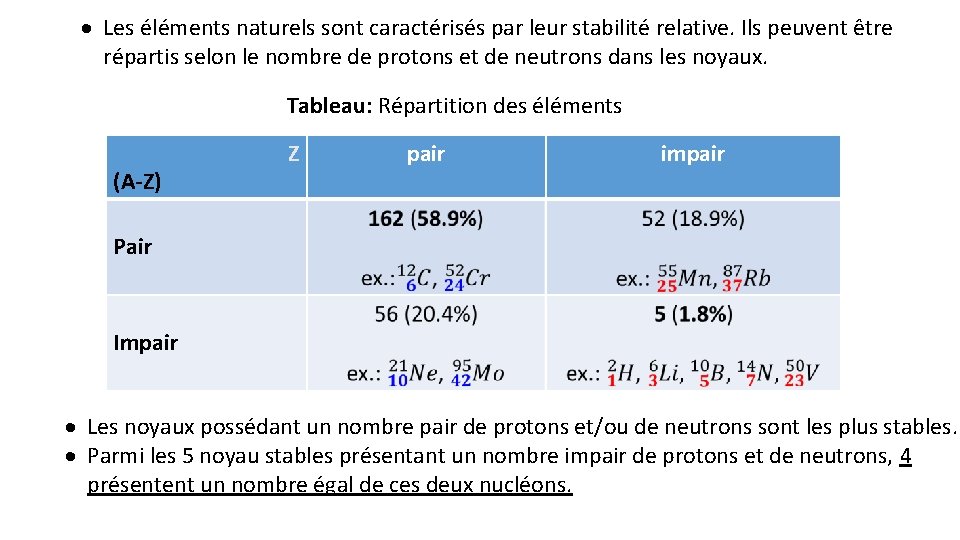
· Les éléments naturels sont caractérisés par leur stabilité relative. Ils peuvent être répartis selon le nombre de protons et de neutrons dans les noyaux. Tableau: Répartition des éléments (A-Z) Z pair impair Pair Impair · Les noyaux possédant un nombre pair de protons et/ou de neutrons sont les plus stables. · Parmi les 5 noyau stables présentant un nombre impair de protons et de neutrons, 4 présentent un nombre égal de ces deux nucléons.

· Les éléments possédant les noyaux peu stables ou excités se transforment en émettant l’excès de leur énergie sous forme de radiations particulaires ou photoniques. On parle de Radioactivité · Les réactions radioactives se différencient des réactions chimiques par: 1. les éléments ne sont pas conservés (transmutation) 2. Les énergies mises en jeu sont très élevées

Z et (A-Z) impairs: instable Z et (A-Z) pairs : stable

stable
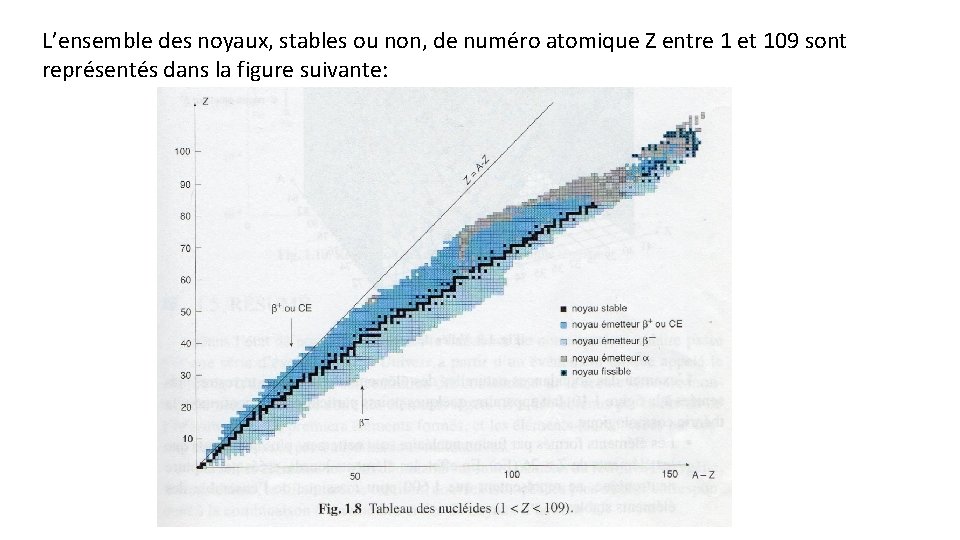
L’ensemble des noyaux, stables ou non, de numéro atomique Z entre 1 et 109 sont représentés dans la figure suivante:

- Slides: 38


























































