Ecole Nationale Suprieure de Biotechnologie ENSB AliMendjeliConstantine Ractions

Ecole Nationale Supérieure de Biotechnologie (ENSB) Ali-Mendjeli-Constantine Réactions de Complexations Dr. Ammar Azioune ENSB, 25/04/2015
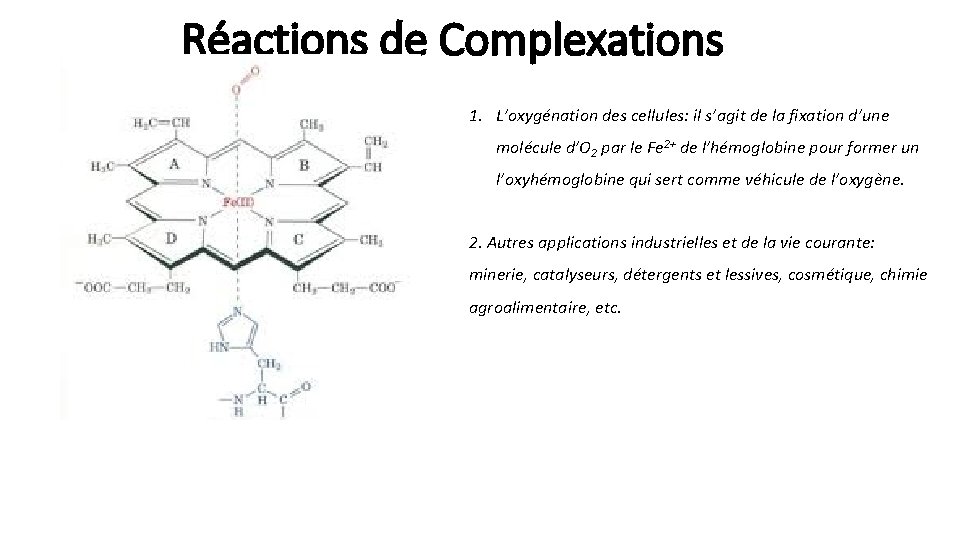
Réactions de Complexations 1. L’oxygénation des cellules: il s’agit de la fixation d’une molécule d’O 2 par le Fe 2+ de l’hémoglobine pour former un l’oxyhémoglobine qui sert comme véhicule de l’oxygène. 2. Autres applications industrielles et de la vie courante: minerie, catalyseurs, détergents et lessives, cosmétique, chimie agroalimentaire, etc.
Objectifs 1. Mise en évidence des complexes 2. Définition 3. Nomenclature des complexes 4. Equilibre de complexation

Notions de complexes 1) Mise en évidence On mélange une solution de nitrate d ’argent et une solution de chlorure de sodium. K = 1, 0 1010 On ajoute une solution d ’ammoniac : le précipité se redissout. [Ag(NH 3)2]+est un ion complexe encore appelé composé de coordination.

2) Définitions. Un complexe est un édifice polyatomique constitué d ’un atome ou d ’un cation métallique central auquel sont liés par coordination des molécules neutres ou des anions appelés ligands ou coordinats. • L ’atome ou l ’ion central doit pouvoir accepter des doublets d ’électrons ; c ’est souvent un élément de transition : Cu 2+, Fe 3+, Co 2+, Ni 2+, . . les ions Ca 2+, Mg 2+ peuvent aussi donner des complexes. • Les ligands sont des molécules ou des ions possédant au moins un doublet d ’électrons libres La coordination (ou formation d’une liaison covalente dative) est une réaction acide-base de Lewis: l’atome ou l’ion métallique central, qui accepte les doublets est un acide de Lewis (il possède des lacunes électroniques) Les ligands qui donnent les doublets, sont des bases de Lewis (ils possèdent des doublets libres disponibles)

2) Définitions. • La formule du complexe et écrite entre crochets. • Le complexe peut être neutre (ex. [Cr(CO)6]), cationique (ex. [Co(NH 3)6]+) ou anionique (ex. [Al. F 6]3 -). • • Les complexes cationiques et anioniques possèdent un contre-ion; la formule du complexe comprend d’abord le cation, puis l’anion: [Co(NH 3)6]Cl ou Na 3[Al. F 6] Les ligands liés à l ’atome central par une seule liaison sont des ligands monodentates : H 2 O, NH 3, CN-. . ; Les ligands liés à l ’atome central par plusieurs liaisons sont des ligands polydentates Le nombre de liaisons simples formées par l ’atome ou l ’ion central avec les ligands est appelé indice de coordination.
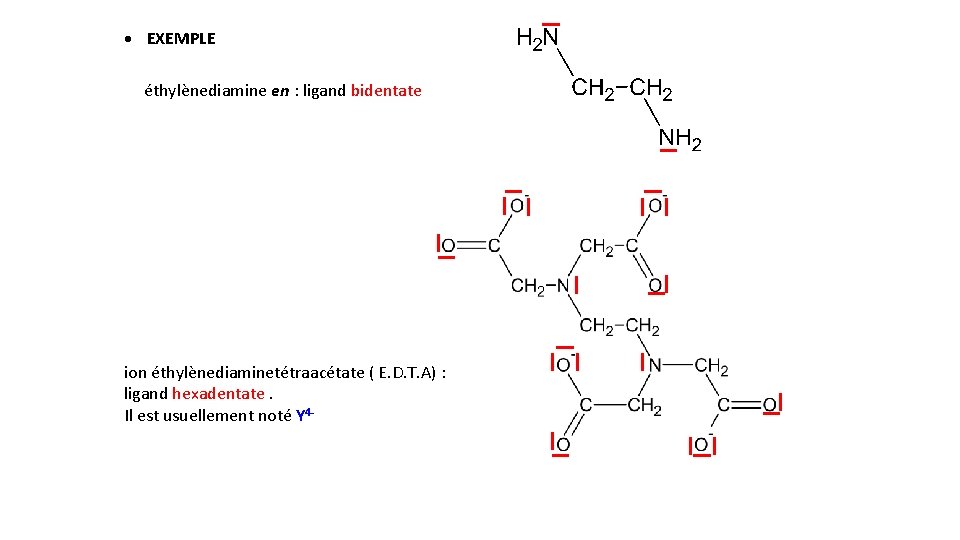
EXEMPLE éthylènediamine en : ligand bidentate ion éthylènediaminetétraacétate ( E. D. T. A) : ligand hexadentate. Il est usuellement noté Y 4 -

3 ) Nomenclature des complexes Les noms des ligands neutres les plus courants sont: NH 3: ammine H 2 O: aqua CO: carbonyle Les noms des ligands anioniques se terminent par « o » . Exemples: OH-: hydroxo. F-: fluoro. Le nom du complexe est constitué dans l’ordre: des noms des ligands dans l’ordre alphabétique, précédé si nécessaire, du préfixe multiplicateur (di, tri, tétra, etc. ), sans trait d’union, sauf si deux voyelles sont côte à côte. Les préfixes bis, tris, tétrakis, etc. servent à ne pas répéter un des préfixes précédents s’il a été déjà donné, ou précédent les ligands possédants plusieurs atomes donneurs comme l’éthylènediamine (en).

3 ) Nomenclature des complexes du nom de l’élément auquel appartient l’atome central suivi de son nombre d’oxydation en chiffres romains et entre parenthèses; quand le complexe est neutre ou cationique, l’élément garde son nom: Ex: [Cr(H 2 O)6]3+ est l’ion: hexa-aquachrome (III) quand le complexe est anionique, le nom de l’élément prend la terminaison –ate;
![3 ) Nomenclature des complexes exemple 1 : [Co(NO 2)3(NH 3)3] tri nitrito tri 3 ) Nomenclature des complexes exemple 1 : [Co(NO 2)3(NH 3)3] tri nitrito tri](http://slidetodoc.com/presentation_image_h/d347d1be27daf5e0e281c5d562812b6f/image-10.jpg)
3 ) Nomenclature des complexes exemple 1 : [Co(NO 2)3(NH 3)3] tri nitrito tri ammine cobalt (III) nombre de ligands exemple 2 : [Cr. Cl 2(H 2 O)4]+ : exemple 3 : [Fe(CN)6]4 - : ligands élément central nombre d ’oxydation de l ’élément central ion dichlorotétra-aquachrome (III) ion hexacyanofer rate (II) terminaison indiquant que l ’ion complexe est un anion

Equilibres de complexation Soit la réaction bilan de complexation suivante: La constante de dissociation globale (Kdg) est la constante de dissociation. Elle est l’inverse de bn La constante de dissociation globale (Kdg) est généralement donnée par la forme p. Kdg

Equilibres de complexation Soit la réaction bilan de complexation suivante: L’inverse de Kfi est la constante de dissociation Kdi :

Analogie avec les équilibres acido basiques. Couple donneur accepteur de ligand Soit l’équilibre de dissociation de l’ion complexe [Ca. Y]2 - ; Couple acide base Couple donneur accepteur de ligand [Ca. Y]2 - ; donneur de ligand Y 4 - A- ; accepteur de proton H+ Ca 2+ ; accepteur de ligand Y 4 - particule échangée ; Y 4 - AH ; donneur de proton H+ H+ KA 0 ; constante d’acidité p. H = - log([H 3 O+]) Kd ; constante de dissociation p. Y = - log([Y 4 -])
- Slides: 13